脑血管内皮细胞(Brain endothelial cells, BECs)作为血脑屏障的核心,其功能异常与脑卒中、脑血管畸形等多种疾病密切相关。而高效、特异性靶向这类细胞的工具,长期以来是神经血管研究的关键瓶颈。从2016年首个特异性载体到2025年精准建模工具升级,包括AAV-BI30、AAV-BR1、AAV-X1家族及rAAV-miniBEND四大载体系统,从衣壳工程到启动子优化,构建起多元化靶向策略,见证从“能靶向”到“精准用”的跨越式发展!
AAV-BR1:基于AAV2改造,插入NRGTEWD肽段
特点:
✅ 内皮特异性>60%
✅ 脱靶表达极低,外周器官几乎无转基因活性
✅ 表达稳定持久,可实现跨血脑屏障
✅ 主要靶向毛细血管,动脉/静脉转导较弱
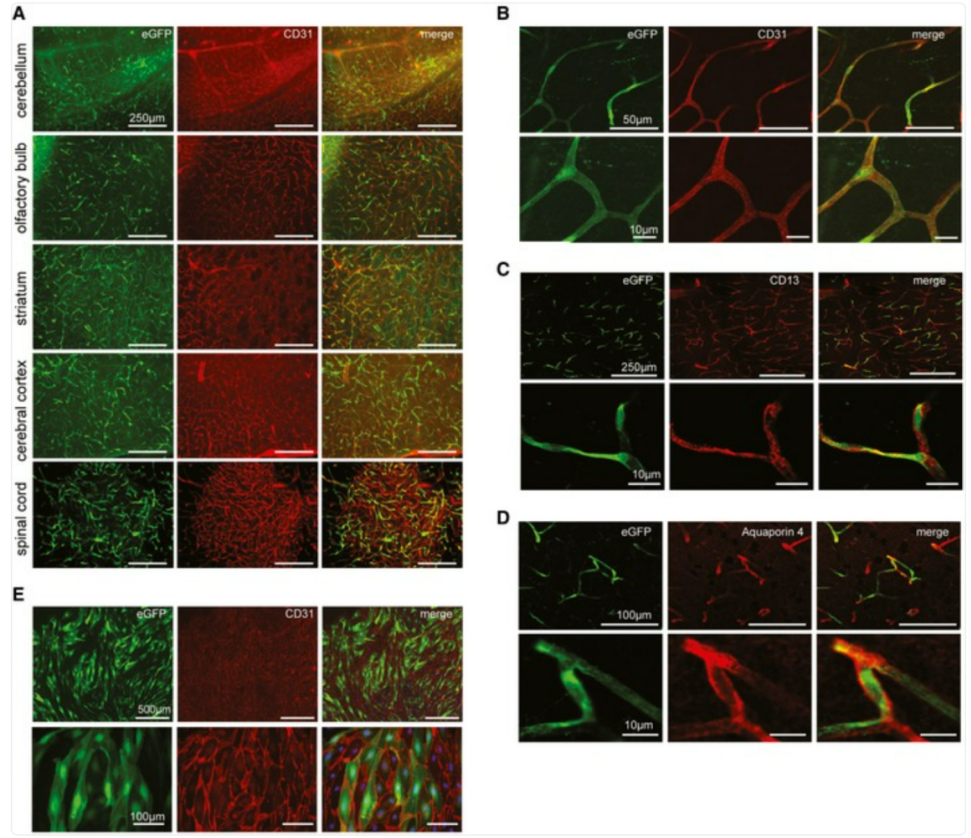
图1 AAV-BR1有效感染脑、脊髓毛细血管内皮细胞,少量感染神经元和星形胶质细胞
应用案例
小鼠:新生Nemo−/+小鼠
病毒:AAV/BR1-CAG-NEMO
注射方案:尾静脉注射,6x1010vg/鼠,表达8天
结果:色素失禁症(IP)由X染色体上Nemo基因失活突变导致,患者常出现癫痫等神经系统症状,伴随脑毛细血管丢失和血脑屏障破坏。通过AAV-BR1静脉递送Nemo基因,可显著减少模型小鼠脑内“空血管基底膜链”(stringvessels)形成,降低内皮细胞凋亡率,恢复血脑屏障完整性,同时改善小鼠体重增长迟缓的表型,为IP的靶向治疗提供了proof-of-concept。
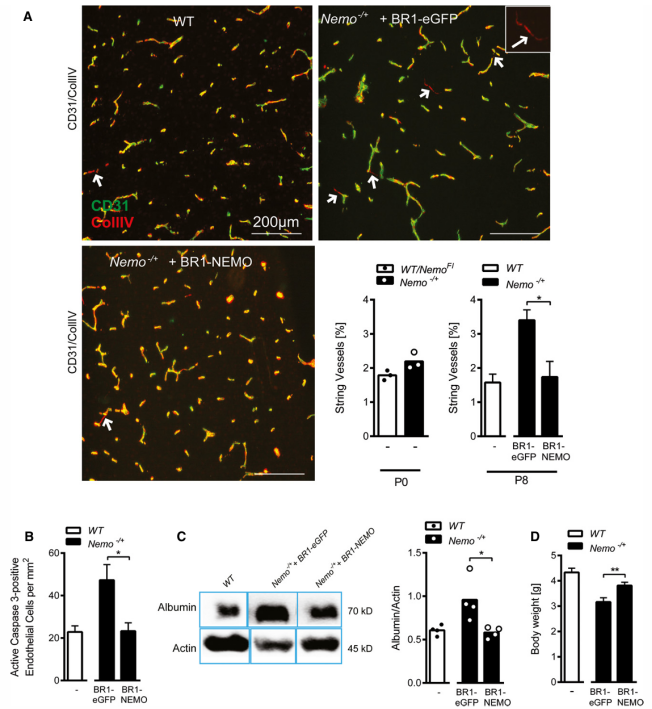
图2 AAV-BR1可用于实现高效的内皮细胞特异性基因操作
AAV-BI30:基于AAV9改造,插入7-mer肽段NNSTRGG
特点:
✅ 内皮特异性>80%
✅ 高效转导全血管层(动脉+毛细血管+静脉)
✅ 跨物种兼容(小鼠/大鼠/人源细胞)
✅ 搭载miR-122系统,显著降低肝毒性
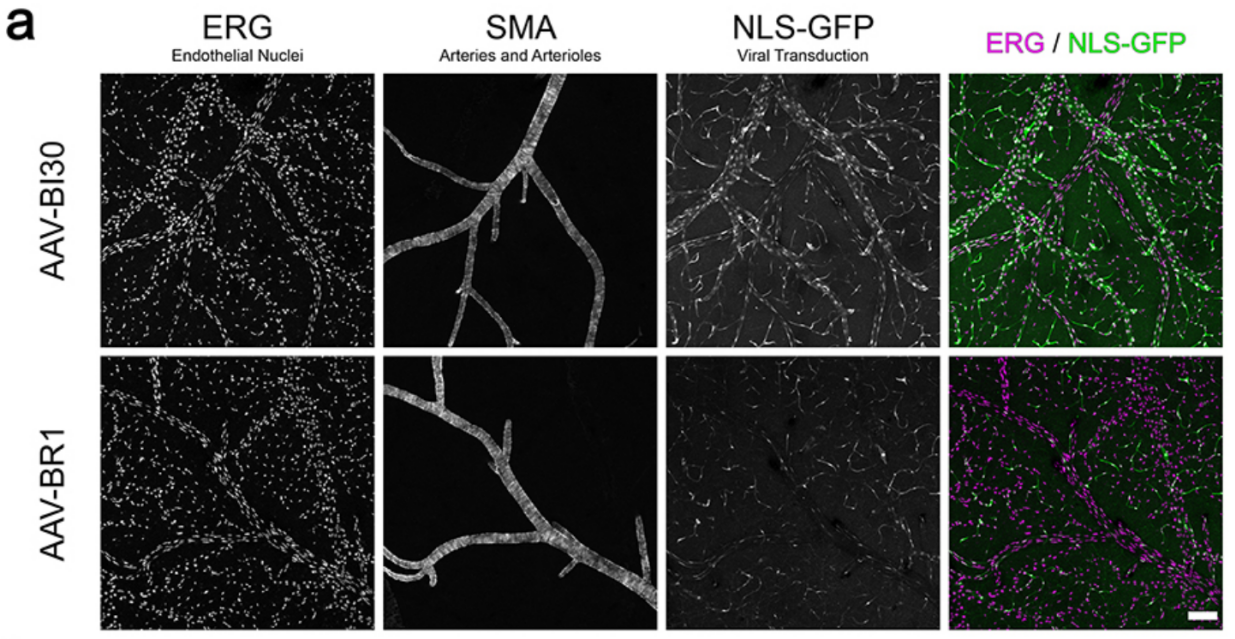
图3 AAV-BI30能有效转导动静脉内皮细胞
应用案例
小鼠:Cav1fl/fl小鼠
病毒:rAAV/BI30-CAG-Cre-miR122-WPRE
注射方案:尾静脉注射,1×1011vg/鼠,表达4周
结果:Caveolin-1(Cav1基因编码)蛋白是细胞膜小凹的核心组分,参与血脑屏障动态平衡与神经血管耦合。通过向Cav1ⁿˡ/ⁿˡ小鼠注射携带Cre重组酶的AAV-BI30实现特异性降低脑内皮细胞的Caveolin-1蛋白水平,不影响CNS内动脉平滑肌细胞及外周心脏微血管内皮细胞Caveolin-1表达。精准验证了内皮细胞特异性基因功能,为血脑屏障相关疾病的靶点筛选提供了可靠工具。
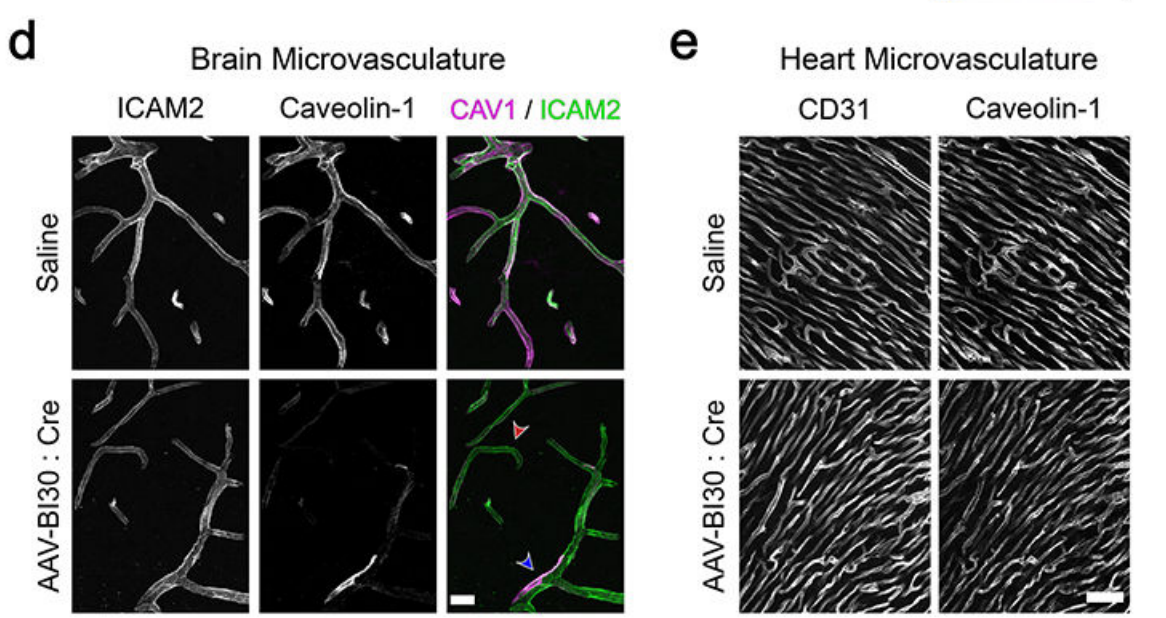
图4 AAV-BI30可用于实现高效的内皮细胞特异性基因操作
AAV-X1家族:M-CREATE定向进化技术,在AAV9衣壳引入特异性肽段
特点:
✅ 内皮细胞靶向特异性超90%
✅ 不依赖Ly6a受体,打破小鼠品系限制,在BALB/cJ等非许可品系中高效发挥作用。
✅ 实现血清型切换,解决重复给药时的中和抗体问题,为长期治疗提供可能。
✅ X1.1变体在非人灵长类(绒猴、恒河猴)和人类脑切片中表现出强大的中枢转导能力,人脑微血管内皮细胞转导率较AAV9提升180倍,加速临床转化进程。
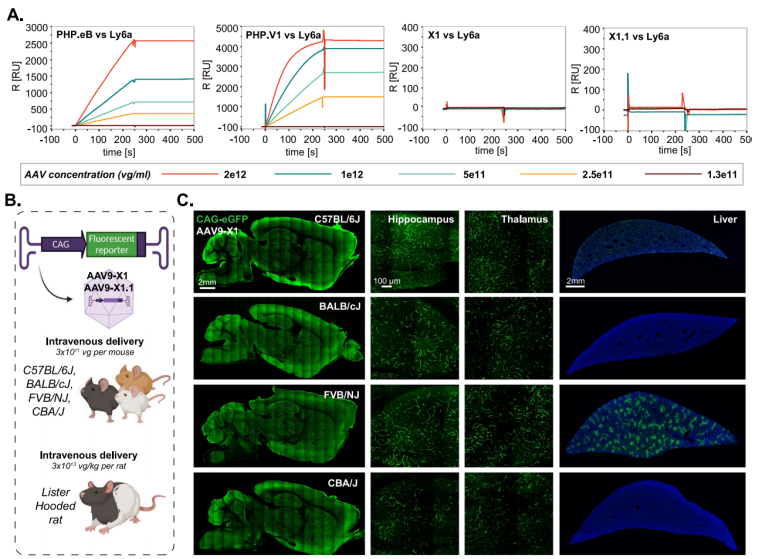
图5 AAV9-X1和AAV9-X1.1可实现多种小鼠品系内皮细胞
应用案例
小鼠:HevinKO小鼠
病毒:rAAV/X1.1-CAG-Hevin
注射方案:尾静脉注射,1×1011vg/鼠,表达3周
实验结果:Hevin(又名SPARCL1)是SPARC家族分泌型糖蛋白,表达于中枢神经系统的星形胶质细胞及部分神经元(内皮细胞仅检测到mRNA),作为“桥梁”调控丘脑-皮层突触的形成、成熟与可塑性,与自闭症、精神分裂症、阿尔茨海默病等神经系统疾病相关。通过AAV-X1.1载体向Hevin敲除小鼠眶后注射外源Hevin基因,3周后脑内皮细胞可特异表达并分泌Hevin,成功挽救小鼠丘脑-皮层突触缺陷,为自闭症等Hevin相关神经系统疾病提供了潜在治疗策略。
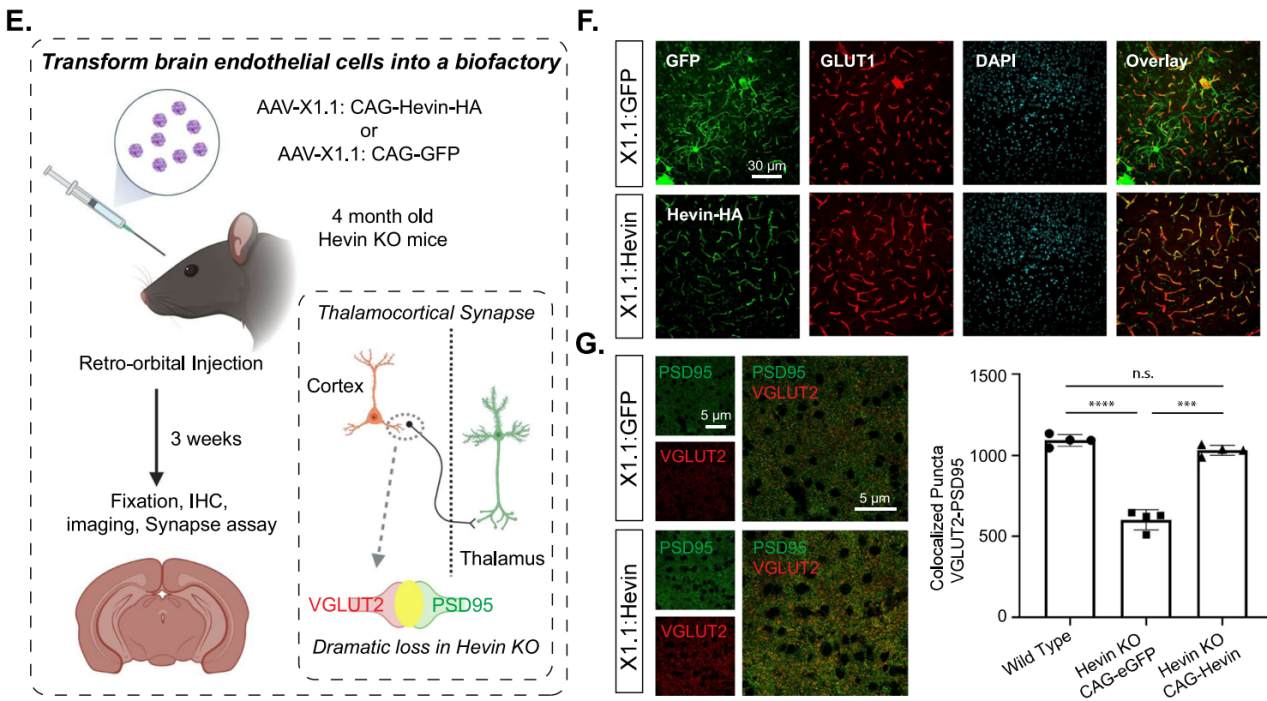
图6 AAV-X1可用于实现高效的内皮细胞特异性基因操作
AAV-miniBEND系统通过结合从小鼠Tek基因中分离的最小启动子和优化的顺式作用元件,实现了在小鼠和大鼠脑内皮细胞中特异性的基因表达。
特点:
✅ 高特异性与高效率:通过颅内注射或静脉注射实现脑内皮细胞的特异性标记。
✅ 节省载体容量:节省2.5kb载体空间,可容纳更大的外源基因。
✅ 靶向性:外周器官脱靶表达可忽略
✅ 多阶段适用:适用于胚胎期、新生期和成年期,支持局部(颅内、玻璃体)或全身性递送(静脉)。
✅ 跨物种兼容:已在小鼠、大鼠等多种动物中验证有效。
✅ 兼容多种AAVcapsid(PHP.eB、BI30等),可实现脑内局部精准靶向,解决传统载体局部给药效率低的问题。
✅ 脑血管畸形疾病精准建模:支持体细胞突变介导的疾病模拟;适配内皮细胞特异性基因敲除、过表达和基因编辑,适用于不同发育阶段的神经血管研究。
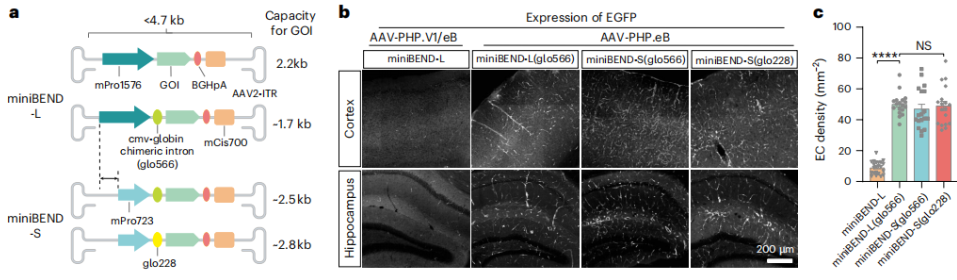
图7 rAAV-miniBEND启动子的优化及高靶向内皮细胞
应用案例
1.脑海绵状血管瘤(CCM)
小鼠:成年小鼠
病毒:rAAV-PHP.eB-miniBEND-MAP3K3I441M
注射方案:脑立体定向注射至大脑皮层,~1.5-5×109vg/鼠;静脉注射~1.5-5×1011vg/鼠,表达2-3周
结果:通过rAAV-miniBEND表达系统,将携带I441M点突变的人源MAP3K3基因递送至小鼠脑血管内皮细胞,通过静脉注射实现全脑病变诱导、局部注射实现局灶性病变构建,成功建立散发性脑海绵窦畸形(CCM)小鼠模型;该模型呈现出与临床Ⅳ级CCM一致的爆米花样出血、血脑屏障渗漏、血管海绵状扩张等病理特征,经MRI及多种组织学染色验证,且rAAV-miniBEND系统相比传统AAV血清型靶向性更优,适用于CCM病变的活体延时成像研究。
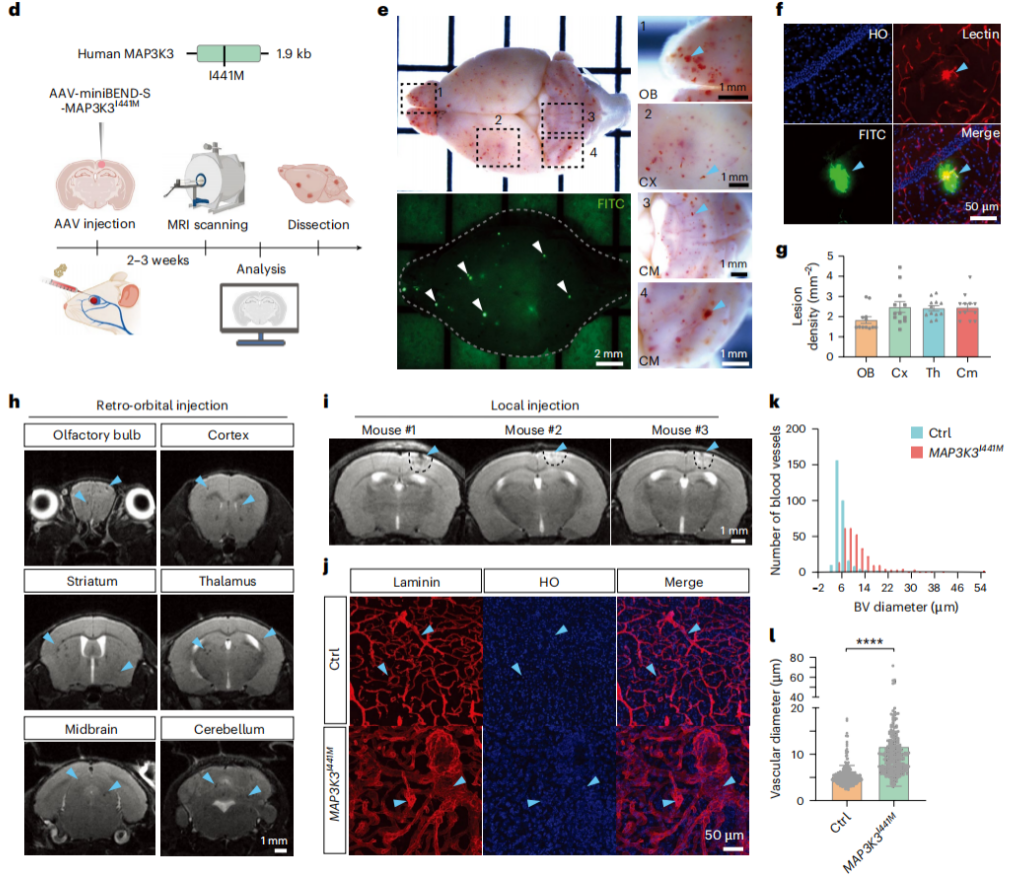
图8 利用rAAV-miniBEND系统建立CCM模型
2. 脑动静脉畸形(AVM)建模
小鼠:30-50日龄Braf-CAfl/fl小鼠
病毒:rAAV-PHP.eB-miniBEND-Cre
注射方案:脑立体定向注射至大脑皮层或海马体,~1.5-5×109vg/鼠;表达2周后开始检测
结果:向Braf-CAfl/fl小鼠局部递送Cre重组酶,特异性激活其携带的BrafV600E致癌突变,成功在数周内构建出快速进展的脑动静脉畸形小鼠模型。该模型再现了人类bAVM的核心病理特征:包括脑出血、水肿、异常扩张的畸形血管团、组织坏死以及血脑屏障破坏;模型小鼠表现出偏瘫、癫痫等临床症状,且死亡率高。进一步研究揭示了血管扩张伴随的血流动力学改变、内皮-间充质转化以及关键的动静脉分流结构,为深入理解bAVM的发病机制和药物筛选提供了有力工具。
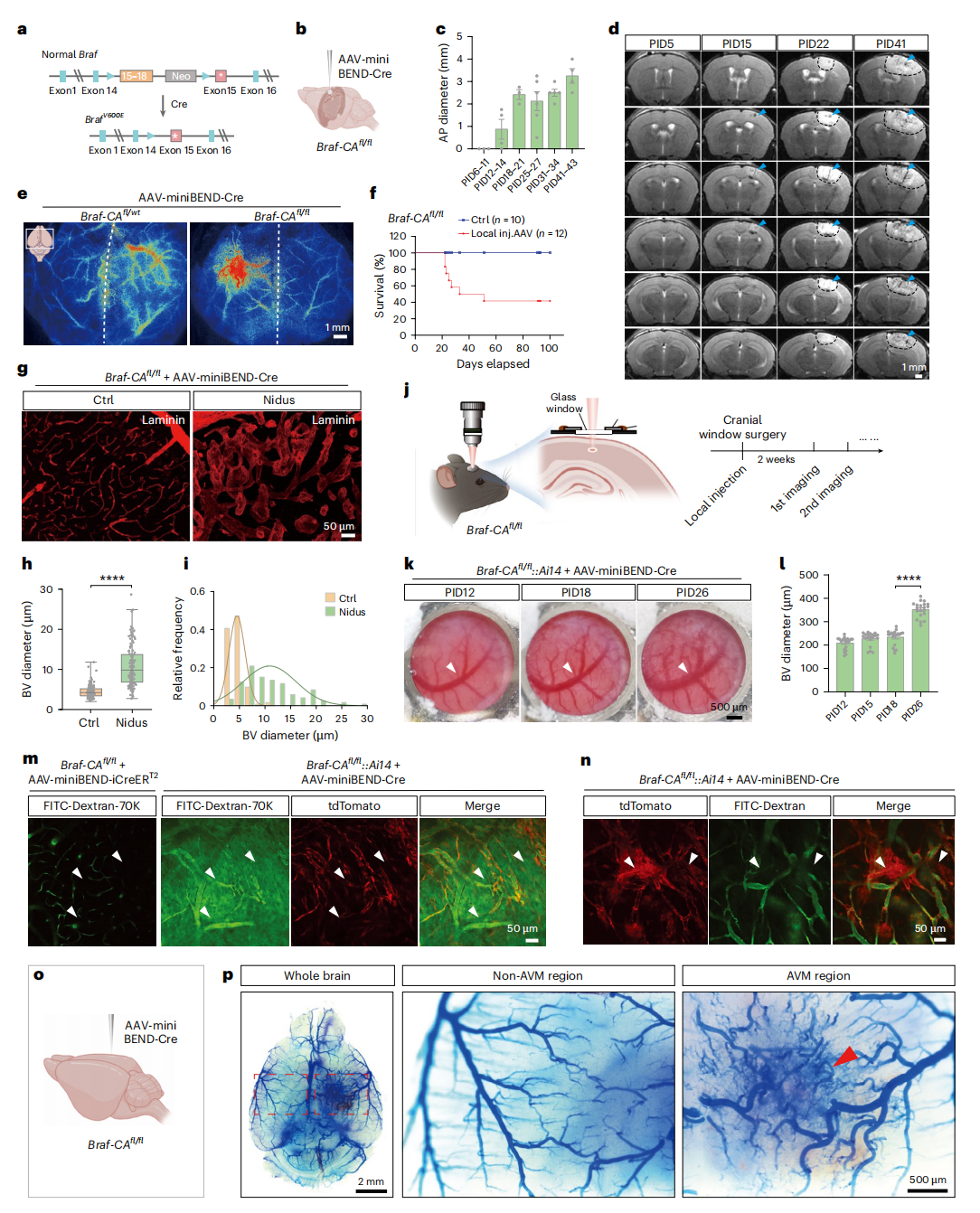
图9 利用rAAV-miniBEND系统建模bAVM
从2016到2025年,AAV靶向脑血管内皮技术实现四大关键突破:靶向范围从毛细血管聚焦到全血管段覆盖、跨物种兼容;特异性从脑内特异性到外周脱靶极小化;功能从单纯转导扩展到基因编辑、重复给药、疾病建模。这些工具不仅解决了神经血管研究的技术瓶颈,更推动了脑血管畸形、脑卒中后遗症等疾病的基因治疗研发。
靶向脑血管内皮细胞病毒策略汇总

参考文献
[1]Körbelin J, Dogbevia G, Michelfelder S, et al. A brain microvasculature endothelial cell-specific viral vector with the potential to treat neurovascular and neurological diseases. EMBO Mol Med. 2016;8(6):609-625.
[2]Krolak T, Chan KY, Kaplan L, et al. A High-Efficiency AAV for Endothelial Cell Transduction Throughout the Central Nervous System. Nat Cardiovasc Res. 2022;1(4):389-400.
[3]Chen X, Wolfe DA, Bindu DS, et al. Functional gene delivery to and across brain vasculature of systemic AAVs with endothelial-specific tropism in rodents and broad tropism in primates. Nat Commun. 2023;14(1):3345.
[4]Li JL, Bi Z, Chen XJ, et al. A targeted vector for brain endothelial cell gene delivery and cerebrovascular malformation modelling. Nat Biomed Eng. Published online October 29, 2025.