监测动物模型的血液循环对理解生理现象、疾病发展至关重要。目前通过向血浆中注射荧光示踪剂来观察毛细血管血流,但常用的荧光标记葡聚糖存在增加血液粘度、信号衰减快、需重复注射等问题,会给动物带来应激并影响实验结果的生理相关性。
2022年哥本哈根大学研究人员在Cell Reports Methods发表题为“Liver-secreted fluorescent blood plasma markers enable chronic imaging of the microcirculation”研究论文,作者开发出一种基于病毒的创新方法,通过单次腹腔或静脉注射腺相关病毒(AAV),使肝脏表达荧光分泌型白蛋白融合蛋白(如白蛋白albumin融合mNeonGreen, Alb-mNG),从而实现对小鼠血浆长达数月的标记。该方法克服了传统荧光染料标记的局限性,可用于宏观和微观层面长期观察脑血管和外周血管循环,且不会引起炎症或影响动物行为。
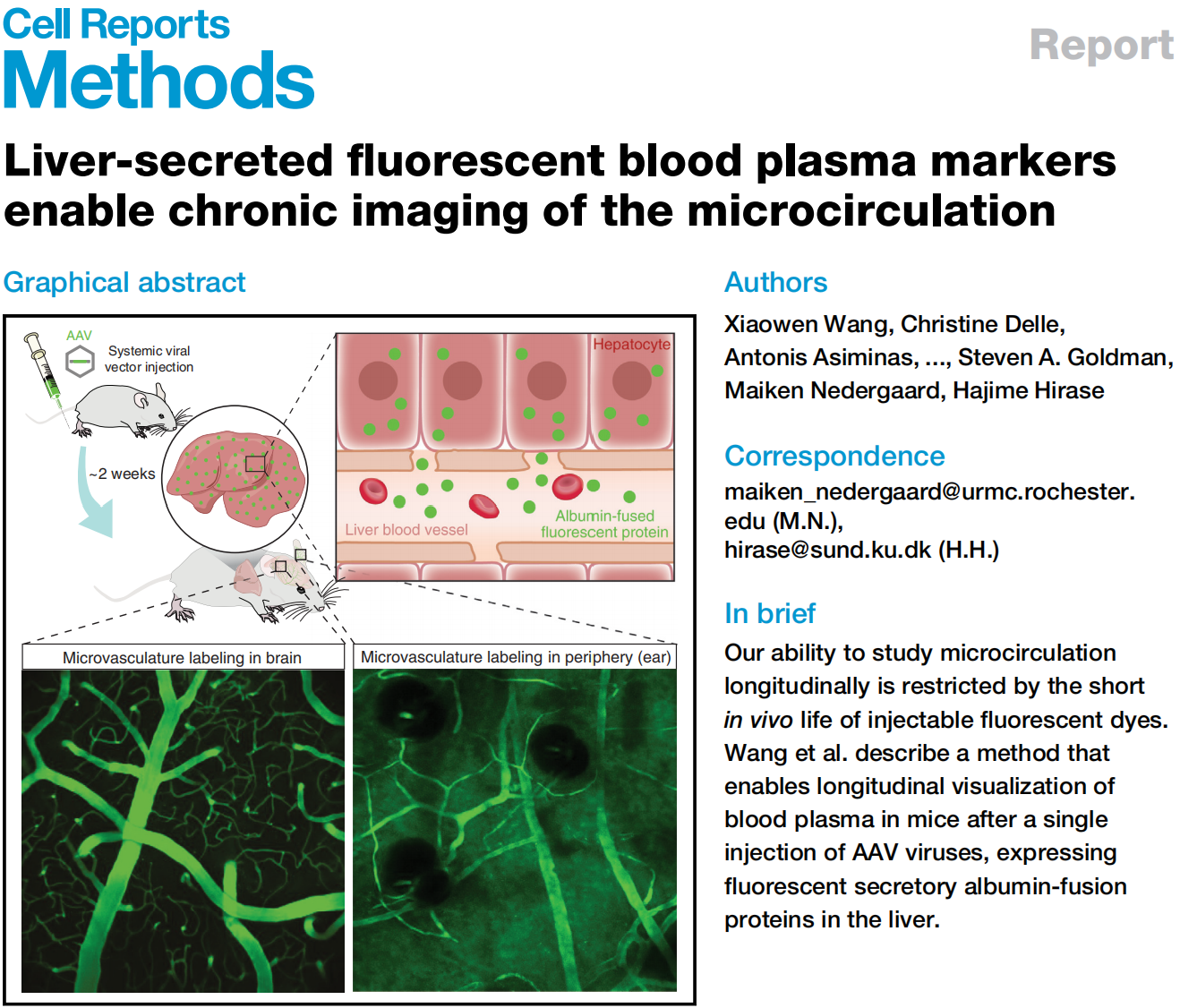
基于肝细胞中分泌型成熟白蛋白的加工过程,研究人员推测将mNG融合到白蛋白C端(Alb-mNG)可使其分泌到细胞外,而N端融合(mNG-Alb)会导致其在细胞质中积累。将含有Alb-mNG和mNG-Alb构建体的哺乳动物表达质粒转染HEK293细胞(图1A和1B),并以含有免疫球蛋白K(IgK)前导信号肽的分泌型mNG(IgKL-mNG)作为阳性对照。在转染后1天和2天对HEK293T细胞进行成像观察(图1C-1E)。IgKL-mNG和Alb-mNG表达导致细胞质荧光信号较弱,培养基荧光明显,且细胞内定位不均匀;mNG-Alb则在细胞质中呈现明亮荧光表达(图1C)。通过测量培养基荧光强度进一步证实了IgKL-mNG和 Alb-mNG的分泌(图1E),且培养基荧光强度随时间增加,表明分泌蛋白具有稳定性和积累性。结果表明白蛋白与荧光蛋白的C端融合可作为基因编码的分泌型示踪剂,在体内肝实质细胞表达时,白蛋白融合荧光示踪剂可通过肝血窦进入血液。
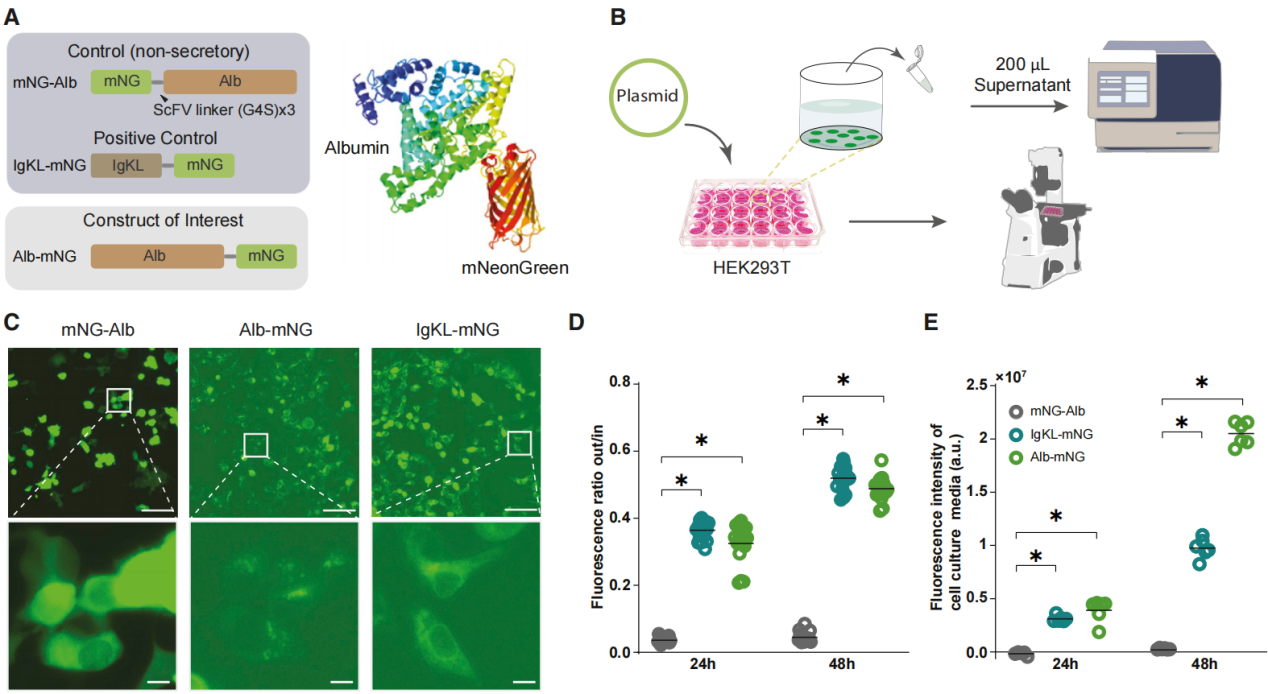
图1 分泌型荧光蛋白标记白蛋白的构建与验证
为了在肝脏中实现Alb-mNG的体内表达,研究使用了腺相关病毒8(AAV8),因为它对肝细胞具有高亲和力。采用最小甲状腺素运载蛋白启动子 P3来实现肝细胞特异性表达(图2A)。通过全身注射AAV8-P3-GFP(静脉注射,2×10¹¹vg,注射后3周;图2D),证实了AAV在肝细胞中的强表达。结果发现感染AAV8-P3-Alb-mNG的肝脏荧光信号相对较弱,这很可能是由于Alb-mNG的分泌特性所致(图2D)。在注射AAV8后的8周内采集血液样本(图2A和2B)。对血液样本进行检测,结果显示注射后最早2天就能检测到荧光信号,到第5天信号变得更亮。对血浆荧光进行纵向定量分析表明,信号在注射后3-4周达到峰值,且表达持续超过8周(图2C)。在这8周内,进一步对血浆中mNG和白蛋白的浓度进行了定量分析(图2E和2F)。结果表明在注射后2周及以后,血浆中Alb-mNG的浓度约为1mM(图2E)。此外,总血浆白蛋白浓度(内源性和Alb-mNG)保持稳定(图2F),且处于已发表的小鼠血清白蛋白浓度范围内(图2F),这表明白蛋白相关的渗透稳态正常。
为检测重组蛋白表达可能引发的免疫反应,测量了血浆中C反应蛋白(CRP)的水平,CRP是一种用于衡量组织炎症的标准全身性标志物。结果显示,注射AAV的小鼠血浆CRP水平与注射生理盐水的对照组相当(图2G)。通过IBA1免疫组织化学方法观察了肝脏巨噬细胞和脑小胶质细胞(图2H)。结果表明,注射AAV8的小鼠肝脏巨噬细胞和脑小胶质细胞的形态并未显示出任何炎症迹象(图2H)。此外,在给予AAV8-P3-Alb-mNG或AAV8-P3-IgKL-mNG 4周后,小鼠的体重和旷场活动行为均未受到影响。综上所述,这些实验表明这种血浆标记方法对宿主的生理和行为影响极小。
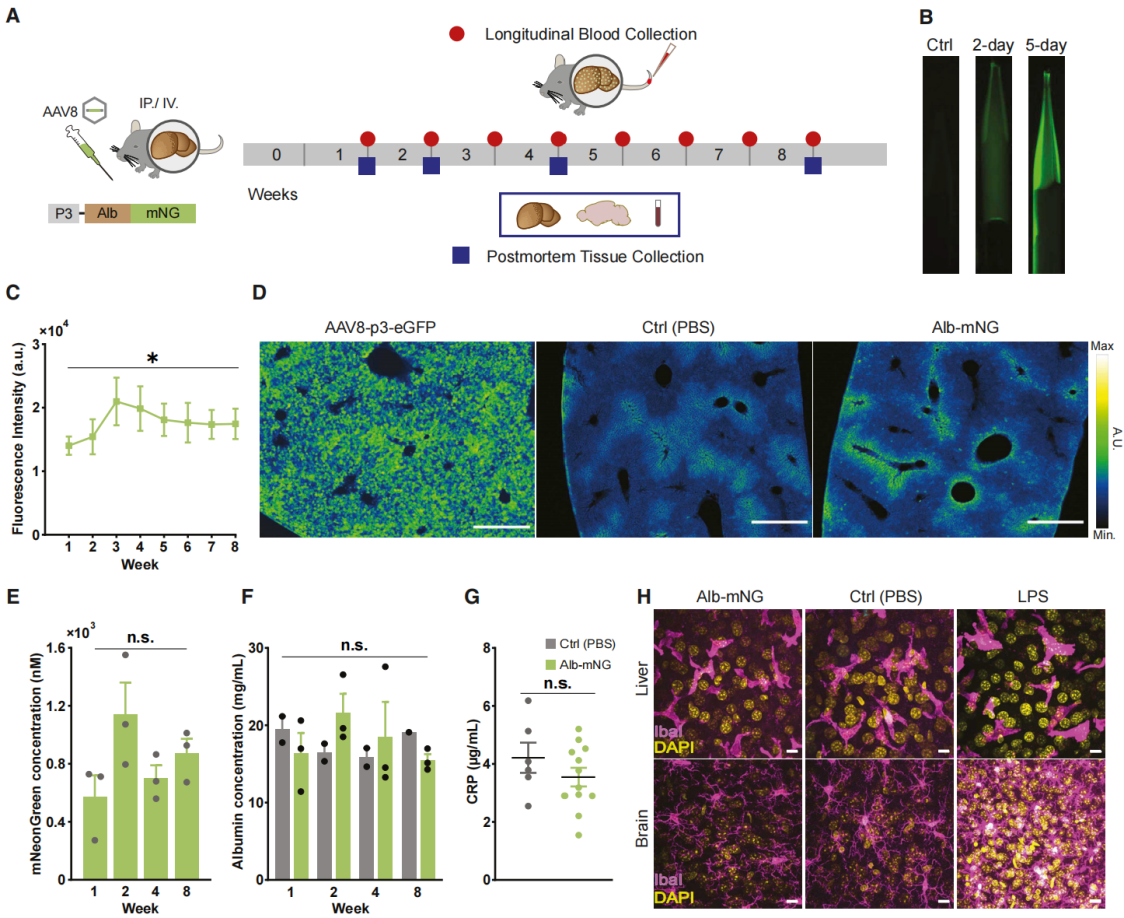
图2 肝细胞表达Alb-mNG对血浆进行稳定和长期可视化
确认单次腹腔注射AAV使血浆产生荧光后(通过肠系膜血管血流进入肝脏),利用慢性颅骨窗对小鼠脑血管成像(图3A)。给表达Alb-mNG的小鼠注射70kDa Texas Red葡聚糖,对比二者荧光效果(图3A和3B)。发现注射10分钟时,标记葡聚糖与Alb-mNG显示的血管模式匹配,但前者信号在1小时内大幅下降,而Alb-mNG在2小时记录过程中信号稳定,证明Alb-mNG在长时间成像中优势明显(图3C)。在AAV注射后3周和7周对皮质微血管成像,观察到多数微血管结构相似,但存在血管可塑性现象(图3D和3E)。通过对含单个毛细血管区域进行高帧率成像,证实AAV注射3周后白蛋白融合示踪剂表达满足快速成像要求(图3F和3G)。在刺激小鼠触须时对触须桶状皮层微血管成像,证明触须刺激可使血浆标记小鼠产生功能性充血。该方法能在AAV注射7周后长期评估功能性充血,且血管类型与时间存在交互作用(图3I和3J)。
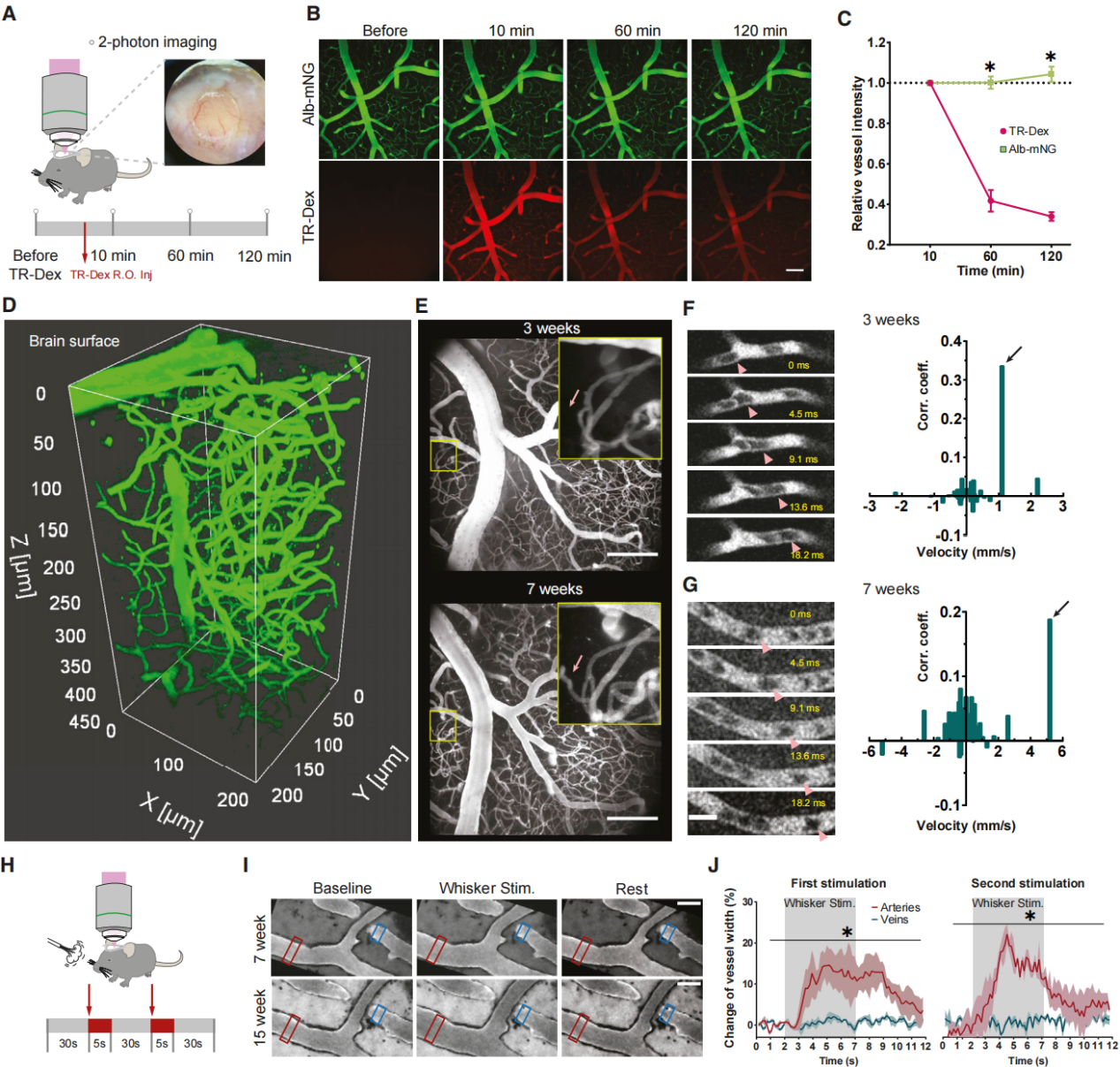
图3 Alb-mNG基因表达在长时间成像过程中优于荧光葡聚糖
作者还开发了多种白蛋白融合蛋白示踪剂(如 Alb-mScarlet 等),且证明不同给药途径对血浆荧光强度影响不大。即使在单次腹腔注射 Alb-mNG 病毒构建体10周后,荧光信号仍然很强,足以对外周毛细血管中的红细胞流动进行快速成像。最后,测试了Alb-mScarlet 和 Alb-mNG是否适合用于脑血管的宏观研究。在注射Alb-mScarlet和Alb-mNG 4周后,通过宽场荧光显微镜可轻松通过颅骨窗对大脑表面的主要血管进行成像(图4A)。结果表明Alb-mScarlet 增强了血管与实质背景之间的图像对比度,导致血管成像的信噪比显著提高(图4B和4C)。
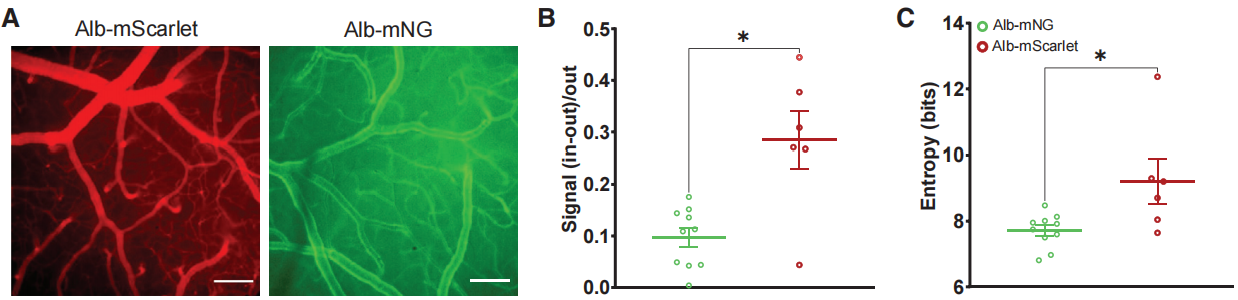
图4 Alb-mNG与Alb-mScarlet宏观荧光成像的比较
血管疾病研究:纵向监测血管畸形、炎症性血管损伤、血脑屏障通透性变化;
发育与衰老研究:追踪小鼠生命周期中(如数月)毛细血管网络的形成、重塑及衰老相关变化;
药物疗效评估:长期观察血管靶向药物对血流动力学、血管可塑性的改善效果,减少动物分组和使用量;
多模态成像:与内皮细胞、周细胞等特异性标记工具结合,研究血管细胞与血流的相互作用。
无法重复给药:首次 AAV 注射后产生中和抗体,后续注射无法有效感染肝细胞;
探针大小限制:AAV 载体的包装容量(4.7kb)制约了荧光蛋白或功能模块的大小;
物种局限性:目前仅在小鼠中验证,大型实验动物(如大鼠、小型猪)的应用需优化病毒剂量和给药方式。
2025年1月8日,哥本哈根大学转化神经医学中心Maiken Nedergaard团队在Cell上发表了文章Norepinephrine-mediated slow vasomotion drives glymphatic clearance during sleep,研究探讨了非快速眼动(NREM)睡眠期间,脑内淋巴系统清除废物的机制。用AAV8/P3-alb-mScarlet慢性标记小鼠血液血浆(图5),通过单次腹腔或静脉注射靶向肝脏肝细胞表达,使荧光蛋白mScarlet与白蛋白融合并分泌至血液循环,实现对血液的长期荧光标记,支持自由活动小鼠在清醒、非快速眼动睡眠(NREM)、快速眼动睡眠(REM)等不同脑状态下的血液动力学动态监测;该工具与脑脊液荧光示踪剂、去甲肾上腺素(NE)荧光探针(GRABNE2m)及脑电图/肌电图(EEG/EMG)记录相结合,揭示NE介导的缓慢血管运动与脑脊液流动的反相关关系,明确其在 NREM 睡眠期间驱动类淋巴系统清除代谢废物的核心作用。
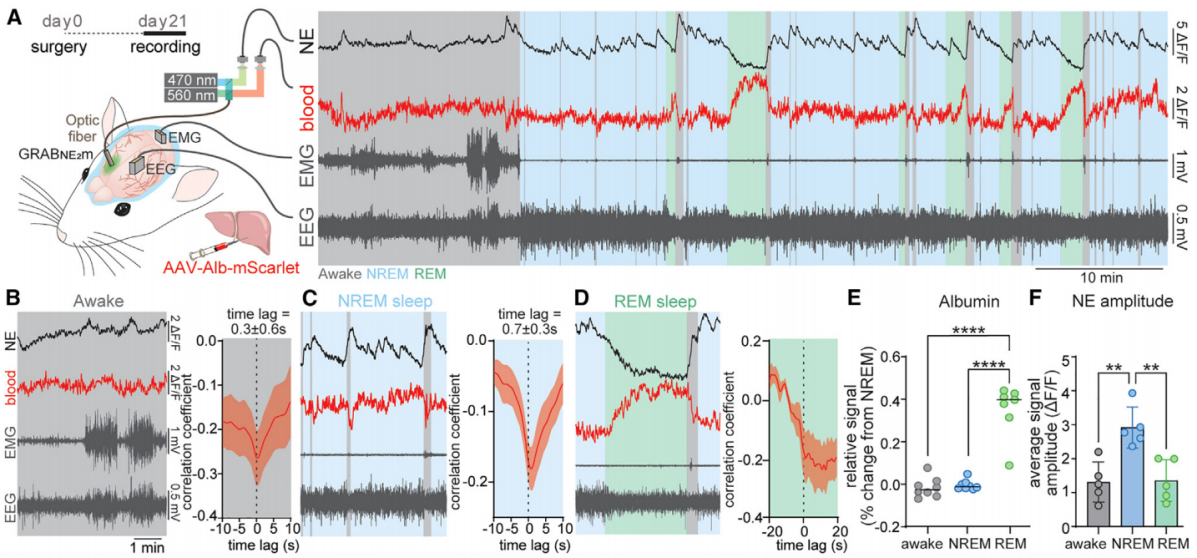
图5 NE介导状态依赖性血管舒缩