骨骼系统通过其支撑身体、保护内脏器官、参与运动和造血功能以及调节矿物质平衡等维持身体健康,但由于多种因素的相互作用,机体功能易出现退化,导致包括骨质疏松、骨不连、遗传性骨病等发生。腺相关病毒AAV是基因治疗领域最常用的基因递送载体,在骨骼系统中的应用常选择特定血清型AAV载体将治疗性基因如抗炎因子IL-1Ra、软骨保护因子PRG4等递送至关节软骨、骨髓间充质干细胞(AAV2、AAV6.2)或成骨细胞(AAV9)等,改善骨关节炎症,实现骨组织修复再生和骨代谢平衡等,为骨骼疾病的治疗提供新策略。
骨骼系统骨组织细胞包含有:骨祖细胞、成骨细胞、骨细胞、破骨细胞(吸旧骨),及关节软骨中维持软骨弹性与抗压性的软骨细胞。体外实验中,rAAV1,rAAV4,rAAV5,rAAV6,rAAV7,rAAV9,rAAVrh.10和rAAVrh.39可转导成骨细胞(COB);rAAV1,rAAV4,rAAV5,rAAV6,rAAV7和rAAV9可转导的破骨细胞前体(BM-OCP);rAAV1,rAAV6,rAAVrh.10和rAAVrh.39可转导软骨细胞祖细胞(ATDC5)。体内实验中,AAV9能够有效转导成骨细胞、破骨细胞和骨细胞。AAV2和AAV6.2在体内外实验中均可有效转导软骨细胞。
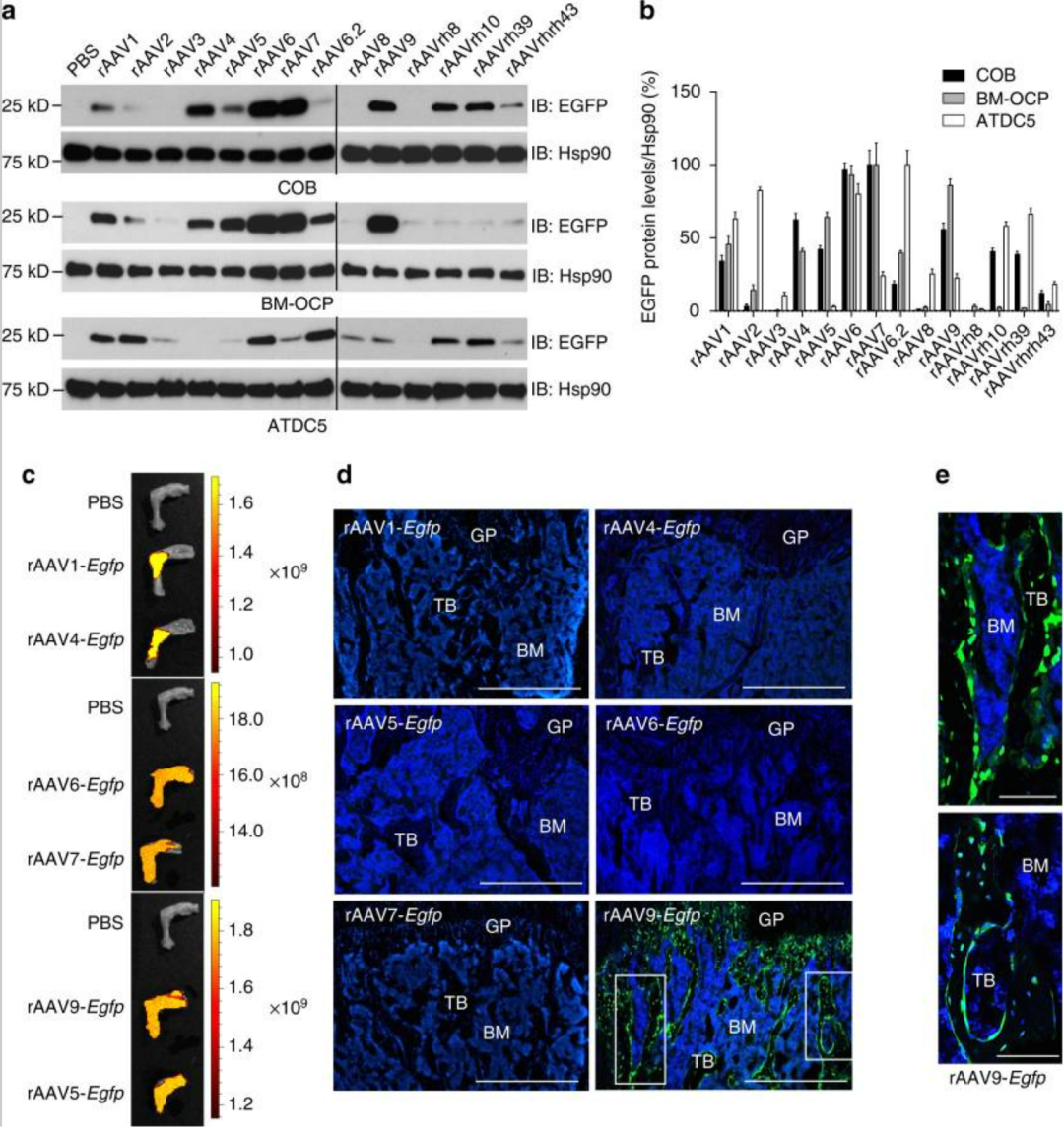
图1 鉴定在体外和体内不同血清型AAV对骨骼组织的转染效率[1]
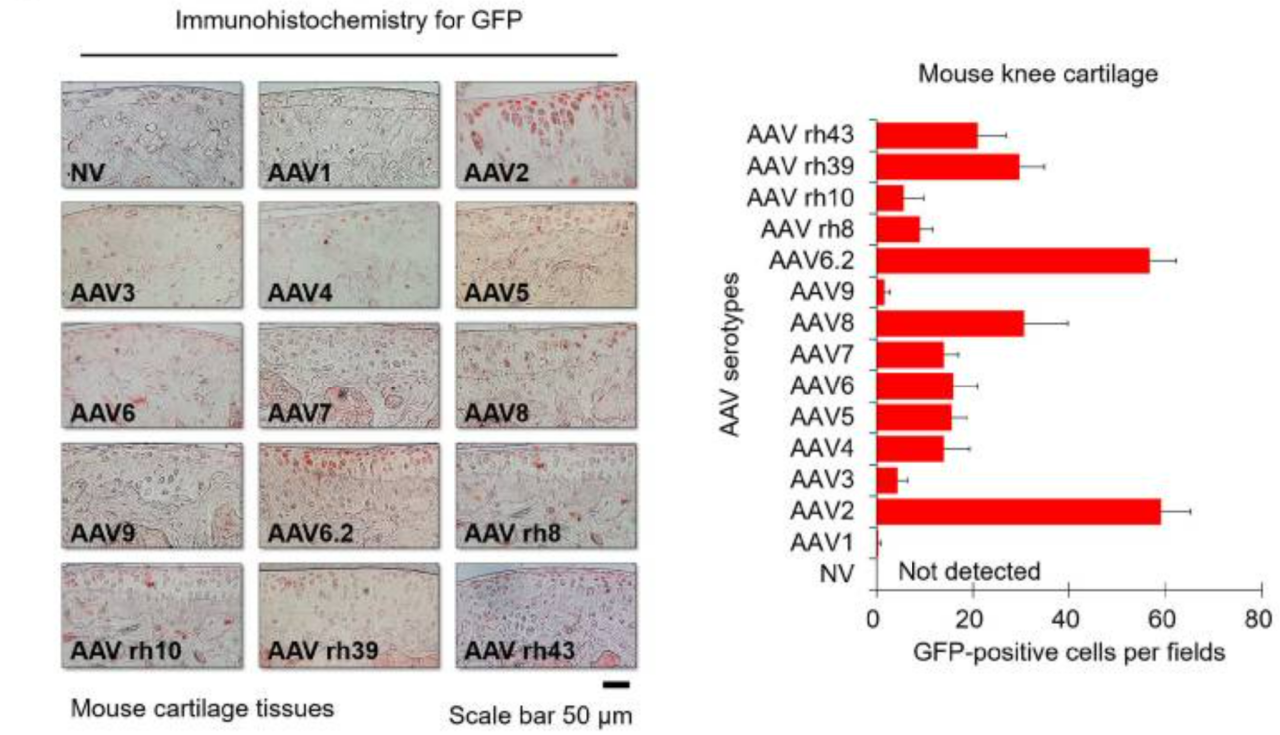
图2 不同血清型AAV体内对软骨细胞的转染效率[2]
感染骨骼系统常见的注射方式有尾静脉注射、骨关节腔注射、骨内注射等。
尾静脉注射是系统性给药,其操作简单、损伤性小,但特异性相对较差,病毒用量较大。
骨关节腔注射和针对骨髓的骨内注射特异性提高,感染效果较好但操作相对繁琐。
实例1:
TIPE2治疗患有膝关节OA(骨关节炎 )的Z24−/−小鼠[3]
血清型:AAV6
启动子:CMV
实验动物:加速衰老Z24−/−小鼠
注射方案:膝关节腔注射,2.5×10^12 vg/只,表达8周
实验结果:为实现向Z24−/−小鼠膝关节递送TIPE2,将rAAV-CMV-TIPE2-GFP注射到Z24−/−小鼠膝关节腔内,表达8周后,荧光显微镜下可见小鼠膝关节软骨组织有GFP 荧光,且GFP阳性细胞与HE染色共定位;对3只小鼠的统计显示,注射侧膝关节超89%软骨细胞呈GFP阳性,这表明该基因递送系统在小鼠膝关节软骨细胞中效率较高。
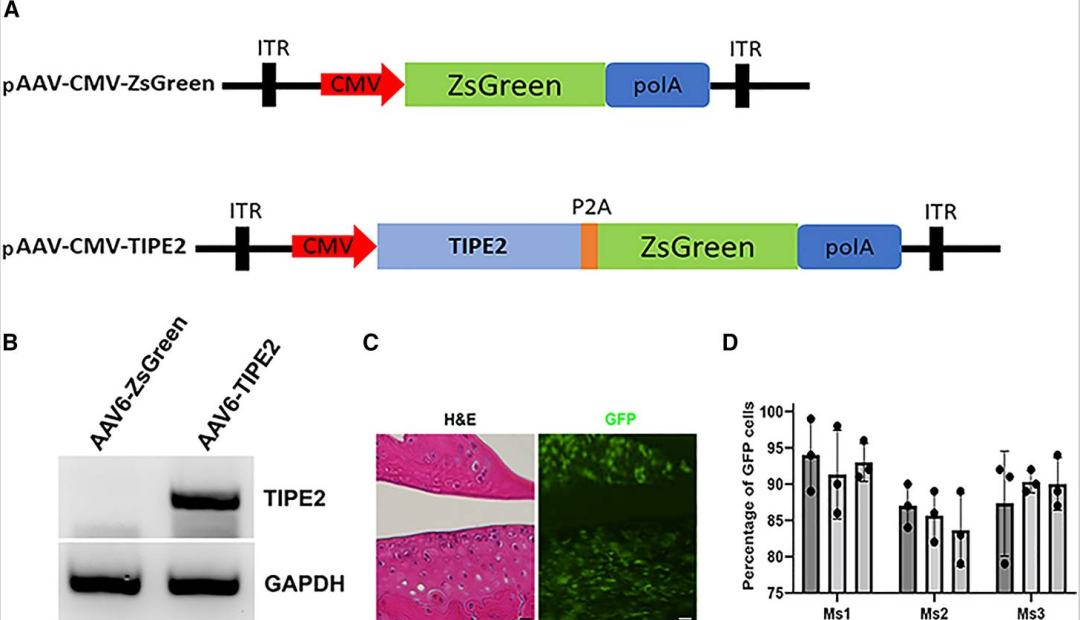
图3 AAV6-TIPE2载体成功递送至Z24−/−小鼠膝关节软骨
实例2:
AAV递送调控成骨/破骨细胞的miRNAs治骨质疏松[4]
血清型:AAV9
启动子:CBA
实验动物:C57BL/6J小鼠
注射方案:尾静脉注射,5×10^13 vg/只,表达8周
实验结果:给10周龄小鼠静脉注射单剂量携带对照、miR-214-3p或miR-34a-5p TuD的rAAV9;8周后,RT-PCR和microCT评估胫骨和血清中miR-214-3p和miR-34a-5p的表达水平和股骨骨量。荧光显微镜观察股骨骨骺区的EGFP阳性细胞提示其靶向骨内成骨细胞和破骨细胞。microCT发现miR-214-3p或miR-34a-5p TuD组比对照组股骨骨量低,小梁骨体积/组织体积(BV/TV)、小梁数量及厚度均显著降低。这表明rAAV9载体的全身递送在成骨细胞和破骨细胞谱系细胞中有效表达miR-214-3p和miR-34a-5p TuD,并导致体内骨质流失。
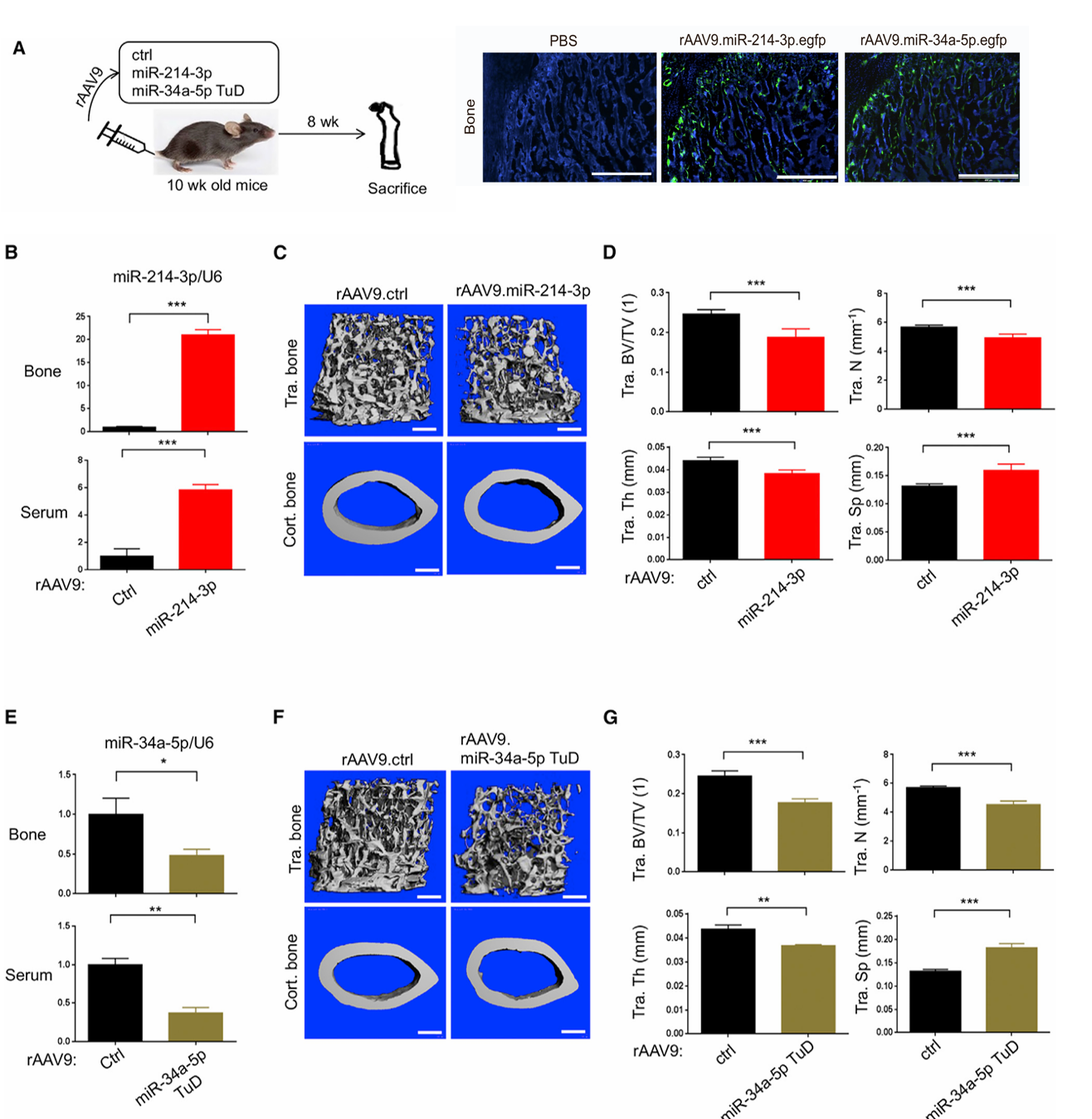
图4 rAAV9介导的miR-214-3p或miR-34a-5p TuD表达诱导小鼠骨质流失
实例3:
miR-378a过表达增加肥胖小鼠的骨量[5]
启动子:CMV
实验动物:肥胖小鼠
注射方案:髓内注射,1×10^11 vg/只,表达8周;
实验结果:肥胖小鼠髓内注射AAV-miR-378a-3p-EGFP实现骨组织过表达 miR-378a。注射8周后。显微CT分析发现,与对照组相比,miR-378a 治疗组小鼠显示出明显更大的小梁骨体积和骨小梁数。免疫组织化学染色发现给予miR-378a-3p治疗增加了肥胖小鼠骨小梁表面的成骨细胞数量,减少了骨髓中脂滴的数量和面积。这些结果表明miR-378a 治疗减轻了肥胖小鼠的骨退化。
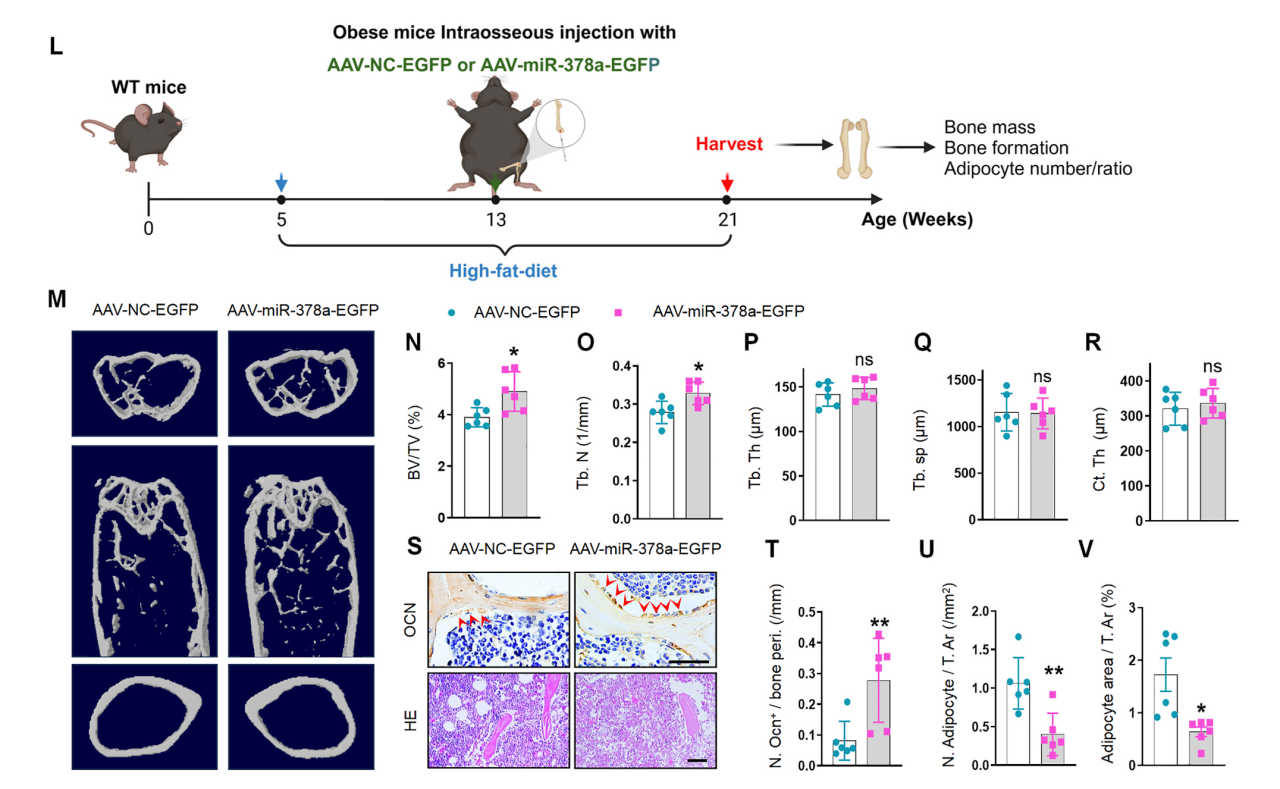
图5 miR-378a 过表达调节骨量和骨髓脂肪积累
参 | 考 | 文 | 献
1. Yang YS, Xie J, Wang D, et al. Bone-targeting AAV-mediated silencing of Schnurri-3 prevents bone loss in osteoporosis. Nat Commun. 2019;10(1):2958.
2. Yoon DS, Lee KM, Cho S, et al. Cellular and Tissue Selectivity of AAV Serotypes for Gene Delivery to Chondrocytes and Cartilage. Int J Med Sci. 2021;18(15):3353-3360.
3. Guo P, Gao X, Nelson AL, et al. TIPE2 gene transfer ameliorates aging-associated osteoarthritis in a progeria mouse model by reducing inflammation and cellular senescence. Mol Ther. 2024;32(9):3101-3113.
4. John AA, Xie J, Yang YS, et al. AAV-mediated delivery of osteoblast/ osteoclast -regulating miRNAs for osteoporosis therapy. Mol Ther Nucleic Acids. 2022;29: 296-311. Published 2022 Jul 11.
5. He C, Hu C, He WZ, et al. Macrophage-derived extracellular vesicles regulate skeletal stem/progenitor Cell lineage fate and bone deterioration in obesity. Bioact Mater. 2024;36:508-523. Published 2024 Jul 4.