葡萄糖是脑的主要能量底物,其代谢与神经活动、突触可塑性及认知功能密切相关;代谢紊乱与阿尔茨海默病、癫痫、2型糖尿病等疾病相关。但传统技术(酶传感器、微透析-质谱)时空分辨率低,无法满足细胞/亚细胞层面动态监测需求。

2025 年 11 月 12 日,发表于《Science Advances》上题为“iGlucoSnFR2: A genetically encoded fluorescent sensor for measuring intracellular or extracellular glucose in vivo in mouse brain”的文章,开发了第二代基因编码荧光葡萄糖探针iGlucoSnFR2,其通过将iGlucoSnFR1的环形排列增强型绿色荧光蛋白(cpeGFP)替换为环形排列超折叠绿色荧光蛋白(cpSFGFP)、优化小鼠密码子提高体内表达量等改造,具备更高的荧光变化幅度(∆F/F接近5)、更适配的葡萄糖结合亲和力(解离常数Kd约500 μM)及更优的亚细胞定位效率;该探针可靶向细胞质、细胞膜和内质网(ER),在细胞培养中能监测葡萄糖消耗、糖异生及ER葡萄糖外流,在小鼠体内通过光纤记录等技术,可实时检测脑内胞内/胞外葡萄糖动态,还能通过校准实现清醒小鼠脑内胞外葡萄糖绝对浓度测量,为哺乳动物葡萄糖代谢研究提供高时空分辨率工具。
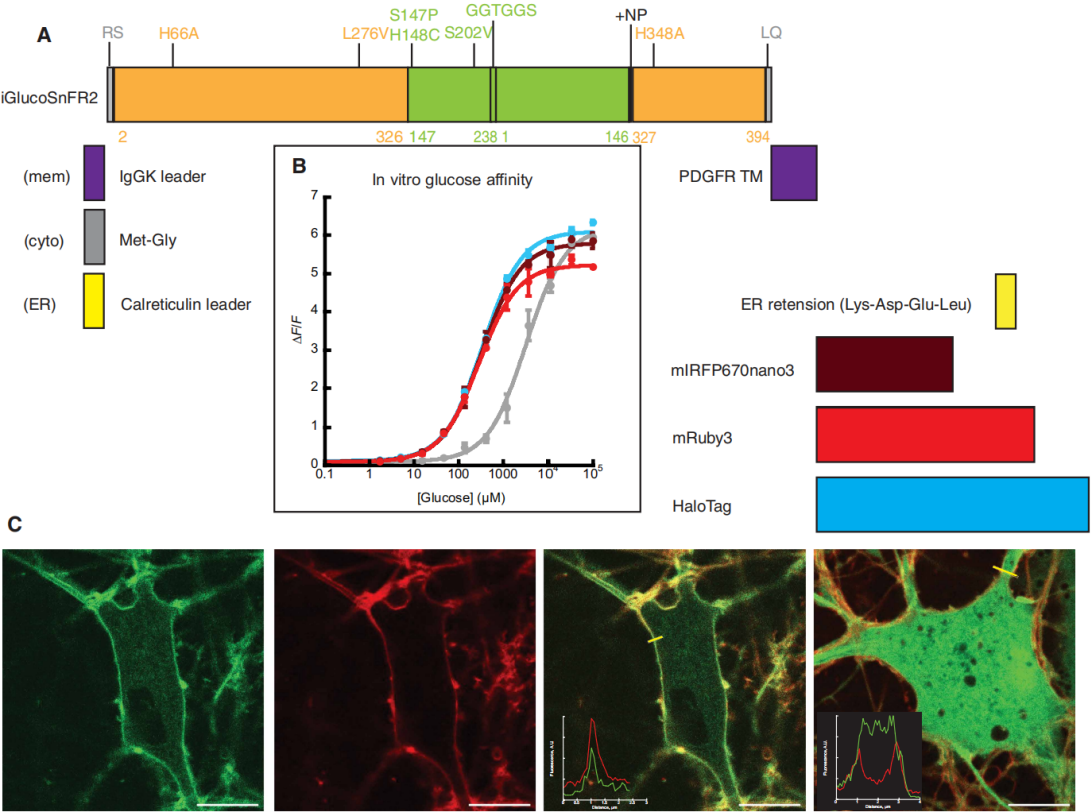
图1 iGlucoSnFR2的设计与初步表征
为了验证iGlucoSnFR2对细胞内葡萄糖浓度变化的监测能力,研究人员将细胞质靶向的该探针及对照(cpSFGFP-HaloTag)、iGlucoSnFR1-HaloTag质粒瞬时转染HeLa细胞(图2),通过将iGlucoSnFR2与信号稳定的标签(如mRuby3)融合,实现绿色探针信号相对于无响应红色/远红色信号的归一化(校正蛋白质表达量差异、成像焦点漂移等非分析物因素导致的荧光波动,确保信号变化仅反映分析物浓度变化),经JFX650孵育后用多孔成像仪观察,以含不同浓度葡萄糖的缓冲液平衡细胞后加入10 μM Glutor(抑制双向葡萄糖转运体GLUT-1/2/3)处理,结果显示iGlucoSnFR2因更高的∆F/F与亲和力,荧光下降幅度显著优于iGlucoSnFR1且在5 mM外部葡萄糖时饱和,该结果在HEK293、U2OS、COS-7细胞系中得到验证;同时构建的高亲和力变体iGlucoSnFR2.H348H(Kd≈3 μM)在葡萄糖耗尽后监测到细胞质葡萄糖缓慢回升(浓度3~500 μM),提示细胞内储存库的葡萄糖释放,灌流实验进一步验证了探针的快速响应与恢复能力;ER靶向的iGlucoSnFR2在1 mM外部葡萄糖时即饱和,表明ER葡萄糖浓度高于细胞质(图2C),Glutor处理后其浓度下降,提示葡萄糖可从ER流出。
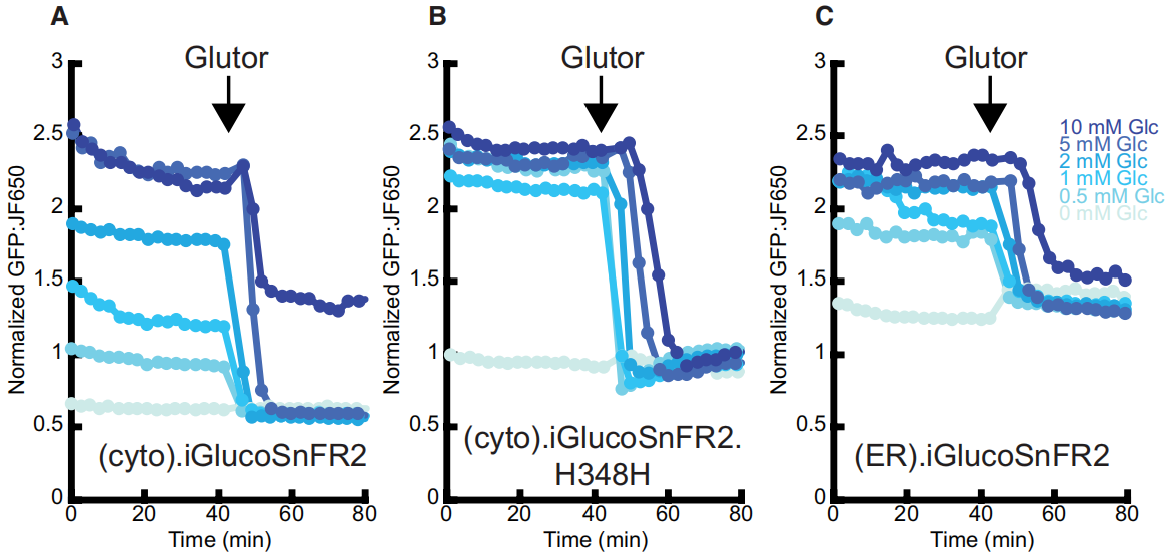
图2 iGlucoSnFR2报告了GLUT抑制对HeLa细胞内葡萄糖的影响
除了监测细胞质(及ER)葡萄糖耗竭外,iGlucoSnFR2可观察原代肝细胞(体内主要葡萄糖调节细胞)的糖异生(是指生物体利用丙酮酸、乳酸、甘油、生糖氨基酸等非糖物质,在肝脏(主要场所)和肾脏(次要场所)中合成葡萄糖或糖原的代谢途径)过程。将含肝脏特异性TBG启动子调控的cyto-iGlucoSnFR2-mIRFP670nano3的AAV8感染小鼠,提取肝脏后在多孔成像仪中观察肝细胞响应(图3)。肝细胞经2小时葡萄糖饥饿后,分别用“丙酮酸+乳酸(糖异生底物)”或“丙酮酸+胰高血糖素(直接刺激糖异生)”处理,均使iGlucoSnFR2荧光升高,且胰高血糖素效果更优。鉴于GLUT介导葡萄糖双向转运,探究BAY876(阻断GLUT-1)与Glutor(阻断GLUT-1/2/3)对胞质葡萄糖的影响,两种药物均提升胞质葡萄糖浓度,Glutor效果更显著(图3,红/橙色vs黄/绿色曲线);且仅在Glutor存在时,胰高血糖素可显著提高葡萄糖浓度(图5,红vs橙、黄vs绿曲线)。
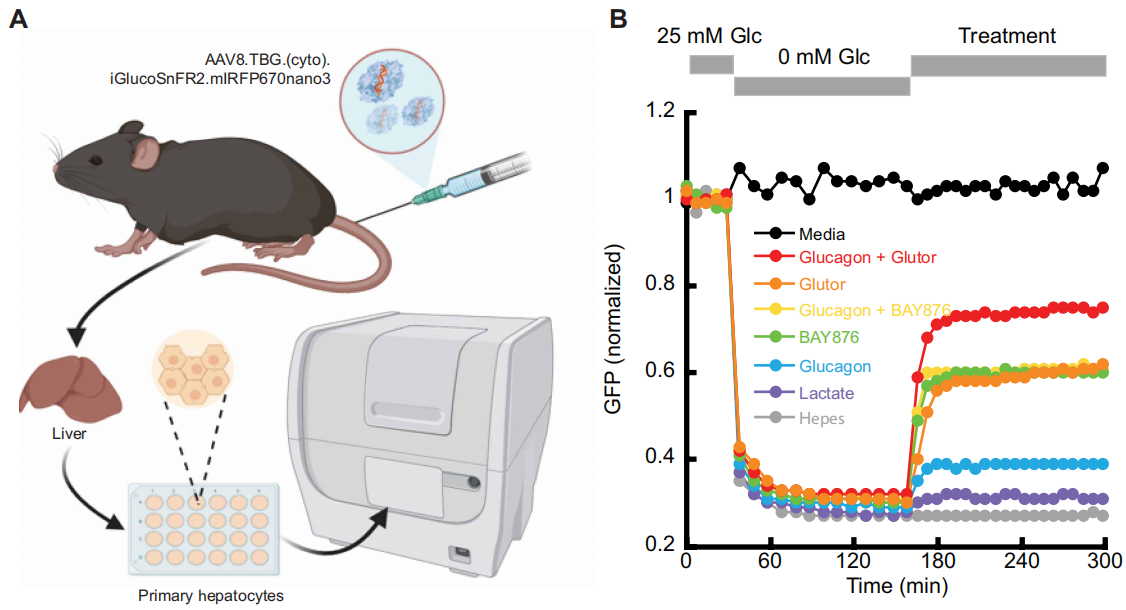
图3 iGlucoSnFR2可检测肝细胞在刺激性处理及葡萄糖转运抑制条件下的糖异生反应
此前研究显示,iGlucoSnFR1可报告果蝇脑外植体及斑马鱼胚胎的胞内葡萄糖变化,但在哺乳动物体内的实用性未被证实。基于iGlucoSnFR2在细胞培养中的优异性,研究在小鼠下丘脑腹内侧区(MBH,调控能量平衡与葡萄糖稳态的关键脑区)对比两者性能(图4A),向下丘脑腹内侧区注射编码cyto-iGlucoSnFR2-mRuby3或cyto-iGlucoSnFR1-mRuby2的AAV,2-4周后以光纤记录监测荧光。结果表明,iGlucoSnFR1对腹腔注射葡萄糖(图4B-D)、胰岛素(图4E-G)的响应幅度温和且信号嘈杂;而iGlucoSnFR2响应强烈且信号清晰,还能监测去甲肾上腺素处理后的胞内葡萄糖变化(去甲肾上腺素通过刺激肝糖生成等升高血糖)。综上所述,iGlucoSnFR2比iGlucoSnFR1更灵敏可靠,可用于观察哺乳动物活体脑内胞质葡萄糖动态。
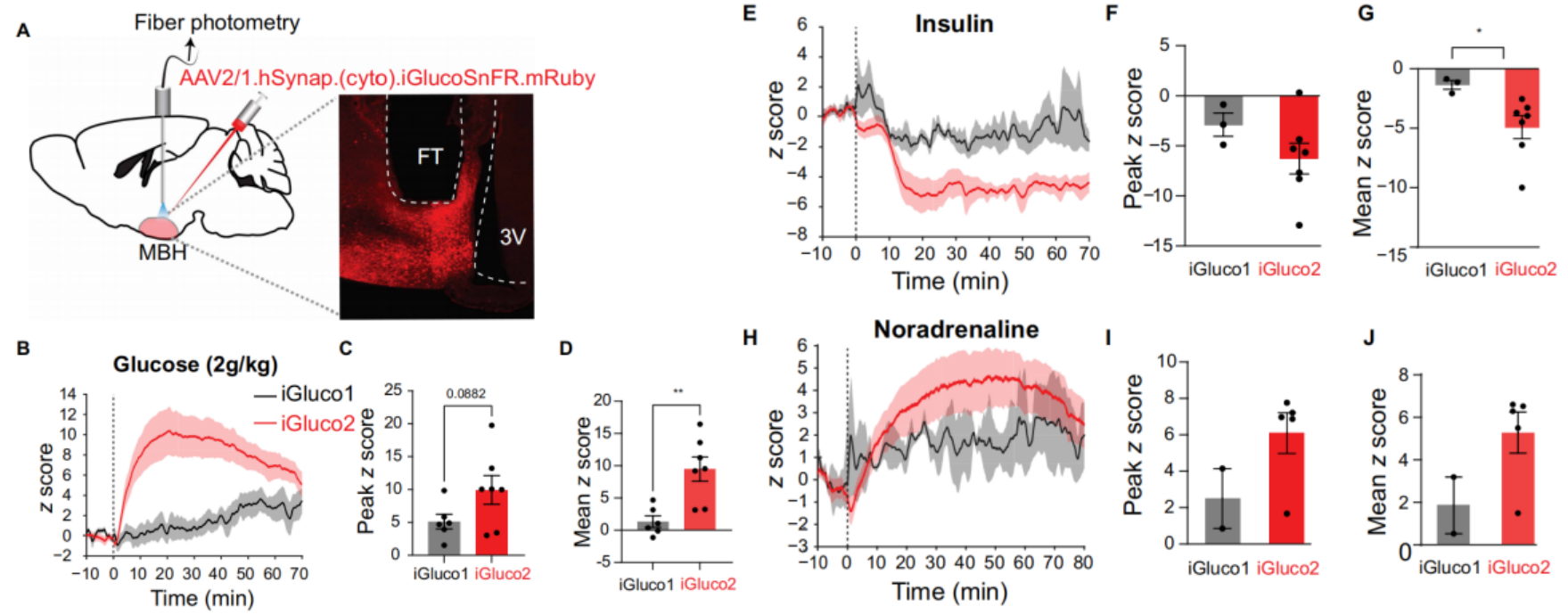
图4 比较cyto-iGlucoSnFR2与cyto-iGlucoSnFR1在检测体内神经元葡萄糖动态变化时的灵敏度
iGlucoSnFR1难以有效靶向哺乳动物细胞膜,而采用SFGFP及啮齿动物优化密码子的修饰,显著提升了mem-iGlucoSnFR2的膜定位效率(图1C),mem-iGlucoSnFR1则完全无法定位。神经元培养中,膜定位iGlucoSnFR2可即时响应胞外葡萄糖浓度变化,细胞质探针响应略慢。基于此,在小鼠背外侧纹状体神经元中表达mem-iGlucoSnFR2-mRuby3(图5A),免疫染色证实其定位于细胞膜(图5B),并通过光谱分辨光纤记录法进行体内检测,该技术可经光谱解混分析消除信号串扰与血红蛋白吸收干扰。自由活动小鼠实验中,探针对腹腔注射葡萄糖呈强烈荧光升高响应,对生理盐水无响应(图5C-G);注射多巴胺D1受体拮抗剂SCH23390后,神经元放电受抑制、葡萄糖利用减少,胞外葡萄糖积累被成功检测(图5E-G)。
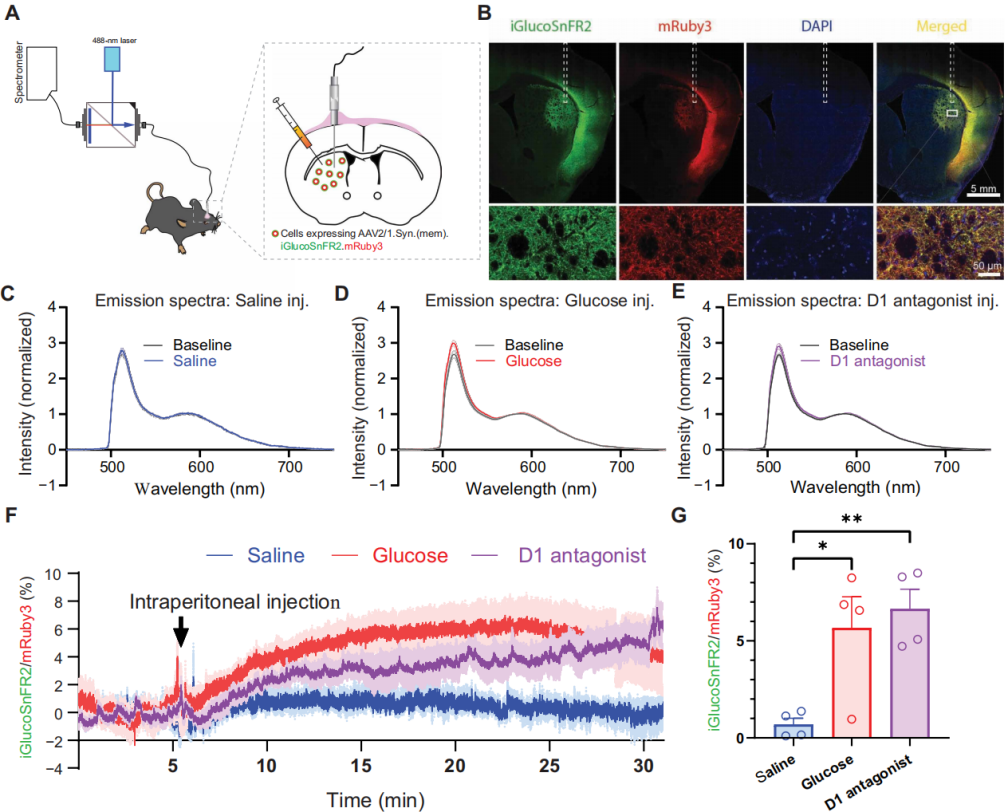
图5 自由活动小鼠纹状体细胞外葡萄糖动态变化
为了验证皮层内电刺激对胞外葡萄糖的影响,监测M1(向纹状体有谷氨酸能投射,图6A)电刺激后的纹状体动态,刺激引发胞外葡萄糖快速(~100ms内)瞬时升高,600 μA刺激响应显著强于300 μA且持续更久,自由活动动物中还观察到刺激后约1秒的二次升高(图6B-E)。这些结果证实,iGlucoSnFR2可通过神经血管耦合机制介导的刺激强度依赖性响应,监测脑内胞外葡萄糖动态,验证了其在活体实时代谢传感中的灵敏应用价值。
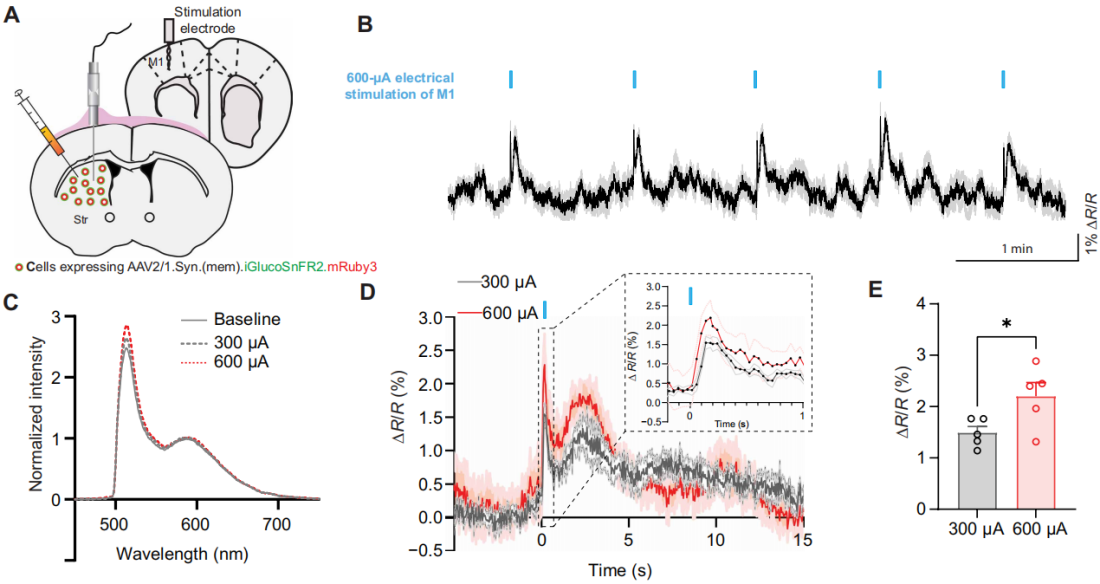
图6 皮层刺激对自由活动小鼠纹状体细胞外葡萄糖水平的影响
为了验证iGlucoSnFR2高分辨率成像能力,在小鼠桶状皮层星形胶质细胞和神经元表面(CAG启动子调控)表达该探针,采用双光子荧光+自适应光学技术(AO2P)校正像差,成像深度达480 μm(图7A)。静脉注射D-葡萄糖后iGlucoSnFR2-mRuby3荧光比值升高,胰岛素处理后降低,L-葡萄糖无响应(图7D);用葡聚糖偶联染料Cy5.5标记血管避开血红蛋白干扰,借助mRuby3发射光进行平移运动校正。
为了在体内校准膜靶向iGlucoSnFR2的荧光信号,小鼠过夜禁食后静脉注射胰岛素(2 IU/kg)降至低糖水平,再以递增剂量(0.25-4 mmol/kg)注射葡萄糖,同步用体外37℃预校准的电化学(EC)探针来测量sV1区胞外糖浓度(图7B),可直接测量D-葡萄糖的绝对浓度变化。结果显示,0.08~0.62 mM范围内,探针荧光与胞外葡萄糖浓度呈线性相关(图7C)。
对清醒小鼠初级体感皮层sV1皮层I层进行AO2P成像,以1 Hz时间分辨率、亚微米空间分辨率绘制胞外葡萄糖空间分布图(图7D),按1分钟荧光强度权重计算像素∆F/F0,绘制胰岛素(2 IU/kg)、L-葡萄糖(8 mmol/kg)、D-葡萄糖(8 mmol/kg)处理后的分布及无血管重叠区域的时间动态曲线;对微小血管放大成像获更高分辨率(图7E)。两种尺度下,静脉注射葡萄糖在胞外均匀分布,探针荧光峰值晚于血糖峰值,表明脑内葡萄糖摄取受血脑屏障(BBB)转运速率限制。
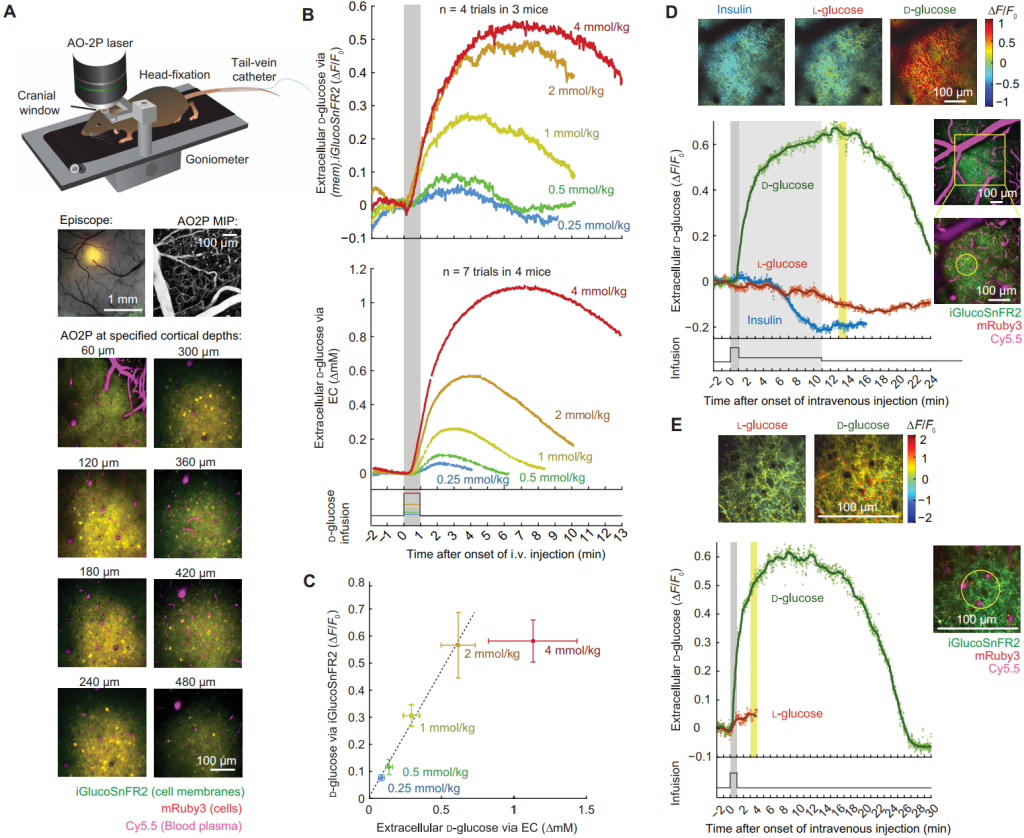
图7 利用电化学测定的葡萄糖浓度对胞外iGlucoSnFR2荧光进行体内校准
第二代葡萄糖探针iGlucoSnFR2能实现亚秒级时间分辨率(如电刺激响应)、亚微米空间分辨率(AO2P成像);可靶向细胞质、膜、ER,适配细胞培养与活体动物;结合EC探针可实现体内葡萄糖绝对浓度测量。荧光信号受探针表达量影响,需依赖mRuby3等归一化标签。可用于探索神经血管耦合机制、细胞间葡萄糖转运;可用于糖尿病、阿尔茨海默病等疾病模型的脑葡萄糖代谢异常定量评估,为药物研发提供精准的体内疗效评价指标。
布林凯斯可提供各类定制及病毒包装服务,请联系小布或者当地销售工程师,获取更多信息及咨询服务,联系电话(微信同号) 18971216876。