2025年9月24日,苏州大学马全红团队与大连医科大学李韶团队联合在《Science Advances》发表题为“Impaired macroautophagy in oligodendrocyte precursor cells suppresses neuronal plasticity via a senescence-associated signaling”的研究论文。该研究聚焦于既往被忽视的少突胶质前体细胞(OPCs),首次明确其自噬缺陷通过非髓鞘依赖机制加剧脑衰老相关的认知衰退。

在脑衰老过程中,认知能力下降涉及复杂的细胞与分子机制。传统研究多关注神经元、小胶质细胞等细胞类型的作用,而对OPCs这一重要细胞类型的非经典功能关注不足。OPCs作为中枢神经系统中的主要增殖细胞,不仅能分化为少突胶质细胞(OLs)形成髓鞘,保障神经信号快速传导;近年研究还发现其能通过分泌可溶性因子、与神经元形成突触连接等非髓鞘依赖方式调控脑网络功能。基于此,研究团队提出核心科学问题:老年小鼠OPCs的自噬功能下降,是否会通过非髓鞘依赖方式诱导细胞衰老,进而抑制神经元可塑性,最终加剧认知衰退?
为系统解析OPCs自噬缺陷的作用机制,研究人员通过自噬缺陷小鼠模型构建→细胞/分子水平验证→膜片钳电生理检测→行为学认知评估→干预实验验证的五步研究流程,层层递进解析其分子与细胞机制。
2.1 模型构建:
利用Cre-LoxP基因编辑技术,构建特异性敲除自噬关键基因Atg7的小鼠模型:cKONGC小鼠特异性敲除OPCs中的Atg7;cKONGCE小鼠通过他莫昔芬(TAM)诱导,仅在成年期敲除OPCs的Atg7;cKOPαCE小鼠排除PDGFRα阳性周细胞的干扰;cKOPLCE小鼠特异性敲除OLs的Atg7,用于区分OPCs与OLs自噬缺陷的功能差异。
2.2 细胞验证:
通过免疫荧光、Western blot、RNAscope 原位杂交等技术,在细胞与分子层面证实了OPCs自噬缺陷引发的一系列变化(图1)。
(1)自噬流随衰老下降:与3月龄年轻小鼠相比,26月龄老年小鼠海马和皮层OPCs中自噬受体P62荧光强度显著升高,表明老年OPCs自噬功能受损;
(2)OPCs形态早衰:Sholl分析显示,26月龄老年小鼠OPCs的分支数、突起长度显著增多,而12月龄cKONGCE小鼠的OPCs形态已呈现与老年对照一致的早衰样改变;
(3)OPCs衰老标志物升高:中年cKONGCE小鼠(12-16月龄)OPCs中衰老标志物P21、P16INK4A的阳性比例显著升高,且该现象具有细胞类型特异性;
(4)SASP因子CCL3/CCL5上调:RNAscope原位杂交发现,中年cKOPαCE小鼠的自噬缺陷OPCs中CCL3、CCL5的mRNA表达水平显著增多,提示二者是衰老OPCs SASP的关键组成部分。
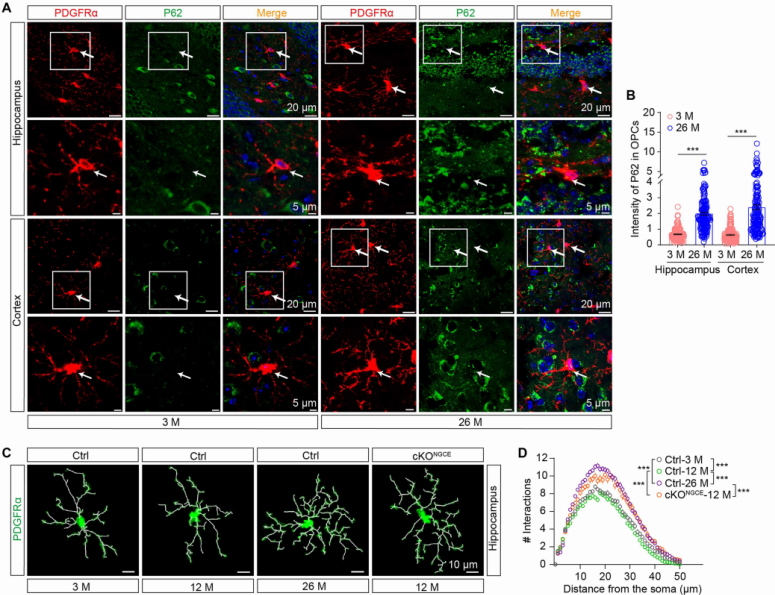
图1 OPCs自噬流随衰老变化及自噬缺陷诱导OPCs早衰样形态
2.3 电生理检测:
通过膜片钳技术记录海马CA1区神经元的电生理活动,量化谷氨酸能传递、神经元兴奋性及突触可塑性变化,明确OPCs自噬缺陷的功能影响。
2.4 认知评估:
通过新物体识别(检测短期记忆)、物体位置(检测空间记忆)、Morris水迷宫(检测空间学习与记忆)等行为学测试(图2),评估受损的OPC特异性自噬对认知的影响,结果发现成年OPCs自噬的失活加剧了与衰老相关的认知能力下降。
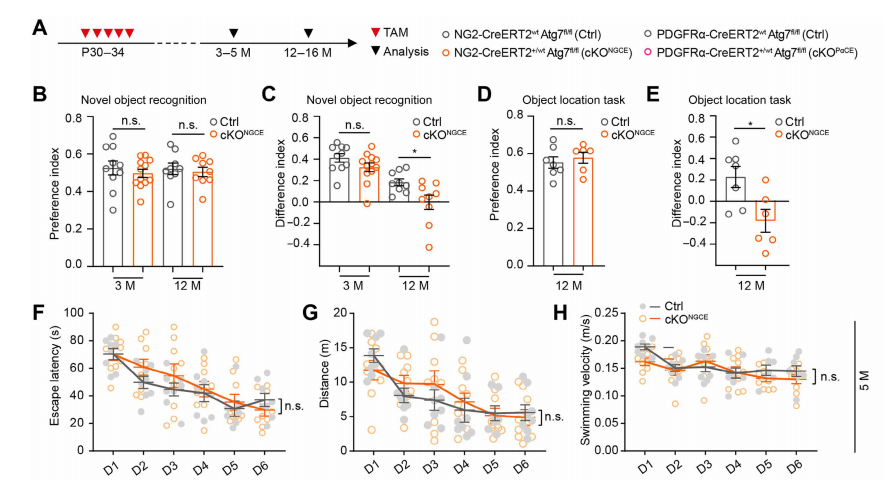
图2 OPCs自噬缺陷小鼠与对照小鼠认知行为学测试
2.5 干预验证:
研究人员通过3种干预手段,验证验证OPCs自噬缺陷→CCL3/CCL5-CCR5→认知衰退的特异性。使用达沙替尼+槲皮素清除衰老细胞、抗CCL3抗体+抗CCL5抗体中和SASP因子、CCR5抑制剂马拉维若(MVC)阻断下游受体。三种干预均能逆转电生理异常与认知缺陷,证明OPCs自噬缺陷通过CCL3/CCL5-CCR5通路导致认知衰退。
膜片钳技术是本研究的核心实验方法,其优势在于能高分辨率记录单个神经元或突触的电生理活动,将OPCs自噬缺陷这一细胞层面的变化,转化为可量化的神经元功能异常。
3.1 膜片钳实验准备
脑切片制备:小鼠经异氟烷深度麻醉后,快速取脑并置于冰浴的人工脑脊液(ACSF)中,用振动切片机切成300μm厚的冠状切片。ACSF持续通入95% O₂+5% CO₂混合气体,维持pH 7.4-7.45、渗透压305-315 mosmol。切片在ACSF中室温平衡至少1小时,待神经元恢复活性后,转移至记录槽,持续灌流 ACSF,保持稳定的记录环境。
电极与模式:研究根据不同电生理指标,研究采用两种核心记录模式。电压钳模式用于记录突触后电流(如sEPSCs、sIPSCs、mEPSCs),需固定细胞膜电位,电极内液含CsCl(阻断钾电流,减少干扰),电阻控制在 2-5 MΩ;电流钳模式用于记录动作电位(sAPs、eAPs),不固定细胞膜点位,电极内液含 KCl(模拟细胞内钾离子环境),直接记录神经元的膜电位变化与放电情况。
3.2 核心记录指标
为全面评估OPCs自噬缺陷对神经元功能的影响,研究人员选择了5类关键电生理指标,分别对应突触传递效率(sEPSCs、sIPSCs、mEPSCs)、神经元兴奋性(sAPs、eAPs)、突触可塑性(LTP)三个维度,完整评估OPCs自噬缺陷的影响。
(1)谷氨酸能和GABA能突触传递:区分兴奋性与抑制性传递
在电压钳模式下,将海马CA1锥体细胞分别钳制在- 80mV(记录sEPSCs,兴奋性电流)和10mV(记录sIPSCs,抑制性电流),连续记录5-10分钟,自动检测电流事件。结果显示,与对照小鼠(Ctrl)相比,中年cKONGC小鼠的sEPSC频率显著降低,但振幅无变化(图3B-D)。而sIPSC的频率和幅度在两组间无显著差异(图3E-G)。这些结果表明OPCs中自噬缺陷选择性损害谷氨酸能传递,不影响抑制性传递。
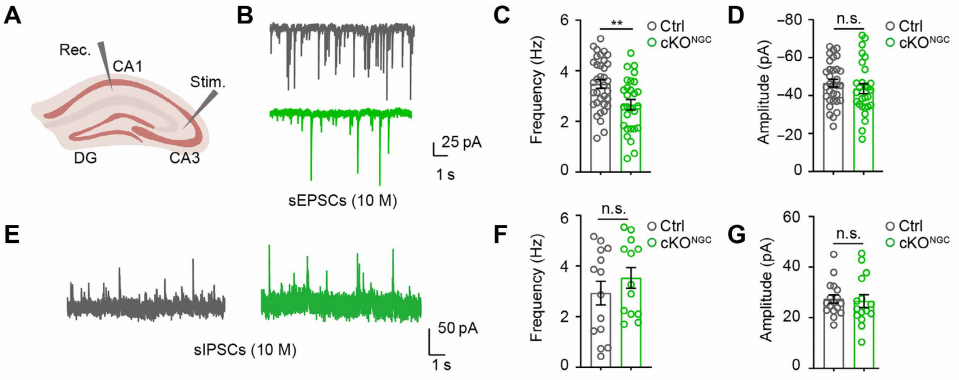
图3 OPCs自噬缺陷影响海马CA1神经元突触传递
(2)微小兴奋性突触后电流(mEPSCs):锁定突触前机制
在ACSF中加入1μM河豚毒素(TTX)孵育至少5分钟,阻断钠离子通道,抑制动作电位产生(仅保留突触前随机释放的神经递质引发的电流),记录mEPSCs。结果发现,与Ctrl小鼠相比,中年cKONGCE小鼠的mEPSC频率显著降低,振幅无变化(图4N-S),表明谷氨酸能传递受损源于突触前神经递质释放概率降低,而非突触后受体功能异常。
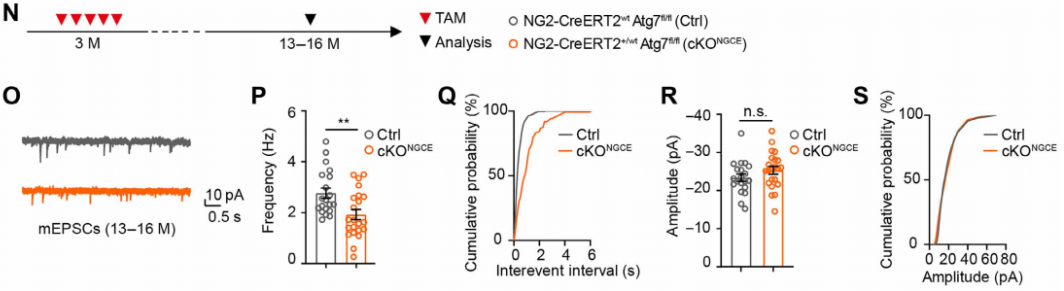
图4 OPCs自噬缺陷影响海马CA1神经元突触前传递
(3)自发性与诱发性动作电位(sAPs、eAPs):评估神经元兴奋性
在电流钳模式下,无外界刺激时记录神经元自主放电情况(sAPs),反应神经元基础兴奋性;给予20-200pA、步长20pA的200ms电流脉冲,记录神经元被诱导产生的动作电位(eAPs),反映神经元响应刺激的能力。结果显示,与Ctrl小鼠相比,中年cKONGC小鼠的sAP频率降低,振幅无变化(图5H-J),说明神经元自主放电能力减弱;而eAP的数量、振幅在两组间无差异(图5K-M),表明神经元本身的刺激响应能力正常,兴奋性降低源于突触前信号输入不足。
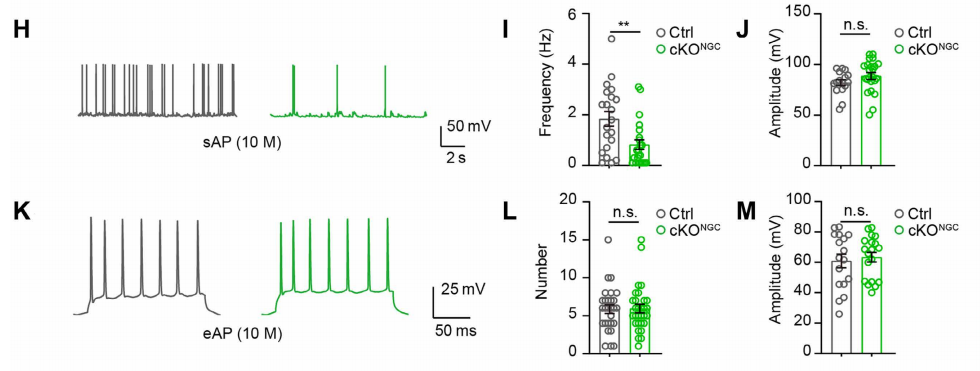
图5 OPCs自噬缺陷影响海马CA1神经元动作电位
(4)长时程增强(LTP):认知功能的“细胞层面指标”
刺激电极置于CA3区Schaffer侧支(突触前纤维),记录电极置于CA1区辐射层(突触后区域),以0.033Hz频率记录基线场兴奋性突触后电位(fEPSP),用4组100Hz、持续1秒、间隔20秒的高频刺激(HFS)诱导LTP,记录60分钟内 fEPSP 斜率和振幅变化。结果显示,中年cKONGCE小鼠在高频刺激后,fEPSP斜率峰值较对照降低,且60分钟后仍未恢复(图6T-V),表明突触可塑性长期受损。
同时通过输入-输出(I/O)曲线(刺激强度 0.05-1.0mA)评估突触效能,通过配对脉冲比率(PPR)(刺激间隔150ms,测第二个EPSP与第一个EPSP的斜率比)评估突触前Ca2+释放概率。结果显示,在150ms刺激间隔下,中年cKONGCE小鼠的PPR显著降低(图6W-Y),表明OPCs自噬缺陷通过降低突触前Ca2+释放,抑制 LTP。
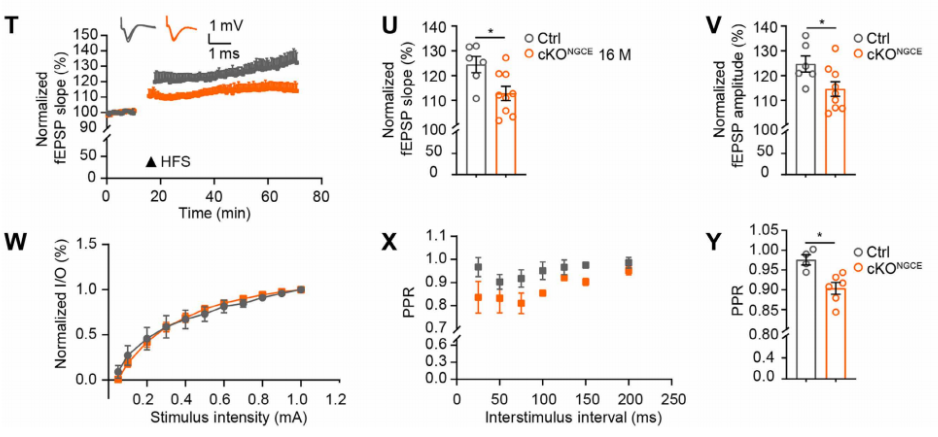
图6 OPCs自噬缺陷影响海马CA1神经元LTP
(5)机制验证:阻断CCL3/CCL5-CCR5可逆转电生理异常
在电生理记录前,对中年cKOPαCE小鼠急性分离的脑切片使用抗CCL3/CCL5抗体孵育20分钟,记录sEPSC、sAP、LTP等电生理表型。结果显示,sEPSC频率升高(图7I-K)、sAP频率升高(图5L-N)、LTP峰值升高(图7O-Q),电生理缺陷被完全逆转。
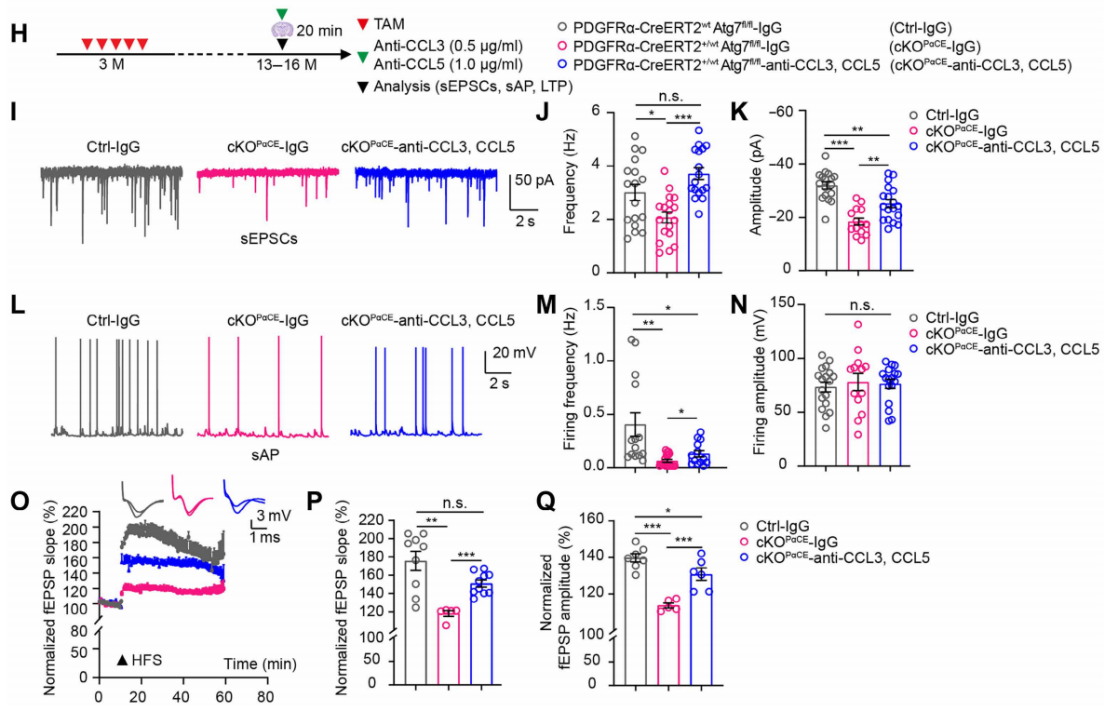
图7 抗CCL3/CCL5抗体逆转cKOPαCE小鼠海马神经元电生理异常
同样,使用CCR5拮抗剂马拉韦罗(MVC,15nM)孵育20分钟,记录sEPSCs、sAP、LTP等电生理表型。结果显示,MVC处理可逆转谷氨酸能传递受损(图8F-H),神经元兴奋性降低(图6I-K)、LTP抑制等现象(图8L-N),表明自噬缺陷OPCs引起的神经元可塑性抑制确实归因于CCR5信号通路的激活。
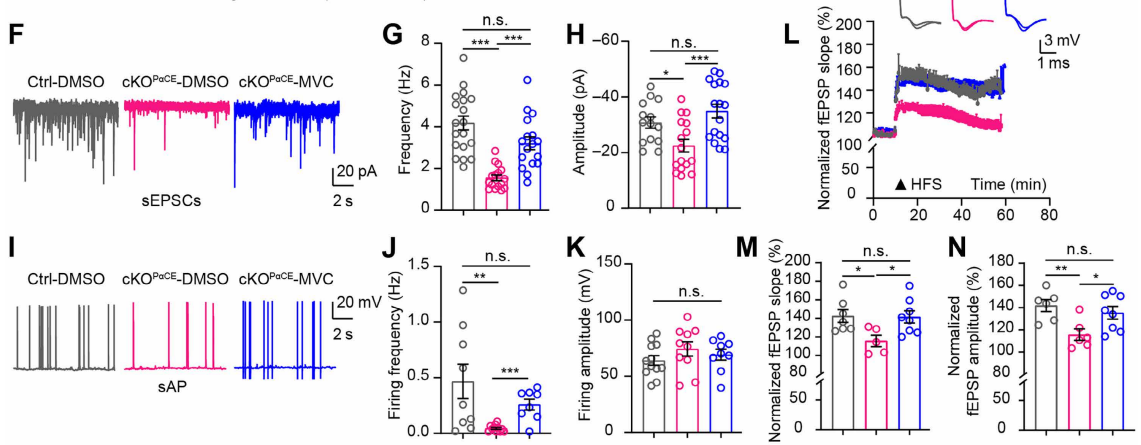
图8 CCR5抑制剂马拉维若逆转cKOPαCE小鼠海马神经元电生理异常
综合所有实验结果,本研究最终揭示了OPCs自噬缺陷加剧脑衰老认知衰退的完整机制:老年小鼠OPCs自噬流下降→OPCs无法清除衰老相关垃圾,引发细胞衰老→衰老OPCs分泌SASP因子CCL3/CCL5→CCL3/CCL5结合谷氨酸能神经元上的CCR5受体→抑制突触前Ca2+释放→谷氨酸能传递受损、神经元兴奋性降低、LTP 抑制→神经元可塑性下降→最终导致认知衰退,且这一过程完全独立于OPCs的髓鞘形成功能(图9)。
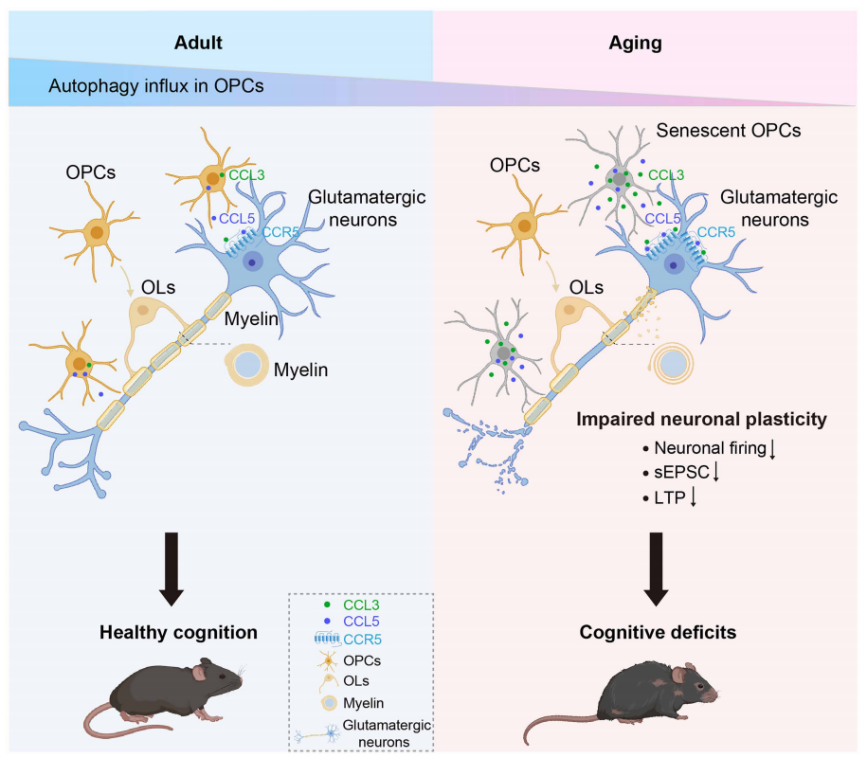
图9 OPCs自噬缺陷加剧脑衰老认知衰退的机制示意图
布林凯斯(Brain Case)可专业承接本研究涉及的各类电生理检测服务,同时提供脑切片制备、实验方案优化及数据量化分析的全流程支持,能精准匹配不同研究实验需求。若您想了解更多服务细节或定制专属实验方案,欢迎电话咨询 189 7121 6876,获取针对性技术支持!
参考文献
Chen H, Sun YY, Li QF, et al. Impaired macroautophagy in oligodendrocyte precursor cells suppresses neuronal plasticity via a senescence-associated signaling. Sci Adv. 2025 Sep 26;11(39):eadq7665. doi: 10.1126/sciadv.adq7665. Epub 2025 Sep 24. PMID: 40991686; PMCID: PMC12459396.