L-乳酸不再是代谢废物,而是参与神经(如ANLS假说)、肿瘤微环境、免疫调节的关键能量来源和信号分子,其跨细胞/亚细胞动态研究需求迫切。2021年开发的初代胞外探针eLACCO1.1存在膜定位聚集、荧光响应弱(ΔF/F=4)问题;现有胞内探针均为绿色荧光,无法与绿色工具(如GCaMP)协同使用,且响应强度有限。

2023年发表于《Nature Communications》的研究文章“Lactate biosensors for spectrally and spatially multiplexed fluorescence imaging”,开发了一对光谱和功能正交的基因编码L-乳酸荧光生物探针(图1):绿色荧光细胞外探针eLACCO2.1(第二代升级产品)与红色荧光细胞内探针R-iLACCO1(首款红色胞内探针)。eLACCO2.1基于TTHA0766蛋白,经定向进化优化后ΔF/F达14(是初代eLACCO1.1的3.5倍),通过HA引导序列+NGR GPI锚定实现高效膜定位,Kd=1.9mM适配胞外生理浓度,可检测脑切片及活体小鼠胞外L-乳酸动态;R-iLACCO1基于LldR蛋白,插入cpmApple,ΔF/F达20(为现有胞内探针最高),且开发了R-iLACCO1.1/1.2亲和力变体(Kd分别为3.0mM/4.0mM),无Ca²⁺依赖。二者可协同实现培养细胞(如HeLa、神经元)、脑切片及活体小鼠中胞外-胞内L-乳酸的光谱/空间多通道成像,还首次观测到L-乳酸在线粒体和内质网间的穿梭,为代谢研究提供新工具。
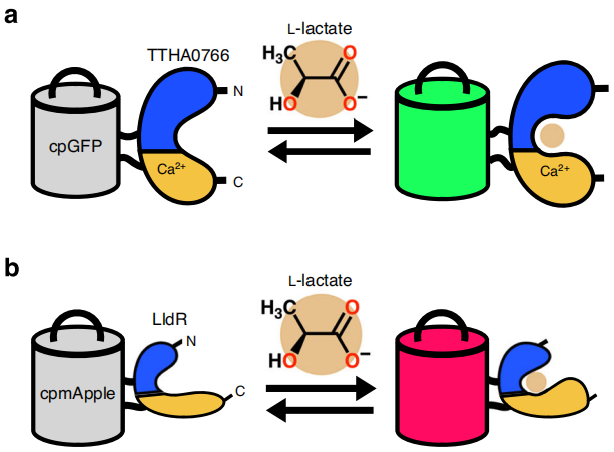
图1 eLACCO和R-iLACCO示意图及其对L-乳酸的响应机制
在哺乳动物细胞中表达HA-eLACCO2.1-NGR,其膜定位良好(图2a),而CD59-eLACCO1.1-CD59会形成荧光斑点。向表达eLACCO2.1的HeLa细胞加10mM L-乳酸,荧光强度显著升高,ΔF/F=8.8±0.2(图2b、c),为eLACCO1.1(ΔF/F=6.4±0.2)的138%(图3c)。对照探针deLACCO1膜定位正常且对L-乳酸无响应(图2a-d),eLACCO2.1对L-乳酸的原位表观Kd=580μM(图2d)。eLACCO2.1荧光依赖Ca²⁺,表观Kd=270μM,远低于脑组织(1.5-1.7mM)和血清(0.9-1.3mM)的胞外Ca²⁺浓度(图2e)。动力学测试显示,其快于eLACCO1.1(图2f)。无L-乳酸时,eLACCO2.1光稳定性与EGFP相当,高于eLACCO1.1;有L-乳酸时,其光稳定性低于eLACCO1.1(图2g)。deLACCO1光稳定性始终低于EGFP。
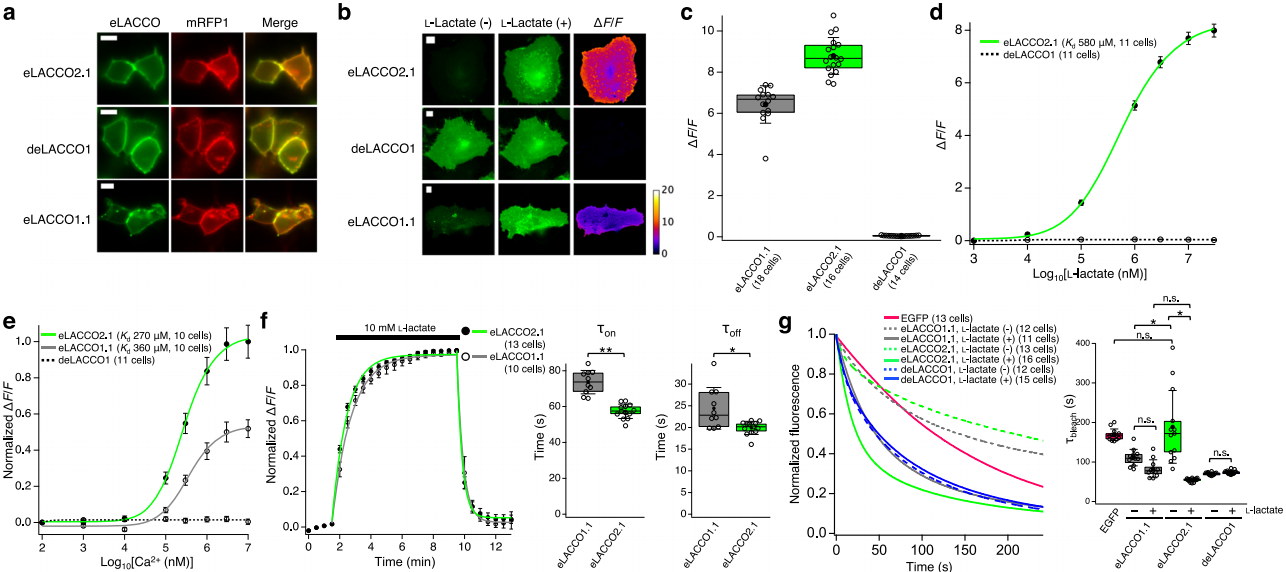
图2 eLACCO2.1在HeLa细胞的表征
为了表征eLACCO2.1在神经元表面的性能,在hSyn启动子调控下,HA-eLACCO2.1-NGR在大鼠原代皮质/海马神经元中呈明亮膜定位荧光,而CD59-eLACCO1.1-CD59有荧光斑点(图3h)。加10mM L-乳酸后,eLACCO2.1的ΔF/F=8.1±0.7,为eLACCO1.1(ΔF/F=1.5±0.2)的5.4倍(图3i-j)。
为了验证eLACCO2.1是否可用于检测星形胶质细胞表面的L-乳酸浓度变化,在gfaABC1D启动子调控下,eLACCO2.1在大鼠原代皮质/海马星形胶质细胞中表达良好(图3h),加10mM L-乳酸后ΔF/F=7.3±1.0(图3i、k),优于eLACCO1.1(ΔF/F=4.9±0.5),deLACCO1无响应。综上,优化引导序列和锚定域的eLACCO2.1性能优于eLACCO1.1,可成像神经元、星形胶质细胞表面胞外L-乳酸动态。
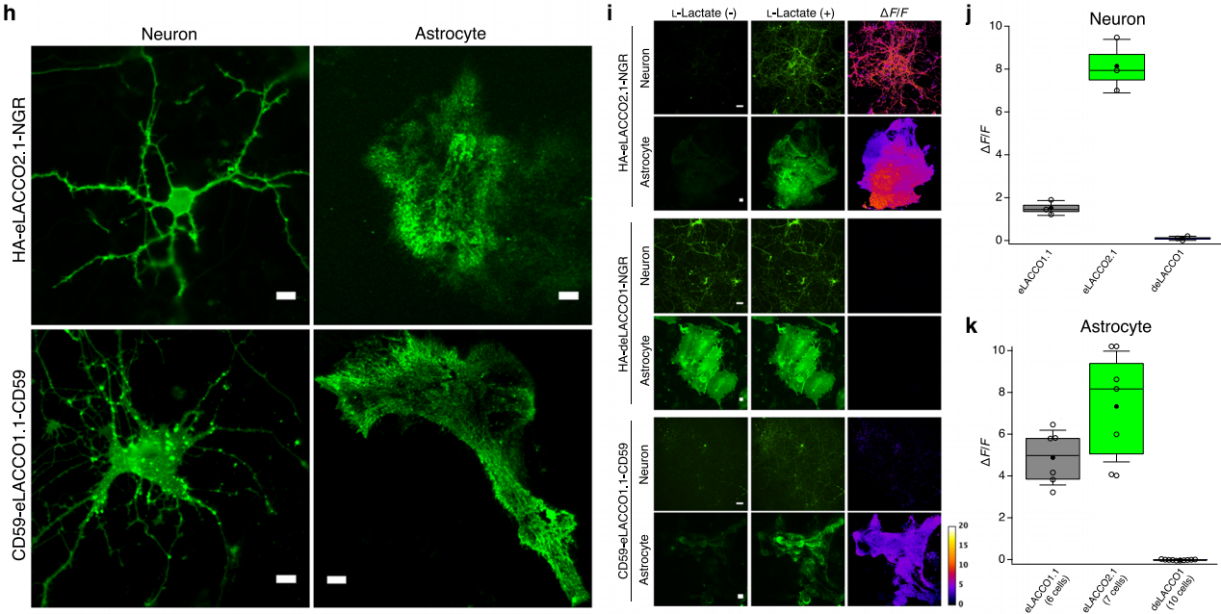
图3 eLACCO2.1在神经元和星形胶质细胞的表征
为了确定eLACCO2.1是否可用于检测完整组织中内源性L-乳酸浓度的变化,将AAV(hSyn启动子调控HA-eLACCO2.1-NGR)转染小鼠新皮质(图4l),脑切片离体实验中:无糖刺激使eLACCO2.1荧光降低(图4m),与胞外L-乳酸摄取一致;theta爆发刺激(一种特定模式的电刺激)使荧光显著升高,15分钟未消退(图4n),与高频刺激升高胞外L-乳酸的报道一致。综上,eLACCO2.1可检测完整组织中胞外内源性L-乳酸变化。
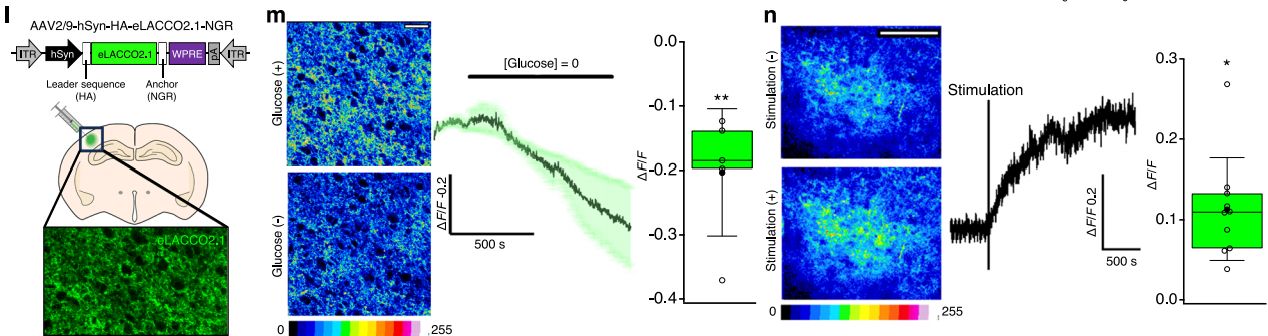
图4 eLACCO2.1在急性脑切片中的表征
为了验证R-iLACCO系列变体对哺乳动物细胞内源性L-乳酸动态的监测能力,在多种细胞及刺激条件下进行活细胞成像,并与已知L-乳酸探针对比(图5g-j):在葡萄糖饥饿细胞经葡萄糖处理后,糖酵解增强使胞内L-乳酸升高,R-iLACCO系列荧光均升高(图5g),其中低亲和力R-iLACCO1.2响应最强,远超其他探针;单羧酸转运体(MCT)抑制剂可抑制细胞内L-乳酸的外流,从而导致细胞内L-乳酸浓度升高。向HeLa细胞施加MCT抑制剂AR-C155858后,R-iLACCO1/1.1/1.2的ΔF/F分别为0.08±0.01、0.19±0.03、0.30±0.02(图5h),R-iLACCO1.2响应仅次于iLACCO1;原代神经元与星形胶质细胞加AR-C155858后,R-iLACCO系列荧光均显著升高(图5i、j)。虽胞内L-乳酸升高常伴随pH下降(可能降低荧光蛋白探针信号),但所有条件下R-iLACCO系列均呈显著荧光升高(图5)。综上,R-iLACCO系列变体在监测哺乳动物细胞内L-乳酸动态中具显著优势与应用价值。
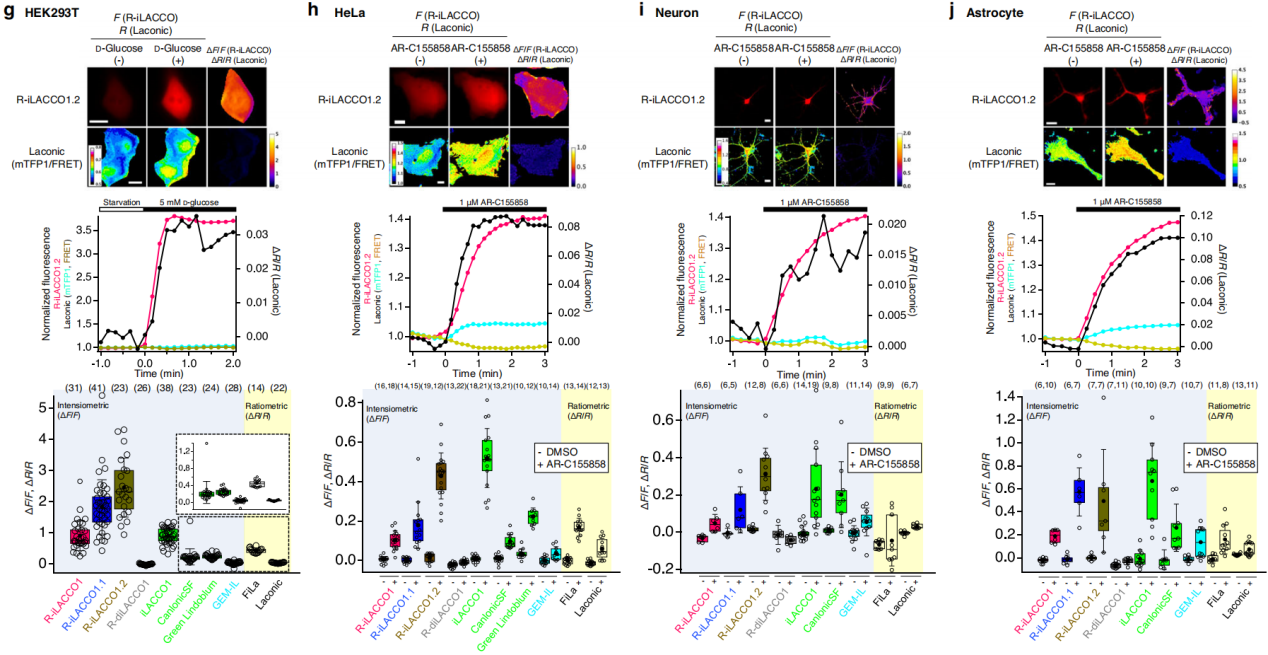
图5 哺乳动物细胞中R-iLACCO变异体的表征
为了验证eLACCO2.1体内性能,检测清醒小鼠视觉皮层神经元中eLACCO2.1在侧脑室(i.c.v.)注射L-乳酸后的荧光响应(图6a)。结果显示,与生理盐水相比,L-乳酸组eLACCO2.1荧光响应显著(图6b),对照deLACCO1荧光几乎无变化(图6c),表明eLACCO2.1是体内功能性胞外L-乳酸探针。
为了探究eLACCO2.1对自由活动小鼠内源性L-乳酸的检测能力(已知胰岛素注射会降低小鼠脑内胞外L-乳酸),在小鼠海马神经元中表达eLACCO2.1,记录腹腔(i.p.)注射胰岛素后的荧光响应(图6d)。结果显示,与生理盐水相比,胰岛素组eLACCO2.1荧光显著降低,deLACCO1无明显变化(图6e),表明其可检测自由活动小鼠内源性L-乳酸动态。
为了验证R-iLACCO1.1体内监测胞内L-乳酸的能力(已知刺激小鼠胡须会升高躯体感觉皮层神经元胞内L-乳酸),在小鼠躯体感觉皮层神经元中表达R-iLACCO1.1,观察胡须刺激后的荧光响应(图6f-g)。浅麻醉小鼠成像显示,R-iLACCO1.1呈刺激依赖性荧光增强(图6h-i),表明其可监测活体小鼠内源性L-乳酸动态。
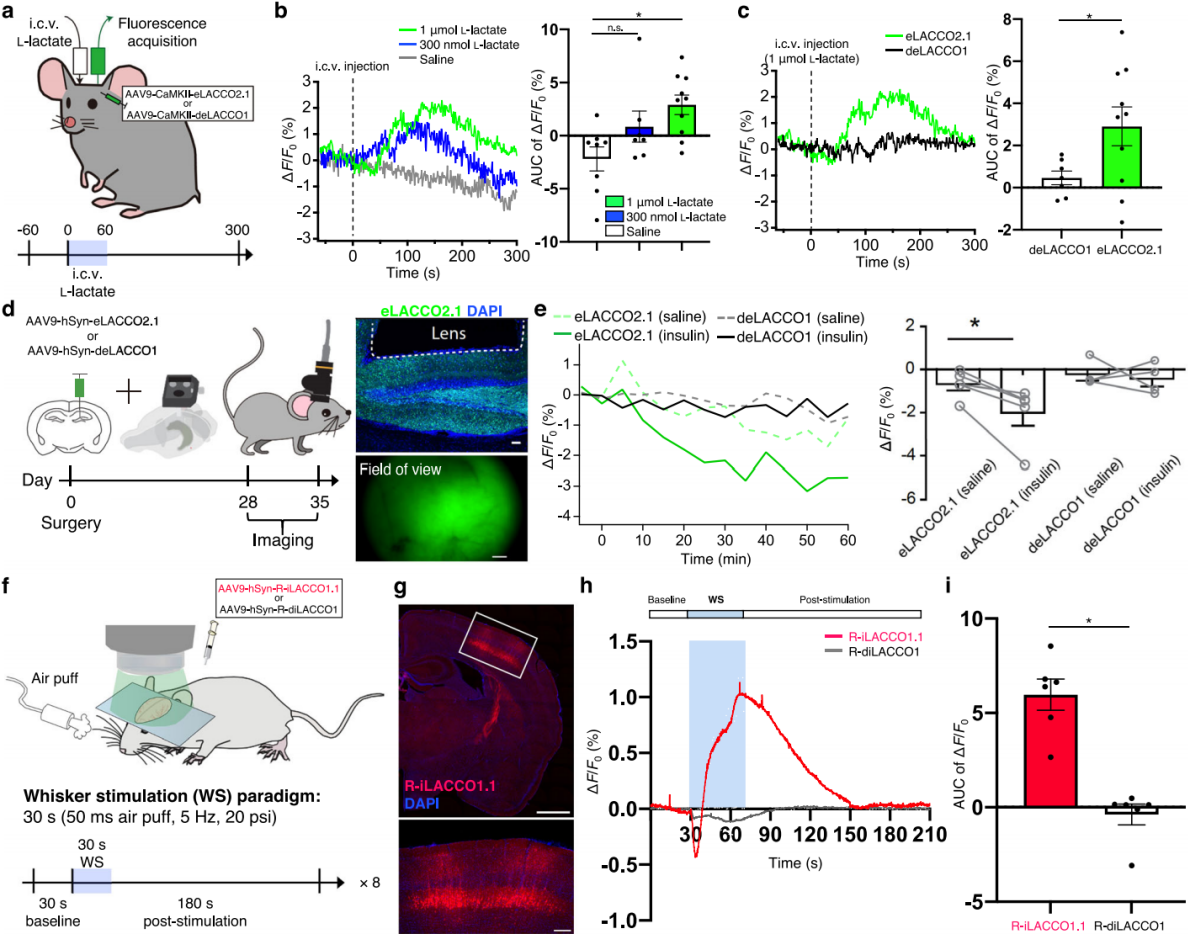
图6 小鼠体内L-乳酸成像
为了观察胶质母细胞瘤细胞胞质L-乳酸生成与胞外释放,在饥饿细胞中共表达eLACCO2.1(胞外成像)与R-iLACCO1.2(胞内成像)(图7a)。葡萄糖刺激后,二者荧光同步升高(图7b-c),表明胞质生成的L-乳酸快速释放至胞外;且胞内L-乳酸信号出现短暂峰值,此时胞外信号斜率显著变小。因MCT抑制剂存在时该峰值几乎消失,推测其为胞质L-乳酸生成与MCT介导外流平衡的结果。为了探究L-乳酸在胞质与细胞器间的穿梭,将R-iLACCO1.2靶向线粒体基质或内质网(ER),并在饥饿细胞中共表达胞质iLACCO1(图7d-i)。葡萄糖处理后,线粒体基质、ER中R-iLACCO1.2的荧光均随胞质iLACCO1同步升高,表明胞质生成的L-乳酸除释放至胞外,还会穿梭至线粒体基质与ER。
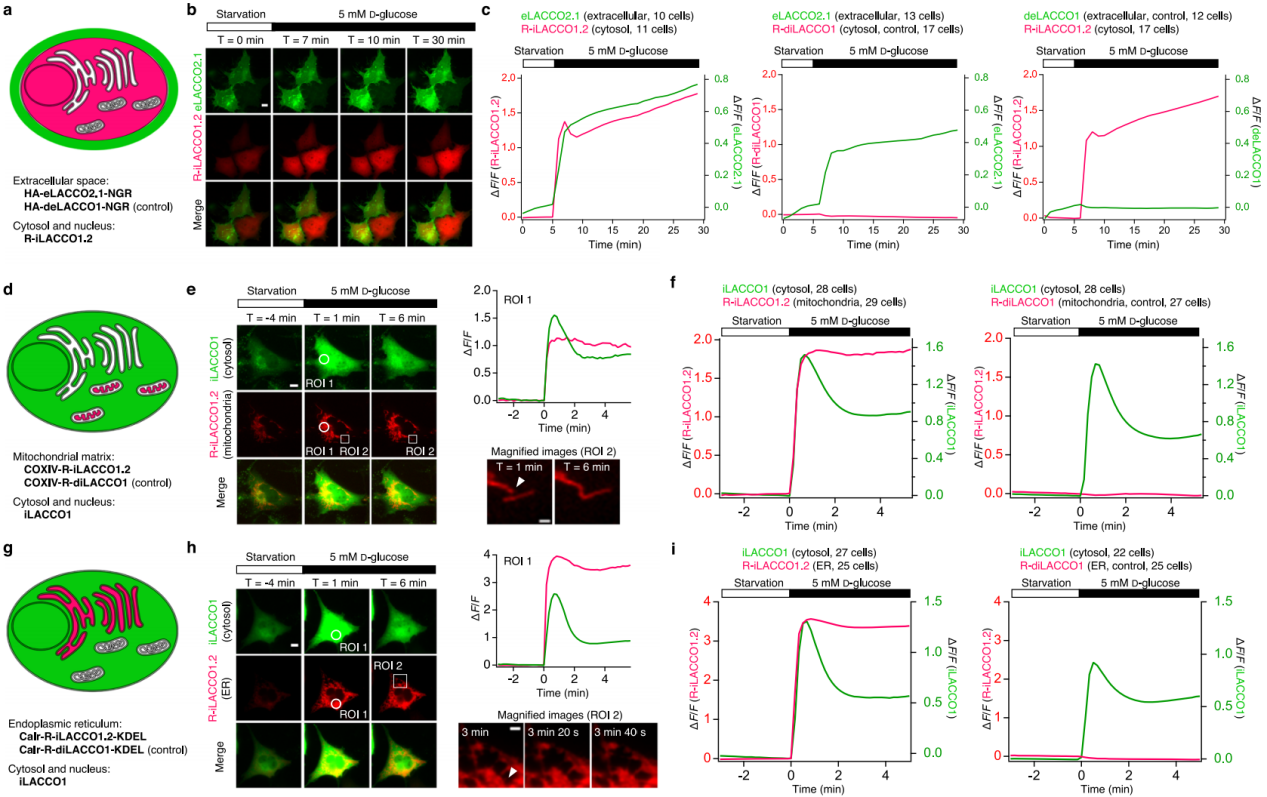
图7 光谱和空间多路复用的L-乳酸成像
R-iLACCO1填补红色胞内L-乳酸探针空白,解决光谱冲突问题;eLACCO2.1 性能全面超越第一代,实现活体胞外L-乳酸动态监测;为神经代谢(如ANLS假说)、肿瘤Warburg效应等研究提供高分辨率工具。