2025年9月4日,来自中国科学院动物研究所和首都医科大学宣武医院等单位的研究团队在国际顶刊Cell上发表了名为Senescence-resistant human mesenchymal progenitor cells counter aging in primates的文章,通过基因工程技术构建了FOXO3基因编辑的抗衰老人间充质祖细胞(SRCs),在为期44周的实验中,向老年食蟹猴静脉输注SRCs,结果显示其能显著降低衰老标志物(如细胞衰老、慢性炎症、组织退化),提升大脑结构与认知功能、改善生殖系统衰退及骨密度,且无明显不良反应;机制上,SRCs的抗衰效应部分依赖其分泌的外泌体(SRC-Exo),该研究为干细胞疗法对抗灵长类衰老提供了关键证据,凸显其作为抗衰再生疗法的潜力。
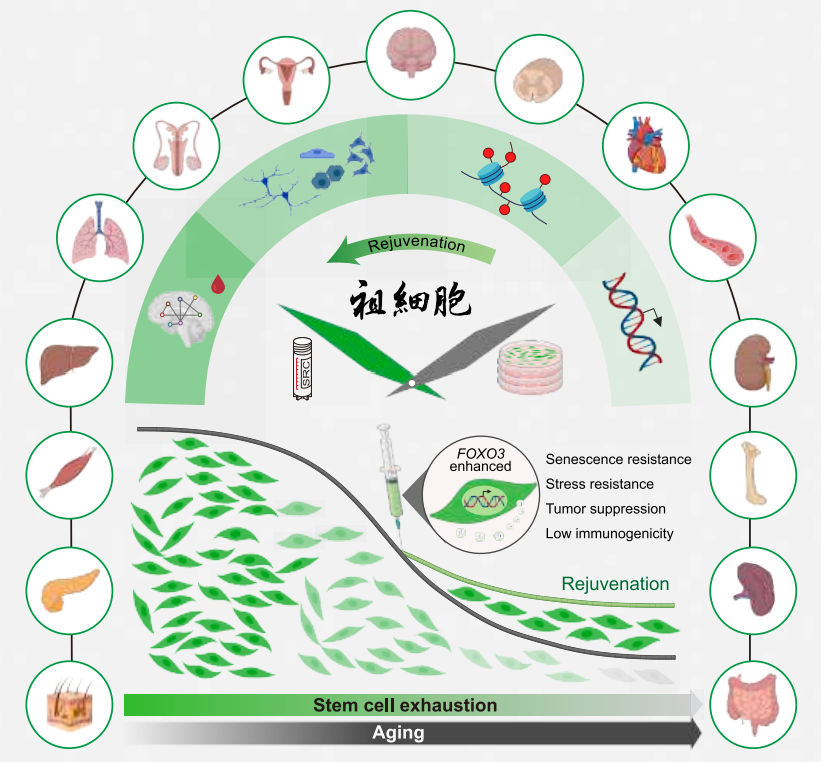
研究团队的首要任务,是打造出能抵御衰老环境的“升级版”干细胞。他们把目光锁定在FOXO3——这个基因是人类长寿的关键“开关”,活性降低会加速细胞衰老。通过基因编辑技术,团队对人胚胎干细胞(hESCs)的FOXO3基因进行了精准改造:将其2个容易被磷酸化失活的位点(Ser253、Ser315)替换成丙氨酸(命名为FOXO3 2SA/2SA hESCs),再将这些改造后的干细胞分化为间充质祖细胞,最终得到“抗衰祖细胞(SRCs)”。
后续的体外实验验证了SRCs的“抗衰能力”,相比野生型祖细胞(WTCs),SRCs的“衰老标志物”显著减少;应激抵抗更强,即使暴露在过氧化氢、紫外线环境中,SRCs也能保持增殖能力;基因表达更“年轻”,上调细胞增殖、肿瘤抑制相关基因,下调氧化应激、炎症反应相关基因。更重要的是,SRCs没有出现肿瘤相关的基因突变,且免疫原性低,为后续的动物实验打下了安全基础。
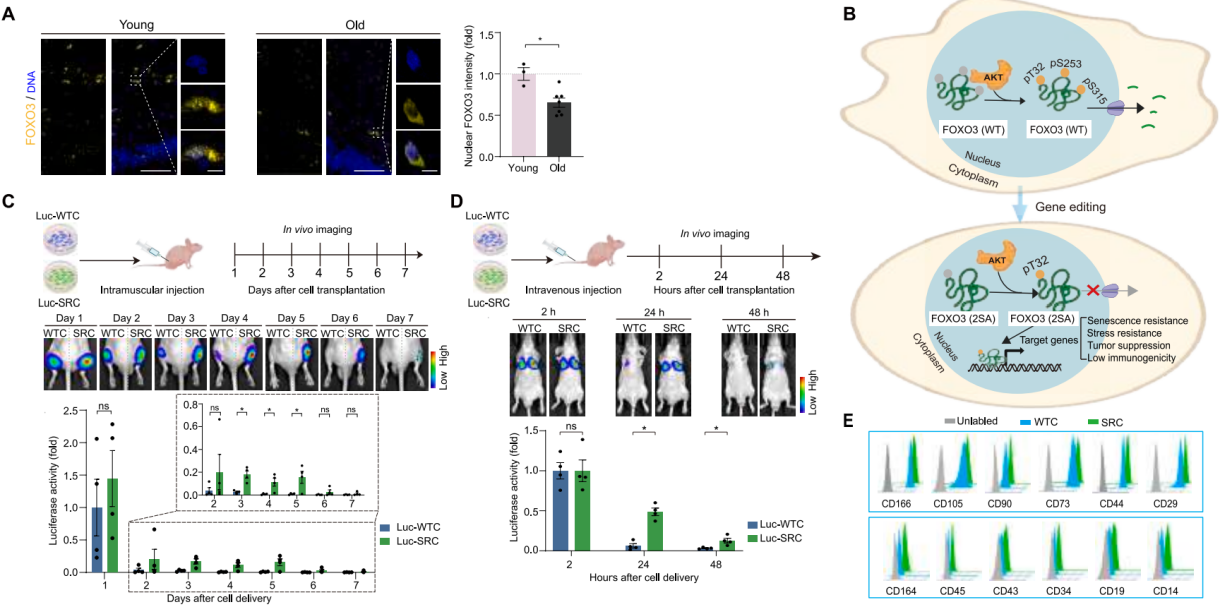
图1 人SRCs的生成和表征
要成为“抗衰疗法”,安全性是第一道门槛。研究团队选择了19-23岁的老年食蟹猴(对应人类57-69岁),将它们随机分为3组:输注生理盐水的对照组(A4-Ctrl)、输注野生型祖细胞的WTC组(A4-WTC)、输注SRCs的实验组(A4-SRC),每2周静脉输注一次,持续44周(约相当于人类3年)。44周的严密监测结果让人安心,无急性副作用,输注后没有出现发热、免疫排斥(淋巴细胞、中性粒细胞等免疫细胞数量稳定);生理指标正常,血糖、体重、BMI(身体质量指数)及各器官重量比例(器官指数)无异常波动;长期安全,实验结束后,所有接受细胞输注的猴子都没有出现肿瘤,肝、肾、心等关键器官也未发现损伤。这意味着,SRCs的长期静脉输注是安全的,为后续观察抗衰效果扫清了“安全顾虑”。
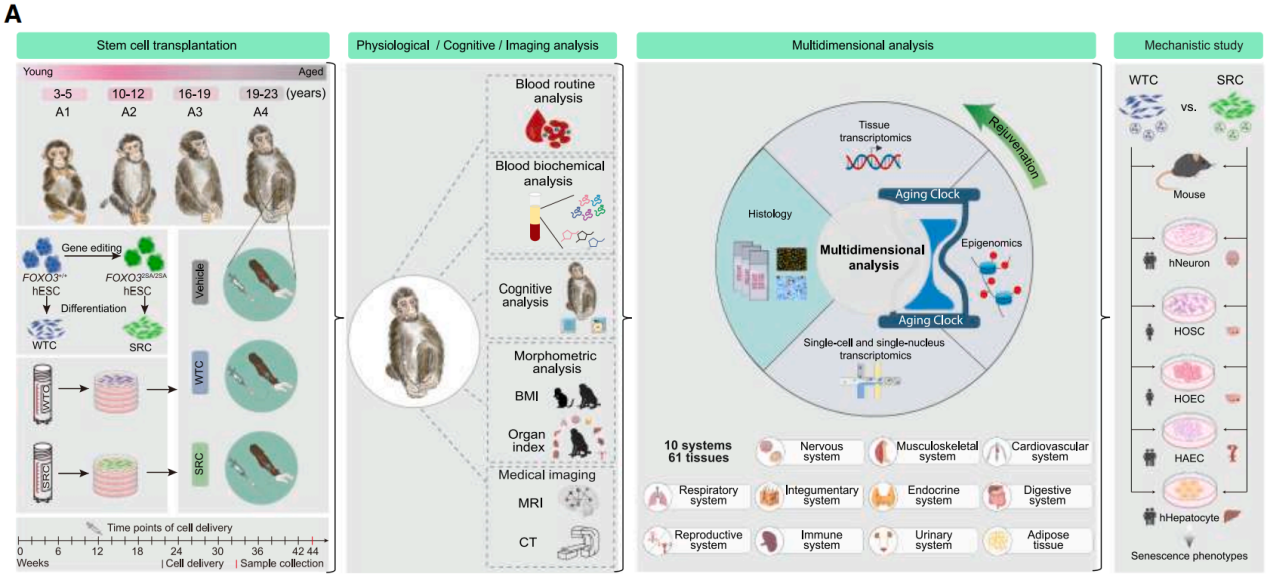
图2 人源WTCs和SRCs多移植后食蟹猴的总体评价
安全过关后,研究团队从“大脑到生殖系统”全面评估SRCs的抗衰效果,结果远超预期。认知层面,显著提升老年猴在记忆任务中的准确率,同时通过修复额叶、顶叶皮质的厚度与体积,减少β-淀粉样蛋白和磷酸化Tau等“老年痴呆相关蛋白”聚集,改善大脑结构与神经功能;骨骼层面,有效减少牙周骨流失,优化骨小梁结构,缓解骨质疏松倾向;血液层面,成功逆转近半数衰老相关基因的异常表达,降低免疫细胞中的衰老标志物和炎症因子水平,实现免疫细胞 “年轻化”;生殖层面,显著改善雌雄老年猴的生殖功能,提升卵母细胞和精子活力,使生殖系统的转录组年龄大幅降低;此外,通过转录组和DNA甲基化两种 “衰老时钟” 量化验证,SRCs平均让老年猴的生物学年龄降低3年以上,其中皮肤、肺、骨骼肌等组织的 “逆龄” 效果最为突出。
SRCs输注后在体内留存时间不长,却能产生长期抗衰效果,这背后的 “秘密” 是什么?研究团队发现,SRCs 分泌的外泌体(SRC-Exo) 才是 “抗衰信使”。
01、SRC-Exo富含“抗衰成分”
通过电镜(TEM)和纳米颗粒追踪分析(NTA),团队确认 SRC-Exo 的形态、大小符合外泌体特征;蛋白组学分析表明SRC-Exo中富含抗氧化、抗炎蛋白;代谢学分析表明SRC-Exo中含有精胺(一种已知的抗衰代谢物,能激活自噬、延缓细胞衰老)。
02、SRC-Exo具有独立抗衰效果
为了验证外泌体的作用,给18月龄的老年小鼠(对应人类56岁)输注SRC-Exo,12周后,小鼠的肝脏、肺、肾、骨骼肌的转录组年龄显著降低,衰老标志物减少;另外,用SRC-Exo体外处理人神经元、卵巢基质细胞、主动脉内皮细胞,这些细胞的衰老程度明显减轻,增殖能力提升。
综上所述,SRCs的抗衰效应并非依赖细胞自身,而是通过外泌体携带的 “抗衰分子”,远距离作用于全身器官,实现系统性 “逆龄”。
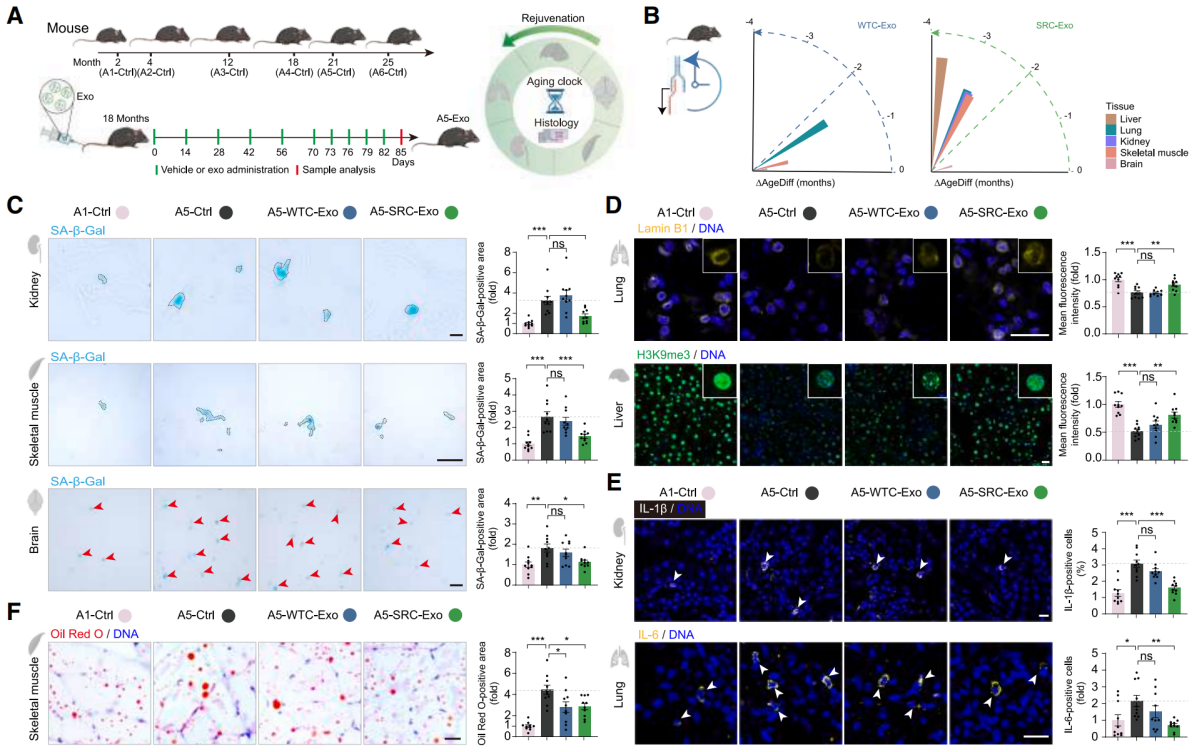
图3 外泌体作为SRCs抗衰老作用的信使
本文首次证实基因编辑干细胞可系统性延缓灵长类衰老,为“干细胞抗衰” 提供灵长类证据;SRCs低免疫原性、高安全性,为开发抗衰再生疗法奠定基础。或许在不久的将来,我们不需要“等待衰老”,而是可以通过类似的细胞疗法,延缓认知衰退、骨质疏松、生育力下降等年龄相关问题,真正实现“健康衰老”。
参考文献
[1]Lei J, Xin Z, Liu N, et al. Senescence-resistant human mesenchymal progenitor cells counter aging in primates. Cell. 2025;188(18):5039-5061.e35. doi:10.1016/j.cell.2025.05.021