2014年7月19日,霍华德·休斯医学研究所研究人员在Cell发表题为“Natural Neural Projection Dynamics Underlying Social Behavior”相关文章,通过光纤记录法记录自由活动小鼠的神经活动,结合光遗传学等技术,发现腹侧被盖区(VTA)到伏隔核(NAc)的多巴胺能投射活动可编码并预测社会互动;光遗传学调控该投射能双向调节社会行为,且其效应依赖NAc中的D1受体(D1R);进一步通过OptoXR方法构建了嵌合型Opto-D1受体和直接刺激NAc的D1R阳性中型多棘神经元(MSNs),证实D1R介导的信号对社会行为的充分性。这些发现揭示了社会行为背后的特定神经环路动态机制。
为了测试表达D1R的中型多棘神经元在社会行为中的充分性,研究人员构建了可光控的嵌合型Opto-D1(替换视紫红质细胞内环为D1R序列,图1C)。在表达Opto-D1-eYFP的HEK细胞中,光可选择性上调cAMP(Gs)信号通路,对IP3(Gq)、cGMP(Gt)无影响(图1D)。通过向Drd1::Cre小鼠NAc注射Cre依赖性Opto-D1腺相关病毒,限制其在D1R MSNs中表达(图1E)。结果显示,473nm光可增加社会互动(图8F),不影响运动及新物体探究。光电极记录发现,光使NAc多单位活动增加约3倍(图1G),其放电变化与自然社交及光遗传学激活VTA时的NAc活动增加一致。
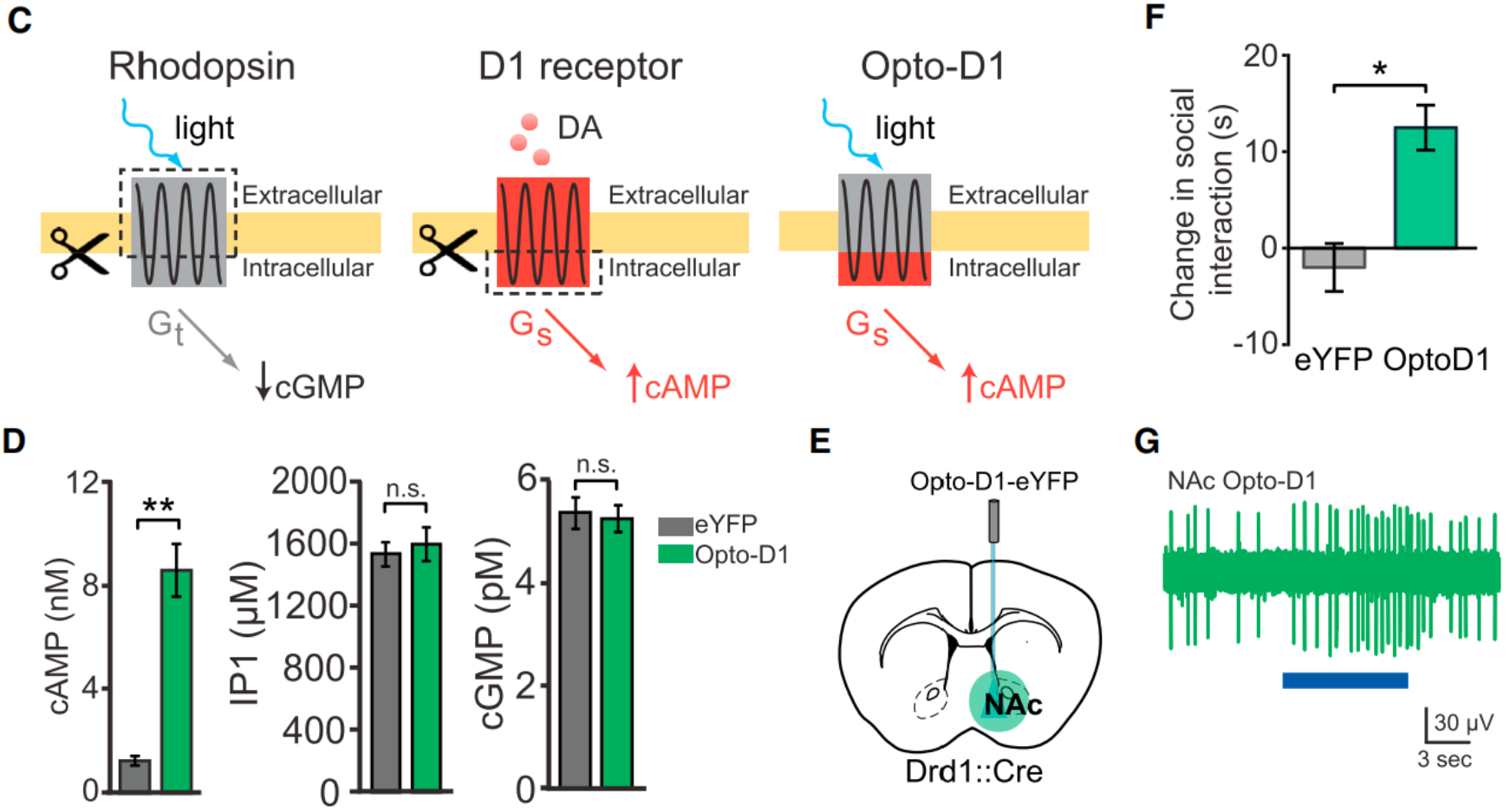
图1 突触后NAc D1细胞和受体在自然和VTA刺激驱动的社会行为中的作用
2022年10月19日,美国加州大学研究人员在Neuron发表题为“A locus coeruleus-dorsal CA1 dopaminergic circuit modulates memory linking”相关文章,发现蓝斑核(LC)到背侧CA1(dCA1)的多巴胺能环路在不影响记忆形成的情况下,特异性调节时间接近的情境记忆连接。研究人员通过opto-D1在dCA1神经元中激活D1受体信号(图2A-B)。以CNO抑制投射至dCA1的LC细胞(探索前30分钟给药),小鼠探索情境A时用蓝光(473nm,50s on-10s off,10mW)激活dCA1的D1受体,之后放回饲养笼。5小时后让小鼠探索情境B,期间无CNO输注或蓝光照射(图2C)。对照组(dCA1表达DIO-GFP)存在情境记忆连接缺陷:情境A冻结水平显著低于受电击的情境B,且与中性情境C相当(图2C)。而激活opto-D1的小鼠,情境A冻结水平显著高于情境C,且与情境B相近,表明记忆连接正常(图2C)。结果显示,探索情境A时激活dCA1的D1受体,可挽救因抑制LC-dCA1投射导致的记忆连接缺失。
为验证opto-D1是否通过恢复dCA1兴奋性挽救记忆连接,按上述方法操作后5小时检测神经元兴奋性。与GFP对照组相比,opto-D1激活提高了dCA1神经元放电频率,提示其通过增强兴奋性挽救记忆连接(图2D),且不改变静息膜电位、输入电阻、最小激发电流、峰后超极化电位及动作电位发放阈值,说明opto-D1没有改变神经元的基础膜属性或动作电位的基本触发机制。
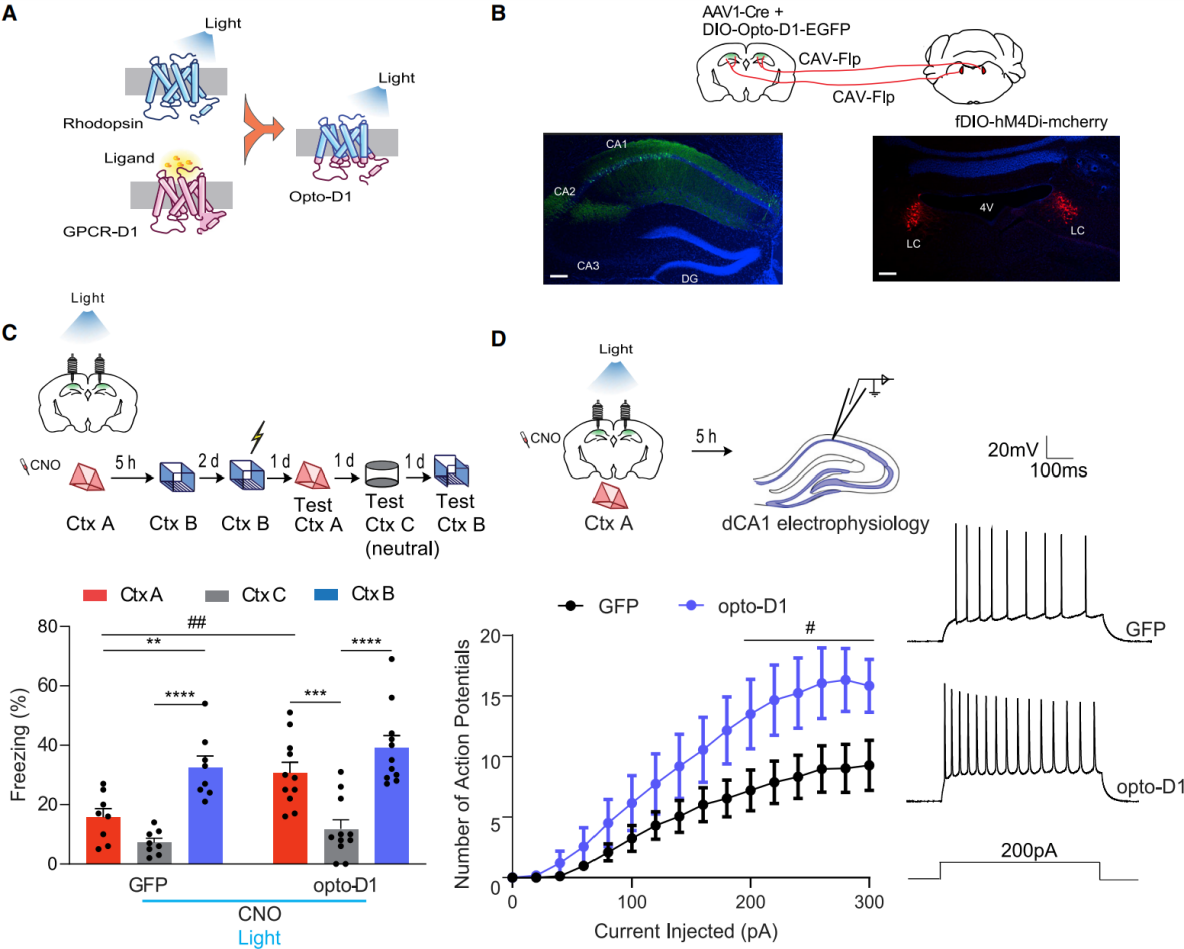
图2 在dCA1中激活光遗传学D1受体可挽救LC到dCA1抑制引起的连接缺陷
2015年5月20日,华盛顿大学研究人员在Neuron发表题为“Spatiotemporal control of opioid signaling and behavior”相关文章,开发并表征了一种光敏μ阿片样受体(opto-MOR),其通过将大鼠视紫红质的胞内环和C端替换为μ阿片受体(MOPR)的对应部分构建而成。opto-MOR在体外可模拟MOPR的经典信号通路,包括抑制cAMP生成、激活MAPK(pERK)、耦合GIRK通道,且内化和脱敏动力学与MOPR相似。该工具为时空精准调控阿片信号及解析相关神经环路提供了新手段。为证明opto-MOR在阿片神经环路与行为研究中的实用性,将AAV5-EF1a-DIO-opto-MOR-YFP注射到vGAT-IRES-Cre小鼠的脚桥被盖腹侧区(RMTg)和腹侧苍白球(VP)(图3A-F),3周后在腹侧被盖区(VTA)及VP上方植入光纤。小鼠置于黑色盒内自由探索两隔间,进入“光刺激”侧时接受10mW473nm激光刺激(图3G、3I),通过实时位置偏好实验评估行为。结果显示,向RMTg注射opto-MOR的小鼠对刺激的偏好显著高于同窝对照(图3G-H)。相比之下,与同窝对照组相比,向VP注射opto-MOR的小鼠对光刺激表现出显著的位置厌恶反应(图3I-J)。
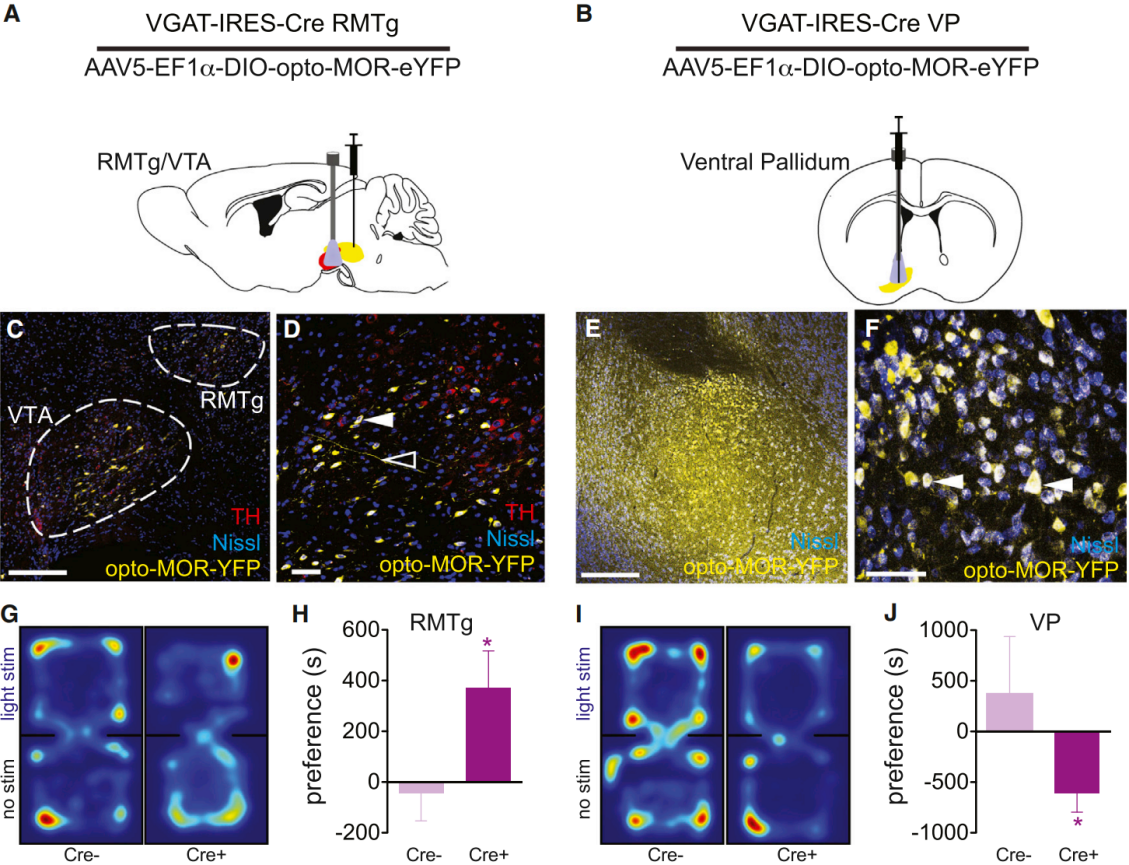
图3 光刺激Opto-MOR引起MOR样行为特征
2023年1月24日,温州医科大学研究人员在Neuropsychopharmacology发表题为“Neuronal and astrocytic CB1R signaling differentially modulates goal-directed behavior and working memory by distinct temporal mechanisms”相关文章,开发了光敏大麻素受体1(opto-CB1R),通过替换牛视紫红质的胞内环和C端为人类CB1R的对应序列构建而成。体外实验显示,光激活opto-CB1R可触发经典CB1R信号(抑制cAMP、激活MAPK通路,不影响cGMP或IP1),并在秒级时间尺度抑制皮质纹状体谷氨酸能神经元的兴奋性突触后电流(EPSCs)。体内实验表明,皮质纹状体谷氨酸能神经元中短暂(3秒)且“时间锁定”的opto-CB1R激活(与奖赏同步)会降低动物对结果贬值的敏感性,抑制目标导向行为(图4);而海马星形胶质细胞中持续(约30分钟)的opto-CB1R激活会损害工作记忆,短暂激活(10或30秒)则无影响。此外,腺苷A2A受体拮抗剂(KW6002)可逆转上述认知损伤,提示A2A受体可能是改善CB1R相关认知功能障碍的潜在靶点。
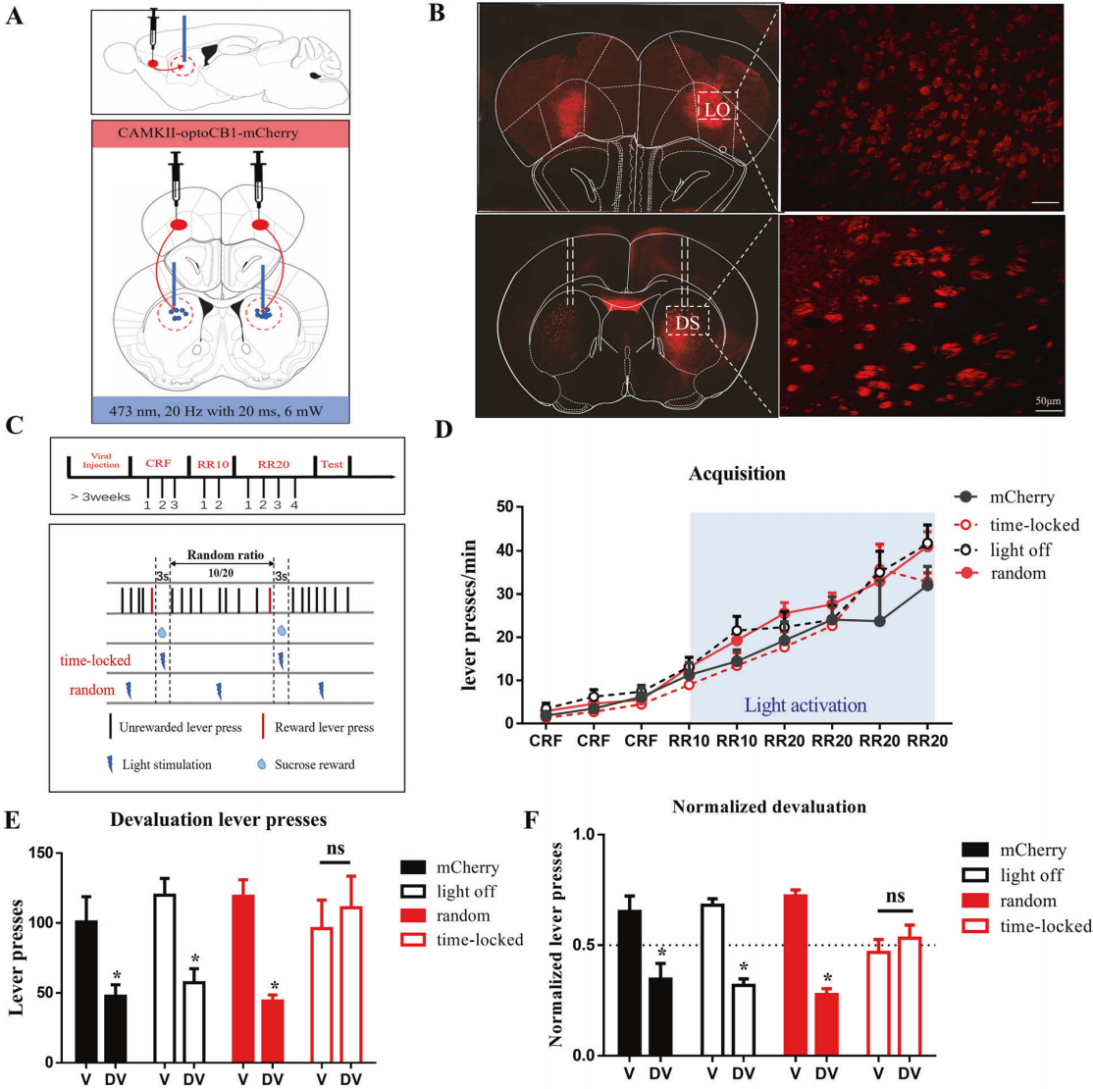
图4 激活皮质纹状体谷氨酸能神经元中opto-CB1R促进习惯形成
2015年2月17日,温州医科大学研究人员在Molecular Psychiatry发表题为“Optogenetic activation of intracellular adenosine A2A receptor signaling in the hippocampus is sufficient to trigger CREB phosphorylation and impair memory”相关文章,为了验证海马区腺苷A2A受体(A2AR)异常激活是否足以导致记忆损伤,研究团队开发了光敏腺苷A2A受体(opto-A2AR)——通过替换牛视紫红质的胞内环1/2/3及C端为人类A2AR的对应序列构建而成,既保留光敏感性,又能介导A2AR特异性信号。体外实验显示,光激活opto-A2AR可选择性激活cAMP/PKA通路和MAPK通路(不影响cGMP或IP1),效应与A2AR激动剂CGS21680一致;体内实验证实,在海马注射AAV5-CaMKIIα-opto-A2AR-mCherry病毒两周后(图5A),激活opto-A2AR会诱导磷酸化CREB(p-CREB)升高(图5B-D),并且显著损害空间记忆,Y-迷宫中新臂探索时间减半(图5E-F),而在伏隔核(NAc)激活则诱导磷酸化MAPK(p-MAPK)升高并增强运动活性(移动距离增加83%)。
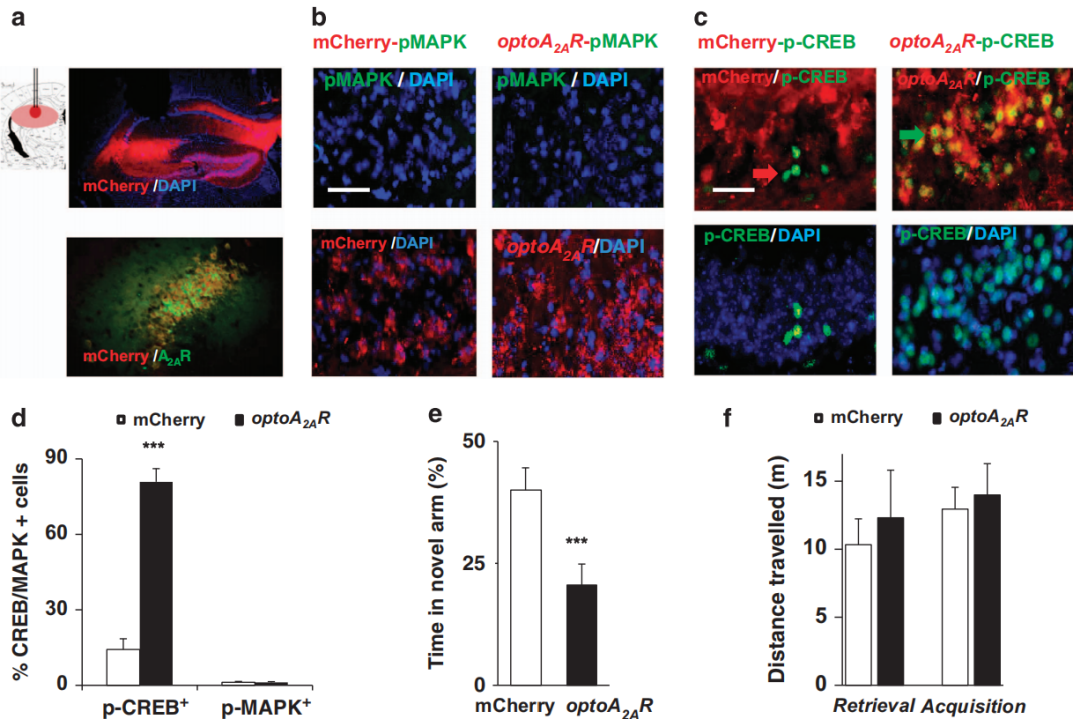
图5 光激活海马opto-A2AR的触发CREB磷酸化和记忆损伤
光敏受体工具无法完全复刻内源性受体的所有功能,限制了对复杂信号网络的全面解析。在不同脑区和实验目的下,也有特定的最佳光刺激时长、频率和强度要求。在长期或高频光刺激实验中,受体内化和脱敏现象可能导致受体功能暂时丧失,严重影响实验的时间窗口选择。实验设计时,必须充分考虑受体的这些动力学特性,预留足够的受体恢复时间,以保证实验过程中受体功能的相对稳定,避免因受体失活而得出错误结论。
参考文献
1、Gunaydin LA, Grosenick L, Finkelstein JC, et al. Natural neural projection dynamics underlying social behavior. Cell. 2014;157(7):1535-1551.
2、Chowdhury A, Luchetti A, Fernandes G, et al. A locus coeruleus-dorsal CA1 dopaminergic circuit modulates memory linking. Neuron. 2022;110(20):3374-3388.e8.
3、Siuda ER, Copits BA, Schmidt MJ, et al. Spatiotemporal control of opioid signaling and behavior. Neuron. 2015;86(4):923-935.
4、Shang H, Li P, Lin X, et al. Neuronal and astrocytic CB1R signaling differentially modulates goal-directed behavior and working memory by distinct temporal mechanisms. Neuropsychopharmacology. 2023;48(10):1520-1531.
5、Li P, Rial D, Canas PM, et al. Optogenetic activation of intracellular adenosine A2A receptor signaling in the hippocampus is sufficient to trigger CREB phosphorylation and impair memory. Mol Psychiatry. 2015;20(11):1339-1349.