环境毒素暴露是神经发育障碍的重要诱因,流行病学证据表明产前农药暴露与自闭症谱系障碍(ASD)相关,但致病机制不明,且缺乏有效干预手段。草铵膦(GLA)作为广泛使用的广谱除草剂,存在食品和水源污染问题,前期研究发现其低剂量产前暴露会导致子代出现自闭症样行为,但其具体作用的脑区、细胞机制及靶向治疗策略尚未明确。
南京医科大学卢应梅、韩峰、刘秀秀团队在Acta Pharmaceutica Sinica B上发表题为“Aberrant astroglial Kir4.1 activation in the anterior cingulate cortex disrupts neuronal excitability and social behavior”的研究论文,发现产前草铵膦暴露会诱导子代小鼠出现社交缺陷、重复理毛等自闭症样行为,其核心机制为小鼠前扣带回皮层(ACC)中星形胶质细胞异常激活并导致Kir4.1钾通道上调,通过破坏星胶-神经元通讯抑制CaMKIIα⁺锥体神经元的兴奋性;利用地昔帕明(DES)药理学抑制Kir4.1或星形胶质细胞特异性敲低Kir4.1,可恢复ACC锥体神经元活性并挽救子代小鼠的社交缺陷,证实Kir4.1是环境因素相关自闭症的潜在治疗靶点,同时揭示了星胶-神经元轴在除草剂诱导神经发育损伤中的新作用。

南京医科大学基础医学院卢应梅为本文最后通讯作者,韩峰、刘秀秀为本文共同通讯作者,李政懋、张怡轩、陈艳为论文共同第一作者。
为探究产前草铵膦暴露对神经发育的影响,研究先检测草铵膦产前暴露组(PGEO)小鼠的脑成熟度与血管结构(图1A),发现该组与对照组小鼠的脑质量、脑含水量无显著差异(图1B-D),经双光子激光扫描显微镜分析,两组的脑血管直径、血流速度也无显著差异。在排除脑组织大体结构和血管异常后,研究进一步评估小鼠行为表型,通过Y迷宫和新物体识别实验发现,两组小鼠的Y迷宫辨别指数、新物体识别实验识别率均无显著差异(图1E-F);高架十字迷宫和旷场实验结果显示,两组小鼠在开放臂、中央区域的停留时间无显著差异,提示产前草铵膦暴露不影响子代小鼠的一般认知功能,也不诱导焦虑样行为。针对自闭症谱系障碍核心的社交缺陷,研究采用三箱社交实验和社交新异性实验检测小鼠社交行为,社交阶段中,对照组小鼠对陌生小鼠S1表现出显著偏好,而PGEO小鼠嗅探空笼和陌生小鼠S1的时间无显著差异(图1I-J),提示其社交互动能力受损;社交新颖性阶段中,PGEO小鼠与对照组一致,对新陌生小鼠S2的嗅探时间显著长于熟悉小鼠S1(图1I-K),提示其社交新颖性偏好正常。此外,PGEO小鼠的自我理毛时间显著延长(图1L),提示其重复性/刻板行为增加。以上结果表明,PGEO小鼠可作为除草剂诱导的社交功能障碍模型,其行为表型与自闭症谱系障碍核心症状一致,与既往研究结果相符。
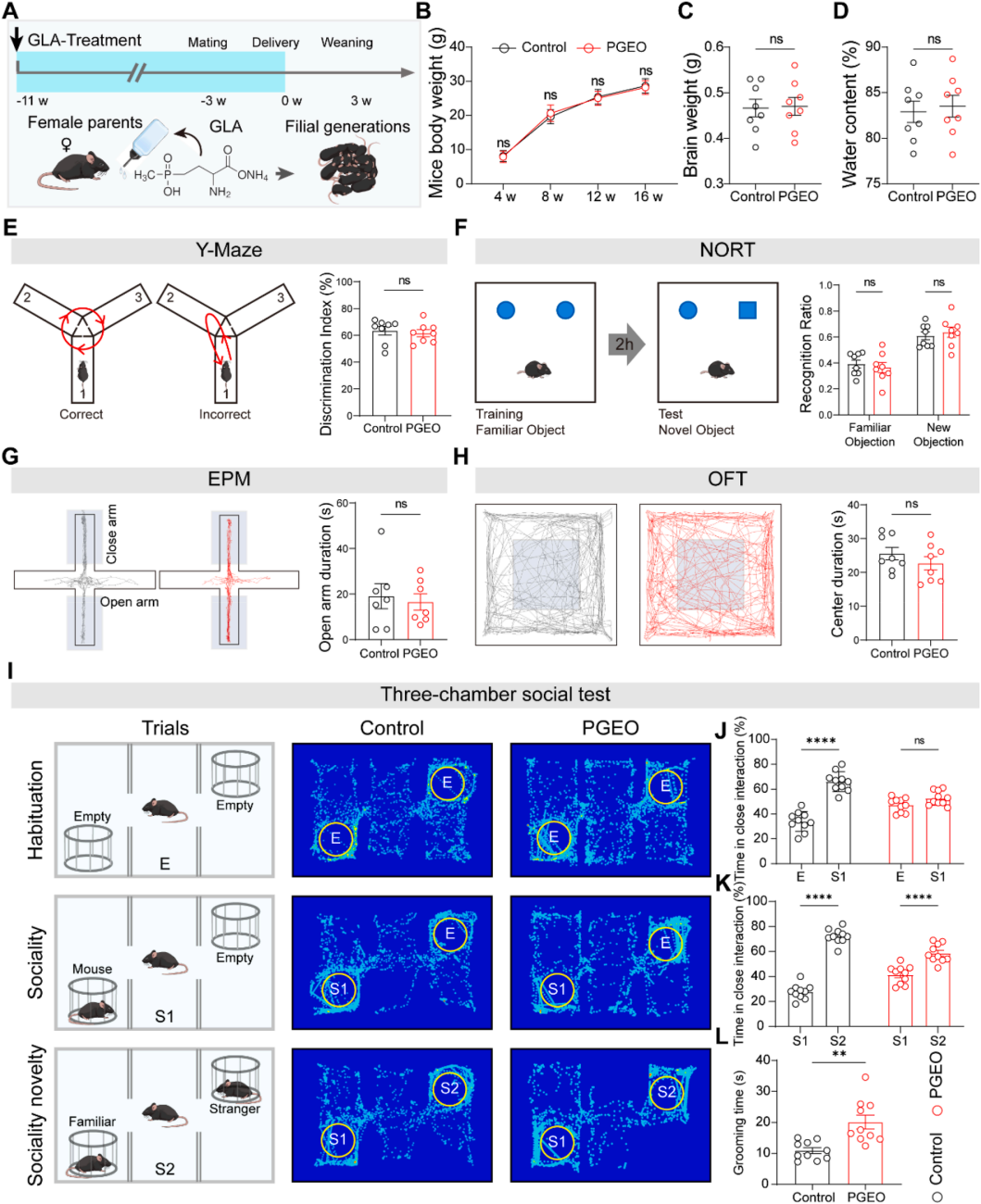
图1 | 产前草铵膦暴露诱导子代小鼠出现自闭症样行为
结合神经元活性及功能连接异常参与自闭症发病的现有研究,检测了小鼠社交行为测试后的神经元激活模式。在三箱社交实验社交阶段结束30分钟后取脑,通过全脑c-Fos免疫组织化学定位神经元活性并对社交相关脑区的c-Fos阳性细胞定量分析,发现与对照组相比,PGEO ACC和海马区的c-Fos阳性细胞数量显著减少(图2A-C)。ACC和海马是调控本能与情绪行为的关键边缘系统结构且存在功能连接,其中ACC作为社交行为调控核心脑区,可向海马CA1区投射兴奋性输入,参与基于特征的情境记忆提取。为明确产前草铵膦暴露影响的ACC特异性神经元群,研究开展免疫荧光共定位分析,结果显示,PGEO ACC中,CaMKIIα⁺兴奋性锥体神经元与c-Fos的双阳性神经元数量较对照组显著减少(图2D),而GABA能神经元标志物GAD67与c-Fos的共定位数量无显著差异(图2E)。以上结果提示,产前草铵膦暴露可特异性抑制子代小鼠ACC锥体神经元的活性。
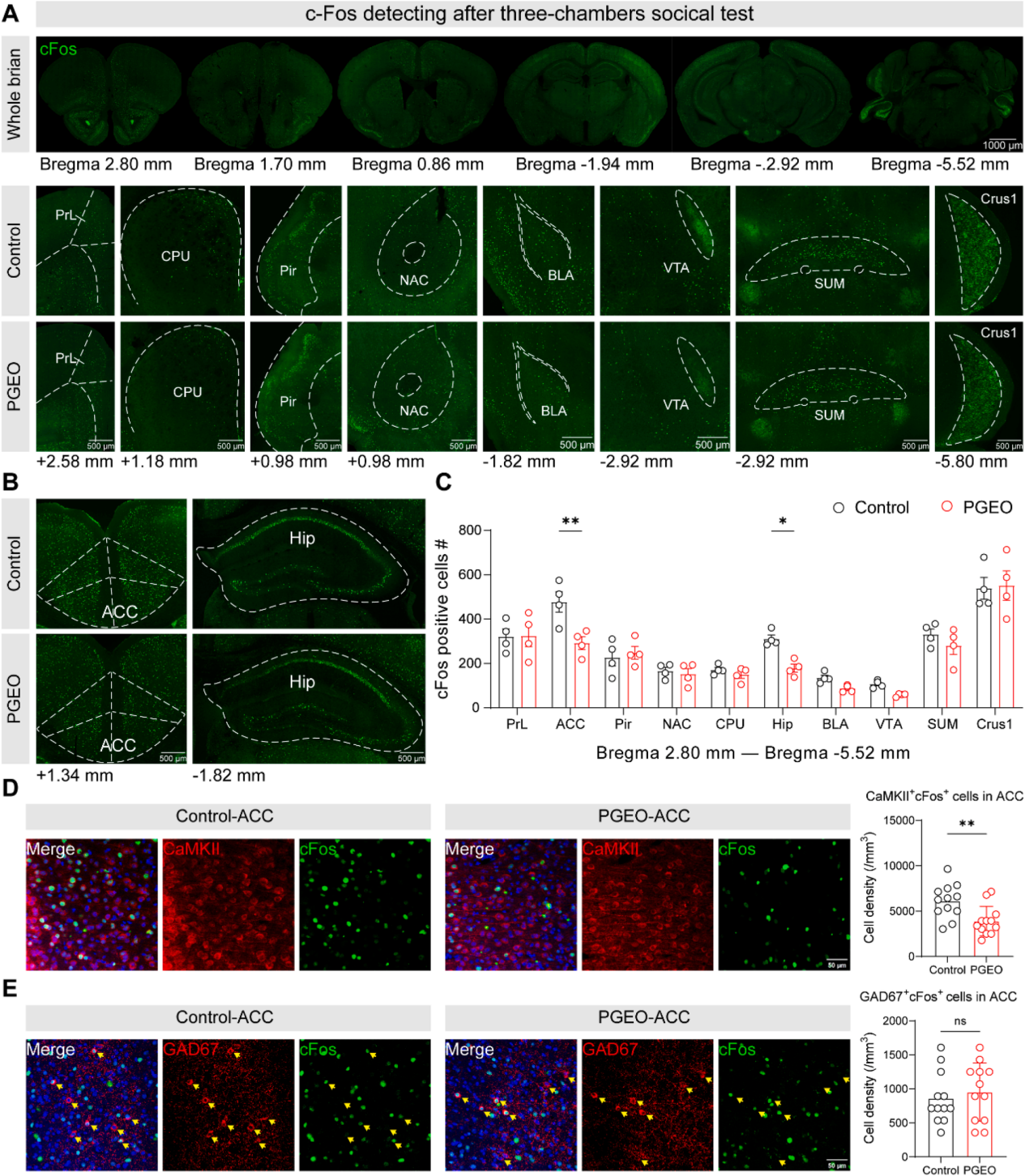
图2 | 草铵膦诱导的自闭症样行为与ACC锥体神经元活性降低有关
实验结果显示ACC的CaMKIIα⁺神经元的c-Fos激活减少(图2D),为进一步验证该现象是否由ACC神经元丢失导致,经神经元特异性标志物NEUN的免疫荧光定量分析,PGEO与对照组小鼠的总神经元密度无显著差异,说明神经元活性降低并非源于细胞丢失。为直接验证ACC锥体神经元功能低下与PGEO社交缺陷的关联,对小鼠ACC开展在体光纤光度记录,向ACC注射rAAV2/9-CaMKIIα-GCaMP(s)病毒,使锥体神经元特异性表达钙离子指示剂GCaMP(图3A-C),结果发现在社交互动过程中,PGEO ACC锥体神经元的钙瞬态振幅显著降低(图3D-F)。
为明确锥体神经元功能低下的内在和突触特性,研究对ACC锥体神经元进行全细胞膜片钳记录(图3G),显示产前草铵膦暴露会显著降低去极化电流刺激下锥体神经元的动作电位发放频率(图3H-I),动作电位幅度、半宽、发放阈值(图3J-L)以及输入电阻、膜电容、膜时间常数(图3M)则无显著差异,且PGEO锥体神经元的静息膜电位呈显著超极化状态(图3M)。研究进一步记录ACC锥体神经元的突触后电流,发现PGEO小鼠锥体神经元的自发性兴奋性突触后电流(sEPSC)频率显著降低、振幅无变化(图3N-P),自发性抑制性突触后电流(sIPSC)的频率和振幅均未受产前草铵膦暴露的影响(图3Q-S)。综上,产前草铵膦暴露可诱导ACC锥体神经元出现功能性功能低下,具体表现为动作电位发放减少、兴奋性突触传入特异性降低。
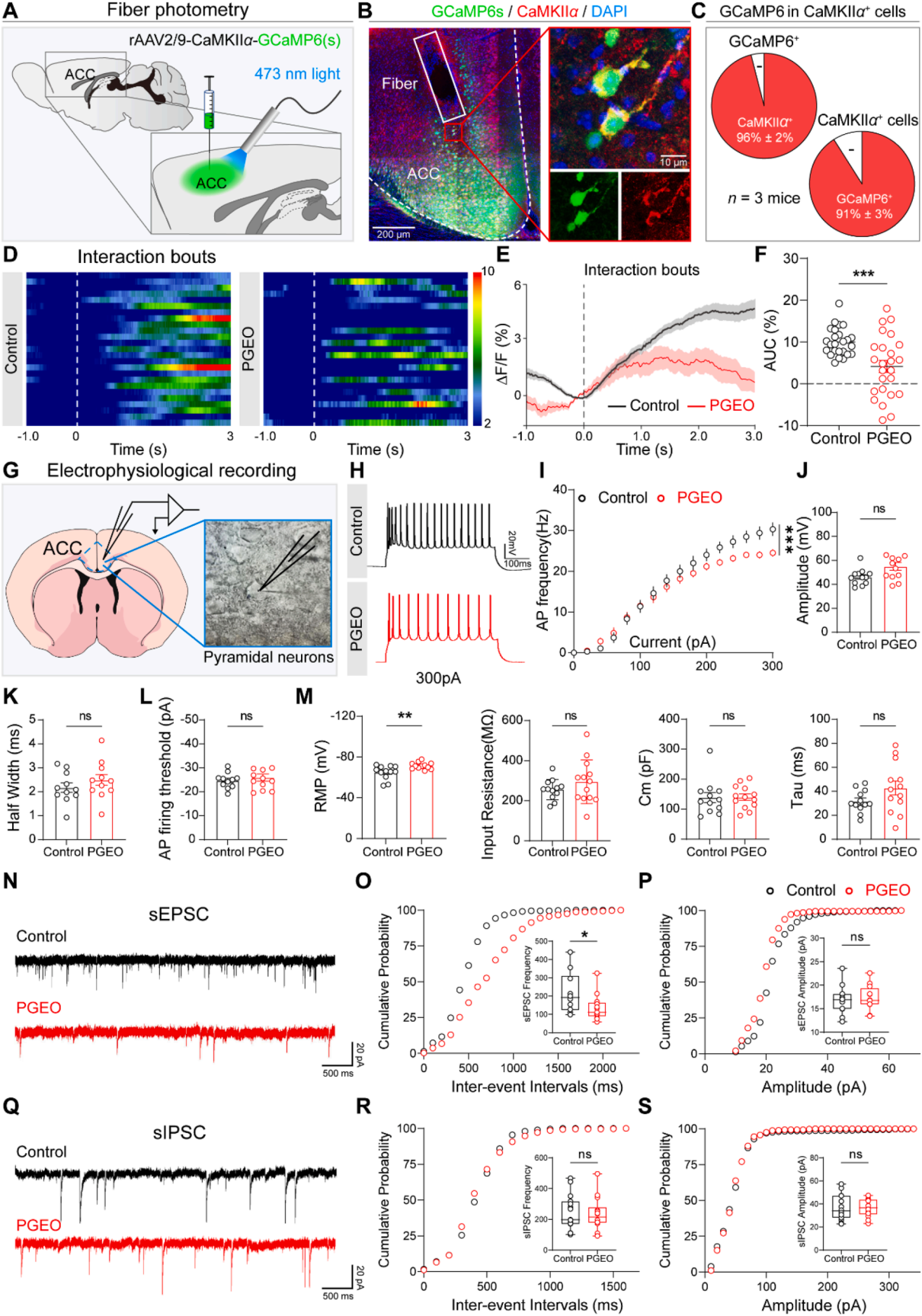
图3 | 产前草铵膦暴露的子代小鼠社交互动时ACC锥体神经元活性降低
为探究ACC锥体神经元活性降低的机制,研究对6只PGEO和5只对照组小鼠的ACC样本开展RNA测序(图4A)。经质控和标准化后获得27117个基因的表达数据,通过t分布随机邻域嵌入(t-SNE)降维分析并将样本的三个t-SNE分量投影至三维坐标系,结果显示PGEO与对照组的转录组谱存在明显分离(图4B)。差异分析发现两组间有3488个差异表达基因(图4C),其中部分自闭症相关基因表达显著上调;基因本体富集分析则表明,这些差异表达基因显著富集于胶质细胞激活等胶质细胞功能相关的生物过程(图4D)。
为验证RNA测序结果,研究对ACC的星形胶质细胞、小胶质细胞等胶质细胞进行免疫荧光分析,结果显示,PGEO小鼠ACC的S100β⁺细胞、GFAP⁺S100β⁺细胞密度,以及GFAP⁺S100β⁺细胞占总S100β⁺细胞的比例均显著升高(图4E-H);相关性分析显示,ACC GFAP⁺/S100β⁺细胞数量与CaMKIIα⁺/cFos⁺细胞数量呈负相关(图4I)。该实验组小鼠的小胶质细胞数量和分支也有所增加,结合RNA测序和小胶质细胞特征谱分析,这种变化或代表小胶质细胞处于激活与静息之间的中间状态。基于以上结果,后续研究将重点探索星形胶质细胞过度激活与神经元功能低下的关联及其分子机制。
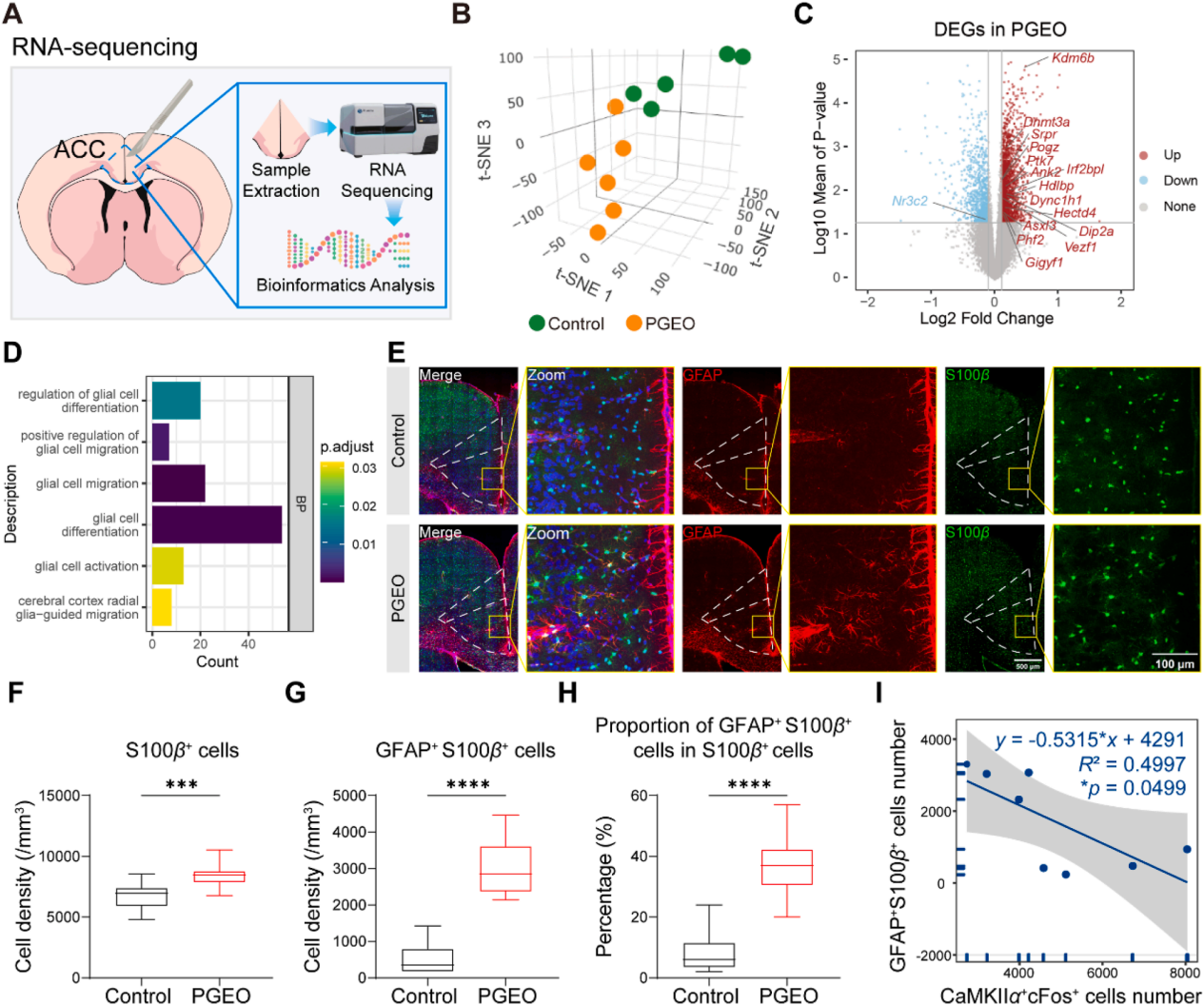
图4 | PGEO小鼠ACC的星形胶质细胞激活
为明确PGEO小鼠ACC锥体神经元功能低下的分子机制,对RNA测序数据进行深入分析。从PGEO与对照组的差异表达基因中,筛选出102个与神经元功能相关的基因进行后续分析,其中21个基因(20.59%)为已报道的自闭症风险基因(图5A),这可能是PGEO小鼠表现出自闭症相关分子特征的原因。鉴于神经元功能低下常与离子通道功能异常相关,对离子通道相关的基因本体条目进行分析,结果显示,所有显著富集的生物过程条目均与钾离子通道特异性相关,包括钾离子通道转运调控、钾离子通道复合物组分、电压门控钾离子通道活性等(图5B);此外,产前草铵膦暴露后,钾离子通道相关基因的表达存在显著紊乱(图5C),为ACC锥体神经元动作电位发放频率异常提供了合理的分子解释。
为验证PGEO小鼠的钾离子通道异常是否适用于人类自闭症,整合已发表的9例自闭症患者和9例健康对照者ACC的单细胞核RNA测序数据集(共42393个细胞核)。通过均匀流形逼近和投影(UMAP)降维后,采用公认的细胞标志物对细胞类型进行注释(图5D)。在该人类数据集中分析PGEO小鼠的钾离子通道差异表达基因,发现自闭症患者星形胶质细胞中的KCNJ10表达较对照组显著升高(图5F)。KCNJ10编码星形胶质细胞Kir4.1钾通道,提示该通道的表达紊乱可能是锥体神经元功能低下的原因。
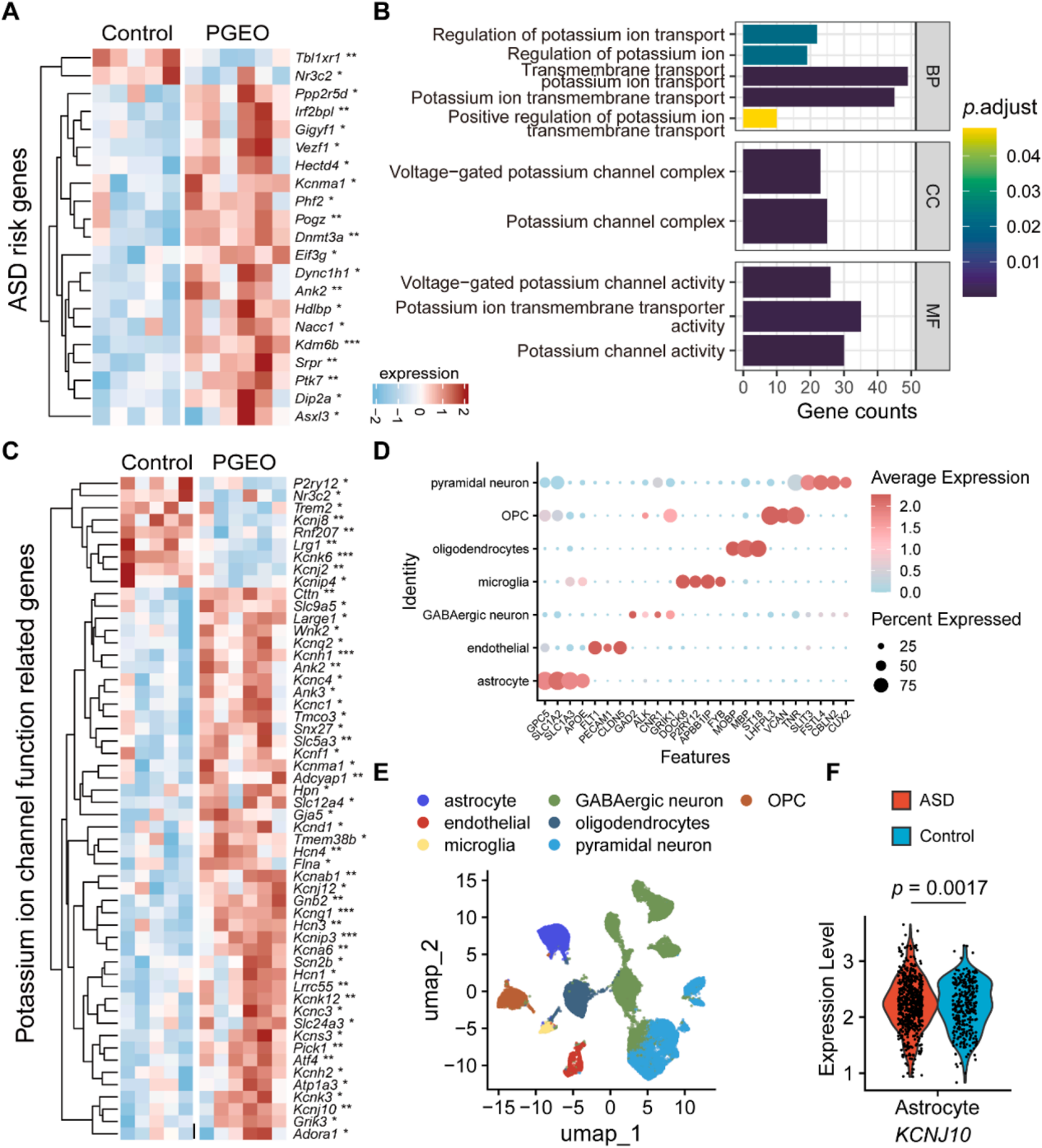
图5 | Kir4.1上调与ACC锥体神经元活性降低相关
为验证Kir4.1通道异常参与锥体神经元功能低下的假说,对PGEO和对照组小鼠的ACC星形胶质细胞做全细胞膜片钳记录,借助氯化钡(100 μmol/L)分离Kir4.1电流后,发现PGEO的钡离子敏感电流显著增强(图6A-D),提示产前草铵膦暴露下Kir4.1电流增强与ACC锥体神经元功能低下相关。
为明确Kir4.1的功能作用,采用两种策略进行验证:一是利用AAV2/5载体结合GFAP(GfaABC1D)启动子,将靶向Kcnj10的shRNA特异性递送至PGEO小鼠ACC的星形胶质细胞。病毒特异性经Western blot和免疫荧光验证。膜片钳结果显示,星形胶质细胞特异性敲低Kir4.1可恢复ACC锥体神经元的动作电位发放频率、逆转其静息膜电位超极化,且不影响其他基础电生理指标。行为学结果表明,该处理可显著改善小鼠的自闭症样核心表型。二是采用Kir4.1抑制剂地昔帕明进行干预,发现该药物能让PGEO小鼠在三箱社交实验中恢复对陌生小鼠的社交偏好(图6E-G),还能逆转其过长的自我理毛时间(图6H)。综上,星形胶质细胞Kir4.1功能缺失或通过药物抑制该通道,均能改善PGEO小鼠的核心自闭症样行为表型。
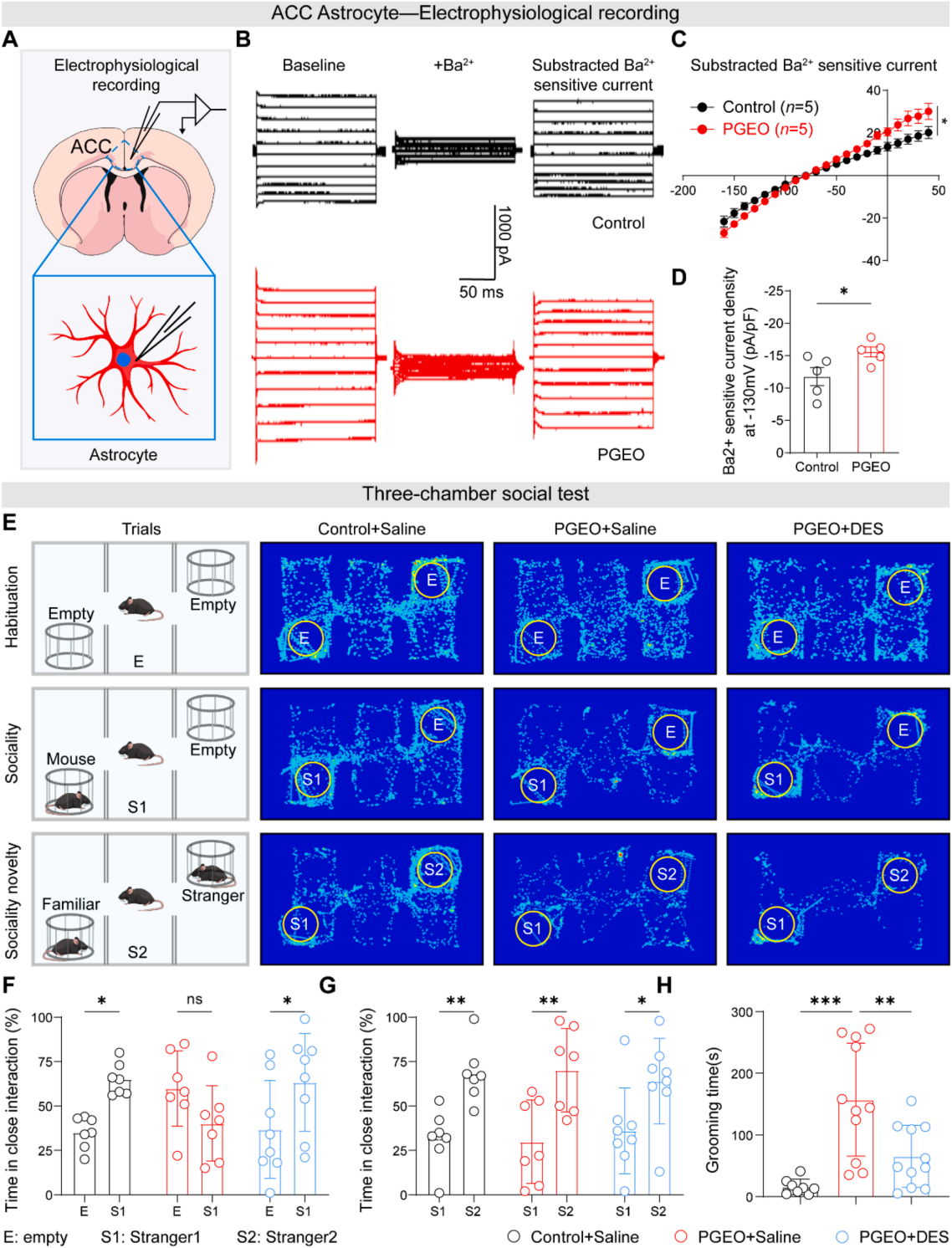
图6 | 药理学抑制Kir4.1可改善PGEO小鼠的社交缺陷
基于上述结果,作者提出假说:Kir4.1表达上调通过破坏星胶-锥体神经元通讯,介导锥体神经元活性降低。将PGEO小鼠的差异表达基因(DEGs)及生物学过程,与人类自闭症患者ACC单细胞核转录组数据关联分析,UMAP降维显示自闭症样本中显著富集“自闭症相关星形胶质细胞(AAAs)”(图7A),其DEGs与PGEO小鼠显著重叠(图7B)。GSEA分析显示AAAs的DEGs富集于细胞通讯、离子跨膜转运等通路(图7C),提示二者存在保守的星胶转录异常。交集分析筛选出221个二者共有的生物学过程,归为10类星胶-锥体神经元通讯相关类别,其中突触形成与功能占比最高(图7D),热图显示自闭症存在特异性通路异常(图7E);PGEO小鼠中,编码Kir4.1的Kcnj10等胶质相关DEGs也参与该通讯过程(图7F)。鉴于地昔帕明可改善PGEO小鼠社交缺陷及理毛行为(图6E-H),膜片钳检测显示,50μmol/L地昔帕明可恢复PGEO小鼠ACC锥体神经元动作电位发放频率(图7G-I),逆转其静息膜电位超极化,但对基础膜特性无显著影响(图7J-M)。综上,星胶中Kir4.1异常破坏星胶-锥体神经元通讯(尤其突触过程),导致神经元活性降低及自闭症核心行为异常。
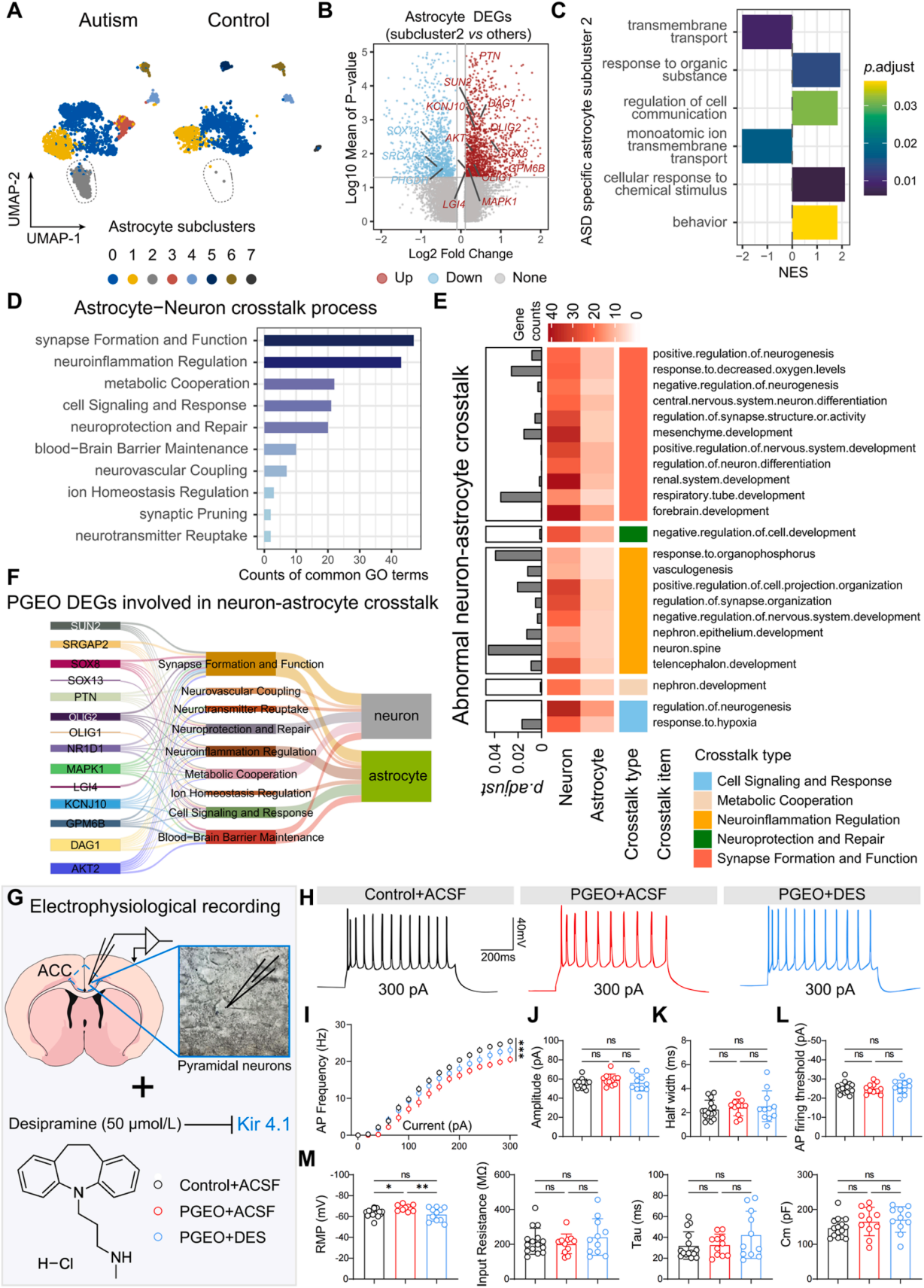
图7 | 星形胶质细胞Kir4.1通过星形胶质细胞-神经元交互作用调控锥体神经元活性
本研究提供了确凿证据,证实产前草铵膦暴露通过ACC中星形胶质细胞Kir4.1钾通道的表达紊乱,以星形胶质细胞介导的全新机制诱导自闭症样行为;该发现显著深化了对环境风险因素在神经发育障碍中作用的理解,并鉴定出自闭症谱系障碍干预的潜在治疗靶点。
本文使用的工具病毒布林凯斯均可提供:
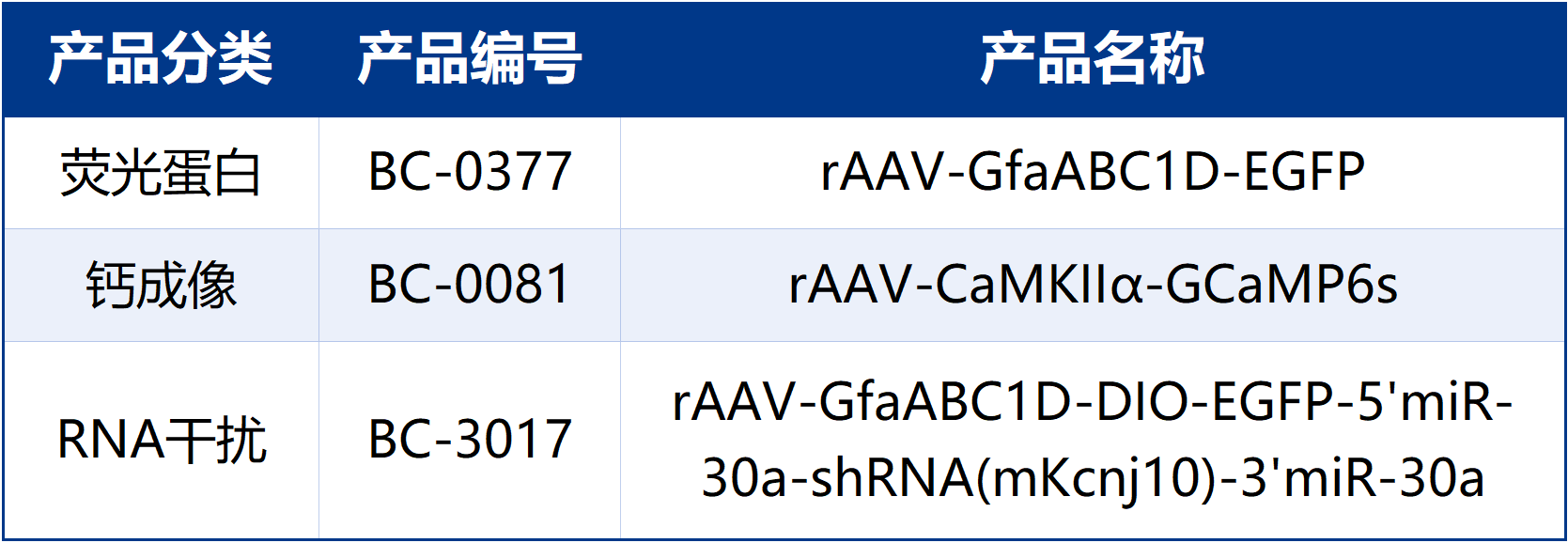
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。