偏头痛是全球患病率约14.4%的高发性、高致残性神经系统疾病,其病理生理机制尚未完全阐明。下丘脑室旁核(PVN)虽可通过分泌神经肽参与疼痛调控,但其调控偏头痛的具体机制仍不清楚,尤其是PVN内促肾上腺皮质激素释放因子(PVNCRF)神经元在偏头痛发病中的功能与相关通路尚属未知。
2026年2月28日,青岛大学徐许峰团队与河南省人民医院王梅云、靖旭团队联合在《Advanced Science》期刊上发表了题为“PVNCRF Neurons Regulate Migraine-Like Allodynia by Activating CRFR2 on Spinal Trigeminal Caudalis Glutamatergic Neurons”的研究论文。该研究首次揭示PVNCRF神经元通过释放CRF神经肽激活SP5C谷氨酸能神经元上的CRFR2受体,驱动偏头痛样异常性疼痛,为偏头痛治疗提供了新靶点。

研究采用10mg/kg硝酸甘油(NTG)间歇性腹腔注射(每48小时1次,共5次)建立小鼠慢性偏头痛模型,于每次注射当天及末次注射后1天进行行为学评估(图1A)。小鼠适应环境1周后,通过Von Frey细丝试验和丙酮试验分别检测头部机械及冷异常性疼痛(图1B)。结果显示,首次NTG注射后1小时小鼠即出现急性机械痛阈值降低,4小时内恢复(图1C、F);第5~10天反复NTG暴露可诱导雄性和雌性小鼠出现持续性偏头痛样眶周机械与冷异常性疼痛,且呈时间依赖性(图1D、E、G、H)。c-Fos免疫组化检测下丘脑室旁核(PVN)的神经元激活情况,结果显示,与溶媒对照组相比,反复NTG处理的雌雄小鼠PVN区域c-Fos阳性神经元数量显著增加(图1I、J),定量分析显示神经元活性升高超过4倍。RNA scope荧光染色发现,反复NTG注射诱导的c-Fos mRNA表达水平在PVN促肾上腺皮质激素释放激素神经元(PVNCRF)中显著高于催产素能神经元(PVNOXT)(图1K、L)。综上,PVNCRF神经元的选择性激活是NTG诱导偏头痛样异常性疼痛的核心中枢机制之一,同时证实反复NTG注射方案可构建具有可靠临床表型的慢性偏头痛模型。
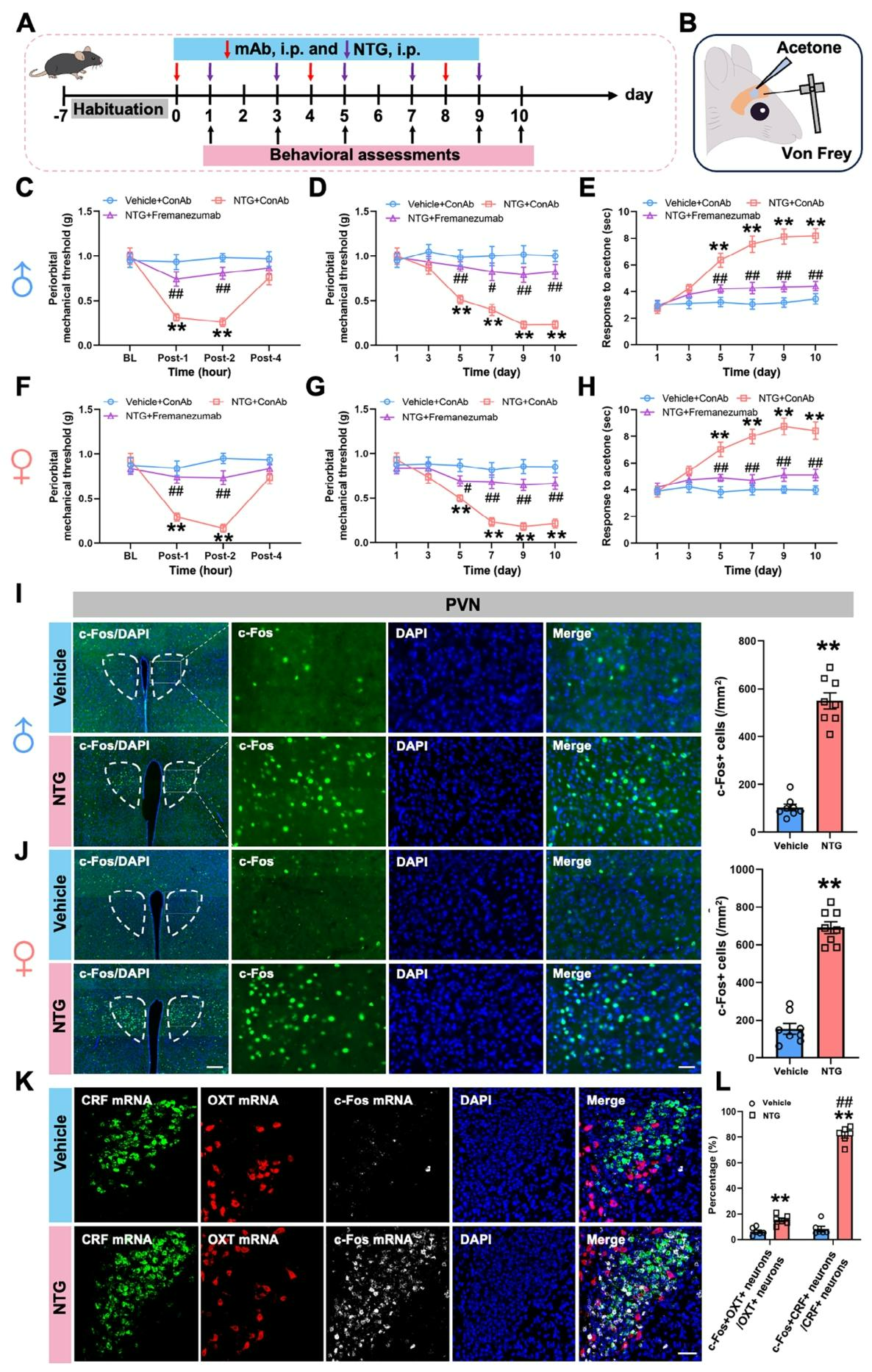
图1. 注射NTG可诱发偏头痛样异常性疼痛并激活PVNCRF神经元
为剖析PVNCRF神经元在偏头痛样异常性疼痛中的作用,采用在体光纤光度钙成像技术,向CRF-Cre小鼠单侧PVN注射AAV2/9-DIO-GCaMP6m以实现特异性监测(图2A),结果显示GCaMP6m表达局限于PVN区域且与内源性CRF mRNA高度吻合,证实靶向成功(图2B-D)。全身给予NTG后,雌雄小鼠PVNCRF神经元钙活性均显著升高(图2E‑J)。在NTG诱导的慢性偏头痛模型后施加短暂异常性疼痛刺激,结果显示,第10天给予刺激后,雄雌小鼠的PVNCRF神经元钙信号均迅速升高(图2K-R)。综上,NTG诱导的偏头痛样异常性疼痛与PVNCRF神经元的过度激活相关。
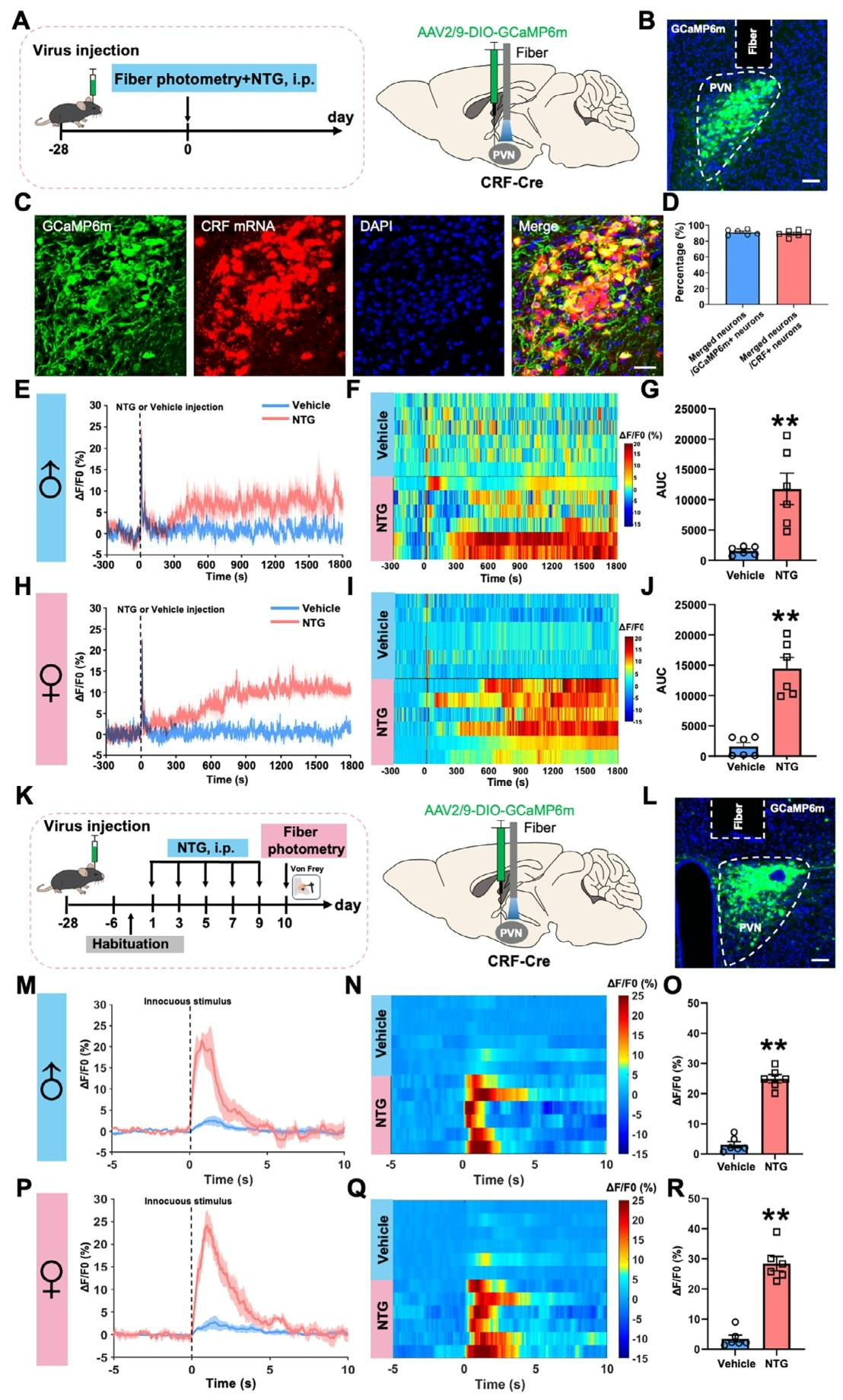
图2. PVNCRF神经元的激活与NTG诱导的偏头痛样异常性疼痛相关
为验证PVNCRF神经元在NTG诱导的偏头痛样反应中的必要性,采用化学遗传学策略,向CRF-Cre小鼠PVN区域注射AAV2/9-DIO-hM4Di-mCherry(对照为AAV2/9-DIO-mCherry),以实现对PVNCRF神经元的特异性抑制(图3A),mCherry荧光与内源性CRF mRNA高度吻合,证实了靶向特异性(图3B-D)。c-Fos免疫组化分析显示,注射CNO可显著抑制NTG诱导的PVNCRF神经元激活(图3E、F)。行为学评估发现,在NTG诱导的慢性偏头痛模型中,雄雌性小鼠均表现出眶周机械痛阈值降低和丙酮诱导的冷异常性疼痛反应增强;而化学遗传学抑制PVNCRF神经元可显著逆转上述异常性疼痛表型(图3G-J)。综上,PVNCRF神经元的激活是NTG诱导偏头痛样异常性疼痛发生所必需的。
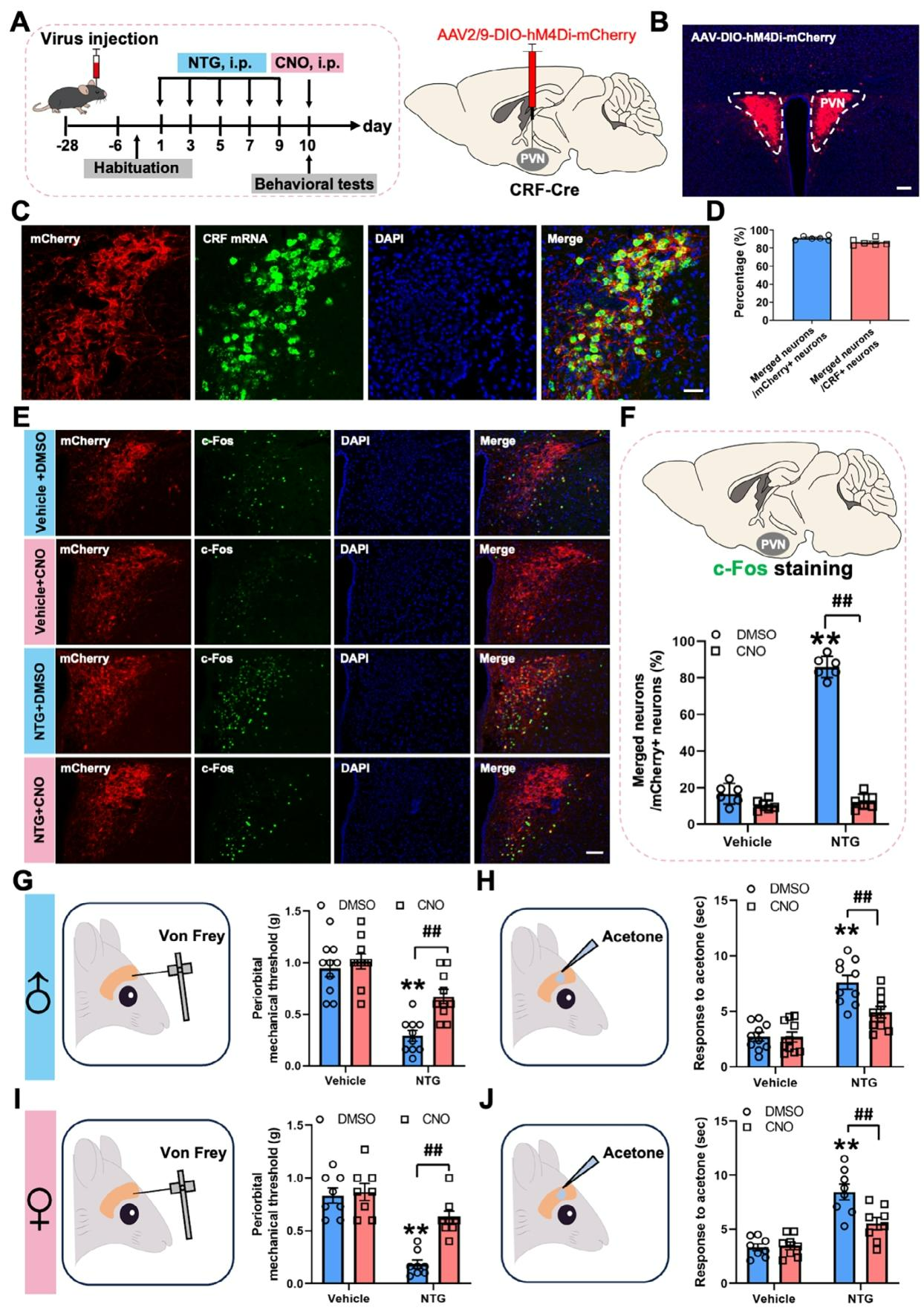
图3. 抑制PVNCRF神经元可缓解NTG诱导的偏头痛样异常性疼痛
为明确PVNCRF神经元在偏头痛样异常性疼痛中的充分性,向CRF-Cre小鼠PVN立体定向注射AAV2/9-DIO-hM3Dq-mCherry(对照组为AAV2/9-DIO-mCherry)以特异性激活PVNCRF神经元(图4A),mCherry表达与RNA scope染色证实病毒靶向准确且特异(图4B–D),CNO注射可显著诱导hM3Dq-mCherry阳性神经元c-Fos表达,证明神经元被有效激活(图4E、F)。行为学检测显示,CNO处理可使雌雄小鼠眶周机械痛阈值显著降低、丙酮诱导的冷伤害性反应明显延长,成功重现偏头痛样异常性疼痛表型;而DMSO对照组无明显异常(图4G–J)。综上,特异性激活PVNCRF神经元足以在雌雄小鼠中重现偏头痛样异常性疼痛,提示其在偏头痛中枢致敏中发挥关键作用。
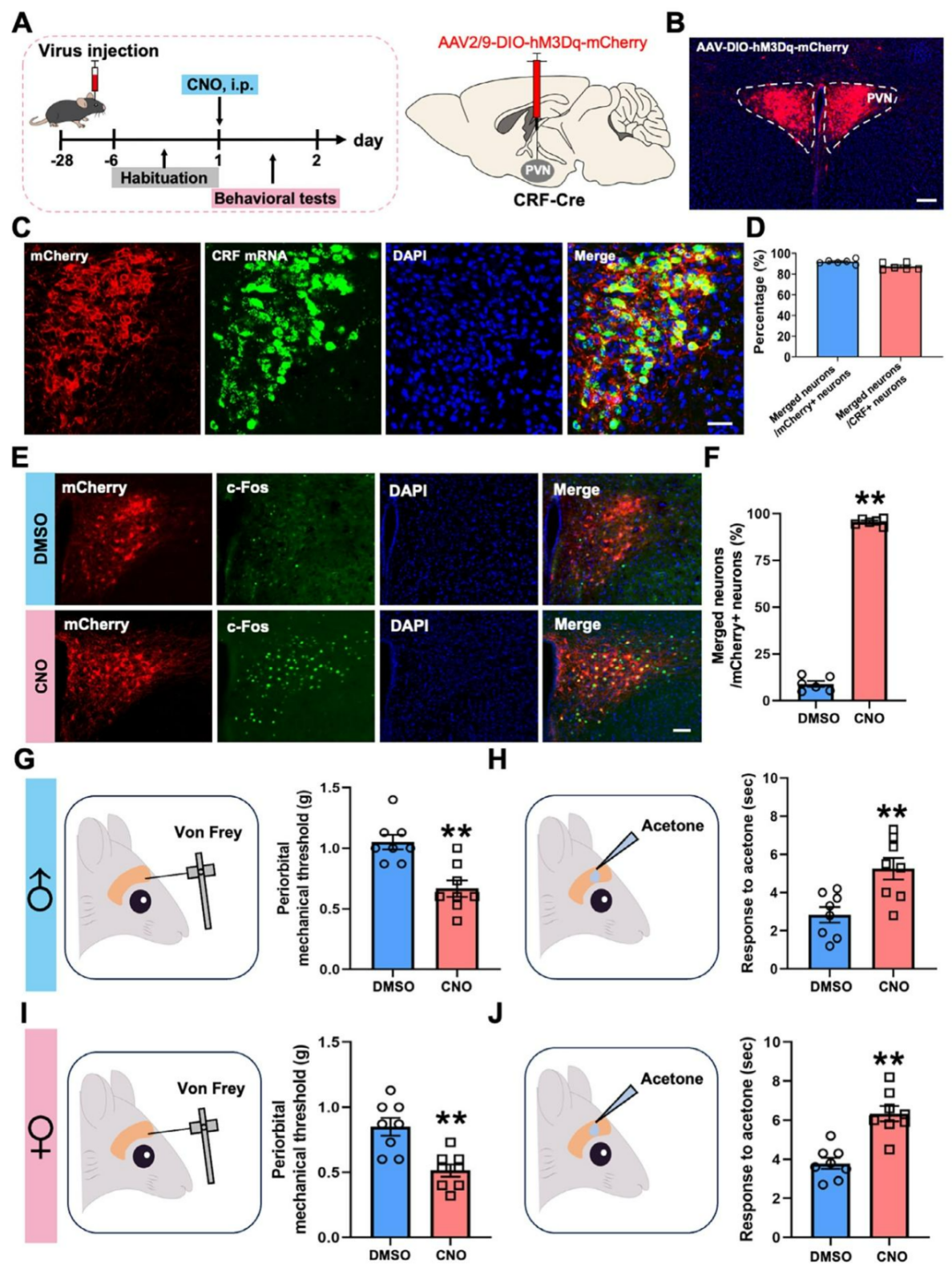
图4. 激活PVNCRF神经元可诱导偏头痛样异常性疼痛
前期病毒示踪结合多重原位杂交实验证实投射至三叉神经脊束核尾侧部(SP5C)的PVN神经元以CRF能表型为主。为验证向SP5C投射的PVNCRF神经元是否参与偏头痛样异常性疼痛,向CRF-Cre小鼠双侧SP5C注射逆行病毒AAV2/Retro-hSyn-DIO-Flp-EGFP,向双侧PVN注射AAV2/9-EF1a-fDIO-hM4Di-mCherry(图5A、B),实现对PVNCRF–SP5C投射神经元的精准靶向,双荧光与RNAscope染色验证了标记的特异性(图5C–F),CNO抑制可显著降低该通路神经元c-Fos表达(图5G、H)。行为学结果表明,抑制PVNCRF–SP5C投射可明显缓解NTG诱导的眶周机械异常性疼痛与冷异常性疼痛(图5I、J)。综上,PVNCRF–SP5C通路是介导偏头痛样异常性疼痛的关键传出通路。
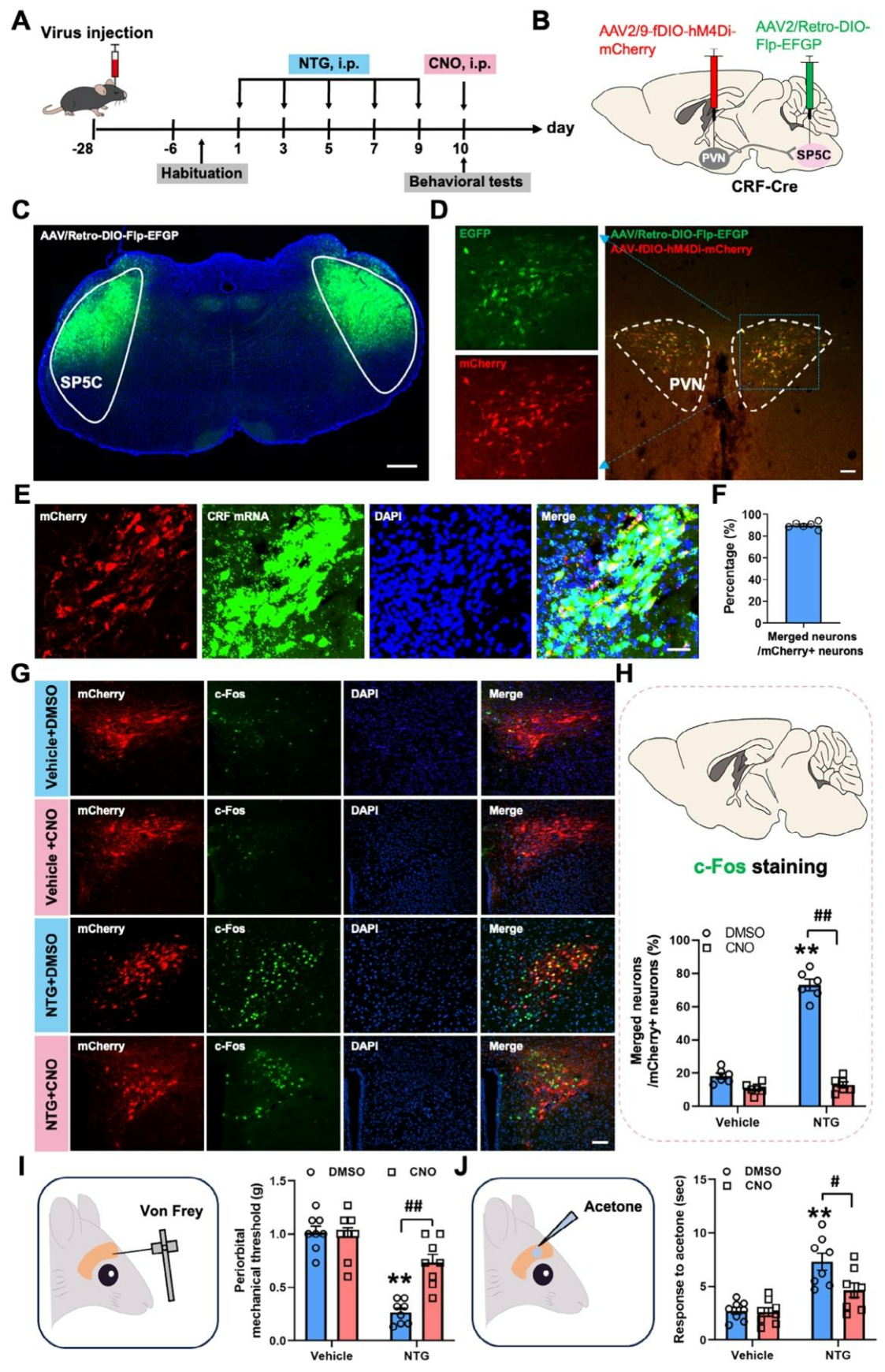
图5. PVNCRF通过输出至SP5C调控NTG诱导的偏头痛样异常性疼痛
为阐明PVNCRF神经元向SP5C投射的解剖与功能意义,在CRF-Cre小鼠中,向PVN共注射利用Cre依赖的跨单顺向突触病毒系统AAV2/9-UL26.5P-DIO-cmgD和AAV2/9-hSyn-DIO-EGFP-T2A-HER2CT9,注射14天后向同一部位注射H129ΔgD-hUbc-mCherry-P2A-scHer2::gD(HS06)。结果发现,PVN起始细胞中观察到EGFP信号,SP5C区域观察到强烈的mCherry信号,证实PVNCRF神经元与SP5C存在直接单突触投射(图6A、B);免疫组化进一步证实其支配的SP5C神经元主要为谷氨酸能兴奋性神经元(SP5CGlu)(图6C)。向PVN注射AAV2/1-hSyn-Cre-EGFP,向SP5C注射AAV2/9-CaMKIIα-DIO-hM4Di-mCherry,使受PVN支配的SP5CGlu神经元选择性表达hM4Di(图6D),结果显示小鼠体内观察到局限于PVN的GFP标记神经元和局限于SP5C的mCherry标记SP5CGlu神经元(图6E)。行为学实验发现,抑制该通路可显著减轻NTG诱导的持续性头部异常性疼痛(图6F、G)。综上,PVNCRF–SP5CGlu通路可能通过调控SP5C向ACC/IC的上行伤害性信号传导间接参与偏头痛样异常性疼痛的调控。
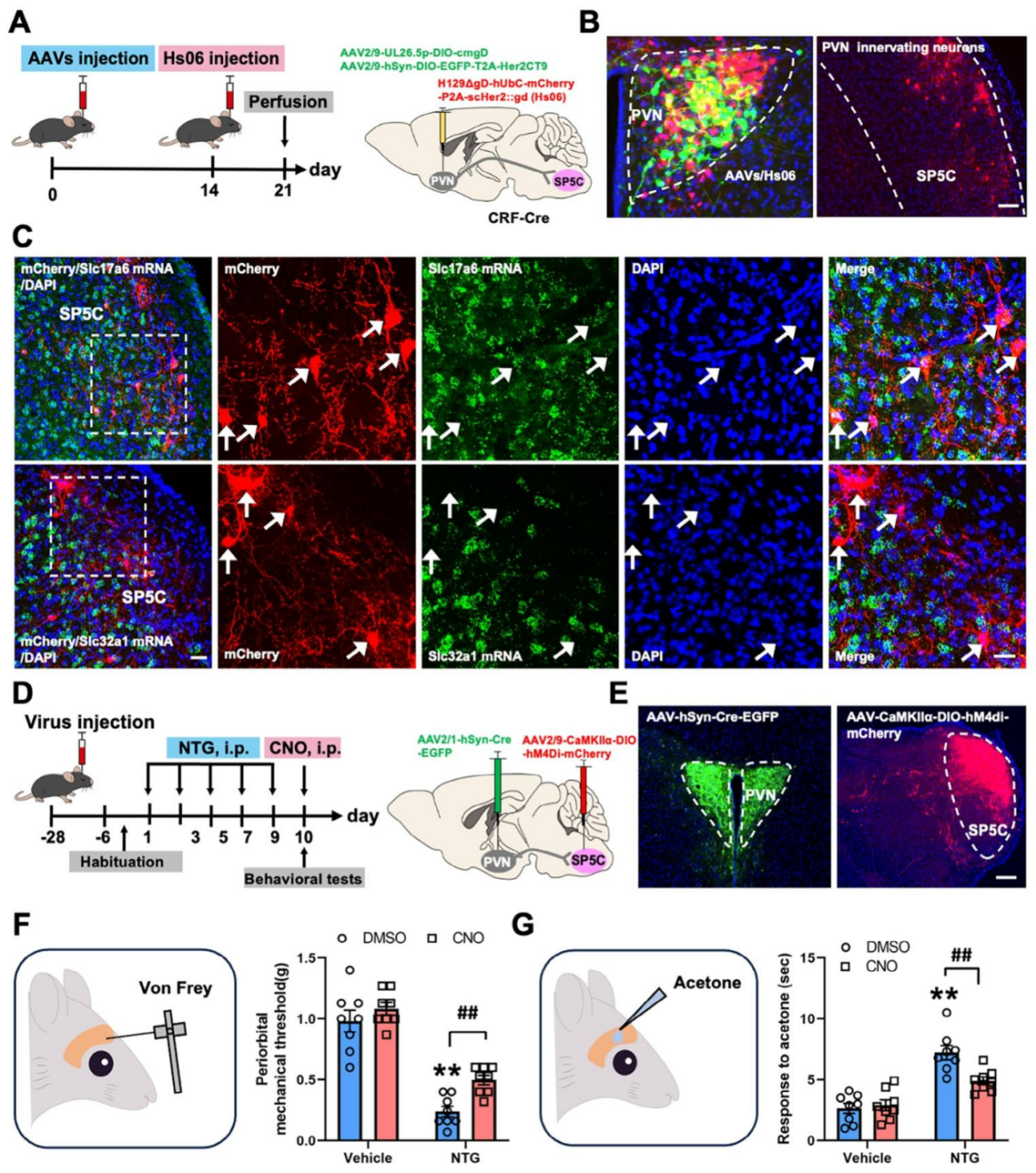
图6. PVNCRF–SP5CGlu通路可介导偏头痛样异常性疼痛
为实时监测NTG给药后SP5C区域CRF神经肽的动态变化,采用双病毒结合光纤记录策略:向PVN单侧注射AAV2/1-hSyn-Cre-mCherry,向同侧SP5C注射AAV2/9-CaMKII-DIO-CRF3.0(AAV2/9-CaMKIIα-DIO-mCherry),结果显示NTG注射后SP5C区域CRF信号显著增强(图7A-E),mCherry荧光信号严格局限于SP5C区域(图7F,G)。全细胞膜片钳记录发现,外源性CRF灌流可显著提高SP5C谷氨酸能神经元的自发放电频率及平均放电频率(图7H,I)。进一步探究CRF对突触传递的调控作用:向三叉神经节注射AAV2/9-TRPV1-Cre与AAV2/9-DIO-ChR2-EGFP混合物,光遗传学激活其向SP5C的投射可诱发出稳定的兴奋性突触后电流,而CRF灌流显著增强该电流振幅(图7J-O)。综上所述,NTG激活的PVNCRF神经元通过释放CRF神经肽,直接兴奋SP5C谷氨酸能神经元并增强三叉神经突触传递效率,诱导偏头痛样异常性疼痛敏化。
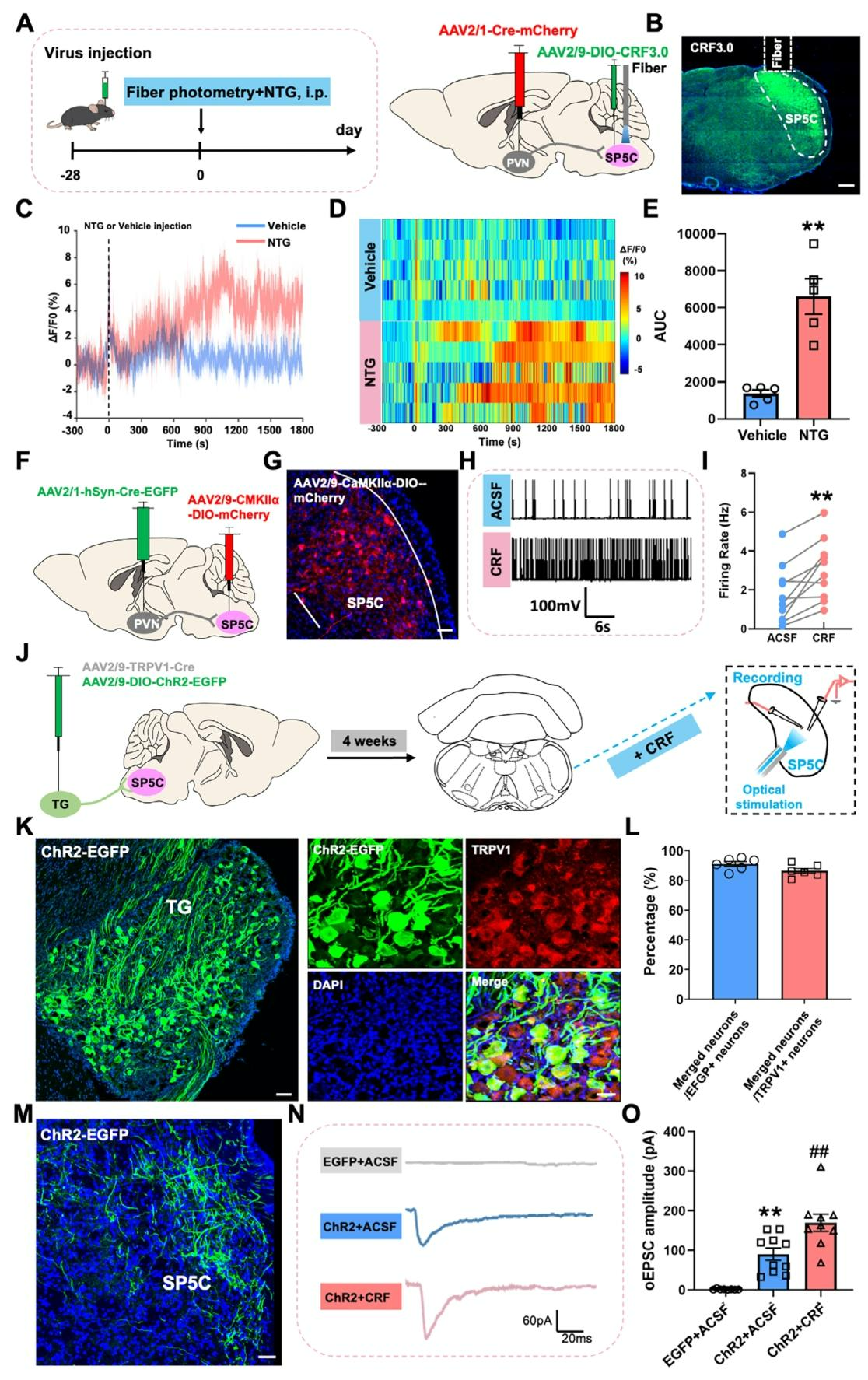
图7. PVNCRF神经元通过释放CRF神经肽激活SP5C并促进三叉神经伤害性传递
为明确CRF调控SP5C兴奋性神经元所涉及的受体亚型,免疫荧光双标染色发现SP5C中兴奋性神经元Vglut2与2型CRF受体(CRFR2)大量共定位,而1型CRF受体(CRFR1)几乎不表达(图8A)。在NTG诱导的慢性偏头痛模型中,向双侧SP5C微量注射CRFR2拮抗剂AS-30可显著缓解眶周机械痛与冷刺激异常性疼痛,而CRFR1拮抗剂Antalarmin无明显作用(图8B–E)。全细胞膜片钳记录表明,外源性CRF可显著增加SP5C神经元的自发放电活性,而预先应用AS-30可有效阻断该兴奋效应(图8F-H);相比之下,Antalarmin预处理未能改变CRF诱导的兴奋性反应(图8I-K),与CRFR1表达缺失的结果一致。综上,SP5CGlu神经元中表达的CRFR2是CRF介导的伤害性信号传导促进作用的关键底物,也是NTG诱导的偏头痛样异常性疼痛的关键介导因子。
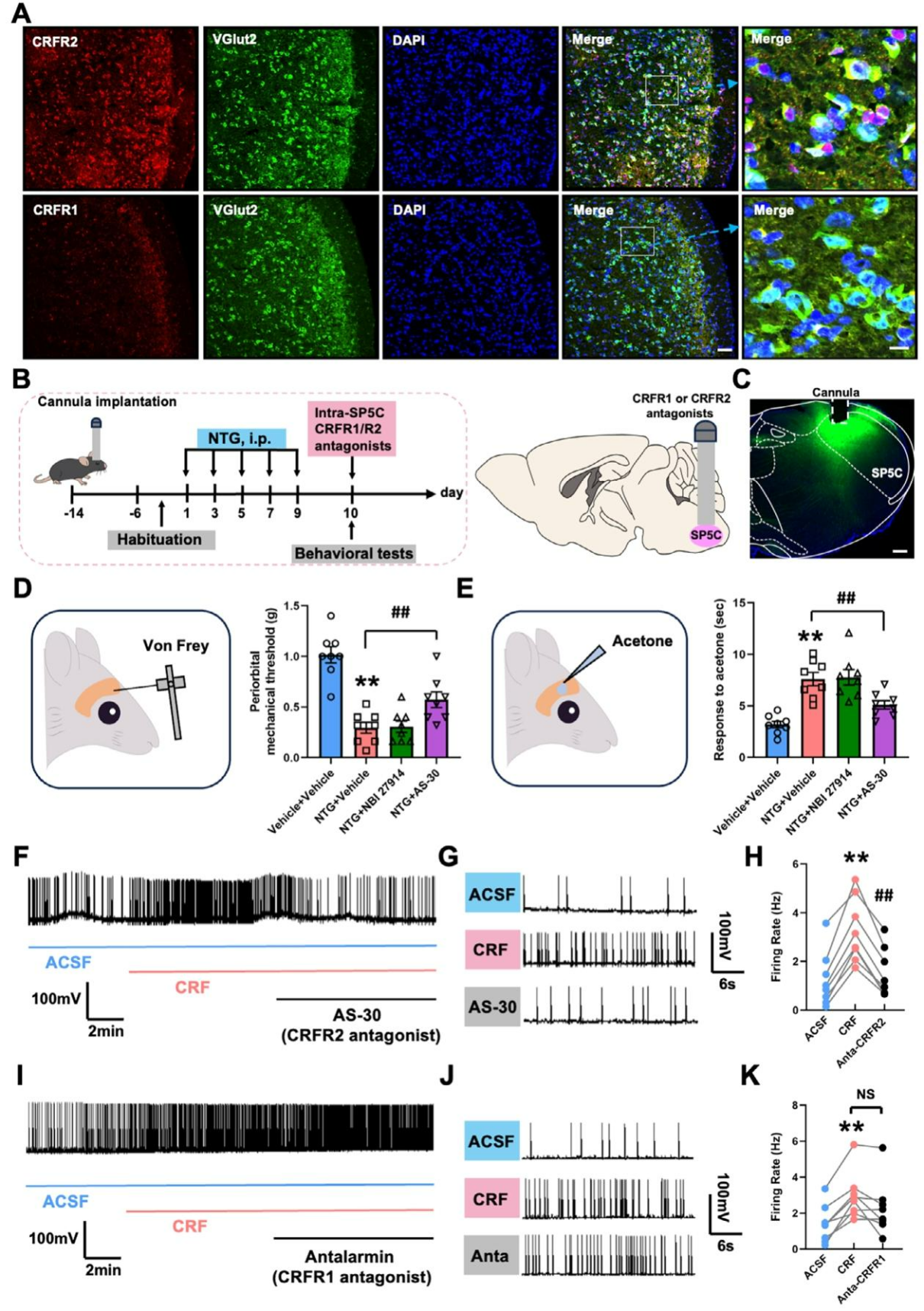
图8. CRF通过激活SP5C中的CRFR2而非CRFR1调控偏头痛样异常性疼痛
为验证动物模型中发现的PVNCRF–SP5CGlu通路是否参与偏头痛患者的发病机制,采用功能磁共振成像检测偏头痛患者与对照组上述脑区的活动差异(图9A、B)。结果显示,与健康对照组相比,8例偏头痛患者双侧大脑半球的PVN和SP5C区域低频振幅值均出现显著改变(图9C-F),提示小鼠模型中鉴定的PVN-SP5C神经环路调控机制可能同样适用于偏头痛患者。
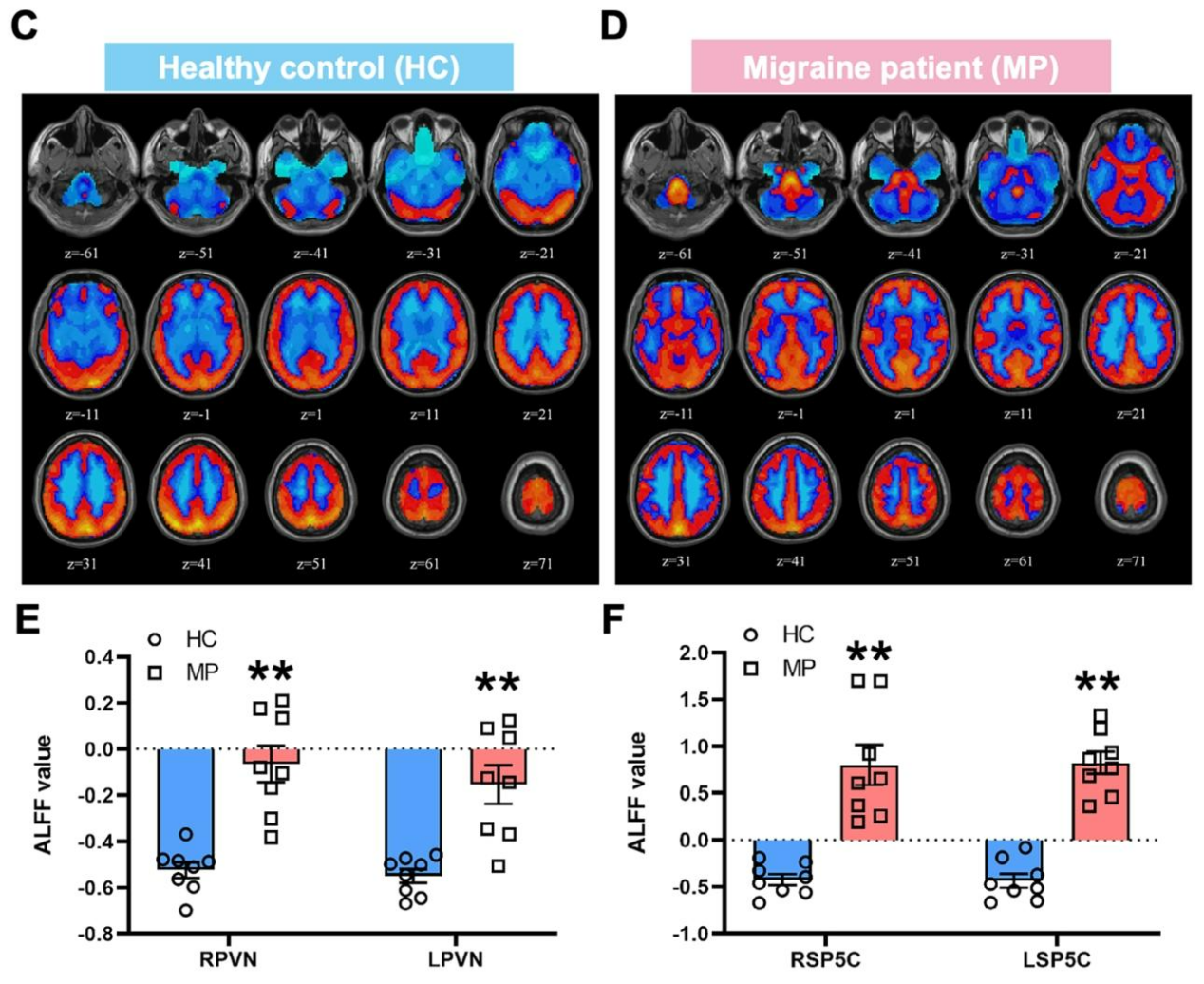
图9. 偏头痛患者PVN和SP5C区域存在功能活动异常
本文揭示了一条全新的偏头痛关键神经环路:PVNCRF通过单突触直接支配SP5CGlu,在偏头痛状态下过度释放CRF神经肽并选择性激活SP5CGlu上的CRFR2受体,增强三叉神经伤害性信号传递,最终引发偏头痛样异常性疼痛,该环路异常在偏头痛患者中也经fMRI得到验证,为偏头痛提供了全新的发病机制解释与精准治疗靶点。
本文使用的工具病毒布林凯斯均可提供:
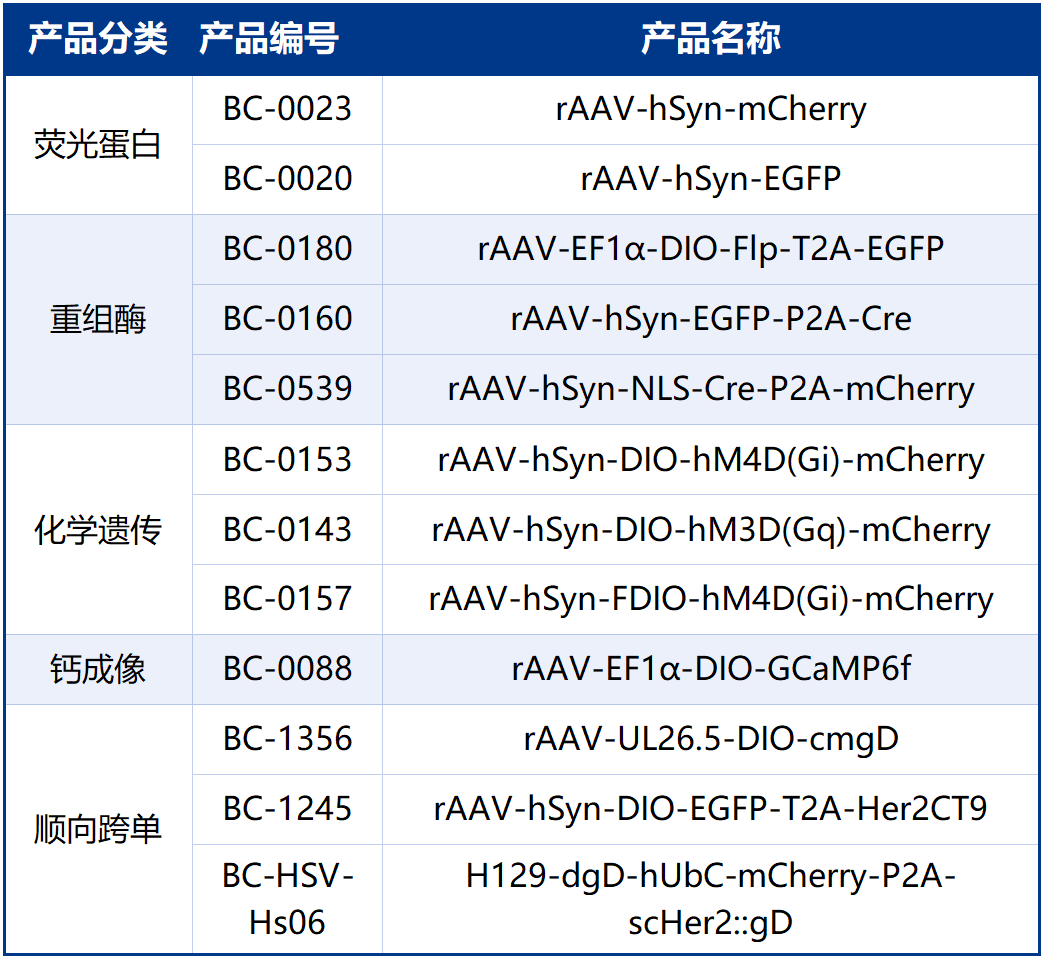
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。