人类痛觉敏感性存在昼夜波动,神经性疼痛、类风湿性关节炎患者的疼痛症状在傍晚显著加剧,但背后神经机制尚未明确。中枢神经系统虽存在节律性变化,但神经元活动昼夜节律与痛觉敏感性的直接关联证据有限;疼痛加工脑区在病理痛下的日间活动模式未被定义,中枢主时钟如何协调疼痛相关脑区活动也未知。
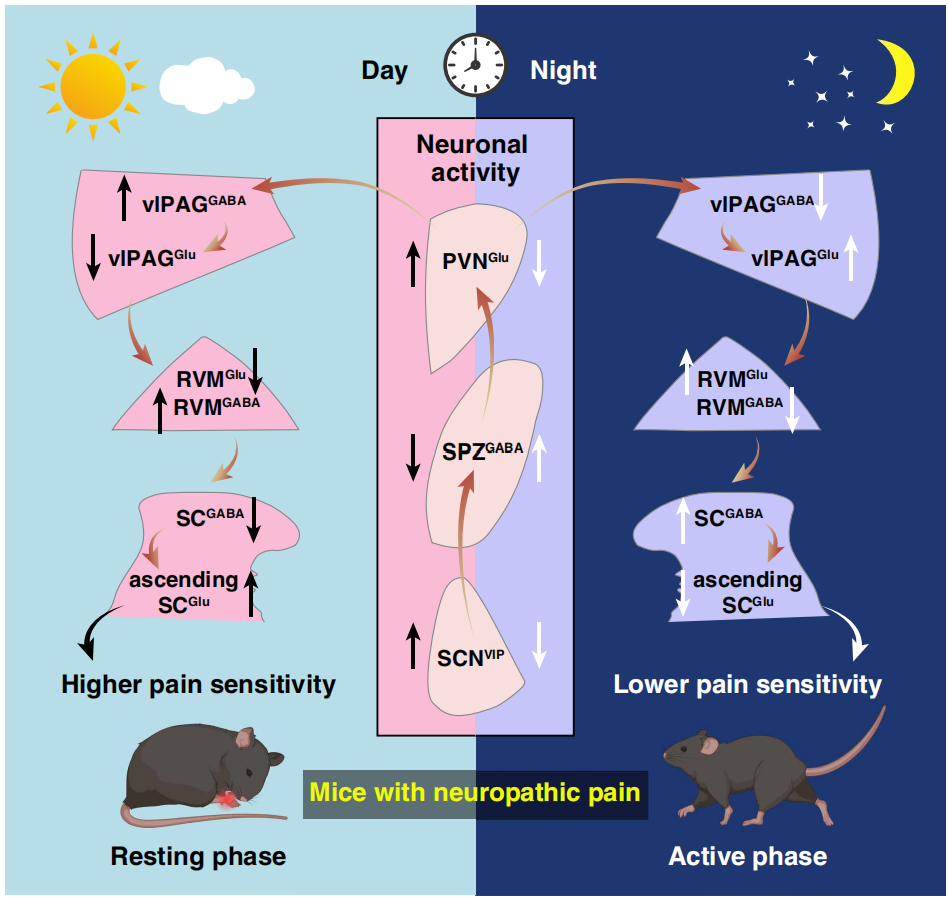
2026年3月19日,中国科学技术大学张智、晋艳、钱俊超团队在Science上发表了题为“Hypothalamic clock governs circadian pain”的研究论文,首次揭示下丘脑主时钟调控慢性疼痛昼夜节律的神经环路机制,发现神经性疼痛小鼠在白天(静息期,ZT5)痛觉敏感性更高、夜间(活动期,ZT14)更低,这一节律由SCNVIP→SPZGABA→PVNGlu→vlPAGGABA多突触环路驱动,并通过vlPAG→RVM→脊髓的下行镇痛系统实现,其中SCN的VIP神经元是核心调控节点,SPZ为关键的抑制性中继站,该发现为慢性疼痛的时间疗法提供了全新的机制框架和靶点方向。
中国科学技术大学博士后卫鸿芮、博士生娄倩倩、博士生李乐娴、博士生唐兰为该论文的第一作者。中国科学技术大学生命科学与医学部张智、晋艳、钱俊超为该论文的共同通讯作者。
小鼠活动集中于夜间、休息于白天。为了探究其昼夜疼痛敏感性差异,作者通过坐骨神经慢性缩窄损伤(CCI)建立神经性疼痛模型,在12h光暗环境中,于8个时间点(ZT2、ZT5等)监测机械及热伤害性感受阈值(图1A)。结果显示,两种阈值呈昼夜波动,ZT17达峰值,ZT5达谷值(图1B)。CCI 7d小鼠在黑暗期首个测试点ZT14的痛阈显著高于ZT5(图1C),后续实验选用ZT14检测。痛阈昼夜节律在CCI术后至少持续14天,且后爪注射完全弗氏佐剂(CFA)诱导的炎症痛模型中也存在类似趋势,表明患有神经性疼痛或炎症性疼痛的小鼠白天(休息期)痛敏更高、夜间(活动期)更低。将CCI小鼠置于持续黑暗环境以消除光照输入,其痛敏仍有昼夜变化,但CT14与CT5的痛阈比值降低,说明痛敏节律由外源性光照和内源性昼夜节律共同驱动。
鉴于下丘脑视交叉上核(SCN)的生物钟功能已有大量报道,作者探究其活动是否与疼痛行为节律相关。参照以往研究,向CCI 7d小鼠SCN注射AAV-jGCaMP7s病毒,结果显示CCI小鼠SCN神经元白天(ZT2、ZT5等)Ca2+事件频繁、峰值高,夜间(ZT14等)则降低;ZT5时Ca2+活动及Fos-TRAP标记神经元数量均高于ZT14,表明SCN神经元活动昼夜变化与痛敏波动相关。已知SCN中血管活性肠肽(VIP)阳性神经元(SCNVIP)和精氨酸加压素(AVP)阳性神经元(SCNAVP)调控节律行为,向其注射AAV-DIO-jGCaMP7s后发现,两种神经元在ZT5的Ca2+事件频率和峰值均高于ZT14(图1D-F)。向VIP-Cre和AVP-Cre小鼠SCN注射病毒以抑制/激活两种神经元(图1G、1J)。化学遗传学抑制ZT4的SCNVIP神经元,可使ZT5痛阈升高至接近ZT14水平(图1H);激活ZT14的SCNVIP神经元,可使痛阈降低至ZT5水平(图1K)。连续抑制/激活也呈现类似效果(图1I、1L)。而调控SCNAVP神经元不影响痛阈昼夜波动。综上,仅SCNVIP神经元的节律性活动是CCI小鼠痛敏昼夜节律所必需的。
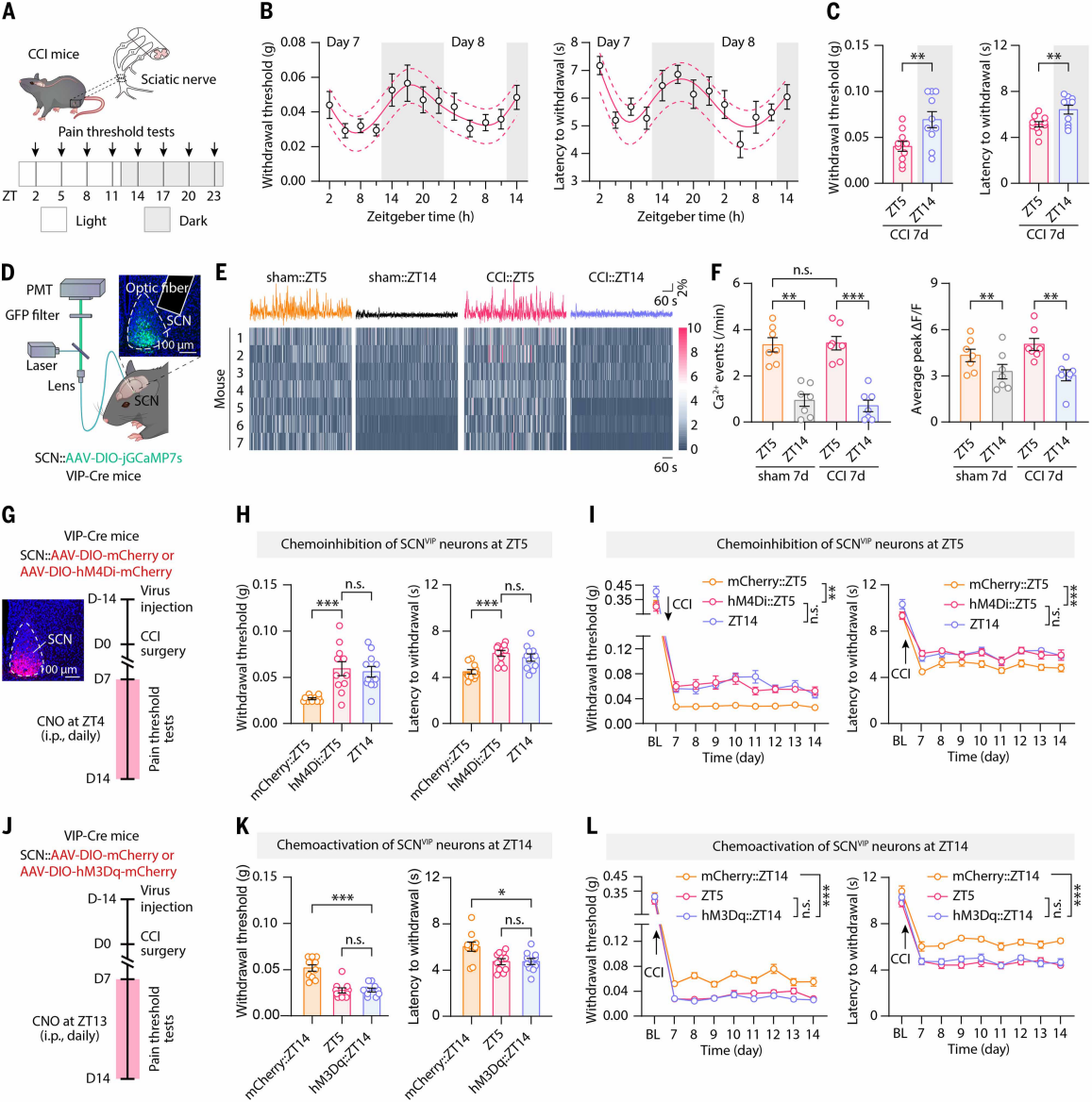
图1. CCI小鼠疼痛敏感性昼夜节律所需的节律性SCN活动
由于SCN并非参与调节或处理疼痛信号的经典脑区,作者接下来试图筛选出具有节律性活动的疼痛相关脑区。Fos-TRAP神经元标记实验显示,与假手术对照组对应脑区相比,CCI小鼠的多个脑区中tdTomato⁺TRAP标记神经元数量更多,包括mPFC、ACC、CeA、lPAG、vlPAG等脑区。标记结果显示CeA、lPAG、vlPAG和DRN区域中,ZT5时的tdTomato⁺TRAP标记神经元数量显著多于ZT14,表明这些脑区在白天的神经元反应性高于夜间。由于在vlPAG中观察到tdTomato⁺神经元的ZT14/ZT5比值最低,且vlPAG是已知的下行镇痛系统组成部分,作者接下来探究该区域是否参与神经性疼痛模型小鼠伤害性感受敏感性的昼夜变化。鉴于vlPAG中的GABA能神经元(vlPAGGABA)此前被证实参与促进伤害性感受反应,作者通过在体多电极记录和微内镜Ca2+成像,评估自由活动的Vgat-Cre小鼠中vlPAGGABA神经元的活动节律性。在对激光刺激(473 nm,20 Hz)诱发的锋电位波形进行特征分析后(图2A-D),发现CCI 7d小鼠中,vlPAGGABA神经元的放电频率ZT5高于ZT14(图2E、2F)。此外,向Vgat-Cre小鼠vlPAG注射AAV-DIO-GCaMP6m病毒后进行微内镜Ca2+成像(图2G、2H),结果显示,与假手术小鼠相比,CCI小鼠vlPAGGABA神经元的Ca2+瞬变频率升高,且ZT5时高于ZT14(图2I-K)。这些数据共同表明,vlPAGGABA神经元的节律性活动与疼痛敏感性的昼夜变化同步。
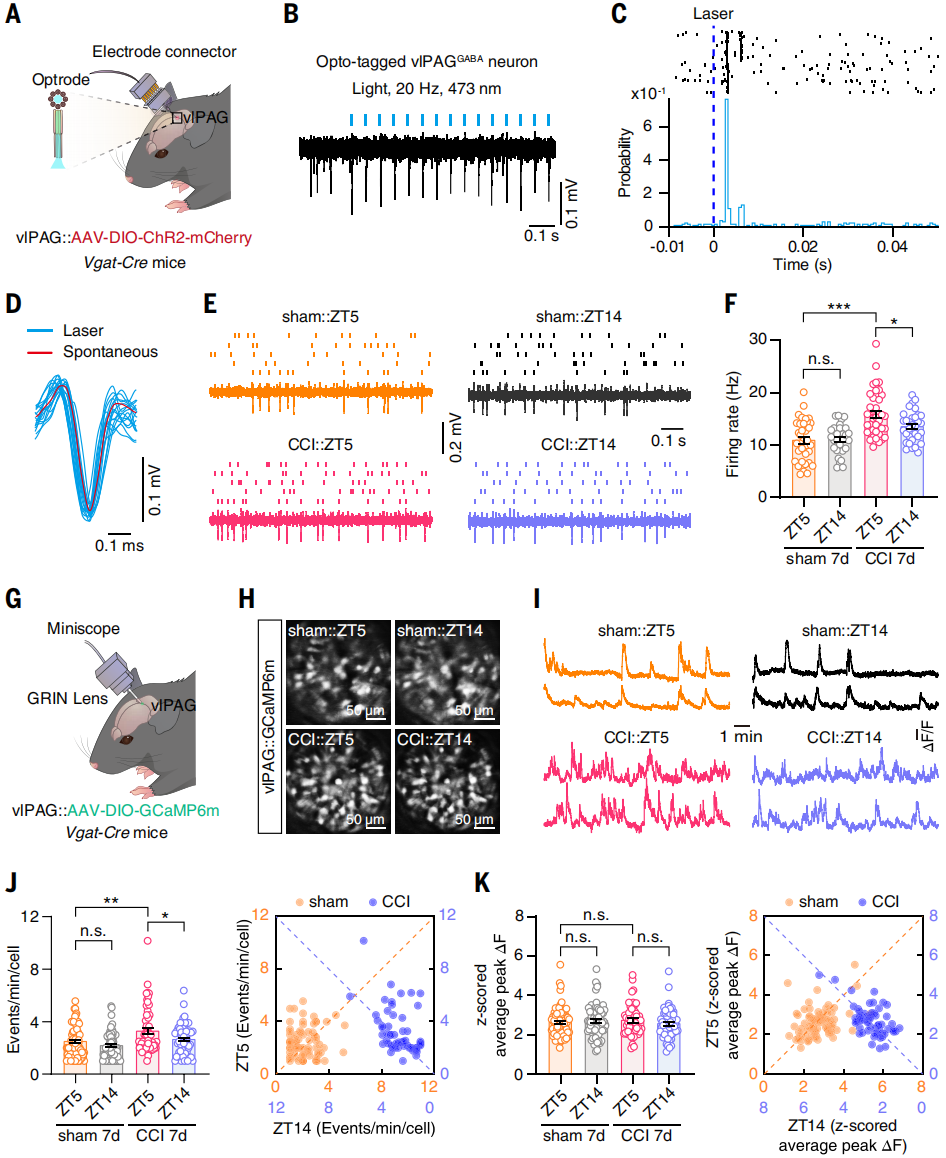
图2. CCI小鼠vlPAGGABA神经元活动的日节律性变化
作者探究CCI小鼠vlPAGGABA神经元的节律性活动是否由SCN直接输入诱导。向Ai9小鼠SCN注射AAV1-hSyn-Cre顺行跨单突触病毒(图3A),结果显示SPZ、PVN等脑区有tdTomato⁺神经元,但vlPAG及经典疼痛相关脑区无此信号(图3B),表明SCN不直接投射至vlPAG。为了寻找SCN下游直接投射至vlPAG的脑区,向Vgat-Cre小鼠vlPAG注射辅助病毒及RV病毒进行逆行示踪(图3C)。作为SCN主要下游区域,PVN的EGFP⁺信号最多(图3D),其中85.3%与谷氨酸抗体共定位(图3E、3F)。向Ai9小鼠PVN注射AAV1-hSyn-Cre顺行示踪(图3G),vlPAG中61.2%的tdTomato⁺神经元与GABA抗体共染色(图3H-J)。为了验证PVNGlu→vlPAGGABA环路的功能性突触连接,向PVN注射AAV-Vglut2-ChR2-EGFP病毒,向Vgat-Cre小鼠vlPAG注射AAV-DIO-mCherry病毒(图3K)。脑片全细胞膜片钳显示,光刺激PVNGlu神经末梢可诱发出vlPAGGABA神经元的EPSCs,该电流可被TTX消除、TTX+4-AP恢复,加入DNQX(AMPA受体拮抗剂)后几乎完全阻断(图3L),证实二者存在功能性单突触谷氨酸能连接。
CCI 7d TRAP2;Ai14小鼠标记显示,PVN的tdTomato⁺神经元ZT5多于ZT14。向vlPAG注射逆行AAV-Vglut2-Cre、PVN注射AAV-DIO-GCaMP6m后,光纤光度记录显示,CCI小鼠中ZT5时PVNGlu神经元Ca2+事件频率高于ZT14(图3M-O),假手术组无差异,表明其存在昼夜节律。光遗传学调控显示,向PVN注射AAV-DIO-eNpHR-EYFP病毒3周后,ZT5光抑制vlPAG中PVNGlu神经末梢,可升高CCI小鼠痛阈(图3P、3Q);ZT14光激活则降低痛阈。综上,PVNGlu→vlPAGGABA环路的节律性活动驱动CCI小鼠痛敏昼夜节律。
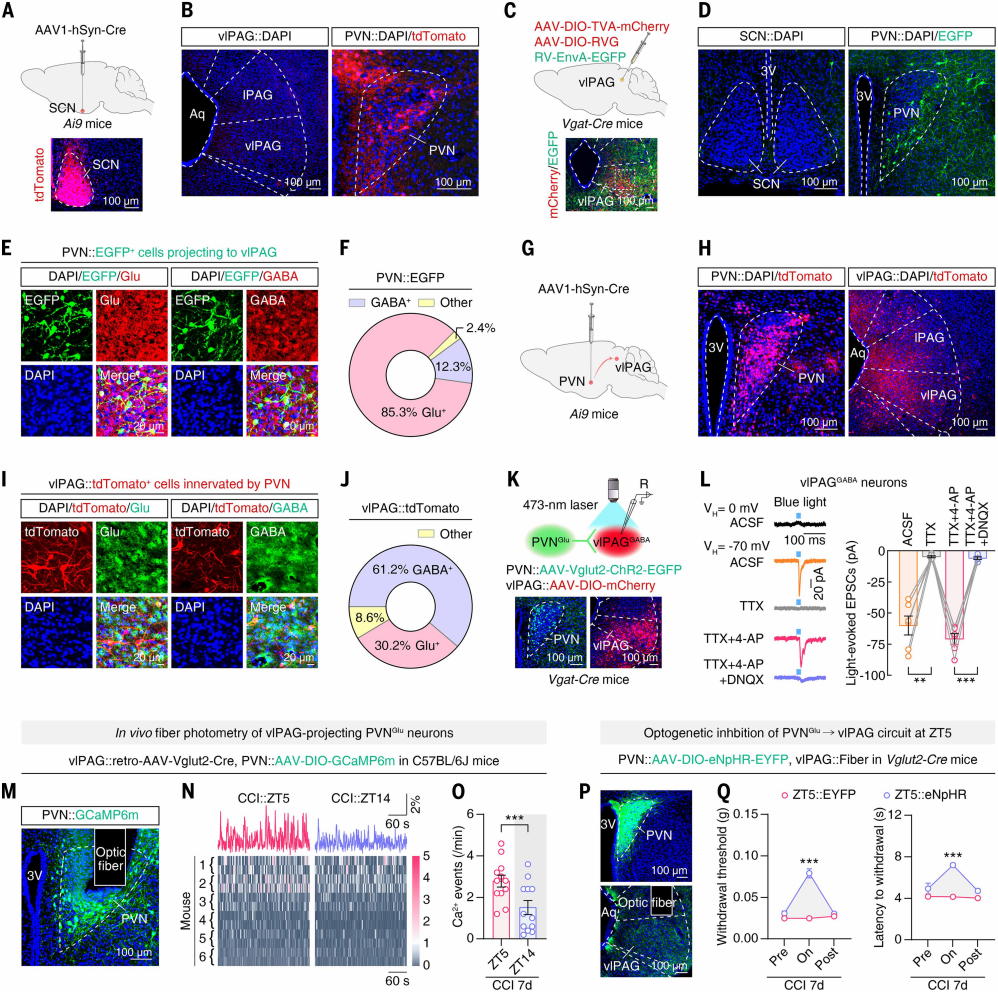
图3. PVNGlu→vlPAGGABA环路的节律性活动介导昼夜疼痛
已知SCN主要由抑制性GABA能神经元构成,也可发挥兴奋性作用。已有研究显示,电刺激SCN可诱发PVN神经元的单突触抑制性和兴奋性突触后电位。为了探究CCI小鼠白天痛敏更高是否由SCN向PVN直接兴奋性输入导致,作者对SCN注射AAV-DIO-ChR2-EYFP、PVN植入光纤的CCI 7d VIP-Cre小鼠,进行光遗传学调控及行为学测试(图4A)。ZT5激活PVN内SCNVIP神经元末梢,可升高痛阈、降低痛敏(图4B);ZT14直接光激活SCNVIP神经元,则降低痛阈(图4C、4D)。Vgat-Cre小鼠中光激活SCN GABA能神经元也获类似结果。这表明SCN不仅直接向PVN投射抑制性信号,还可能通过中间抑制性脑区对PVN发挥去抑制作用,实现两者神经元活动的节律同步。
为了探究SCN下游抑制性核团对PVNGlu→vlPAGGABA环路的调控,采用三重逆行示踪:向小鼠vlPAG注射逆行AAV-Vglut2-Cre 1周后,向PVN注射辅助病毒和RV-ΔG-EGFP(图4E、4F)。结果在SPZ(SCN主要下游靶点,由抑制性GABA能神经元组成)检测到EGFP⁺细胞(图4G),提示SPZGABA神经元支配投射至vlPAG的PVNGlu神经元。向Vgat-Cre小鼠SPZ、PVN、vlPAG分别注射对应病毒后,脑片膜片钳记录显示,蓝光刺激可在mCherry⁺vlPAGGABA神经元中诱发出DNQX敏感的EPSCs(图4H、4I),证实受SPZ支配的PVNGlu神经元向vlPAGGABA神经元发送单突触兴奋性投射。逆行单突触示踪显示,向PVN注射逆行AAV-Vgat-Cre、SPZ注射相关病毒后,SCN中出现大量EGFP⁺细胞(图4J-L),表明SCN支配投射至PVN的SPZGABA神经元。向Vglut2-Cre小鼠相关脑区注射病毒后,光刺激PVN内ChR2阳性末梢,可诱发mCherry⁺PVNGlu神经元产生IPSCs,该电流可被PTX消除(图4M-N),证实受SCN支配的SPZGABA神经元向PVNGlu神经元发送单突触抑制性投射。综上,本研究明确了SPZGABA→PVNGlu→vlPAGGABA及SCN→SPZGABA→PVN环路的解剖连接,提示SPZ是SCN与PVNGlu神经元之间的抑制性中继站。
已有研究表明,SPZGABA神经元可作为必需中继站调控昼夜行为。本研究探究SPZ是否在SCN与PVN→vlPAG环路间发挥作用,维持CCI 7d小鼠痛敏昼夜节律。向C57BL/6J小鼠PVN注射逆行AAV-Vgat-Cre、SPZ注射AAV-DIO-jGCaMP8m后,光纤光度记录显示(图4O),假手术组和CCI组中,投射至PVN的SPZGABA神经元ZT14时Ca2+事件频率和峰值均高于ZT5(图4P、4Q),其节律与SCN活动、痛敏同步但反向。为了验证该神经元活动的必要性,向Vgat-Cre小鼠PVN注射逆行AAV-DIO-Flp、SPZ注射AAV-fDIO-Caspase3、vlPAG注射AAV-DIO-jGCaMP8m(图4R)。光纤记录显示,消融投射至PVN的SPZGABA神经元后,ZT5时vlPAGGABA神经元Ca2+活动低于ZT14(图4S、4T)。痛敏测试显示,CCI小鼠ZT5与ZT14的痛敏差异反转(ZT14痛阈低于ZT5)(图4U、4V),证实该SPZ神经元是维持痛敏昼夜节律、确保CCI小鼠白天痛更重的必需细胞。为了探究化学遗传学调控SCN→SPZ→PVN环路对痛敏节律的影响,向CCI 7d小鼠PVN注射逆行AAV-Vgat-Cre、SCN注射AAV1-hSyn-Flp、SPZ注射双依赖型AAV病毒。结果显示,ZT5激活该环路可升高痛阈;ZT14抑制该环路或局部SPZGABA神经元可降低痛阈。综上,SPZ作为抑制性中继站,人工调控可反转神经性疼痛小鼠的痛敏昼夜节律。
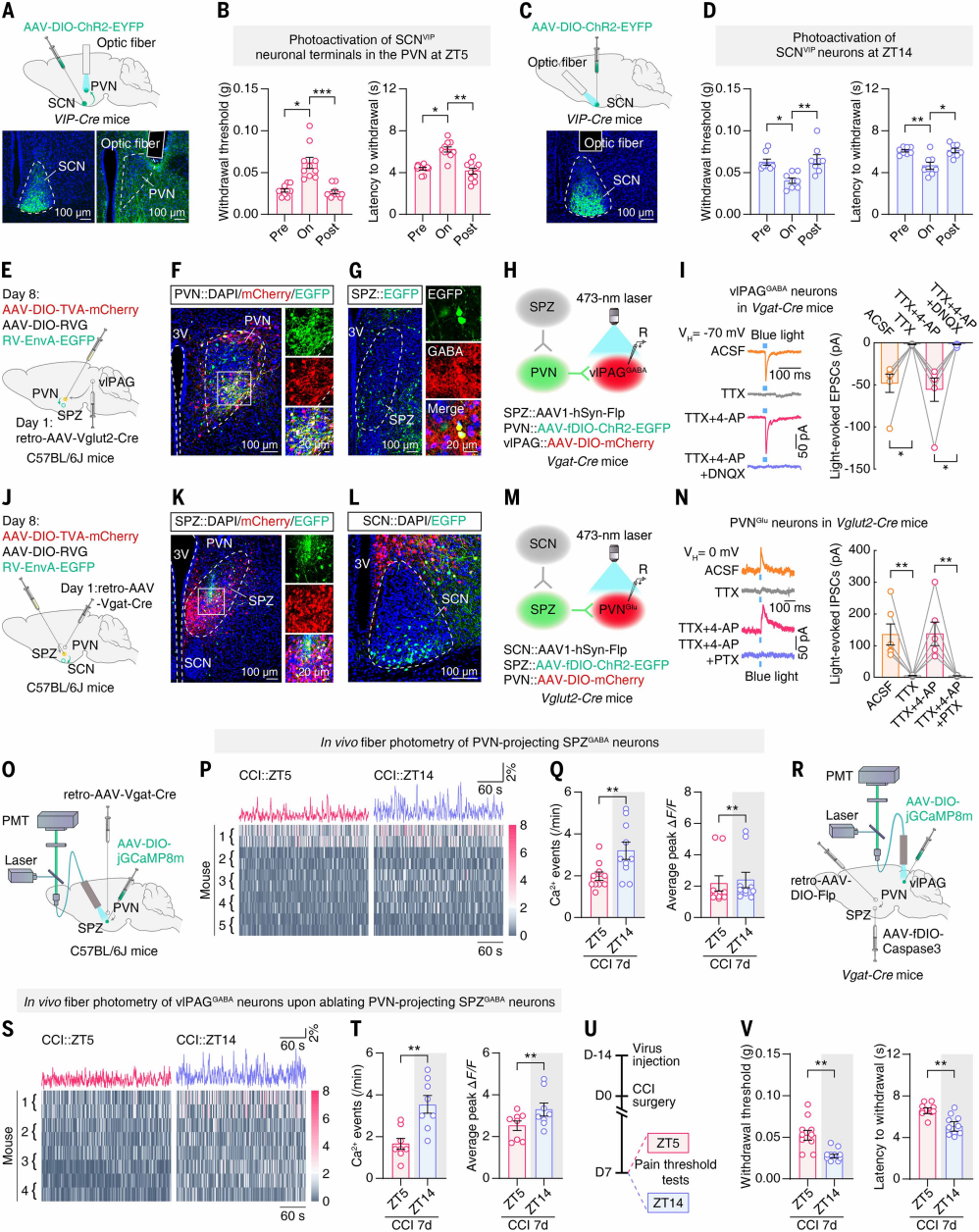
图4. SPZ在维持疼痛敏感度的日常波动中发挥作用
vlPAGGABA神经元是下行疼痛调节网络的关键组成,作者探究其节律性活动对痛敏昼夜节律的调控作用。采用Cre依赖型顺行跨单突触示踪,向C57BL/6J小鼠vlPAG注射AAV1-hSyn-Cre、RVM注射辅助病毒(图5A、5B),两周后向同一RVM位点注射H129-ΔTK病毒。病毒表达后,脊髓背角检测到与GABA抗体共标记的mCherry⁺神经元(图5C),表明受vlPAG支配的RVM神经元投射至脊髓背角GABA能抑制性神经元。向L3-L5脊髓背角注射逆行AAV-hSyn-Cre,再向RVM注射辅助病毒和RV-ΔG-mCherry(图5D、5E)。三周后,vlPAG中mCherry⁺神经元主要为谷氨酸能,少数为GABA能(图5F),说明vlPAGGlu是投射至脊髓的RVM神经元的主要输入来源。
鉴于vlPAGGABA神经元的节律性活动,探究其对环路的驱动作用。在体多电极记录显示,CCI 7d小鼠中vlPAGGlu神经元活动ZT5低于ZT14(图5G、5H),与vlPAGGABA神经元活动相反(ZT5高于ZT14),假手术组无差异,提示vlPAGGlu的节律性活动受vlPAGGABA的抑制性输入调控。多电极记录还显示,CCI 7d小鼠中RVMGlu神经元放电频率ZT5低于ZT14(图5I、5J),RVMGABA神经元ZT5高于ZT14(图5K、5L),假手术组无差异,证实CCI小鼠RVM神经元存在节律性活动。为了验证环路节律对痛敏的调控,向小鼠vlPAG注射AAV1-DIO-Flp、L3-L5脊髓背角注射逆行AAV-hSyn-Cre、RVM注射相应病毒(图5M)。结果显示,ZT5激活该环路可升高CCI小鼠痛阈至接近ZT14水平(图5N);ZT14抑制该环路则降低痛阈至ZT5水平;而ZT14激活或ZT5抑制环路无影响(图5O),表明调控该环路会破坏痛敏昼夜节律。
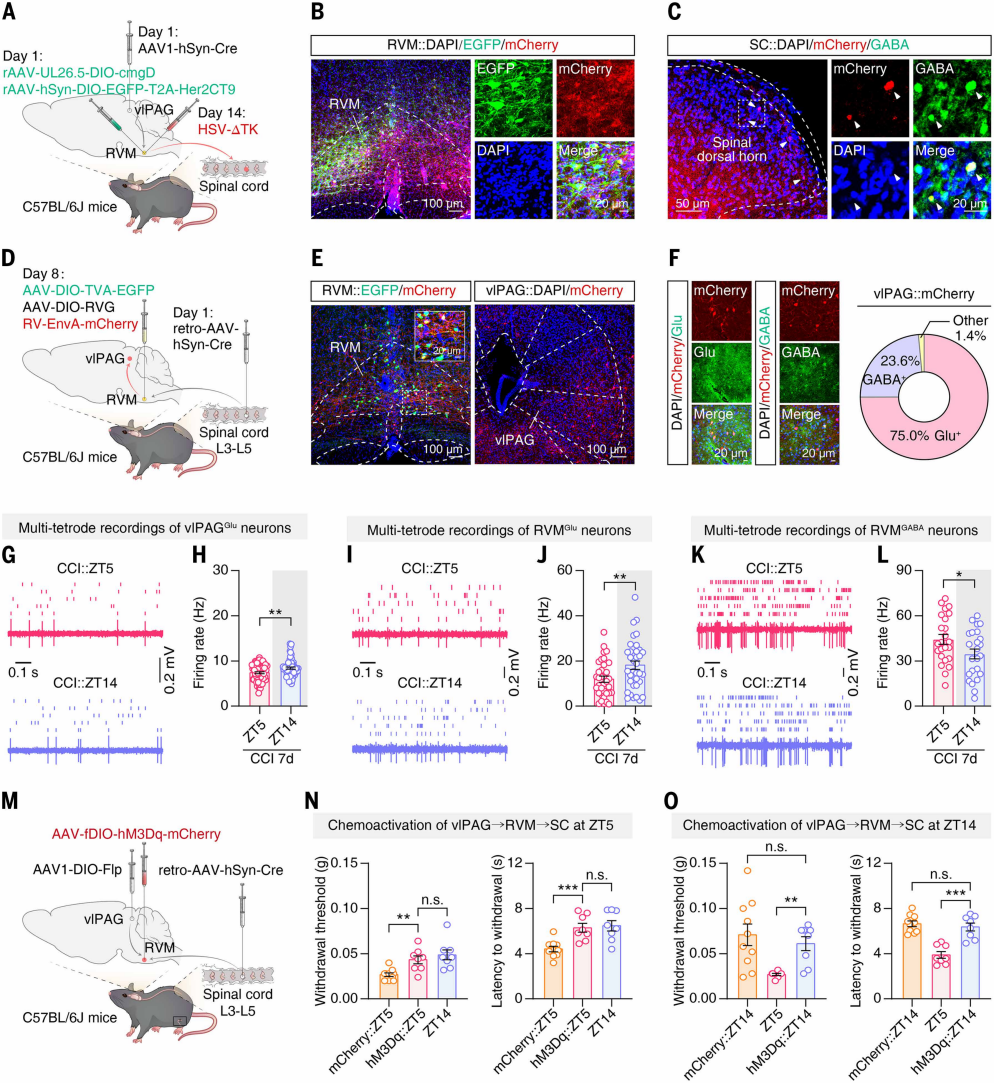
图5. vlPAG→RVM→脊髓环路的节律性活动调控疼痛敏感性的昼夜波动
作者探究下行vlPAG→RVM→脊髓GABA能神经元(SCGABA)环路是否调控脊髓上行投射神经元。已知躯体感觉丘脑腹后外侧核(VPL)是脊髓丘脑束经典中继站,向其注射逆行示踪剂FG,一周后脊髓中出现FG⁺标记,约81.1% FG⁺细胞与谷氨酸抗体共表达。为了明确受RVM支配的SCGABA神经元是否投射至VPL相关SCGlu神经元,将顺行与逆行示踪结合:向RVM注射AAV1-hSyn-Cre,脊髓注射辅助病毒(图6A),后续注射H129-ΔTK病毒和FG。结果显示,EGFP⁺/mCherry⁺共标记细胞为RVM来源起始细胞(图6B),FG⁺细胞(VPL逆行标记)与mCherry⁺细胞共定位(图6C),证实二者存在直接突触连接。为了验证两类神经元的节律性,对脊髓切片进行膜片钳记录(图6D)。CCI 7d小鼠中,受RVM支配的SCGABA神经元,ZT5时动作电位放电频率低于ZT14,基强度无差异(图6E-G);光纤记录显示,其Ca2+活动ZT5低于ZT14,假手术组无差异,证实其存在昼夜节律。此外,CCI 7d小鼠中,VPL逆行标记的FG⁺神经元ZT5兴奋性高于ZT14(图6H-K),SCGlu神经元Ca2+活动ZT5高于ZT14(图6L-N);假手术组无此差异。已知SCGABA神经元可调控脊髓投射神经元,故SCGlu神经元的反相节律可能源于其抑制性输入。
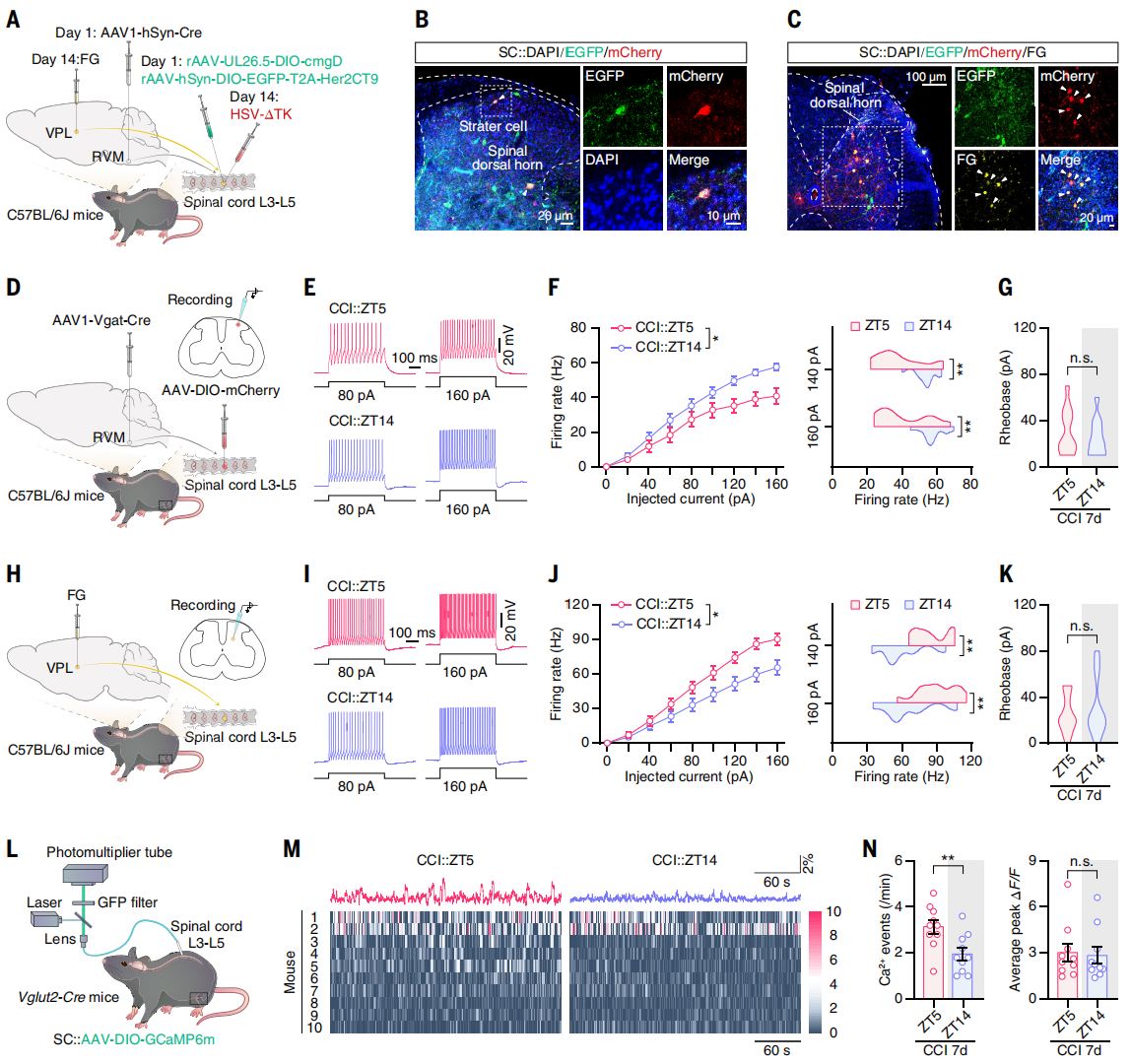
图6. 节律性SCGABA神经元活动通过调节上行SCGlu神经元来同步每日疼痛敏感性
神经性/炎症疼痛小鼠的痛觉敏感性存在内源性昼夜节律,由下丘脑视交叉上核(SCN)这一主时钟调控,SCNVIP神经元是该节律的核心调控节点。疼痛昼夜节律由SCNVIP→SPZGABA→PVNGlu→vlPAGGABA多突触环路驱动,并通过vlPAG→RVM→脊髓的下行镇痛系统实现,其中SPZ是SCN与PVN间不可或缺的抑制性中继站。
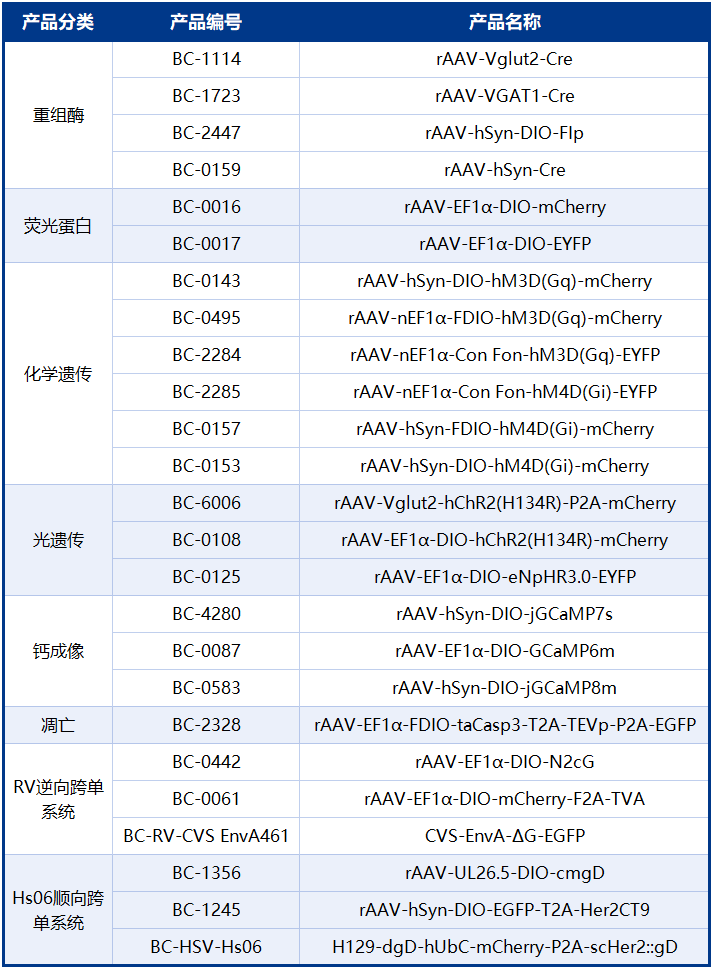
本文使用的工具病毒布林凯斯均可提供:
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。