睡眠紊乱与多种慢性疾病的发病机制相关,包括慢性胃肠道疾病。然而,睡眠紊乱诱导的异常神经信号从大脑传递至肠道的机制仍不明确。肠道作为重要的内分泌器官,负责合成包括5-羟色胺(5-HT)在内的多种神经递质,其中人体内95%的5-HT由肠嗜铬细胞产生,其水平受血清素转运体(SERT)精密调控。5-HT稳态失衡已被证实与多种肠道疾病相关。此外,肠道干细胞(ISC)在维持上皮屏障完整性、损伤修复及稳态维持中发挥关键作用。迷走神经传出纤维作为脑-肠信号传导的核心通路,其功能异常,如慢性应激抑制迷走神经背核(DMV)-迷走神经通路,可显著影响肠道功能。然而,该通路是否通过调控局部5-HT水平,进而影响肠道干细胞功能及肠道上皮稳态,仍有待深入探究。
2026年2月5日,郑州大学于政权、中国科学院深圳先进技术研究院王枫、中国农业大学吕聪、美国加州大学欧文分校MaksimV.Plikus共同通讯在Cell Stem Cell上在线发表题为“Sleep disturbance triggers aberrant activation of vagus circuitry and induces intestinal stem cell dysfunction”的研究论文。该研究揭示了一条睡眠剥夺应答神经环路:DMV神经元感知睡眠剥夺后被过度激活,通过迷走神经释放过量乙酰胆碱,经上皮毒蕈碱受体双向调控(促进释放+抑制再摄取)导致肠道5-HT水平激增,后者通过HTR4介导的氧化应激损害肠ISC功能。靶向该通路的毒蕈碱受体阻断剂(阿托品)、HTR4抑制剂(GR113808)及抗氧化剂(维生素C)可能是缓解睡眠剥夺相关肠道损伤的潜在治疗策略。

郑州大学生命科学学院于政权教授、中国科学院深圳先进技术研究院脑认知与脑疾病研究所王枫研究员、中国农业大学营养与健康研究院吕聪教授和美国加利福尼亚大学欧文分校发展与细胞生物学系教授MaksimV.Plikus为该论文的共同通讯作者。该团队的张明鑫博士、吴茜博士、博士生刘笛为该论文共同第一作者。
为探究睡眠紊乱影响肠道生理功能的脑-肠通讯机制,研究采用机械性睡眠剥夺小鼠模型(图1A),经过2天睡眠剥夺后,小鼠快速眼动(REM)与非快速眼动(NREM)睡眠占比骤降,95%时间清醒,睡眠-觉醒周期严重紊乱(图1B、1C);形态学检测显示小鼠肠道绒毛与隐窝缩短、增殖性上皮细胞减少(图1D、1E),谱系分析显示潘氏细胞数量下降而肠嗜铬细胞数量增加(图1F、1G);Lgr5⁺肠道干细胞与Olfm4⁺干/祖细胞数量显著减少(图1H-1J)。BrdU脉冲追踪实验证实隐窝-绒毛轴细胞迁移减慢(图1K)。体外类器官实验显示睡眠剥夺小鼠隐窝的成类器官能力、生长速度及芽体数量均显著降低(图1L、1M);对睡眠剥夺小鼠进行12Gyγ射线照射后,其肠道再生灶数量及灶内增殖细胞数也明显减少(图1N、1O)。上述结果表明,急性睡眠剥夺可显著扰乱肠道稳态,造成肠道干细胞功能与再生能力的持续性损伤。
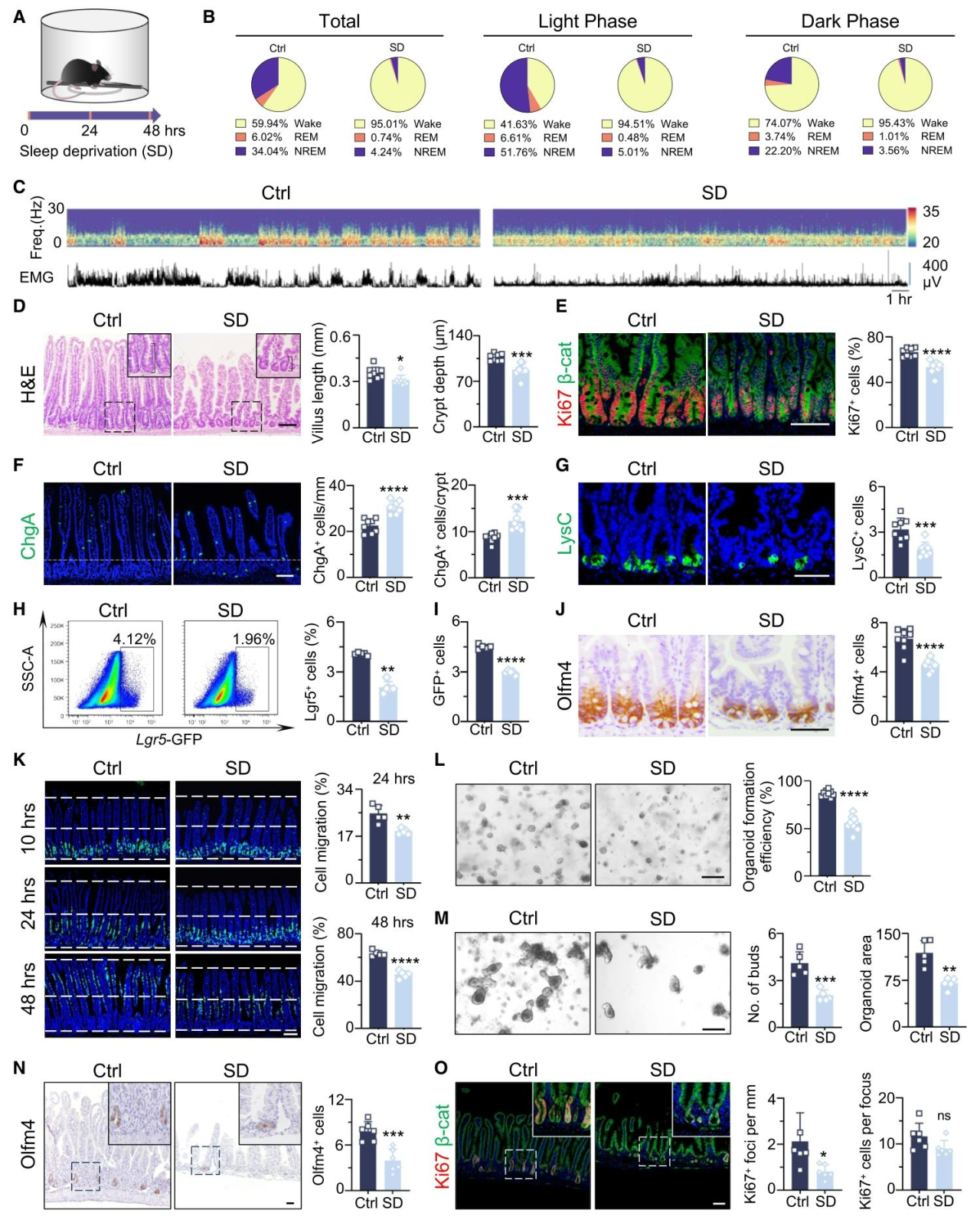
图1.短期睡眠剥夺显著损伤肠道干细胞功能并扰乱肠道上皮细胞更新
为阐明睡眠剥夺损伤肠道干细胞的分子机制,我们对小鼠肠道隐窝进行蛋白质组学分析,GO分析显示“应激应答中的翻译负调控”和“体细胞干细胞群维持的调控”为最富集通路(图2A)。应激诱导的eIF2α磷酸化会促使哺乳动物细胞组装细胞质内非膜结合的致密应激颗粒,是整合应激反应(ISR)的核心触发因子。检测发现,睡眠剥夺小鼠隐窝中翻译应激反应的关键效应因子p‑eIF2α显著升高(图2B),应激颗粒明显增多(图2C),整合应激反应关键分子ATF4、GADD34、GADD153表达上调(图2D),同时自噬体与自溶酶体蓄积(图2E)。KEGG分析显示“泛素介导的蛋白酶体通路”是睡眠剥夺小鼠中第二富集的通路(图2F),泛素化水平在肠道和胃中特异性升高(图2G)。睡眠剥夺可诱导肠道特异性ROS蓄积、DNA损伤增加、抗氧化能力下降(图2H);给予维生素C或N‑乙酰半胱氨酸抗氧化处理,可显著挽救睡眠剥夺导致的肠道损伤,恢复肠道干细胞数量与隐窝结构,并降低p‑eIF2α及泛素化水平(图2I–2M)。以上结果证实,睡眠剥夺诱导的氧化应激会激活肠道干细胞的翻译应激反应,从而损害其功能。
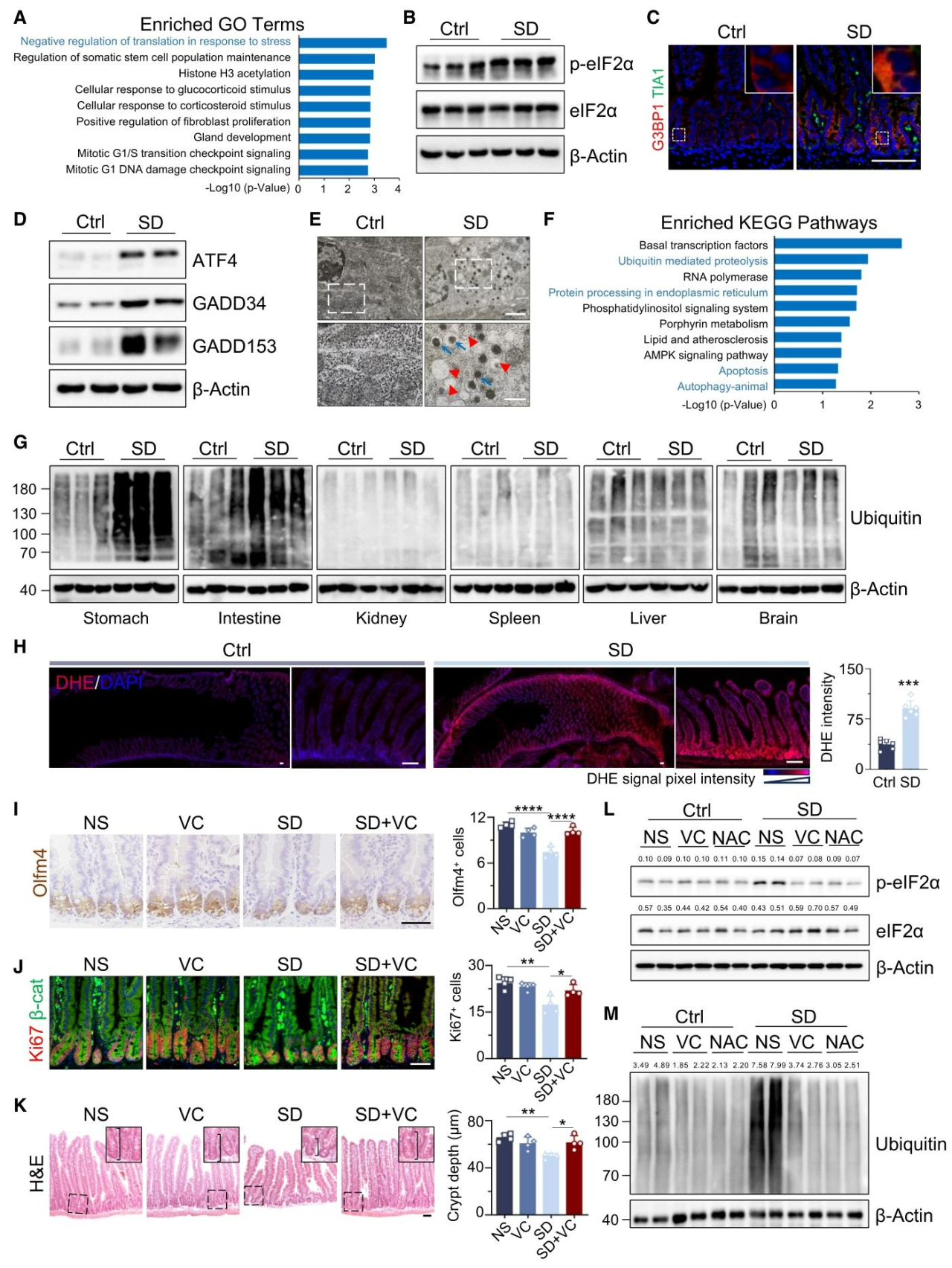
图2.短期睡眠剥夺通过激活翻译应激反应损伤肠道干细胞
利用液相色谱-串联质谱(LC-MS/MS)靶向代谢组学检测发现,睡眠剥夺小鼠肠道内5‑HT及多种色氨酸代谢相关产物(包括TrpA、5-HTP和Kyn,均对5-HT产生至关重要)显著升高(图3A),ELISA进一步证实肠道和血清中5‑HT水平上升(图3B、3C),同时肠道隐窝中5‑HT阳性肠嗜铬细胞数量明显增加(图3D)。体外实验显示,5‑HT处理可诱导肠道类器官发生ROS蓄积与氧化颗粒形成(图3E),并以剂量依赖方式抑制细胞增殖和类器官生长(图3F);体内注射5‑HT可模拟睡眠剥夺表型,引发肠道氧化应激、减少肠道干细胞数量并破坏肠道结构(图3G、3H)。在肠道中,超过90%的5-HT由肠嗜铬细胞合成,色氨酸羟化酶1(Tph1)在此过程中起关键作用,在Tph1敲除小鼠中,睡眠剥夺无法诱导肠道氧化应激升高(图3L)。上述结果证明,睡眠剥夺通过肠嗜铬细胞产生过量5‑HT,进而触发肠道氧化应激,直接导致肠道干细胞功能受损与上皮稳态紊乱。
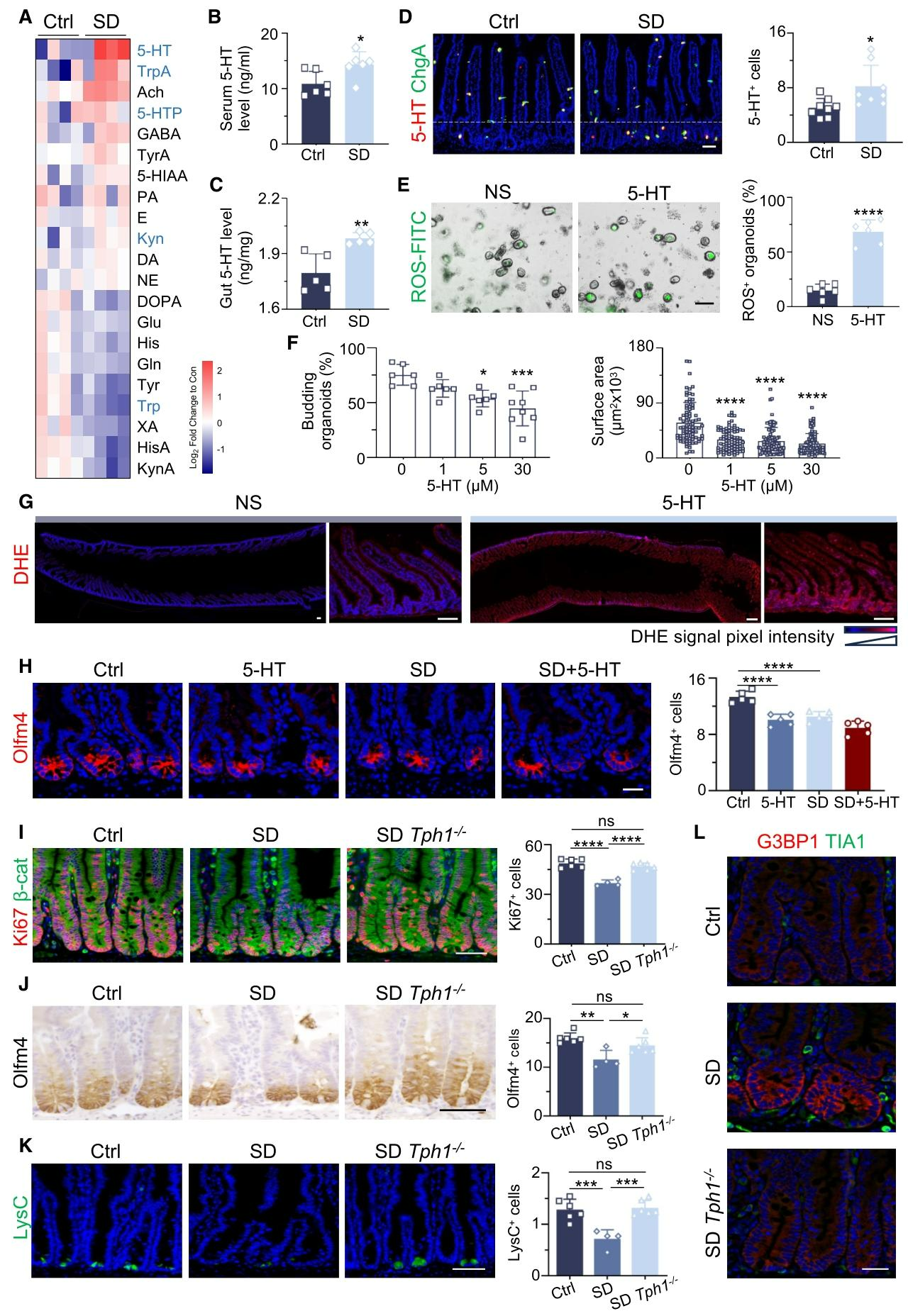
图3.急性睡眠剥夺扰乱5-HT稳态并诱导肠道氧化应激
为阐明肠道干细胞如何响应5-HT,隐窝上皮细胞单细胞测序显示Htr4是肠道干细胞中主要的5‑HT受体(图4A),且睡眠剥夺可显著上调肠道隐窝中HTR4的转录与蛋白水平(图4B、4C)。体外实验表明,HTR4激动剂普芦卡必利可模拟5‑HT效应,抑制类器官生长、增加ROS及泛素化水平;而HTR4拮抗剂SB203186可逆转5‑HT对类器官的损伤(图4D、4E)。体内实验显示,普芦卡必利可复制睡眠剥夺所致肠道损伤;HTR4拮抗剂GR113808则可挽救睡眠剥夺诱导的肠道表型。进一步构建条件性敲除小鼠(Villin‑Cre;Htr4fl/fl),其中Htr4在肠道上皮中特异性缺失,实验证实,敲除Htr4可显著抵御睡眠剥夺引发的肠道损伤(图4F–4H)。以上结果证明,过量5‑HT通过肠道上皮HTR4受体介导睡眠剥夺对肠道干细胞的病理损伤。
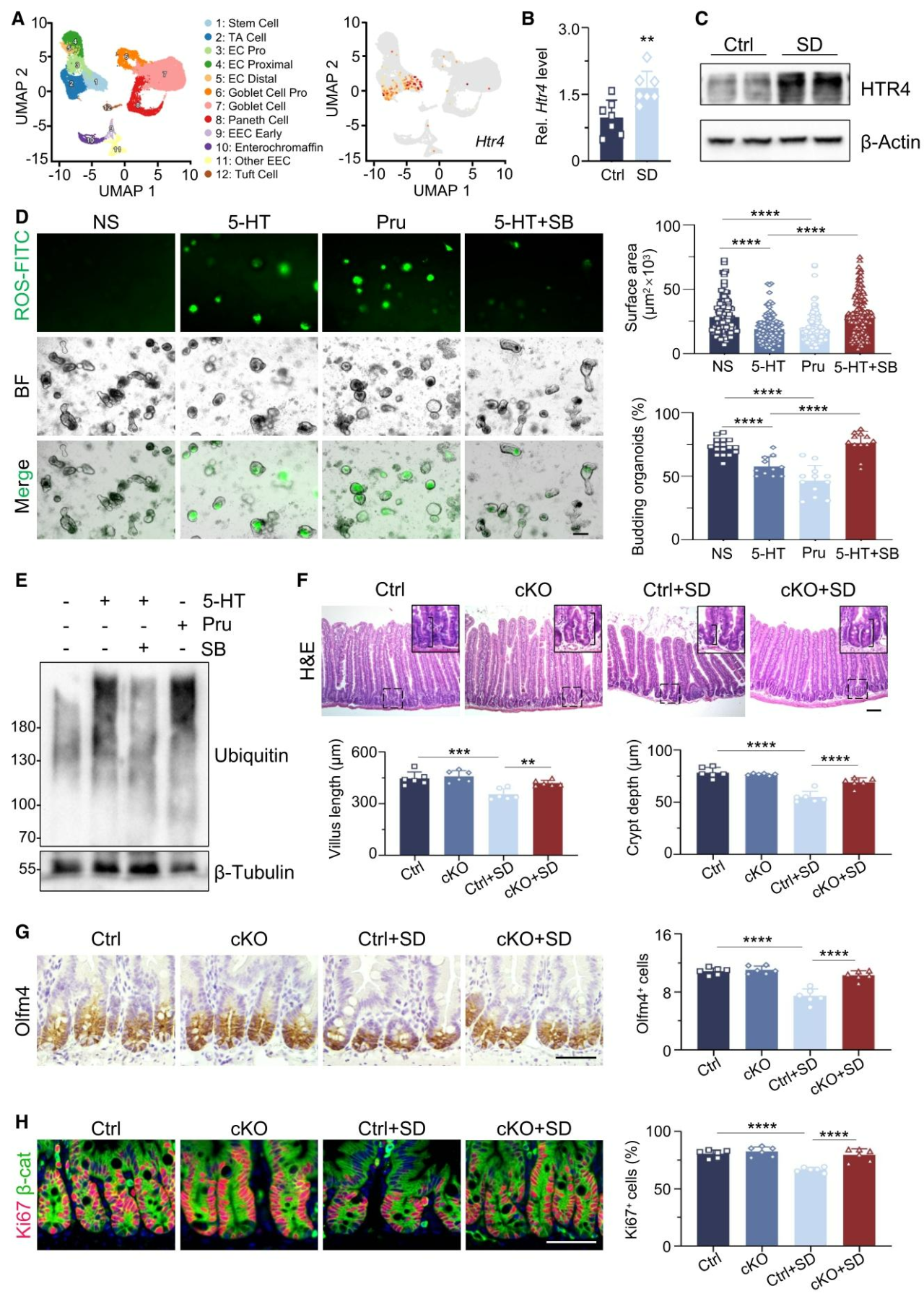
图4.肠道干细胞通过其受体HTR4响应5‑HT信号
睡眠由中枢神经系统调控,为探究睡眠剥夺信号如何改变肠道5‑HT水平与表型,本研究聚焦参与脑‑肠通讯的交感神经系统、下丘脑-垂体-肾上腺(HPA)轴及迷走神经,并通过前期实验排除了交感神经系统与HPA轴的作用;随后对小鼠进行双侧迷走神经切断术(VGX),并给予2天睡眠剥夺(图5A)。荧光金(FG)轴突追踪显示DMV无荧光信号,证实迷走神经完全切断(图5B);迷走神经切断小鼠出现胃扩张与食糜潴留表型(图5C),且相较于未切断迷走神经的睡眠剥夺小鼠,其Olfm4⁺干/祖细胞、Ki67⁺增殖细胞及潘氏细胞数量增多、隐窝深度增加(图5D–5G),应激颗粒减少(图5H),表明迷走神经切断术足以阻断睡眠剥夺对肠道的影响。与此一致,睡眠剥夺的迷走神经切断术小鼠的5-HT水平保持正常(图5I);免疫荧光结果显示ChAT⁺神经纤维分布于肠道上皮周围(图5J)。综上,睡眠剥夺可通过激活迷走神经引发肠道5‑HT水平上升。
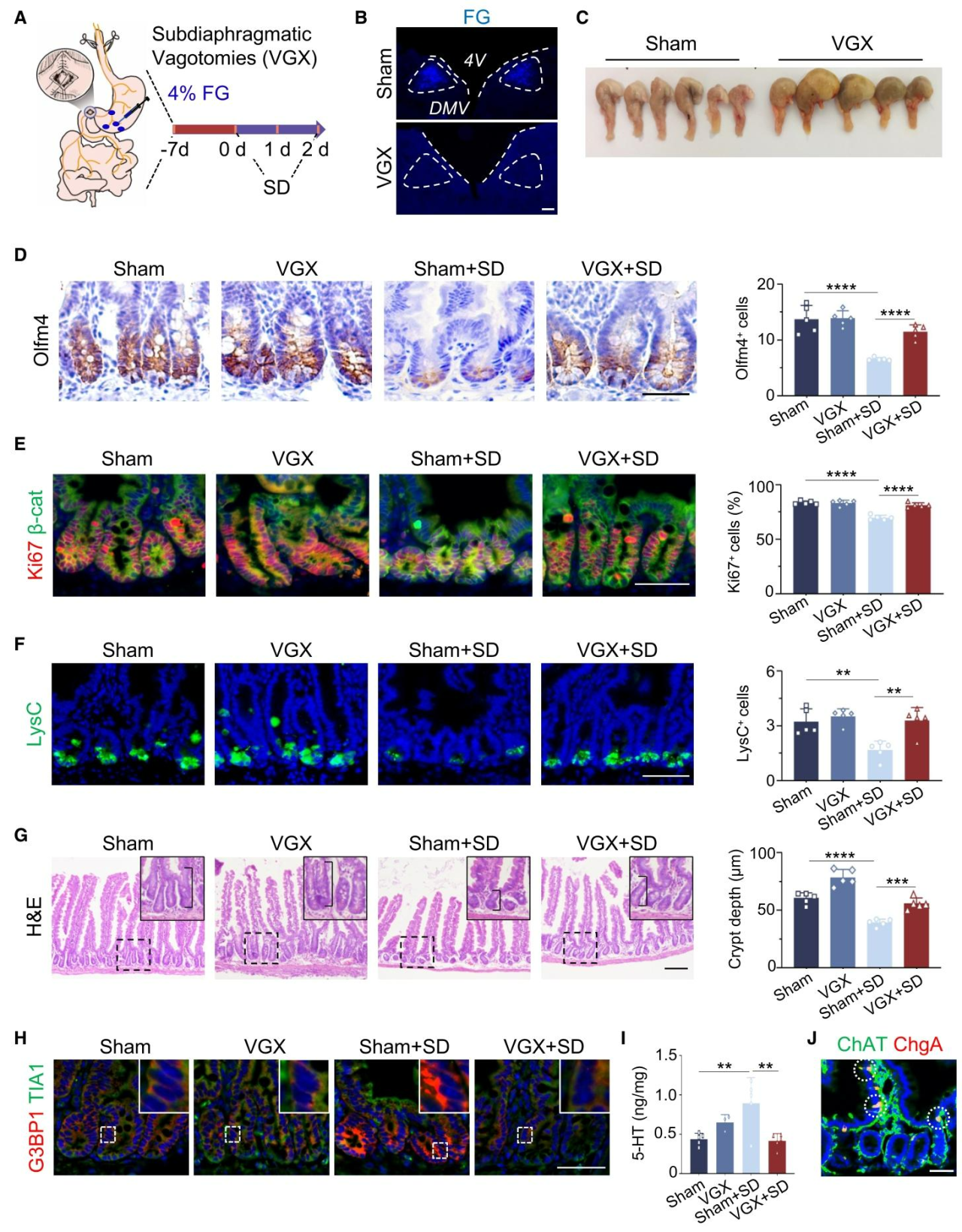
图5.迷走神经激活介导睡眠剥夺与肠道的关联
乙酰胆碱作为迷走神经主要神经递质,在睡眠剥夺小鼠肠道中显著升高(图6A)。向小鼠腹腔注射乙酰胆碱可模拟睡眠剥夺所致肠道损伤,导致隐窝‑绒毛结构变短、肠道干细胞与增殖细胞减少、氧化应激增强及5‑HT水平上升(图6B–6G)。乙酰胆碱有两种类型的受体:烟碱型受体(nAChRs)和毒蕈碱型受体(mAChRs)。为明确乙酰胆碱受体类型在睡眠剥夺调控肠道功能中的作用,研究在2天睡眠剥夺期间分别使用mAChRs拮抗剂阿托品和nAChRs拮抗剂溴化六甲铵处理小鼠,以检测哪类受体介导该效应。阿托品可显著缓解睡眠剥夺诱导的肠道损伤并抑制5‑HT升高,而溴化六甲铵无此作用(图6H–6K)。体外实验显示,乙酰胆碱可直接促进RIN14B肠嗜铬细胞5‑HT分泌,该效应可被阿托品阻断(图6L);同时乙酰胆碱抑制5-HT再摄取转运体(SERT)表达,减少5‑HT再摄取(图6M)。阿托品可恢复睡眠剥夺小鼠肠道SERT水平(图6N)。综上,乙酰胆碱通过毒蕈碱受体,既促进肠嗜铬细胞释放5‑HT,又抑制其再摄取,最终导致肠道5‑HT蓄积与肠道损伤。
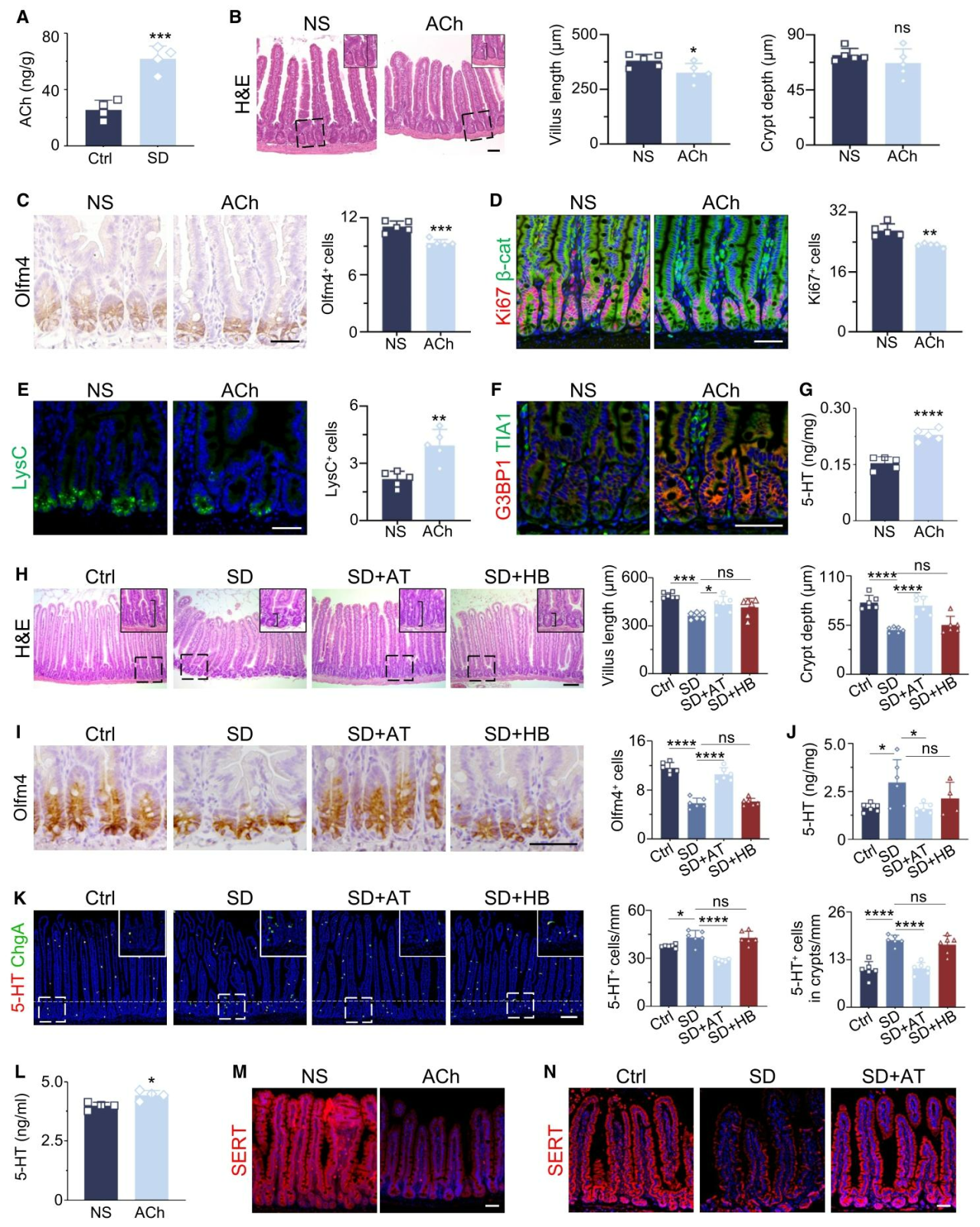
图6.乙酰胆碱水平升高导致肠道中5‑HT过度蓄积
为确定哪个中枢神经系统核团将睡眠剥夺的效应传递至肠道,通过c-Fos染色确认了睡眠剥夺激活的多个脑区,进一步向肠壁注射伪狂犬病病毒(PRV-724),逆行追踪支配肠道的大脑区域,结果表明在睡眠剥夺激活的核团中,只有DMV呈PRV-724阳性(图7A)。钙成像结果表明,睡眠剥夺后DMV钙瞬变的频率和平均振幅显著升高,且该激活状态可持续7天再恢复至基线(图7B‑7E);采用AAV‑hM3Dq‑mCherry化学激活ChAT‑Cre小鼠中ChAT⁺DMV神经元可显著升高小肠乙酰胆碱与5‑HT水平,模拟了睡眠剥夺的效应(图7F‑7I);而利用化学遗传学抑制双侧DMV神经元可逆转睡眠剥夺诱导的肠道乙酰胆碱与5‑HT升高(图7J‑7L)及Olfm4⁺干细胞减少(图7M‑7N)。上述结果表明,睡眠剥夺可引起DMV神经元持续性异常激活,并通过乙酰胆碱传递信号至肠道,进而上调5‑HT、加剧氧化应激、损伤肠道干细胞并最终导致肠道病变。
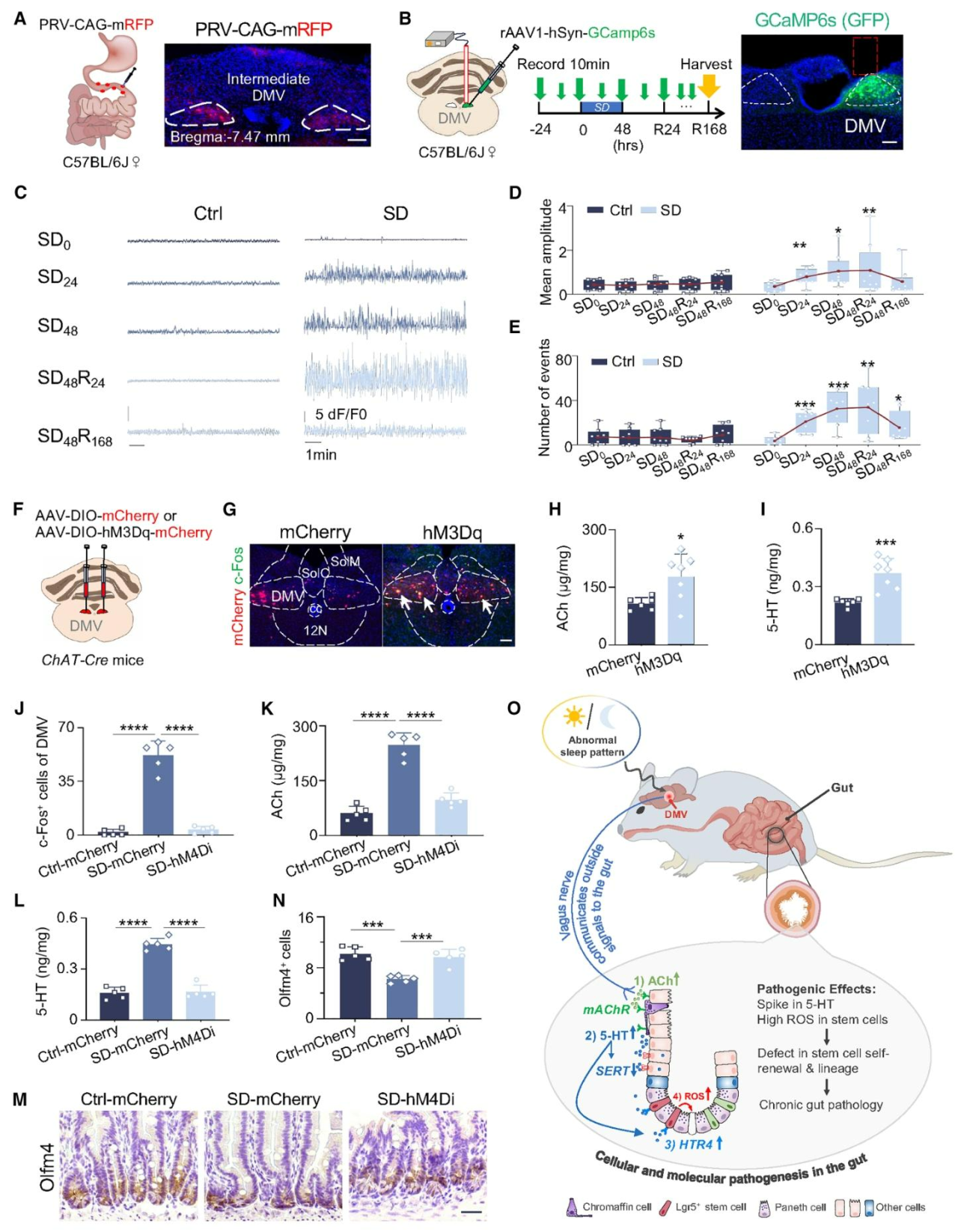
图7.DMV是介导睡眠剥夺对肠道调控作用的中枢神经系统区域
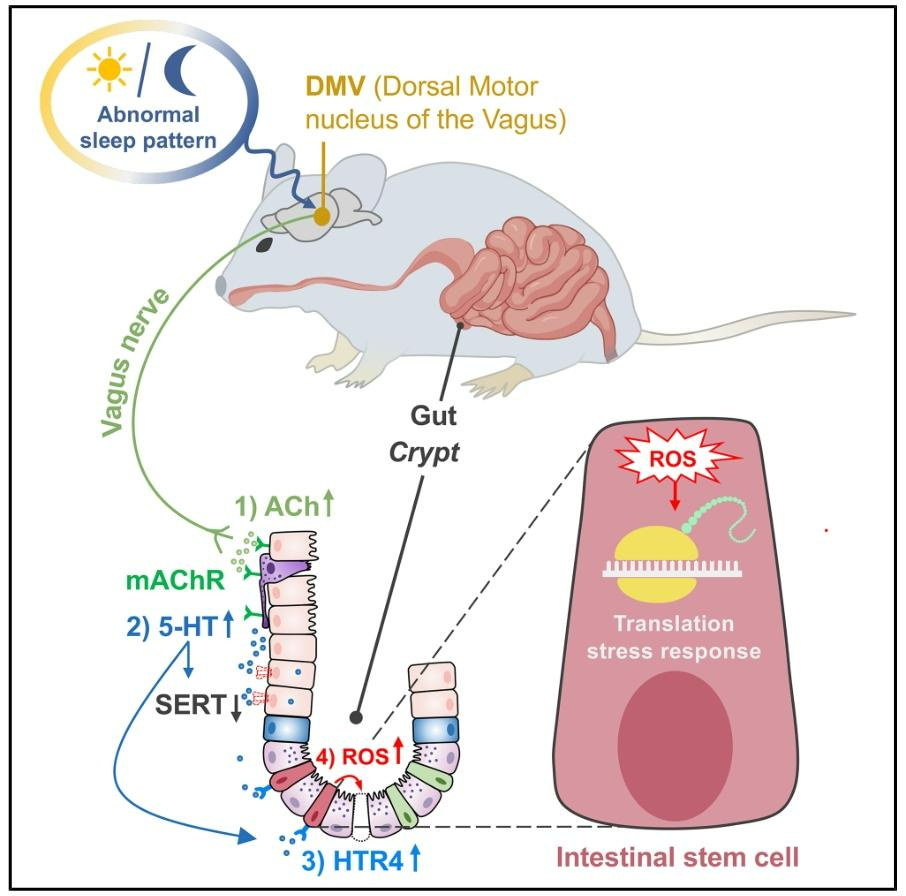
本研究揭示了一条睡眠剥夺损害肠道干细胞的神经机制:睡眠剥夺异常激活迷走神经背运动核(DMV),导致其通过迷走神经释放过量乙酰胆碱,后者经毒蕈碱受体双向调控肠嗜铬细胞,释放大量5-HT并抑制其再摄取,过量5-HT通过HTR4诱导肠道干细胞氧化应激,从而破坏肠道结构。该发现为干预睡眠相关肠道疾病提供了潜在靶点。
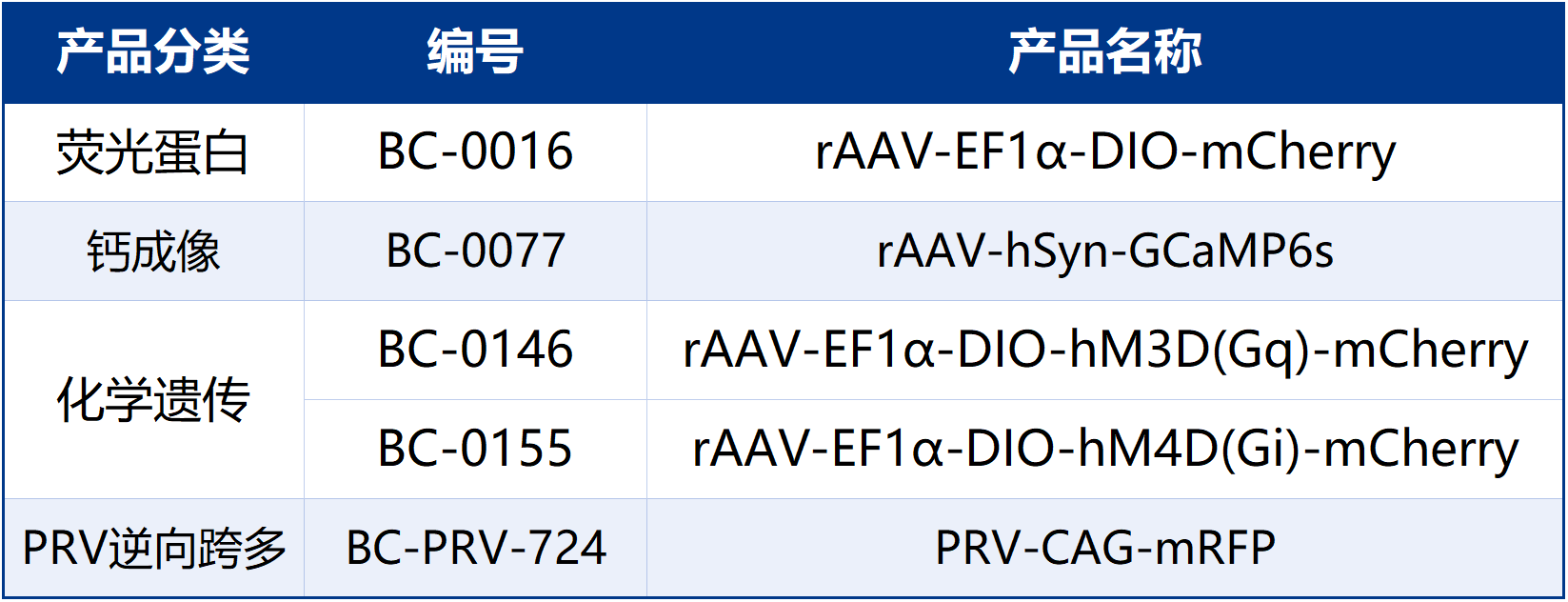
本文使用的工具病毒布林凯斯均可提供:
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。