快速视觉逃避是动物在面对突发威胁时的重要生存行为。然而,使大脑和身体进入“快速行动准备状态”的神经生理机制仍不清楚。腹侧被盖区(VTA)被认为是视觉逃避反应的重要信息中继站,但其神经元兴奋性的调控机制尚未明确。
中国科学院深圳先进技术研究院王立平教授团队在Neuron上发表题为“A bone-derived hormone permits rapid visual escape via GPR37 receptor in a subpopulation of VTA GABAergic neurons”的研究论文,首次揭示骨骼来源的激素骨钙素(osteocalcin,OCN)是快速视觉逃避行为的关键调控因子,其通过OCN-GPR37-cAMP-THIK-1(KCNK13)信号通路,增强VTA的y-氨基丁酸(GABA)能/谷氨酸能共释放神经元的兴奋性,从而为快速逃避行为建立“许可状态”。敲除OCN或G蛋白偶联受体37(GPR37)会显著延迟逃避反应,而恢复该通路功能可逆转行为缺陷。该研究揭示了骨—脑轴在生存防御行为中的重要作用,并为骨质疏松相关抑郁、神经退行性疾病等跨器官疾病提供了潜在治疗靶点。

中国科学院深圳先进技术研究院脑认知与脑疾病研究所/深港脑科学创新研究院王立平研究员为本文最后通讯作者,刘雪梅副研究员、谭力铭研究员、李翔研究员为本文共同通讯作者,刘雪梅副研究员、博士后王帅毓、助理研究员赖娟为论文共同第一作者。
骨钙素(OCN)作为骨骼来源的激素,可穿过血脑屏障,对急性应激反应至关重要。为探究其在视觉防御行为中的潜在作用,比较了3月龄(年轻)和14月龄(老年)野生型(WT)小鼠的循环未羧化OCN(Gla-OCN)水平及逼近性视觉刺激诱发的防御反应(图1A和1B)。老年小鼠的血清OCN水平显著低于年轻小鼠(图1C),且视觉逃避反应延迟(图1D),腹腔注射OCN可恢复其正常逃避行为(图1E)。逼近性视觉刺激可诱导循环OCN水平急性升高并持续至少30分钟,这表明OCN是逼近性视觉刺激诱导防御行为的关键介导因子(图1F)。
通过3D层级行为分析平台监测OCN敲除(KO)小鼠其自发行为,发现野生型和OCN敲除小鼠在中央区域停留时间、运动速度方面以及自发行为组成方面未出现变化。而在逼近性视觉刺激测试中,OCN⁻/⁻表现出与老年野生型小鼠相似的防御表型缺陷,GPR37⁻/⁻小鼠也出现逃避延迟,GPR158⁻/⁻小鼠无异常(图1G)。证实OCN主要通过GPR37介导防御反应。
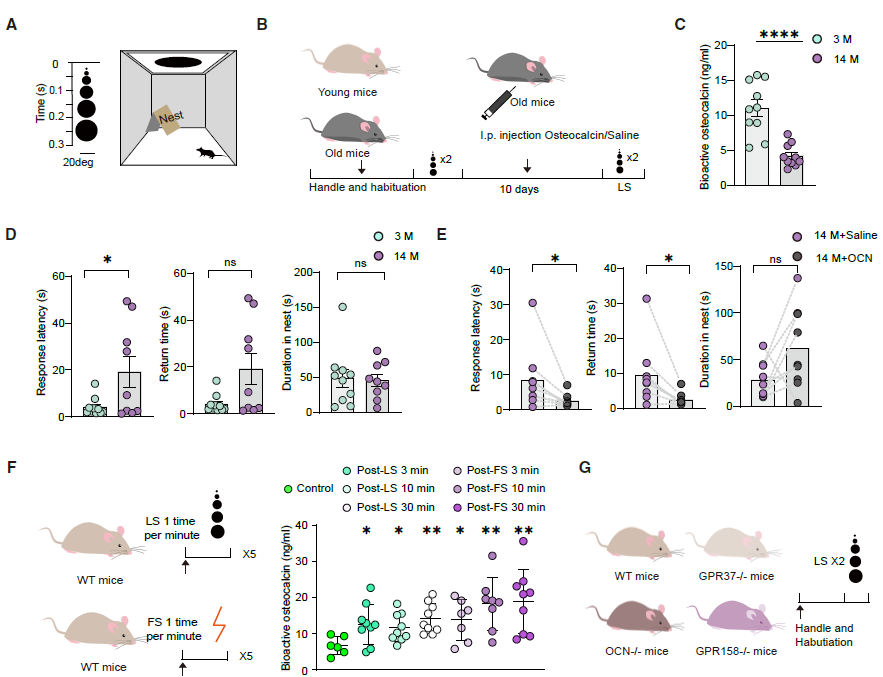
图1 | OCN及其受体介导对逼近性视觉刺激的先天性防御反应
为验证VTA局部OCN信号是否能够挽救OCN敲除小鼠的防御行为缺陷,在OCN敲除小鼠的VTA局部施用OCN(图2A)。结果显示,该处理显著缩短了逃避反应潜伏期和返回巢穴时间,并增加了小鼠在巢穴中的停留时间(图2B和2C)。通过Lenti-GPR37-GFP在GPR37⁻/⁻小鼠的VTA恢复GPR37表达,可以重建快速逃避反应(图2D-2F)。相反,在GPR37⁻/⁻小鼠VTA局部施用OCN并不能挽救其防御行为缺陷(图2G-2H),说明在VTA OCN与GPR37的相互作用,对逼近视觉刺激诱发的逃避行为起到至关重要的作用。为验证OCN与VTA神经元中的GPR37是否存在物理结合,使用生物素化OCN进行免疫染色实验。结果显示OCN可直接结合VTA多巴胺能神经元(TH⁺)和GABA能神经元(GAD67⁺)上的GPR37。
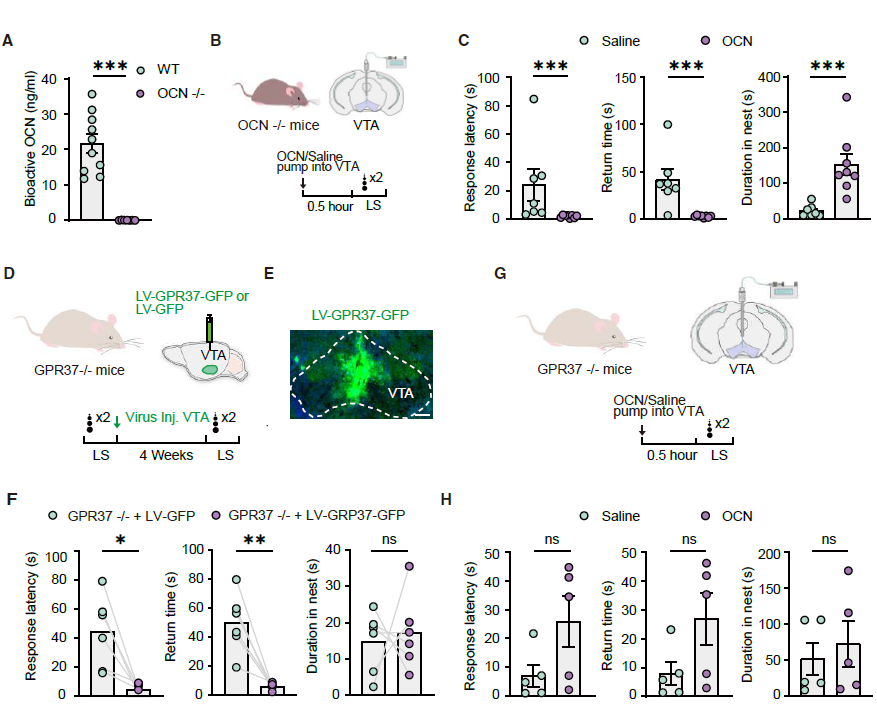
图2 | VTA完整的OCN-GPR37信号通路是快速视觉逃避的关键
为确定介导OCN-GPR37信号的VTA神经元类型,分别在不同神经元群体中敲除GPR37。结果显示,无论是全身性还是VTA特异性在多巴胺能神经元中敲除GPR37,均不影响对逼近性视觉刺激的逃避反应(图3A-3D)。在GPR37flox/flox小鼠中分别注射AAV-CaMKIIα-Cre-GFP或AAV-Dlx5/6-Cre-GFP,选择性敲除VTA谷氨酸能神经元或GABA能神经元中的GPR37。结果显示两类神经元中GPR37的缺失均显著损害逼近性视觉刺激诱导的逃避反应(图3E-3H)。上述结果表明,OCN通过作用于VTA谷氨酸能和GABA能神经元中的GPR37,介导逼近性视觉刺激诱导的逃避行为。
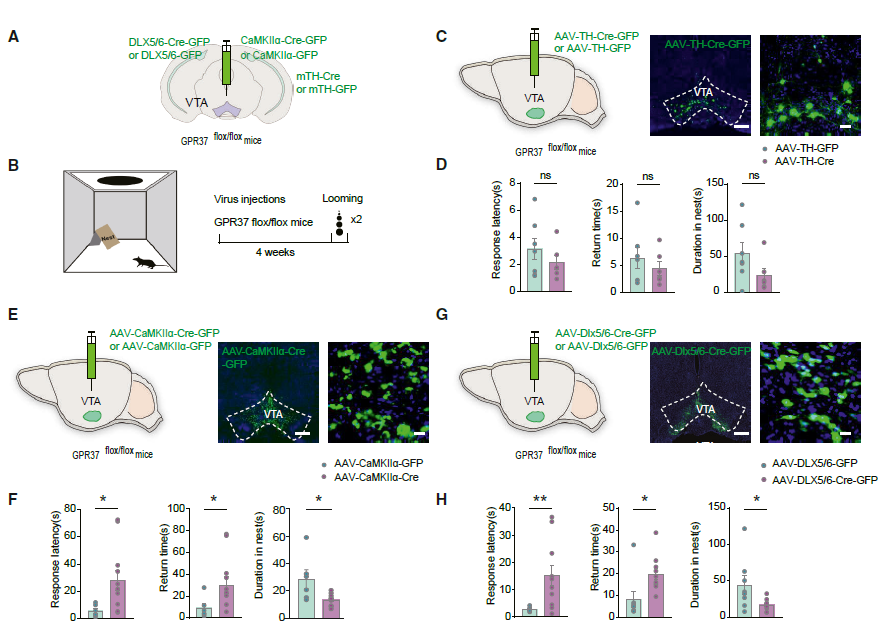
图3 | VTA中GPR37的细胞类型特异性操控及其对视觉防御行为的影响
为探究OCN对VTA GABA能神经元的影响,在GAD2-ires-Cre小鼠VTA注射AAV-DIO-GFP,并进行全细胞膜片钳记录(图4A)。通过单峰-双峰检验,在OCN处理前,这些GABA神经元表现为单一群体;而在10 ng/mL OCN处理15 min后,则被分为两个功能亚群:I型和II型神经元(图4B)。证实OCN可特异性驱动VTA GABA能神经元分化为两个功能不同的亚群。电生理结果表明,基础条件下I型神经元的自发放电频率低于II型神经元;OCN处理后I型神经元自发性动作电位发放频率增加,而II型神经元降低(图4C-4E)。突触电流记录显示sEPSCs和sIPSCs无显著变化,提示该效应源于神经元内在特性改变。
进一步在GPR37⁻/⁻与GPR158⁻/⁻小鼠中注射AAV-Dlx5/6-GFP并进行膜片钳记录,探究它们是否与两种已知的OCN激活受体(GPR37和GPR158)相对应(图4F和4K),GPR158⁻/⁻小鼠输注OCN后,未检测到Ⅱ型(易受抑制型)神经元(图4G),且OCN降低静息膜电位(图4H和4I)、提高神经元兴奋性(图4J)。反之,GPR37⁻/⁻小鼠OCN处理后,无Ⅰ型(易受兴奋型)神经元(图4L),OCN对静息膜电位无影响(图4M和4N),但降低动作电位发放频率(图4O)。已有研究表明OCN可通过调控钾电流调节神经元兴奋性。向GAD2-ires-Cre小鼠注射AAV-DIO-GFP并记录(图4P),发现OCN输注后,神经元峰值及稳态钾电流均低于基线(图4Q和4R)。结果证实,OCN通过GPR37/GPR158将VTA GABA能神经元分为两个兴奋性亚群,并调控其钾离子电流。
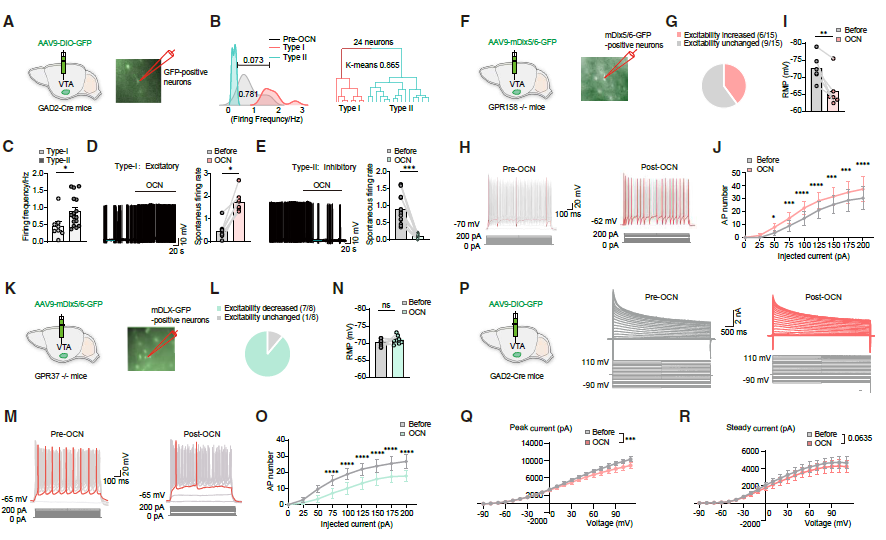
图4 | OCN在VTA GABA能神经元的不同亚群中诱发兴奋性或抑制性反应
为探究GPR37在视觉逃避中的作用。对雄性小鼠的VTA组织进行单细胞核RNA测序(snRNA-seq),并通过均匀流形近似和投影(UMAP)及无监督聚类,构建VTA细胞类型图谱,根据Snap25的表达将细胞分为神经元和非神经元细胞。神经元根据经典标志物分为谷氨酸能(Glu)、γ-氨基丁酸能(GABA)、GABA-谷氨酸能(GABA-Glut)和多巴胺能(DA)四种类型(图5A和5B)。GABA-Glut神经元占所有神经元的一半以上,占表达GABA能或谷氨酸能标志物神经元的70%(图5B)。GPR158广泛高表达,而GPR37仅在多巴胺能和GABA能神经元(纯GABA能和GABA-谷氨酸能)中低水平表达,在纯谷氨酸能神经元中不表达(图5C和5D)。GPR37在GABA-谷氨酸能神经元亚型2中高表达,与钾通道基因Kcnk13(编码THIK-1)高度共表达;GPR158在亚型1中富集,与Kcnj3(编码GIRK1)共表达(图5E-5I)。原位测序揭示两种GAD2阳性细胞(GPR37+KCNK13+和GPR158+KCNJ3+)无明确空间分离,但分子表达特征不同(图5J-5N,和5O)。
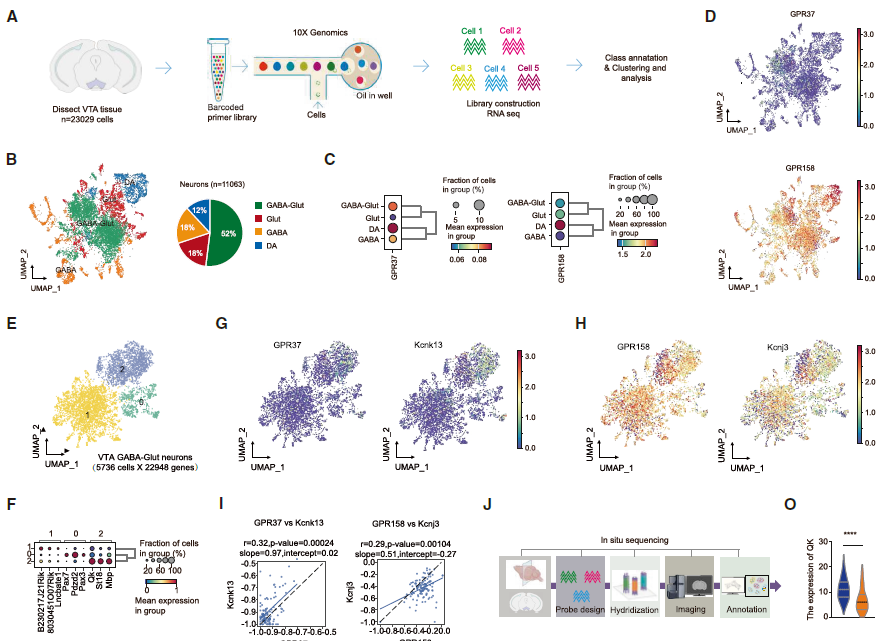
图5 | snRNA-seq鉴定VTA不同神经元群体中GPR37、GPR158受体及其共表达的钾通道
为进一步证实OCN、钾通道和神经元兴奋性之间的受体依赖性关联,在GPR158⁻/⁻和GPR37⁻/⁻的VTA注射AAV-Dlx5/6-GFP。在GPR158⁻/⁻小鼠中,预先施用KCNK13抑制剂CVN293可单独使静息膜电位去极化,并增加一系列正向电流诱发的VTA GABA能神经元兴奋性,后续施用OCN无额外作用(图6A-6D);电压钳记录显示OCN可显著抑制GPR158⁻/⁻小鼠VTA神经元的KCNK13电流(图6E-6H);在GPR37⁻/⁻小鼠中,预先施用KCNJ3抑制剂TPN-Q可单独使静息膜电位去极化并提高神经元兴奋性,后续施用OCN无额外作用(图6I-6L);OCN可增强GPR37⁻/⁻小鼠VTA神经元的KCNJ3电流(图6M-6P)。
腹腔注射KCNK13抑制剂CVN293(5 mg/kg)或向KCNK13flox/flox小鼠VTA注射AAV-Dlx5/6-Cre-GFP(对照组:AAV-Dlx5/6-GFP)特异性敲除GABA能神经元的KCNK13,均会导致野生型小鼠视觉逃避行为缺陷,证实KCNK13是OCN-GPR37通路的关键下游靶点(图6Q-6U)。
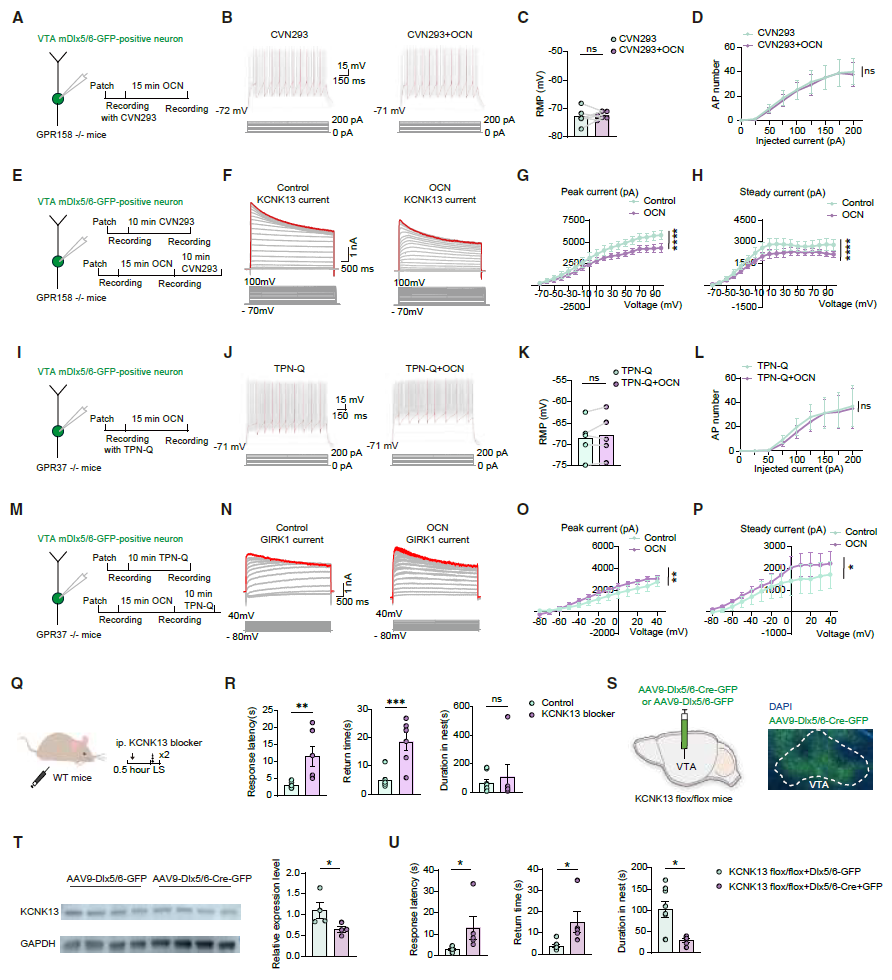
图6 | KCNK13和GIRK1通道在OCN介导的VTA神经元兴奋性及行为调控中的作用
单细胞转录组学和电生理学证据均表明,编码K2P13.1(THIK-1)通道的Kcnk13是OCN-GPR37信号的下游靶点。已有研究显示,GPR37激活会导致环磷酸腺苷(cAMP)减少。为探究cAMP是否参与逼近性视觉刺激诱导的视觉逃避,向GAD-Cre小鼠VTA注射AAV-DIO-GFlamp2和AAV-DIO-FRCaMPi(图7A和7B)。当这些小鼠受到逼近性视觉刺激时,观察到VTA GABA能神经元的cAMP探针荧光强度显著降低,同时钙离子荧光强度增加(图7C和7D)。在OCN敲除小鼠VTA注射AAV-Dlx5/6-GFlamp2和AAV-Dlx5/6-FRCaMPi并受到逼近性视觉刺激时,未观察到cAMP或钙离子荧光的变化(图7E-7H)。
为进一步明确GPR37与OCN介导的cAMP调控的关联,对比了GPR37敲除(GPR37⁻/⁻)小鼠与野生型小鼠VTA GABA能神经元的基线cAMP水平。发现GPR37⁻/⁻小鼠的基线cAMP水平显著升高(图7A-7H)。当向该脑区注射cAMP阻滞剂3'-磷酸腺苷-5'-磷酸硫酸盐(PAPS)后,可以恢复其对逼近视觉威胁的逃避行为,说明降低cAMP对快速逃避反应至关重要(图7K)。机制上,OCN激活GPR37通过非经典Gi通路降低cAMP水平,从而抑制KCNK13(K2P13.1)通道,提高VTA GABA神经元的兴奋性,最终促进面对视觉威胁时的快速逃避行为(图7L),凸显GPR37在cAMP信号和神经元兴奋性调控中的重要作用。
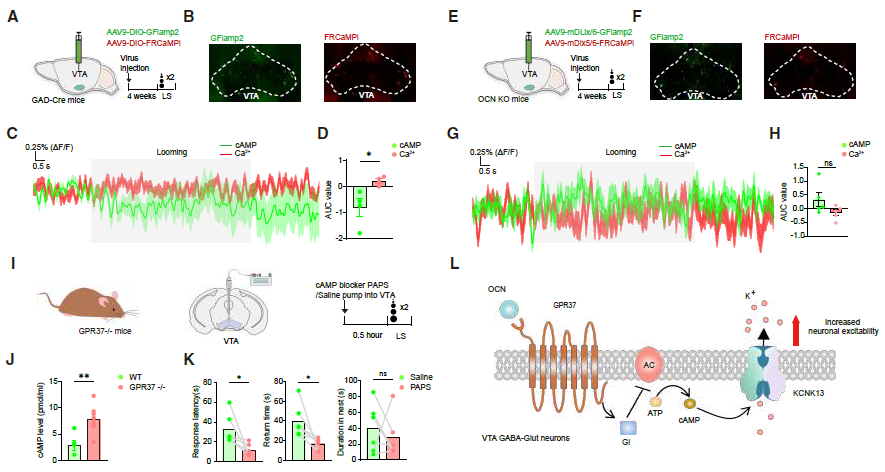
图7 | GPR37介导VTA区cAMP降低,是快速视觉逃避的关键
本研究揭示了一种意想不到的机制:骨骼来源的OCN通过激活VTA GABA能神经元亚群中的GPR37受体,介导快速视觉逃避。OCN-GPR37信号通过非经典通路抑制THIK-1通道,从而增强神经元兴奋性。这些发现突显了OCN在调节VTA环路以实现生存关键行为中的作用,揭示了脑-体通信的新轴。
本文使用的工具病毒布林凯斯均可提供:
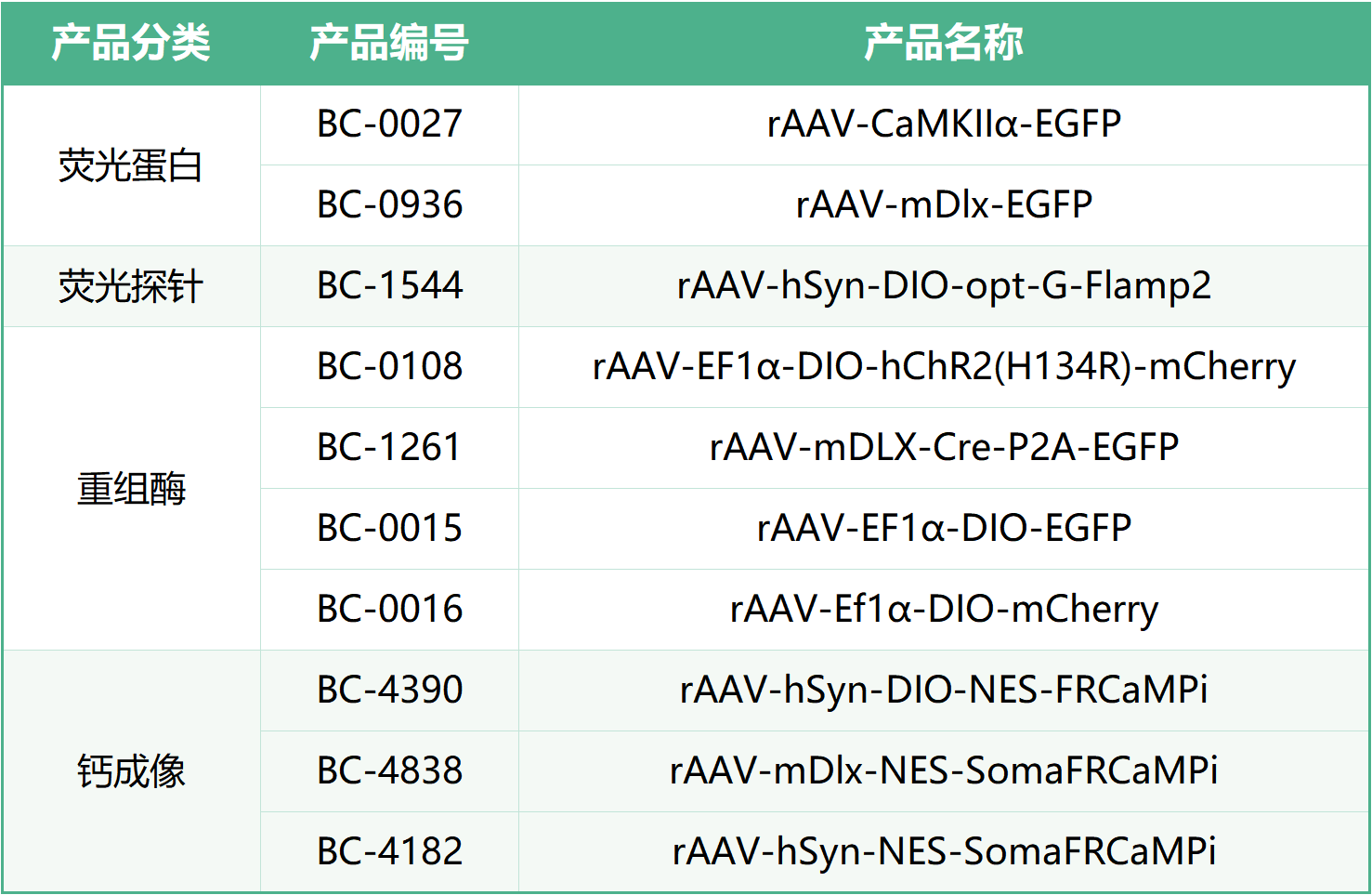
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。