小胶质细胞作为中枢神经系统固有免疫细胞,可直接/间接与兴奋性神经元互作,调控神经发生、突触形成等过程,但与神经元AIS的直接功能互作机制尚未明确。轴突起始段(AIS)是神经元动作电位发放的关键位点,其长度、离子通道分布等严格调控神经元兴奋性,是神经信号传导的核心调控区。已有研究发现小胶质细胞可与AIS接触,但其在生理状态下的功能、分子特征及调控机制均未知。
2026年1月28日,南方医科大学粤港澳大湾区脑科学与类脑研究中心任思强教授团队在Cell Research发表题为“The axon initial segment-associated microglia regulate neuronal activity and visual perception”相关文章,首次发现新皮质中存在轴突起始段相关小胶质细胞(AISa-MGs)这一特殊亚群,其通过与兴奋性神经元的AIS形成紧密的物理和功能相互作用调控神经元活动及视觉感知;机制上,AISa-MGs的短暂去极化会通过THIK-1钾离子通道释放K⁺至神经元AIS区域,引发神经元阈下去极化并促进动作电位发放,体内视觉刺激则通过毒蕈碱受体-NALCN钠离子通道轴诱导AISa-MGs突起的瞬时去极化并触发THIK-1介导的K⁺释放,恢复小胶质细胞膜电位;破坏AISa-MGs与神经元的相互作用(如敲除THIK-1或整合素ITGB1)会特异性损伤AIS相关神经元的钙响应,降低神经集群的协同活动,最终导致小鼠视觉辨别行为受损,该研究揭示了小胶质细胞-神经元AIS功能互作这一新形式。
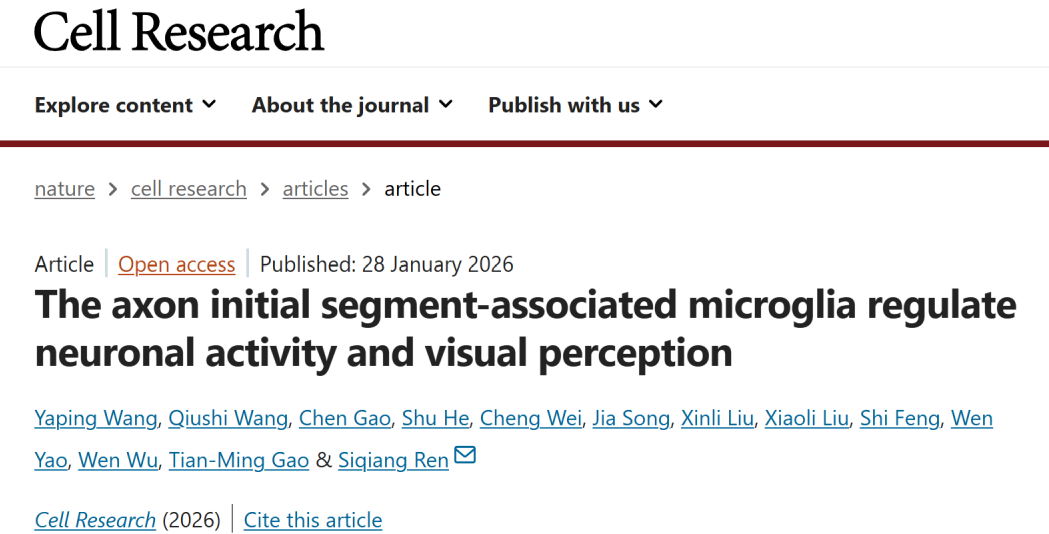
作者通过AIS标志物锚蛋白G的免疫染色,在Cx3cr1-CreERT;YFP小鼠新皮质中,观察到小胶质细胞与AIS的物理接触(图1a)。其中一个小胶质细胞亚群以初级突起(74.42%)或分支突起(25.58%)包裹AIS约69.39%的长度(图1b-d),其胞体可接触AIS起始部(60.47%)、中部(2.32%)或末端(11.63%)(图1c)。总体而言,约21.03%的小胶质细胞与AIS相互作用,且多数仅结合1个AIS(图1e、f),而仅4.88%的AIS与小胶质细胞结合(图1g)。该相互作用在猕猴新皮质中也存在,具有灵长类保守性。电镜及三维重构显示,AIS与小胶质细胞突起的质膜近乎平行,间隙狭窄,且存在散在连接结构,形成紧密稳定的互作(图1h、i)。
部分与AIS起始部作用的AISa-MGs(AIS-associated MGs),其胞体同时接触神经元胞体,即卫星小胶质细胞(图1j、k)。按接触方式将小胶质细胞分为四组:对照组、仅胞体接触组、胞体+AIS接触组、仅AIS接触组,其中AISa-MGs包含后两组(图1k)。仅胞体接触组68.61%的胞体接触神经元顶树突侧,而胞体+AIS接触组胞体仅接触轴突侧(图1l)。形态分析显示,与对照组相比,后三组突起交叉数、分支数更少;仅胞体接触组分支最长,胞体+AIS接触组分支最短(图1m-o)。上述结果表明,与神经元接触的三组小胶质细胞,具有部分相似但独特的形态特征,这可能与其接触神经元的部位相关。
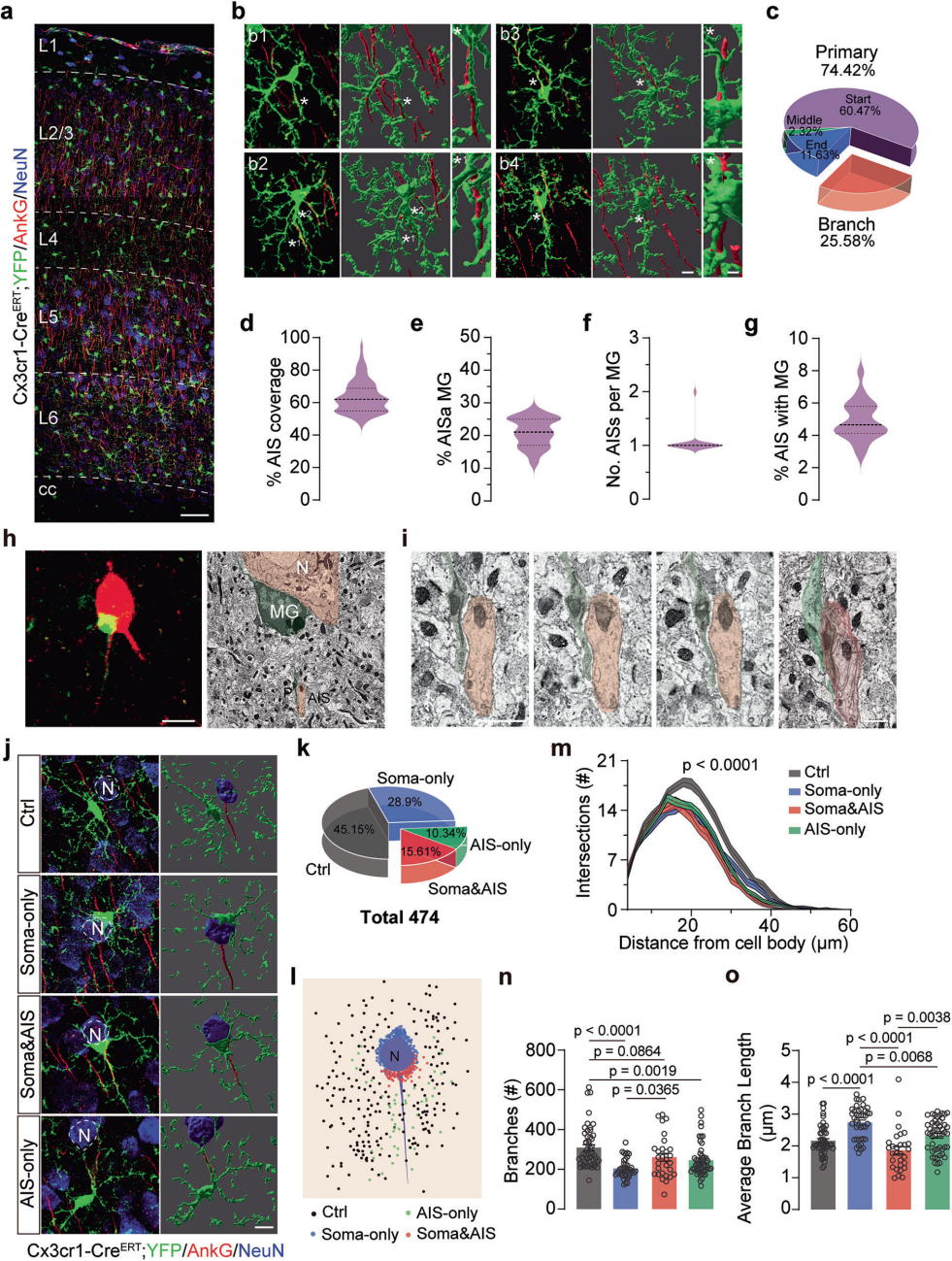
图1 新皮质中与AIS-MGs形态学特征
为明确各组小胶质细胞的分子特异性,利用Cx3cr1-CreERT;YFP小鼠,通过膜片钳测序开展转录组研究(图2a);小鼠胚胎期(E15~16)经子宫内脑室注射相关病毒,以可视化小胶质细胞与锥体神经元AIS的物理接触。Tmem119等稳态小胶质细胞标志物在四组中均有表达(图2b),但仅胞体接触组的多个稳态基因显著下调,倾向于呈现反应性特征。三组与神经元接触的小胶质细胞,各有独特的差异基因集(图2c),同时共享部分差异基因:AIS-only与Soma&AIS共享17个上调基因,Soma&AIS与Soma-only共享12个,AIS-only与Soma-only共享7个(图2d)。其中AIS-only与Soma&AIS共有的上调基因,显著富集于细胞间黏附、信号传导通路(图2e),提示其可能通过AIS与神经元形成紧密的物理和功能互作。
免疫染色验证显示,AISa-MGs(Soma&AIS+AIS-only)突起上的细胞间黏附蛋白整合素β1(ITGB1,Itgb1基因编码)表达,显著高于AISn-MGs(Ctrl+Soma-only;AIS-non-associated MGs)(图2f、g),提示其介导小胶质细胞突起与AIS的物理互作。此外,Tmed2基因编码的细胞内信号蛋白TMED2,在AISa-MGs细胞质中表达显著升高,AISn-MGs中无此变化。综上,小胶质细胞与神经元不同部位的互作,对其转录组谱影响不同;与AIS的互作赋予AISa-MGs独特转录组特征,Itgb1、Tmed2等关键基因可能介导二者的物理和功能互作。
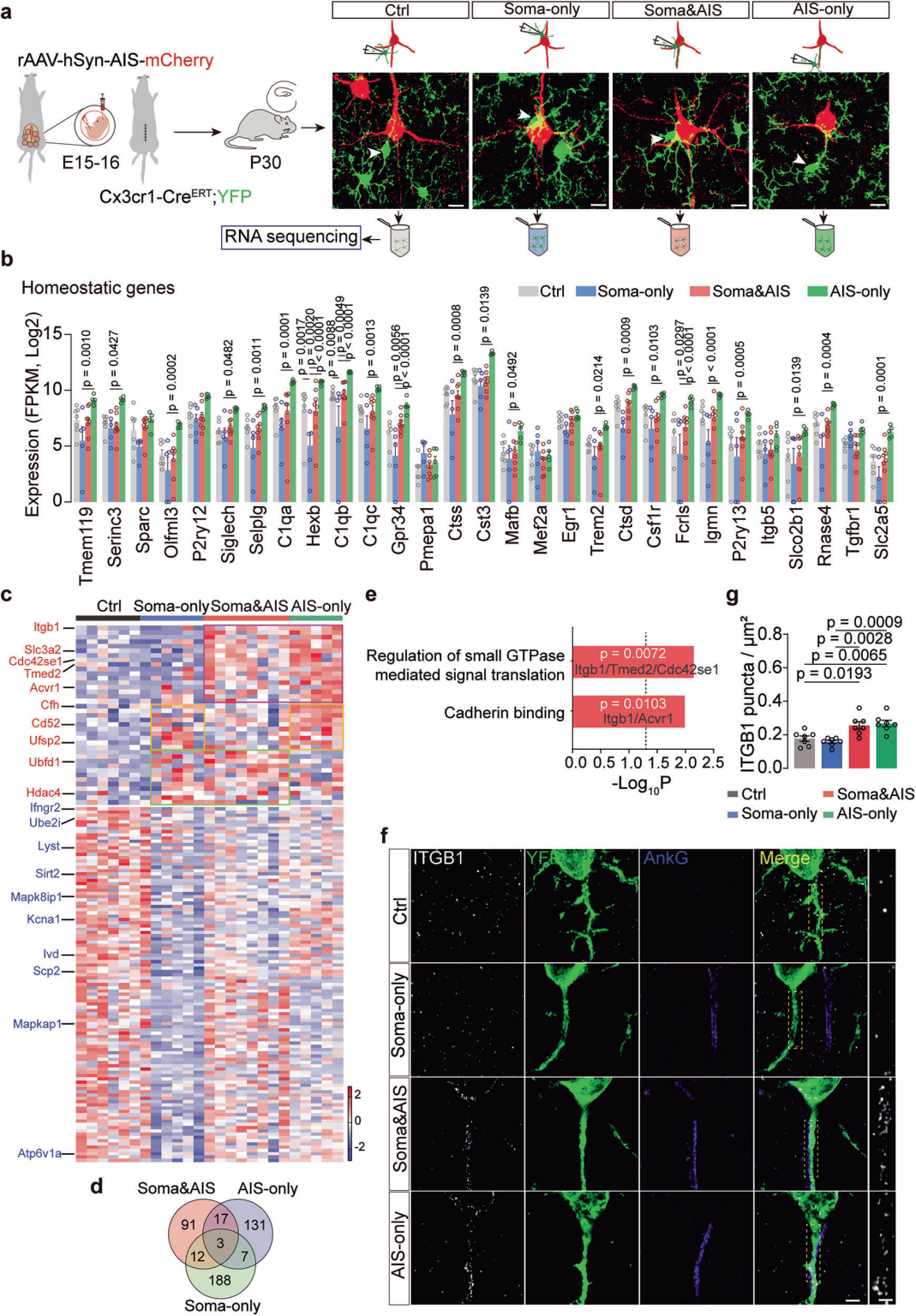
图2 AISa-MGs具有独特的转录组特征
为探究小胶质细胞与神经元的直接相互作用对锥体神经元(PNs)活性的影响,选取胚胎15-16天经病毒注射(rAAV-hSyn-AIS-mCherry)、出生后1-2月龄的Cx3cr1-CreERT;YFP小鼠,在其初级视皮层(V1)2/3层离体脑片中,对PNs与MGs进行双细胞膜片钳记录(图3)。记录均在脑片制备后3小时内完成,此时MGs形态及与PNs的物理接触稳定,无明显细胞凋亡(图3a)。小胶质细胞为非可兴奋细胞,其功能与膜电位(MP)波动相关。为验证AISa-MGs短暂去极化的作用,向其注入去极化电流(诱导MP去极化),同时向PNs注入阶梯电流诱导动作电位(AP)发放(图3b、f)。结果显示,该操作可显著提高关联PNs的AP发放频率、降低AP阈强度(电压阈值不变),效应量为0.68(图3b-e)。AISa-MGs去极化前后,PNs的自发性兴奋性/抑制性突触后电流(sEPSCs、sIPSCs)无差异,说明调控作用不依赖突触传递(图3g-k)。这证实AISa-MGs去极化的调控作用,与胞体接触或间接通路无关。
利用Cx3cr1-CreERT;Cheta-tdTomato小鼠,采用光遗传学技术调控MGs膜电位(图3l、m)。证实470nm光(500ms)照射可使MGs MP平均去极化约16.23mV(图3n、o)。对AIS接触的PNs记录显示,光刺激可显著提高其AP发放频率、降低阈强度(电压阈值不变),效应量为0.64,与电刺激效应相近(图3p-u)。光刺激前后,PNs的sEPSCs、sIPSCs无差异(图3v-z);对无接触/仅胞体接触的PNs光刺激,亦无明显影响。综上,MGs去极化可选择性促进PNs的AP发放,该作用仅通过与神经元AIS的相互作用实现,与突触、神经元胞体接触及间接通路无关。
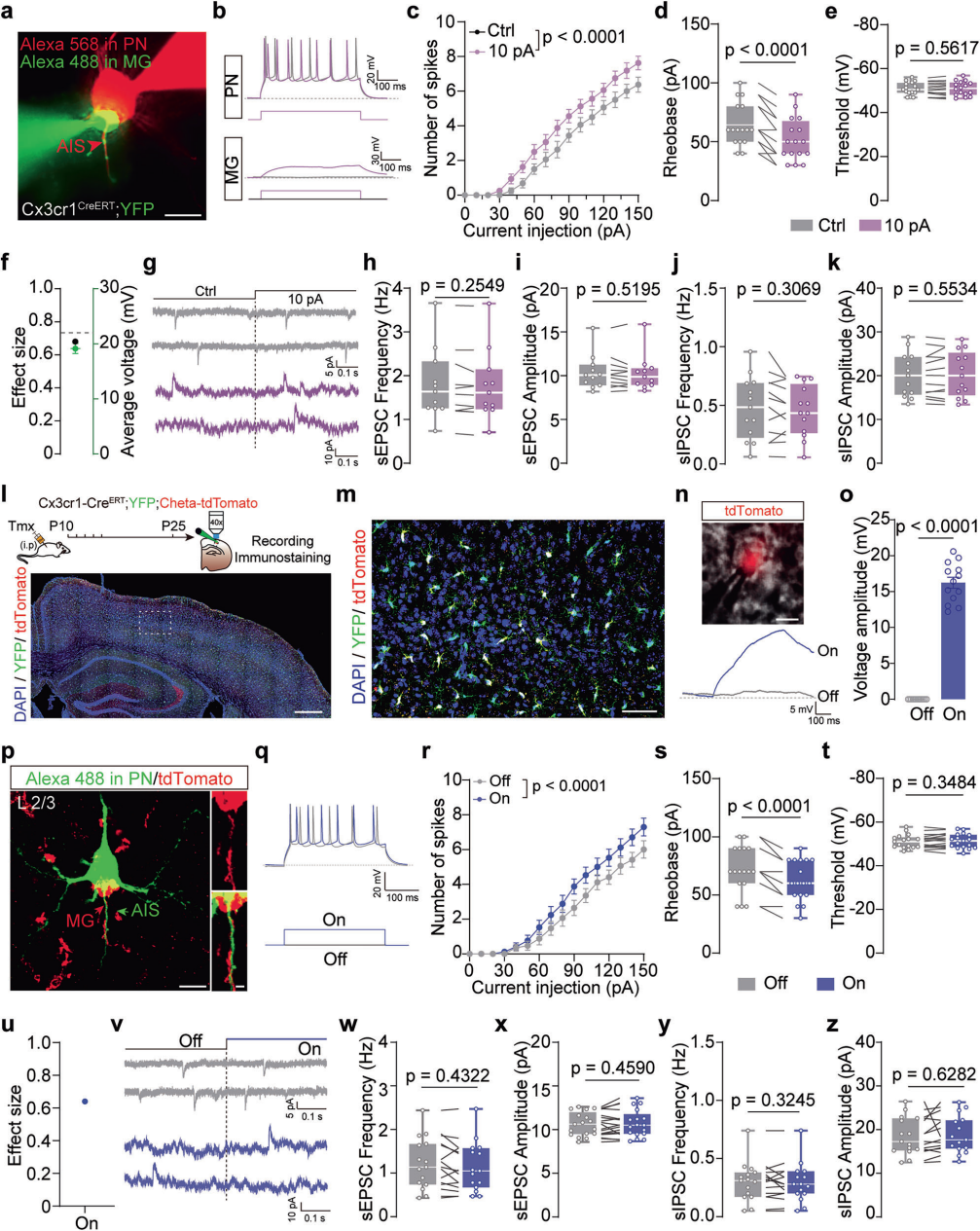
图3 AISa-MGs的短暂去极化促进其相关PNs的动作电位发放
为验证MGs去极化诱导的胞内K⁺释放对锥体神经元动作电位发放的影响,对单个PN(正常内液)及其关联AISa-MGs(无K⁺内液以减少K⁺释放)进行双细胞膜片钳记录(图4a-e)。结果显示,耗尽MGs胞内K⁺后,AISa-MGs去极化对PNs AP发放的促进作用完全消失,同时AP阈强度显著升高,电压阈值无变化(图4c-e),表明该促进作用依赖MGs胞内K⁺释放。为探究K⁺直接释放至AIS的作用,向V1皮层2/3层PNs的AIS区域,直接施加5mM K⁺(较基线高2mM)(图4f)。结果显示,K⁺施加可诱导PNs明显阈下去极化,并显著提高AP发放频率(图4g-j),证实K⁺直接释放至AIS可通过诱导PNs阈下去极化,促进其AP发放。光遗传学刺激AISa-MGs,可诱导PNs在胞体-AIS界面出现特异性阈下去极化,且该效应可被THIK-1拮抗剂C101248阻断,刺激附近AISn-MGs无此效应,证实AISa-MGs去极化可通过THIK-1通道,特异性诱导PNs胞体-AIS界面去极化。
为明确THIK-1活性的必要性,作者发现AISa-MGs中THIK-1的mRNA拷贝数显著高于AISn-MGs,且其通道在与AIS作用的MGs突起上分布更丰富(图4k-m)。短期施加5μM C101248(10分钟)不影响MGs与AIS的接触(图4n-o),但阻断THIK-1后,AISa-MGs去极化对PNs AP发放的促进作用消失,AP阈强度升高、电压阈值不变(图4r-v),表明该促进作用依赖THIK-1活性,推测通过释放胞内K⁺实现。使用Cx3cr1-CreERT;YFP;THIK-1fl/fl(cKO)小鼠实验证实,THIK-1条件性敲除后,MGs中THIK-1表达显著降低、形态简化,但未影响MGs与AIS的物理接触及突触数量和传递(图4p-q)。与野生型(WT)相比,cKO组AISa-MGs去极化不再促进PNs AP发放,且PNs AP阈强度升高、电压阈值不变(图4w-aa),进一步证实THIK-1活性的必要性。综上,AISa-MGs去极化对PNs AP发放的促进作用,通过THIK-1通道依赖的K⁺释放调控AIS区域局部膜电位实现。
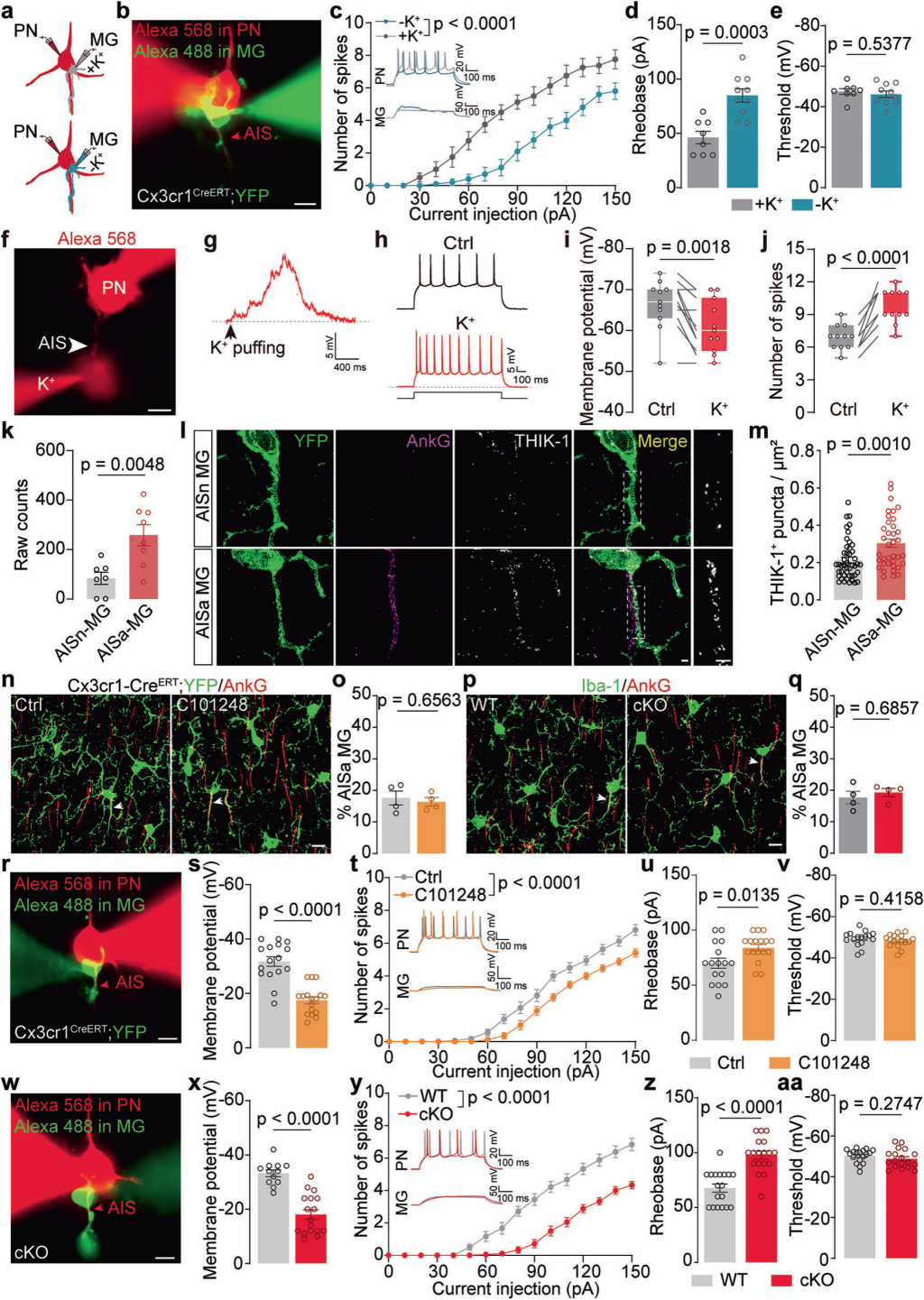
图4 通过THIK-1介导的AISa-MGs细胞内K+释放促进相关PNs的动作电位发放
此前研究表明MGs短暂去极化可通过AIS相互作用促进PNs的AP发放,但生理条件下体内MGs是否发生短暂去极化及机制尚不明确,采用膜电位指示剂ASAP3开展研究。先验证原代培养MGs中,ASAP3荧光强度与THIK-1拮抗剂TPA诱导的MP去极化(膜电位越高)呈负相关,与既往研究一致;构建TMEM119-Cre;ASAP3小鼠,证实ASAP3在MGs中特异性表达(图5a、b)。对其离体脑片的实验证实,–40~0 mV范围内,ASAP3荧光强度与MGs的MP呈负相关(图5c-f)。对头部固定清醒小鼠行双光子成像结合漂移光栅视觉刺激(图5g),发现视觉刺激可诱导MGs发生短暂去极化(主要在突起上),平均幅度约17.33 mV(10~23 mV)(图5h、i)。THIK-1条件性敲除后,视觉刺激仍可诱导去极化,但MP无法恢复至静息水平(图5j、k),证实THIK-1介导的K⁺释放对MP恢复至关重要。
既往研究表明,小胶质细胞表达多种G蛋白偶联受体,如P2Y12受体、毒蕈碱受体和肾上腺素能受体。探究机制发现,阻断P2Y12受体(替格瑞洛)、肾上腺素能受体(普萘洛尔),不影响视觉刺激诱导的MGs去极化;而阻断毒蕈碱受体(东莨菪碱)可显著减少该去极化事件(图5l、m),证实其由毒蕈碱受体介导。AISa-MGs中编码NALCN(TTX不敏感钠通道)的Nalcn基因mRNA拷贝数显著升高,且NALCN在与AIS作用的MGs突起上表达更丰富(图5n-p)。阻断NALCN(CP96345)可减少MGs去极化(图5q、r),提示视觉刺激诱导的MGs去极化可能由NALCN直接介导。
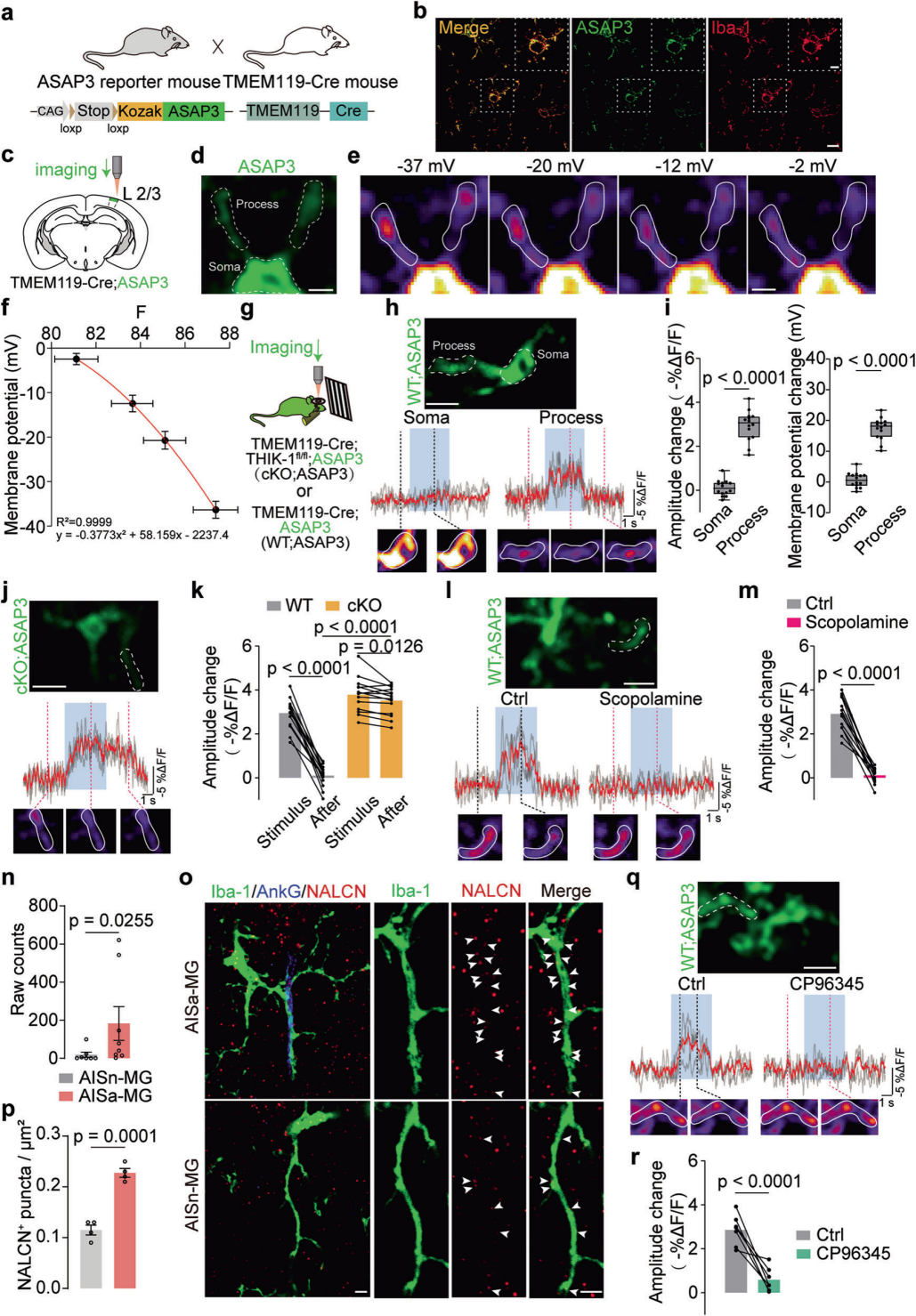
图5 在体视觉刺激通过漂移光栅选择性诱导小胶质细胞突起的瞬时去极化事件
为探究AISa-MGs与PNs的功能性互作对高级脑功能的影响,对头部固定清醒小鼠,结合漂移光栅视觉刺激开展双光子钙成像实验。小鼠V1皮层2/3层预先注射钙成像病毒(图6a),并鉴定出对不同朝向漂移光栅响应的神经元集群。
钙成像前10分钟,向V1皮层施加5μM THIK-1拮抗剂C101248(图6a),结果显示PNs钙瞬变的峰值ΔF/F和频率均显著降低,强响应PNs的下降幅度更明显(图6b-d)。小胶质细胞条件性敲除THIK-1后,部分强响应PNs消失,此时施加C101248不再影响神经元钙反应。综上,C101248通过特异性抑制MGs的THIK-1通道降低神经元钙反应。
为证实AISa-PNs与AISn-PNs对视觉刺激的响应差异,对Cx3cr1-Cre;YFP小鼠行双光子钙成像(图6e)。结果显示,AISa-PNs对视觉刺激的响应显著强于邻近AISn-PNs,且该响应可被C101248抑制(图6f-j)。对Cx3cr1-CreERT;YFP; THIK-1fl/fl(cKO)小鼠行双光子成像(图6m),鉴定出部分MGs-PNs细胞对存在AIS-小胶质细胞突起相互作用(图6n、o)。与WT小鼠相比,cKO小鼠中AISa-PNs钙瞬变显著降低,AISn-PNs无明显变化(图6p-r),表明MGs中THIK-1敲除可特异性影响AISa-PNs的钙反应。既往研究表明,神经元集群中少量神经元是视觉感知的关键,激活最少2个即可触发整个集群激活及视觉辨别行为,可调控集群协同活动并参与认知。实验发现C101248抑制MGs中THIK-1、MGs中THIK-1敲除,均能显著降低神经元同步性和连接性指数(图6k、l、s、t)。综上,小胶质细胞的THIK‑1可增强少数与AIS处小胶质细胞相互作用的PNs钙瞬变反应,进而影响整个神经元集群的协同活动。
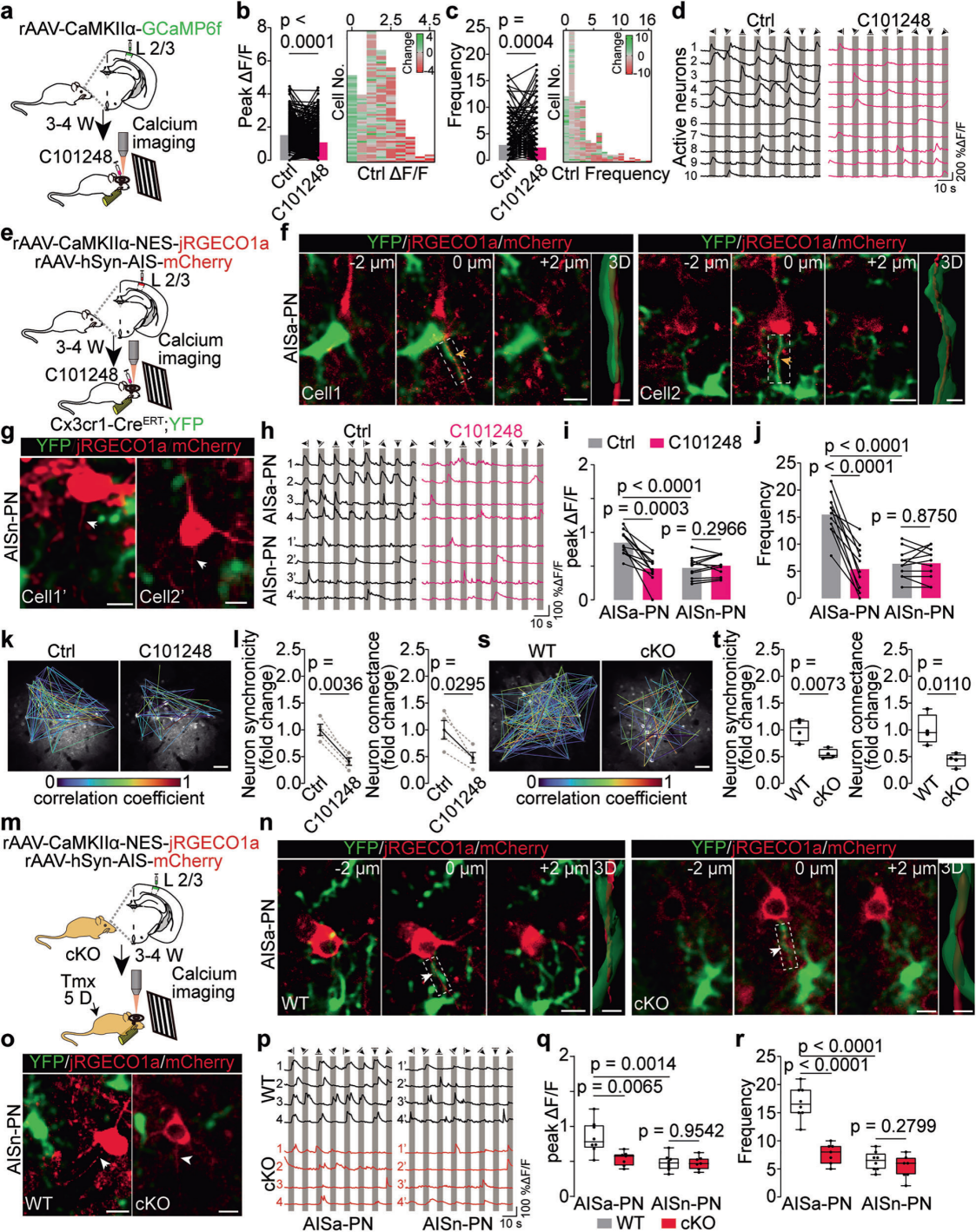
图6 小胶质细胞THIK-1活性特异性调控与MGs在AISs相关PNs的钙反应
检验靶向THIK‑1破坏AISa‑MGs与PNs的功能性互作对视觉辨别行为的影响(图7a)。小鼠先接受Go/No‑Go视觉引导任务训练:垂直漂移光栅为Go刺激(给水奖励),水平漂移光栅为No‑Go刺激(无奖励)。训练期间,小鼠逐渐学会正确舔舐反应,第4天正确率达75%以上并维持(图7d);5天后任务表现提升、FA率降低、舔舐启动更快(图7b、e)。第6天,先检测小鼠任务表现,再向V1区2/3层注射THIK‑1拮抗剂C101248,结果其视觉辨别表现显著下降(图7f、g)。与WT小鼠相比,THIK‑1条件性敲除(cKO)小鼠的视觉辨别能力也显著受损(图7j、k)。对照实验显示,注射ACSF或P2Y12R拮抗剂替格瑞洛,对小鼠视觉辨别任务表现均无明显影响(图7h、i)。
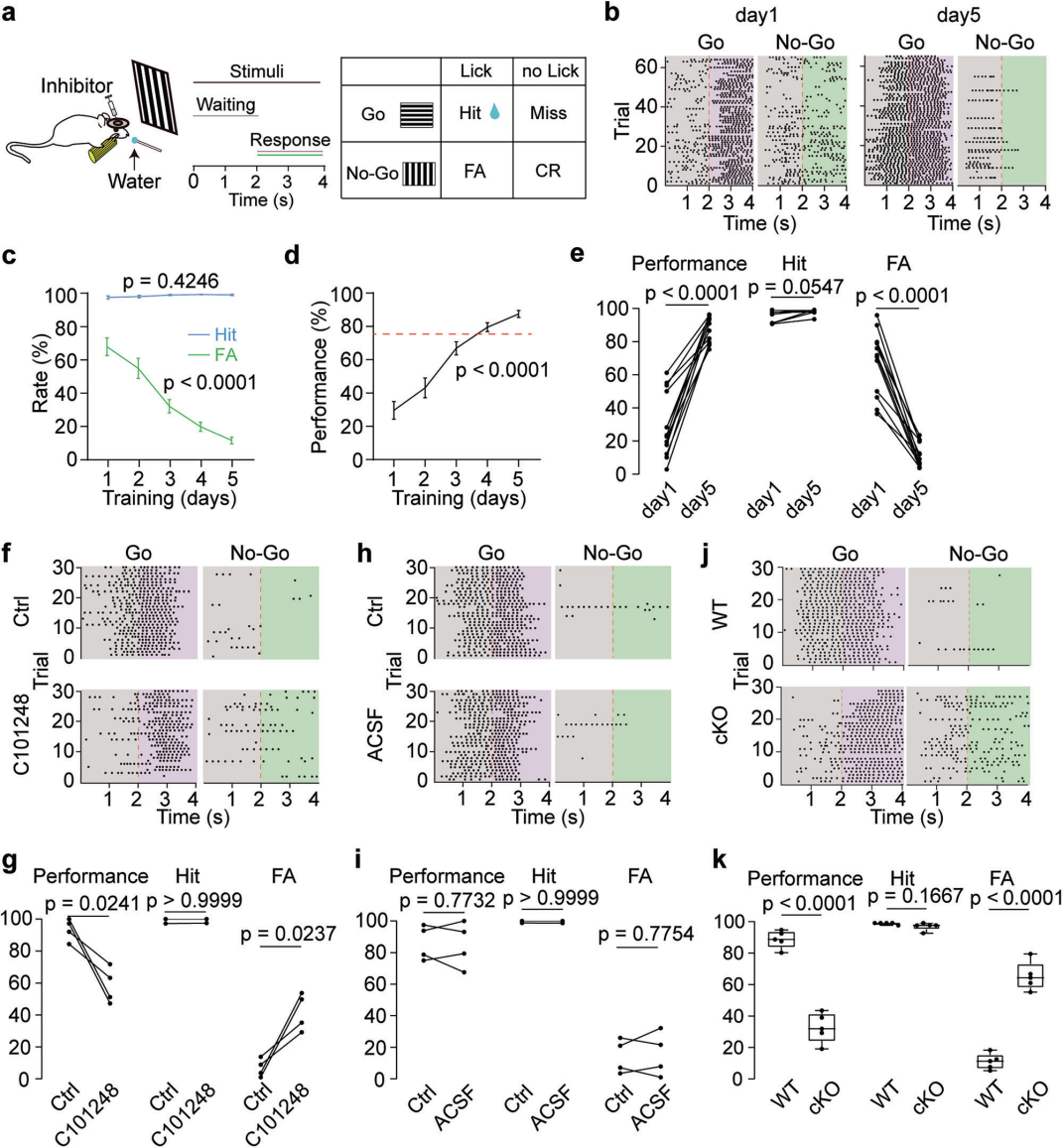
图7 小胶质细胞THIK‑1激活受阻会影响视觉辨别行为
ITGB1在AIS关联的小胶质细胞突起中高度富集(图2f、g),推测其介导二者物理互作。构建Itgb1 cKO小鼠,出生后第7天连续注射他莫昔芬,特异性敲除小胶质细胞中Itgb1(图8a、b)。Itgb1 cKO显著降低AIS-小胶质细胞突起互作比例(图8c、d),但不影响小胶质细胞基本特性及突触功能,是特异性破坏二者互作的有效策略。Itgb1 cKO使强响应PNs消失、PNs钙瞬变降低(图8e-h),并降低神经元集群同步性和连接性(图8i、j);其视觉辨别能力显著弱于WT小鼠(图8k-n),直接证实AIS-小胶质细胞互作的关键作用。综上,AIS-小胶质细胞互作通过THIK-1介导的K⁺释放调控神经元活动及集群协同,参与视觉辨别,揭示其在大脑神经元调控及高级感知中的重要作用。
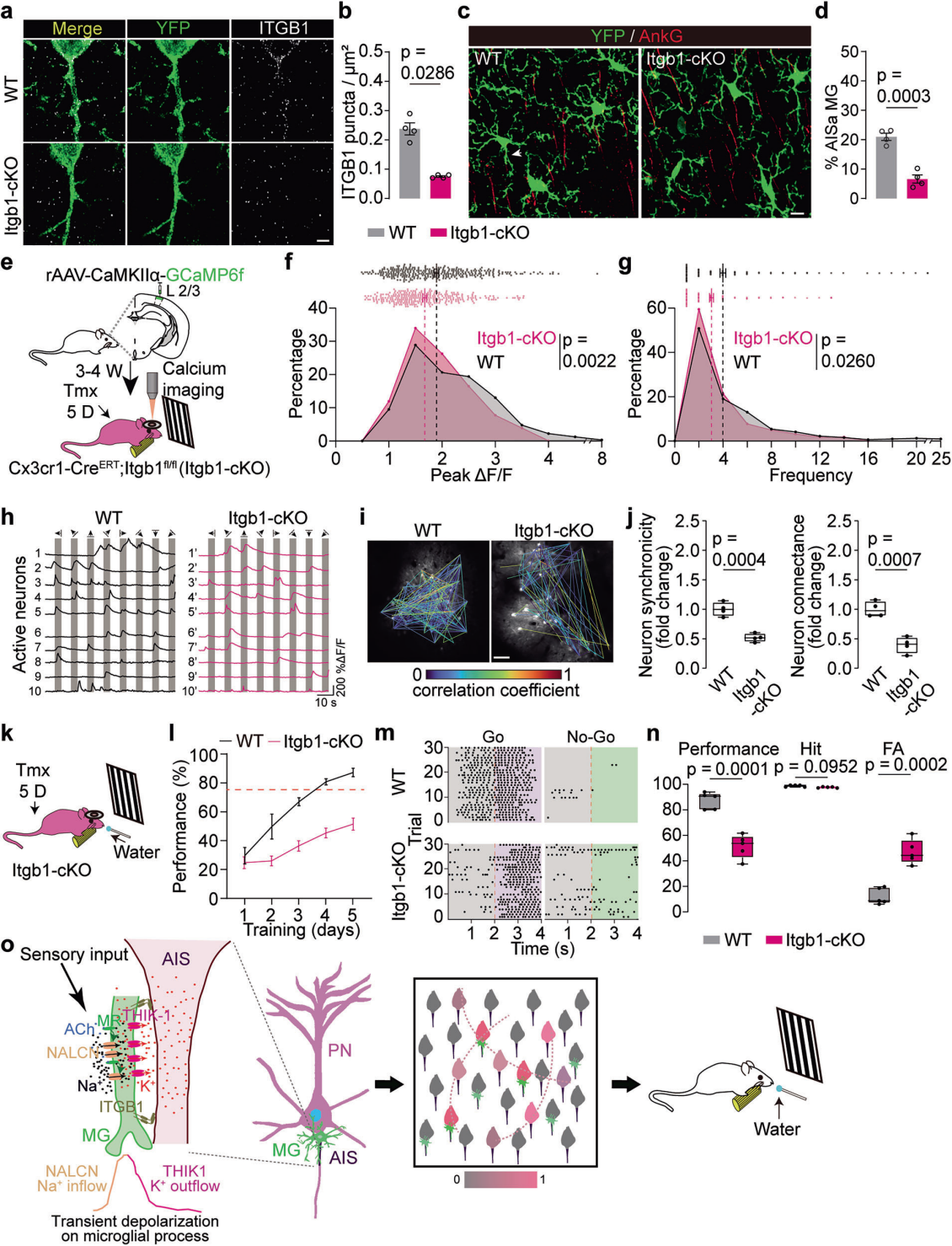
图8 小胶质细胞中Itgb1条件性敲除可特异性阻断AISa‑MGs与PNs之间的物理及功能性相互作用,并影响视觉辨别行为
本文聚焦于轴突起始段相关小胶质细胞(AISa-MGs)对神经元活动和视觉感知的调控作用,首次揭示了小胶质细胞与神经元轴突起始段(AIS)的功能性相互作用及其分子机制和生理意义。
本文使用的工具病毒布林凯斯均可提供:
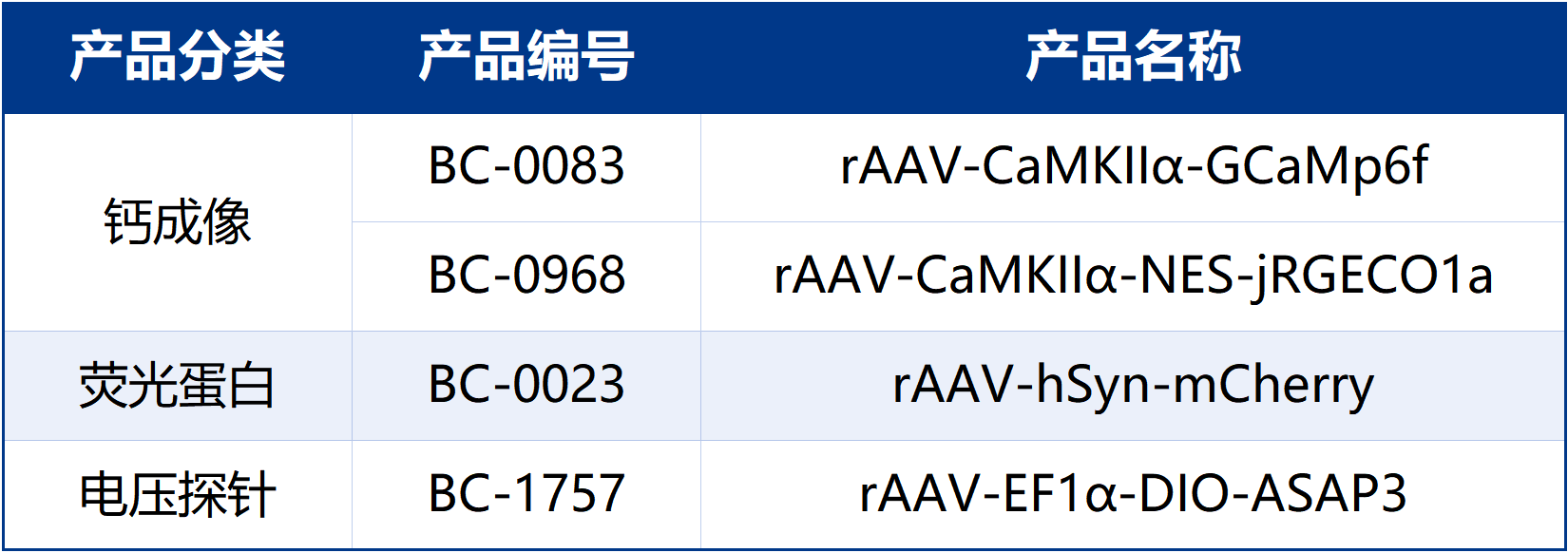
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。