术前急性应激会激活大脑的觉醒系统,从而干扰以异氟醚为代表的全身麻醉效果,导致麻醉深度难以精确调控,并增加术中知晓和苏醒延迟的风险。 当前用于缓解术前焦虑的药物(如苯二氮䓬类)因其作用机制宽泛、缺乏特异性,常伴随呼吸抑制等副作用。因此,阐明急性应激通过何种特定神经环路影响麻醉过程,是开发更安全、更精准的术前干预策略的关键所在。
2025年12月9日,徐州医科大学麻醉学院吴坤伟教授与曹君利教授团队在《Anesthesiology》期刊上在线发表了“Sex-specific Effects of Acute Stress on Emergence from Isoflurane Anesthesia via Brainstem Circuitry in Mice”的研究论文。该研究揭示了急性应激选择性降低雄性小鼠异氟醚麻醉深度并缩短苏醒时间的核心机制。该效应由蓝斑(LC)去甲肾上腺素能(NE)神经元的激活所驱动,通过LCNE→中缝背核(DRN)的γ-氨基丁酸能(GABA)神经元环路,并特异性依赖于DRNGABA神经元α1-肾上腺素能受体(α1-ARs)介导。这一发现为临床围手术期男性患者的应激相关麻醉管理,提供了一个潜在的靶向神经通路优化方向。

为探讨急性应激对异氟醚全身麻醉的影响,对雄性和雌性小鼠进行研究。行为学检测显示,雄性小鼠经30分钟束缚应激后,高架十字迷宫(EPM)开放臂停留时间、旷场试验(OFT)中央区域停留时间减少,焦虑样行为增强(图1A-D);异氟醚麻醉实验中,雄性小鼠应激组苏醒时间(RORR,翻正反射恢复,代表麻醉苏醒时间)显著缩短,诱导时间(LORR,翻正反射消失,代表麻醉诱导时间)无差异(图1E),且焦虑水平与RORR呈正相关(图1F),雌性小鼠应激后苏醒时间无变化(图1L-N);剂量反应曲线显示雄性小鼠应激后异氟醚麻醉敏感性降低23%(图1G);脑电图(EEG)分析表明,应激组雄性小鼠麻醉维持期、苏醒期δ波功率均显著降低,爆发抑制比(BSR)下降(图1H-K)。综上,急性应激通过调节神经动态使雄性小鼠异氟醚麻醉变浅、苏醒加快,且该效应存在性别特异性。
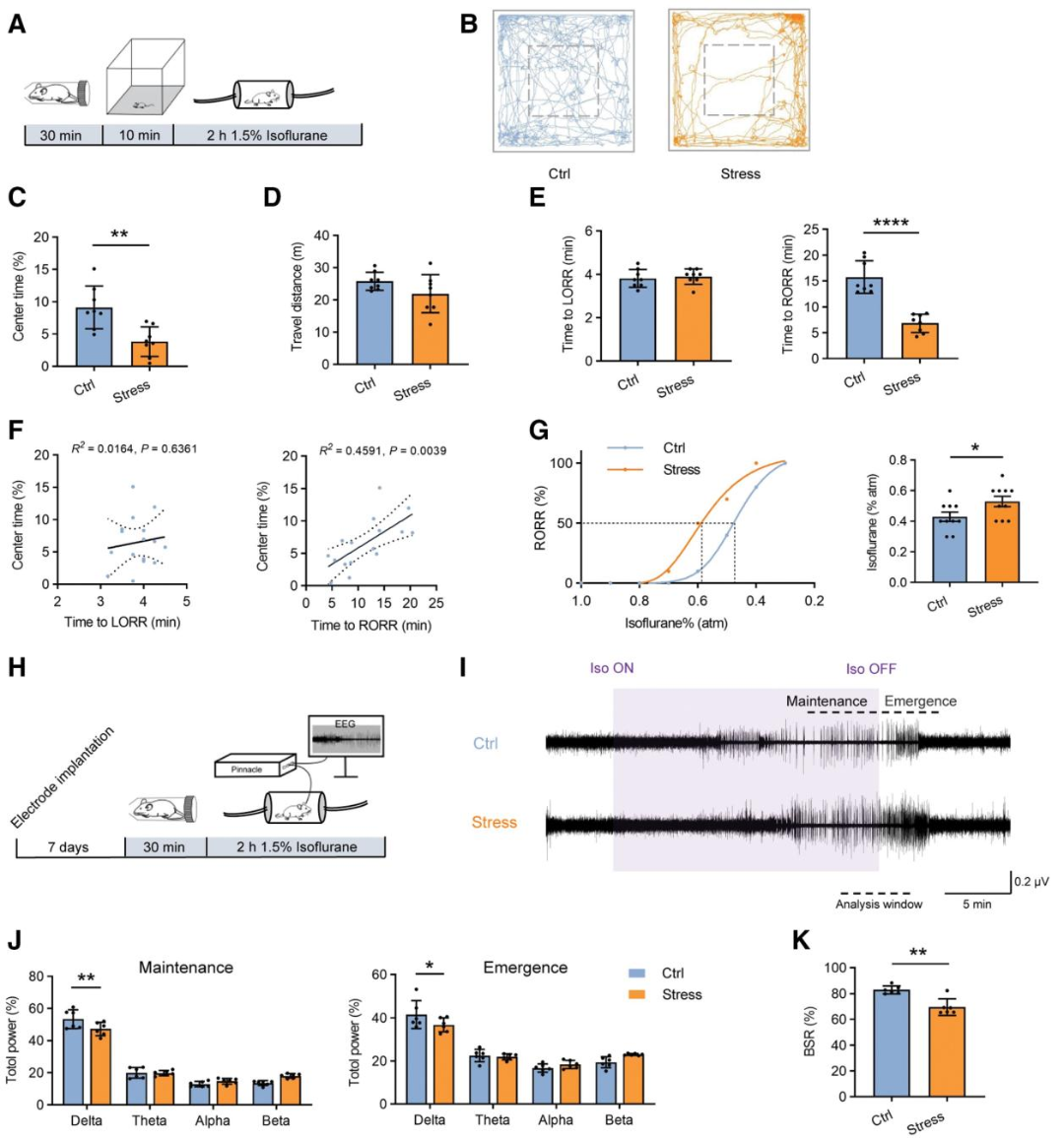
图1.急性应激可加速雄性小鼠异氟醚全身麻醉的苏醒,而雌性小鼠无此效应
为探讨急性应激影响雄性小鼠异氟醚麻醉恢复的潜在细胞机制。c-Fos标记结果显示,雄性小鼠经束缚应激+异氟醚麻醉后,LC和DRN神经元c-Fos表达显著增加,其他脑区无明显变化,且c-Fos与酪氨酸羟化酶(TH)共标记证实应激选择性强烈激活LCNE神经元(图2A-E)。钙信号实时监测显示,应激组RORR缩短,维持期、苏醒期LCNE神经元钙信号显著增强(图2F、G)。对诱导和苏醒期间的钙瞬变进行了阶段特异性分析,结果表明诱导期各亚阶段两组活性无差异,苏醒前期应激组钙信号显著升高、后期无差异(图2H-K)。综上,急性应激通过激活雄性小鼠LCNE神经元(尤其苏醒前期)促进异氟醚麻醉苏醒。
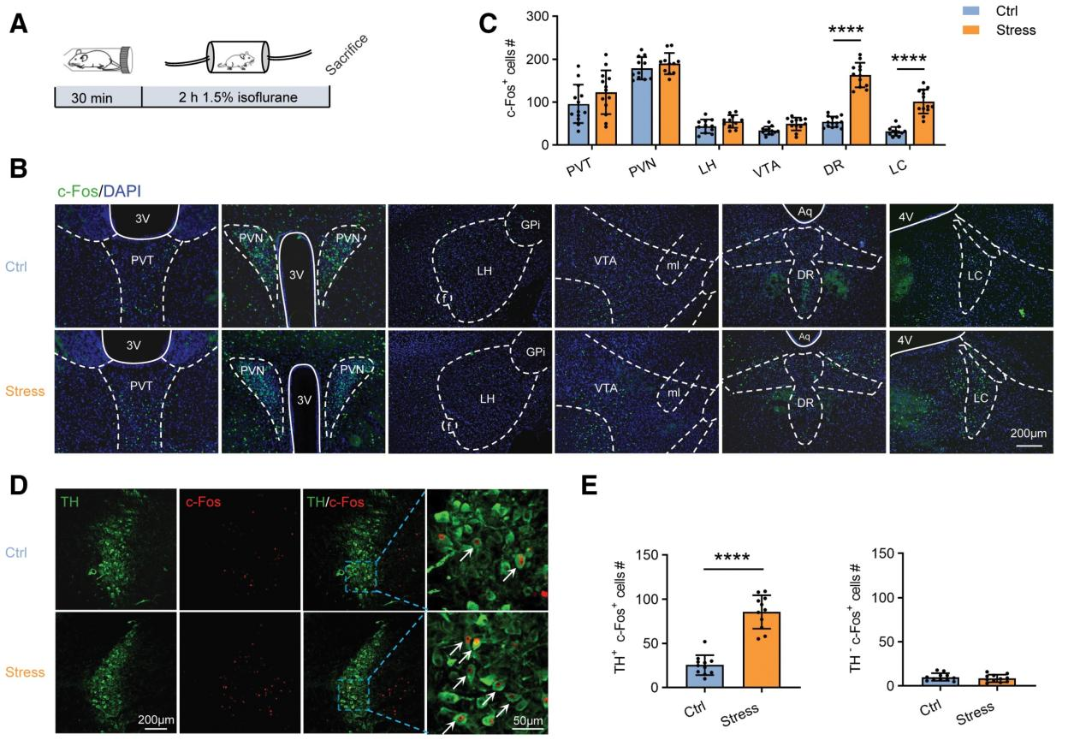
图2.急性应激可增强雄性小鼠麻醉期间LCNE神经元的活性
为探讨LCNE神经元是否对急性应激影响雄性小鼠异氟醚麻醉恢复的重要性。首先通过药理学抑制,即将DSP-4(LCNE选择性神经毒素)处理小鼠后,免疫组织化学分析显示,LC中TH⁺神经元数量减少(图3A-B),还逆转了应激导致的RORR缩短(图3C);另外通过化学遗传学靶向LCNE神经元表达hM4Di,给予CNO后显著抑制应激诱导的苏醒加速(图3D-E),且EEG显示应激诱导的δ波功率及爆发抑制比(BSR)降低也被消除(图3F-H)。综上,LCNE神经元是雄性小鼠急性应激后麻醉苏醒加速的关键因素。
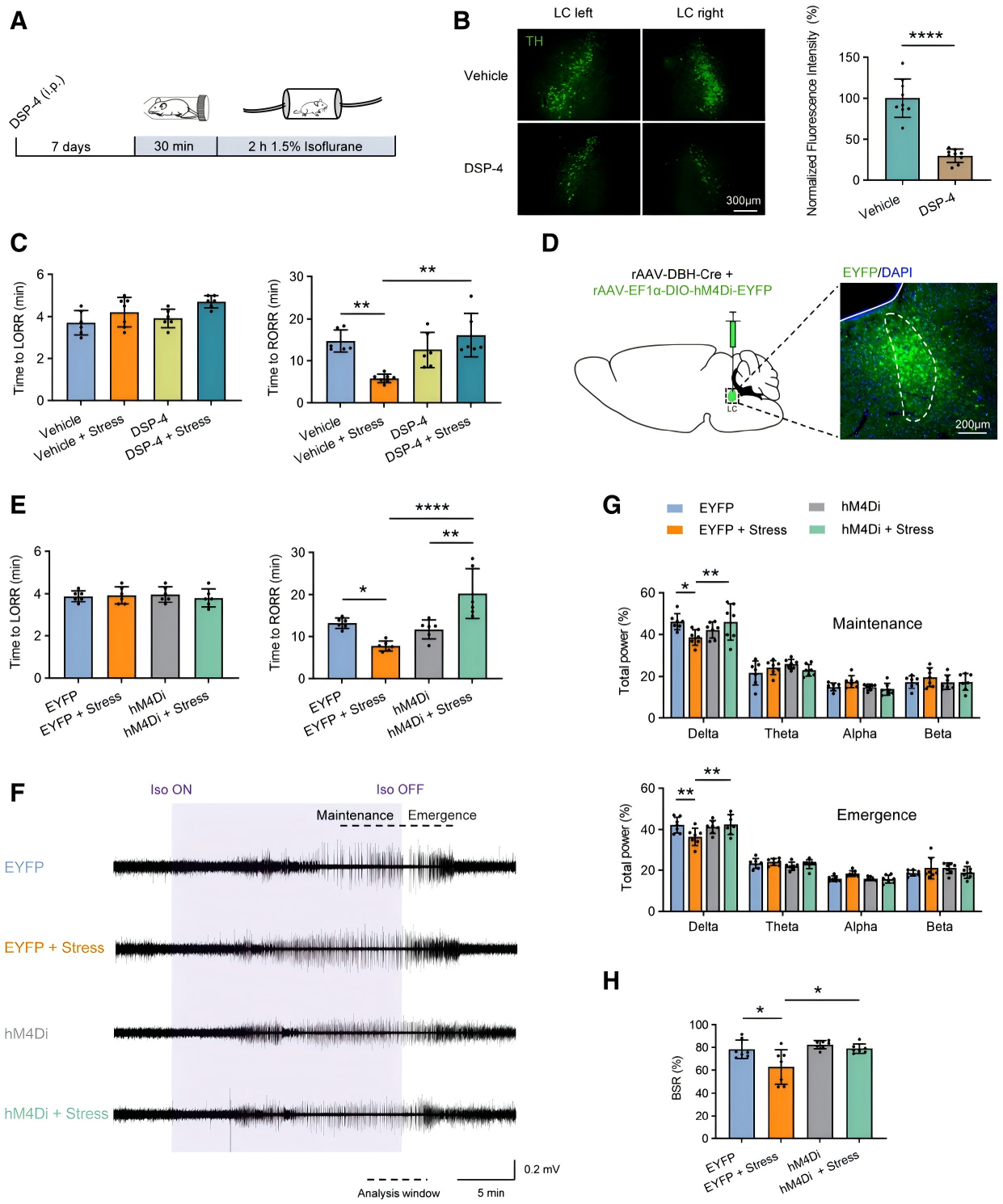
图3. LCNE神经元介导雄性小鼠应激诱导的麻醉苏醒加速
研究通过顺行病毒示踪确认LCNE神经元轴突投射至DRN等多个脑区。DRN是调节情绪处理和意识状态的关键枢纽,应激小鼠的DRN神经元中c-Fos表达显著增加(图2C)。进一步通过化学遗传学在LCNE神经元中表达hM4Di,三周后,在束缚应激和麻醉诱导前30分钟,通过套管向DRN给予CNO抑制投射在DRN的LCNE神经元,发现可有效阻断应激诱导的苏醒时间缩短,而对照组无显著变化(图4A-C);相同的策略利用光遗传学在LCNE神经元表达eNpHR3.0,DRN埋光纤,抑制DRN中LCNE神经元末梢,同样逆转苏醒加速效应(图4D-F)。向VGAT-Cre小鼠LC注射AAV2/1-DIO-FLP病毒、DRN注射AAV-hSyn-fDIO-hM4Di-mCherry,靶向抑制接收LC投射的DRNGABA神经元也有效阻断应激诱导的苏醒加速(图4G-I)。综上,LCNE向DRN神经元的投射在介导雄性小鼠应激诱导的麻醉苏醒加速中起关键作用。
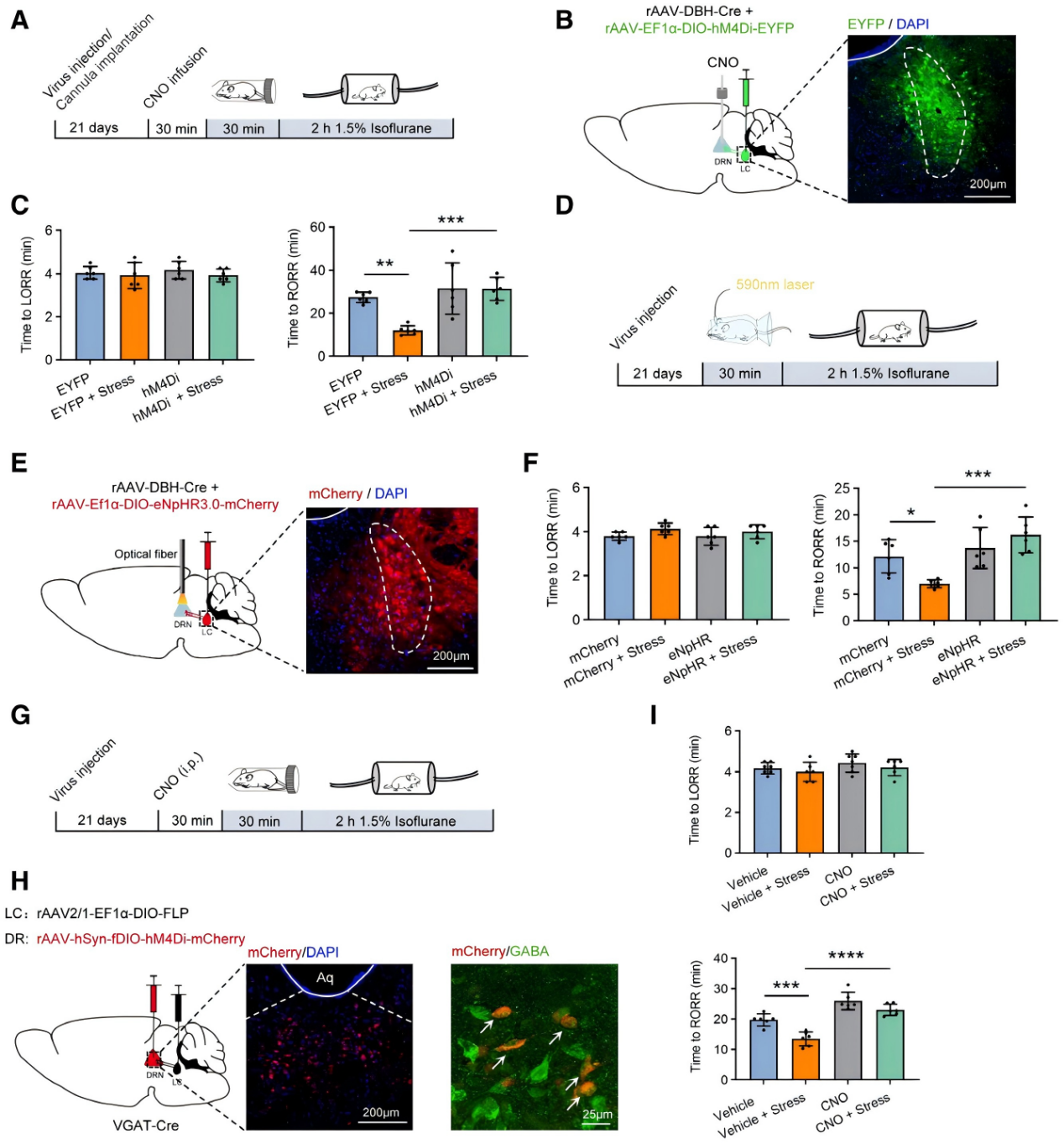
图4.LC→DRN的神经环路介导应激诱导的麻醉苏醒加速
中枢神经系统中的NE信号通过多种G蛋白偶联受体调节,包括α1、α2和β三种肾上腺素能受体(ARs),且只有全身给予α1-AR拮抗剂才能阻止应激引起的麻醉苏醒加速。向DRN给予α1-AR拮抗剂哌唑嗪,可阻断应激诱导的RORR缩短(图5A-B);向VGAT-Cre小鼠的DRN注射AAV携带Cre依赖性shRNA以敲低Adra1,免疫染色证实shRNA在GABA能神经元中表达且蛋白质印迹显示DRNGABA神经元中α1-AR蛋白成功敲低(图5C-E)。行为学上,DRNGABA神经元中α1-ARs敲低对LORR无影响,但消除了应激诱导的RORR加速(图5F);EEG分析显示,应激诱导的δ波功率降低以及相关的爆发抑制比(BSR)降低,可均通过α1-ARs敲低得以消除(图5G-I)。综上,DRNGABA神经元中α1-ARs的激活对于雄性小鼠应激诱导的麻醉苏醒加速至关重要。
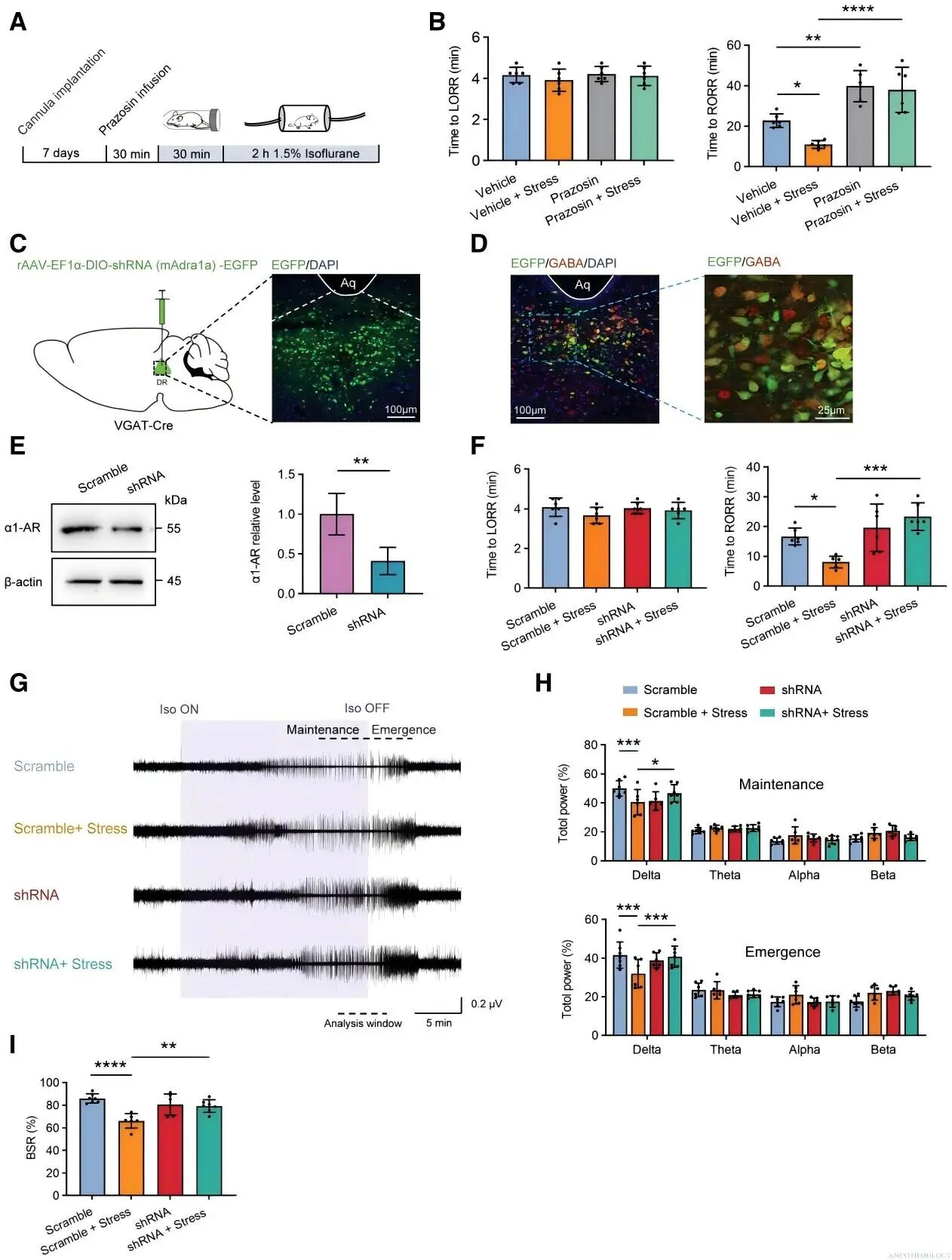
图5.DRNGABA神经元上的α1-AR介导应激诱导的麻醉苏醒加速
本研究强调了LC→DRN环路在急性应激下调节异氟醚麻醉中的作用。应激期间LCNE神经元的激活加速了麻醉苏醒,这主要通过DRNGABA神经元中α1-ARs的去甲肾上腺素能信号传导实现。这些发现强调了在麻醉管理中考虑急性应激的重要性,并表明靶向特定神经通路可能改善手术患者的预后。
本文使用的工具病毒布林凯斯均可提供:
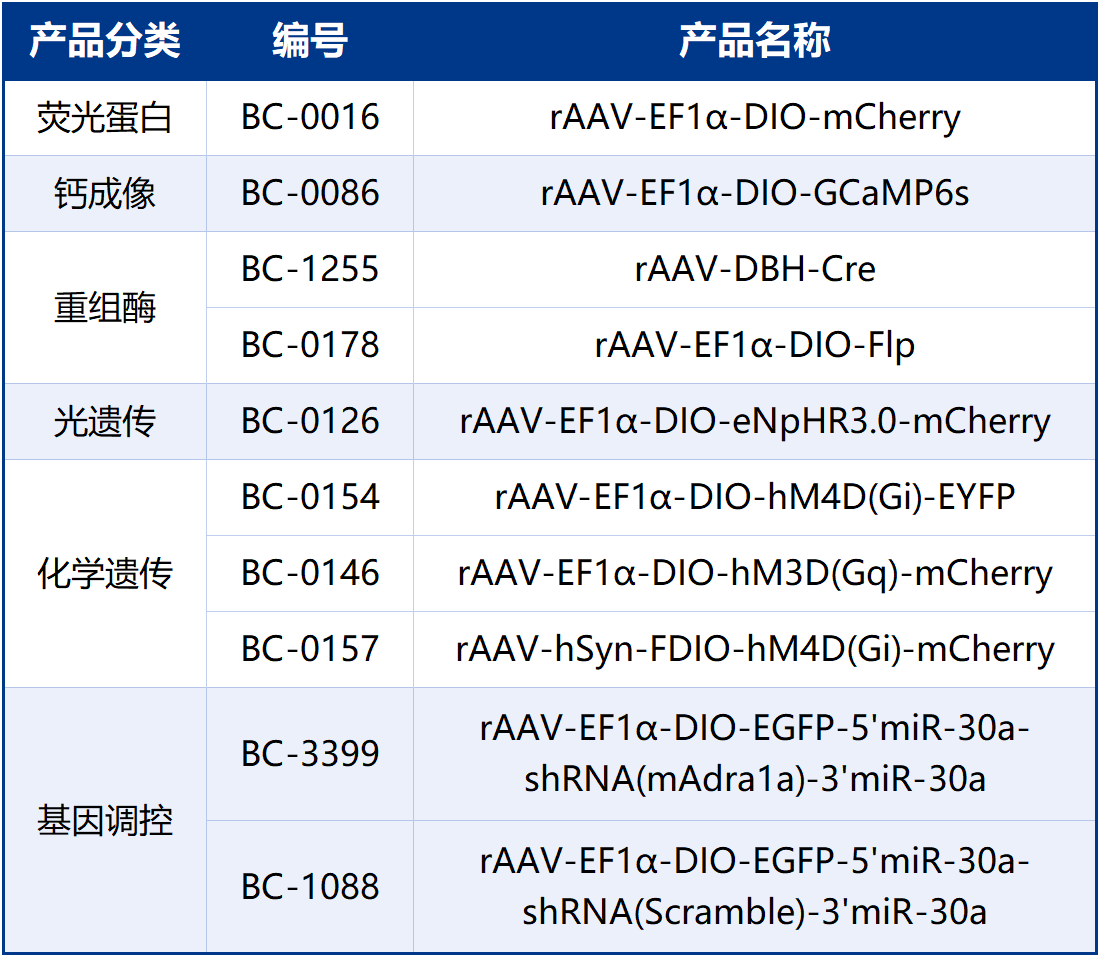
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。