在现代致肥胖环境中,环境线索等认知因素可驱动美味食物过量摄入,进而加剧肥胖流行,但这一现象背后认知因素调控食欲的细胞与分子机制尚未明确;已知内侧前额叶皮层(mPFC)可能参与食欲调控,AMPK作为能量稳态的核心调控因子,其在皮层中的具体作用仍有待深入探索,因此亟需明确相关神经环路与分子信号的调控机制。
2026年1月6日,复旦大学脑科学研究院/脑功能与脑疾病全国重点实验室许智祥教授研究团队在《Cell Discovery》期刊上发表题为Prefrontal cortex-to-hypothalamic outputs orchestrate cuepotentiated palatable food consumption via AMPKβ2 signaling的文章,该研究发现环境线索通过激活前额叶皮层边缘前皮层(PrL)CaMKIIα+神经元AMPKβ2信号,诱导其发生依赖于ATP代谢的细胞可塑性,进而驱动其投射至外侧下丘脑(LH)食欲素神经元的特定环路,最终导致对高脂饮食(HFD)的线索性过度摄食。

研究采用改良的条件性喂养范式,将HFD或普通饲料与特定环境配对(CTX+组)及非配对中性环境(CTX-)进行训练,行为学结果显示,HFD配对环境能显著促进饱腹小鼠对该饮食的摄入量,而普通饲料配对环境无此效应(图1a)。为探究其神经机制,c-Fos染色检测了多个脑区对HFD配对环境的反应,发现仅PrL和中央杏仁核(CeA)Fos⁺细胞数量显著增多(图1b)。免疫荧光显示,大多数被激活的神经元主要为CaMKIIα⁺亚型(图1c,d)。向PrL注射AAV-GCaMP6s(图1e-g),发现这些神经元在HFD摄入时被强烈激活,而在普通进食时仅当小鼠处于禁食状态才被激活,且其活动峰值与进食量正相关(图1h-k)。最后,训练小鼠将HFD与双室箱一侧配对,小鼠仅进入HFD配对侧环境(无食物)即可激活PrLCaMKIIα⁺神经元(图1l-n),且在该环境中实际摄入HFD时,神经激活程度比训练前单纯进食时更强(图1o,p)。综上,PrLCaMKIIα⁺神经元可被HFD摄入及其相关环境线索特异性激活,且参与调控受食物适口性和营养状态影响的食欲动机,揭示了环境背景调控HFD摄入的关键神经机制。
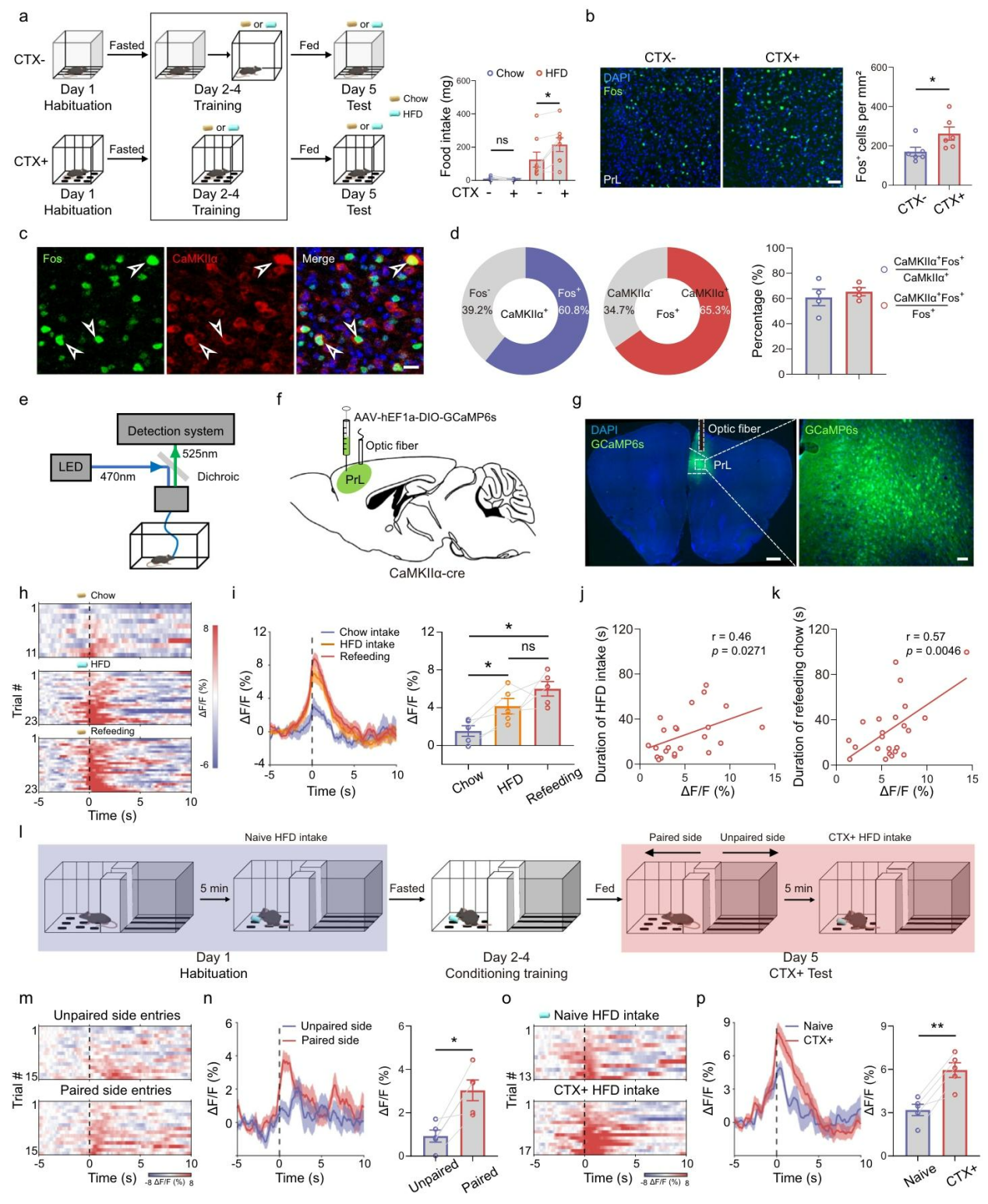
图1 PrLCaMKIIα⁺神经元可被HFD摄入及HFD配对环境激活
为明确条件化环境情境增强HFD摄入期间PrLCaMKIIα⁺神经元活动的机制。单细胞微型显微镜钙成像技术发现(图2a-c),HFD配对环境能特异性激活边缘前皮层神经元群体。选择性反应指数(SRI)分析发现,响应训练后环境线索与训练前naive环境的神经元群体重叠度低,表明PrL神经元能区分高脂食物相关与中性环境(图2d,e)。通过线性支持向量机(SVM)解码分析发现,基于PrLCaMKIIα+神经元群体活动,能以高于随机水平的准确率区分HFD配对环境与中性环境,在进入环境3秒后解码准确率达到峰值。在HFD进食场景中,训练后(CTX+HFD)与训练前(naive+HFD)激活的PrL神经元群体仅有15.2%的重叠,且两组神经元在PrL区域呈混合分布无空间聚类。(图2f-k)。进一步分析表明,边缘前皮层神经元群体的活动能准确预测小鼠进入条件化环境及在该环境中的进食时长(图2l,m),且这种神经活动与进食量增加存在关联。条件化训练后,编码“配对环境-HFD”的神经元对条件化线索的反应显著增强(图2n,o),表现出活动依赖性的可塑性,且这种可塑性是环境特异性的。
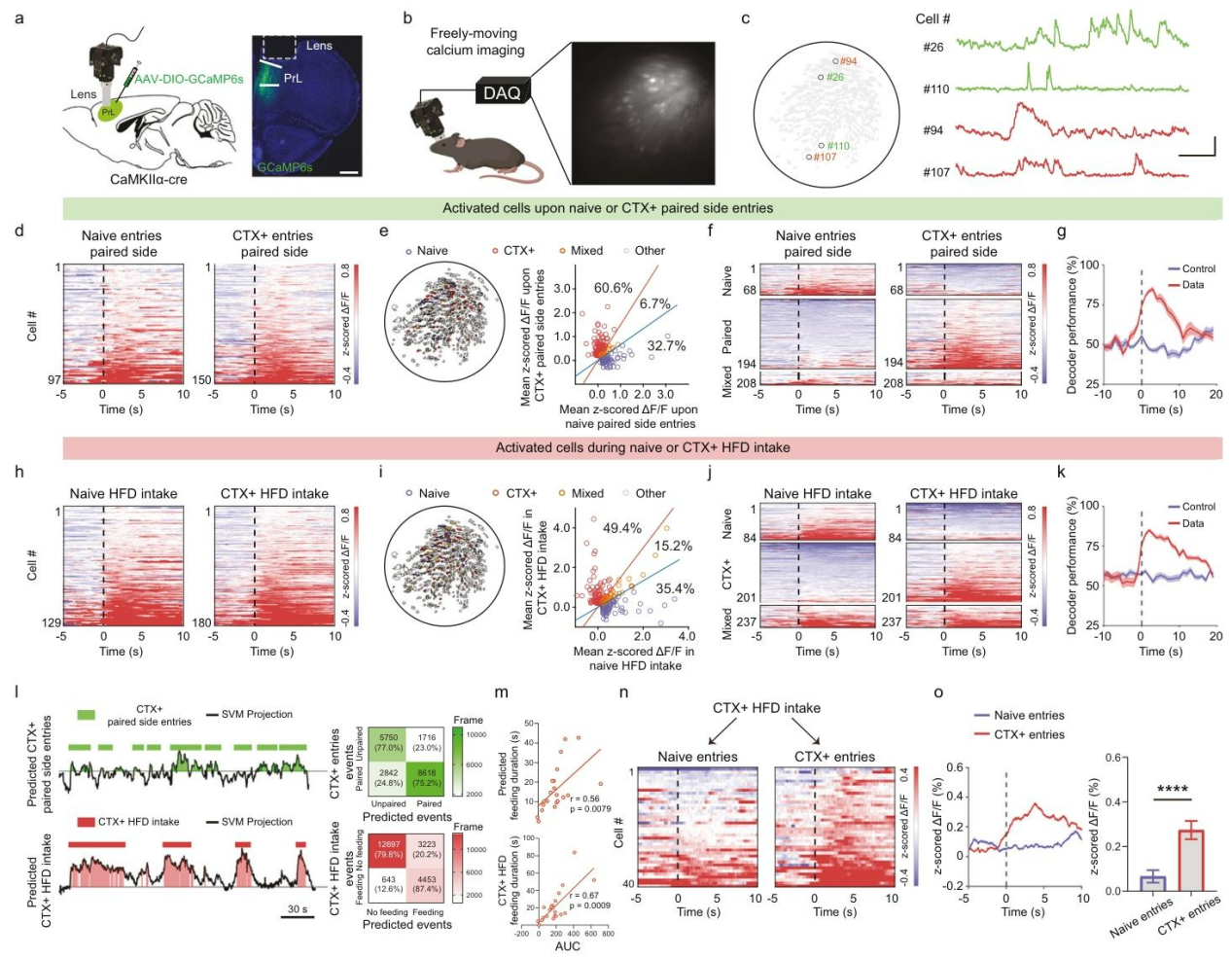
图2 PrLCaMKIIα⁺神经元在环境情境与HFD的关联学习过程中表现出活动依赖性可塑性
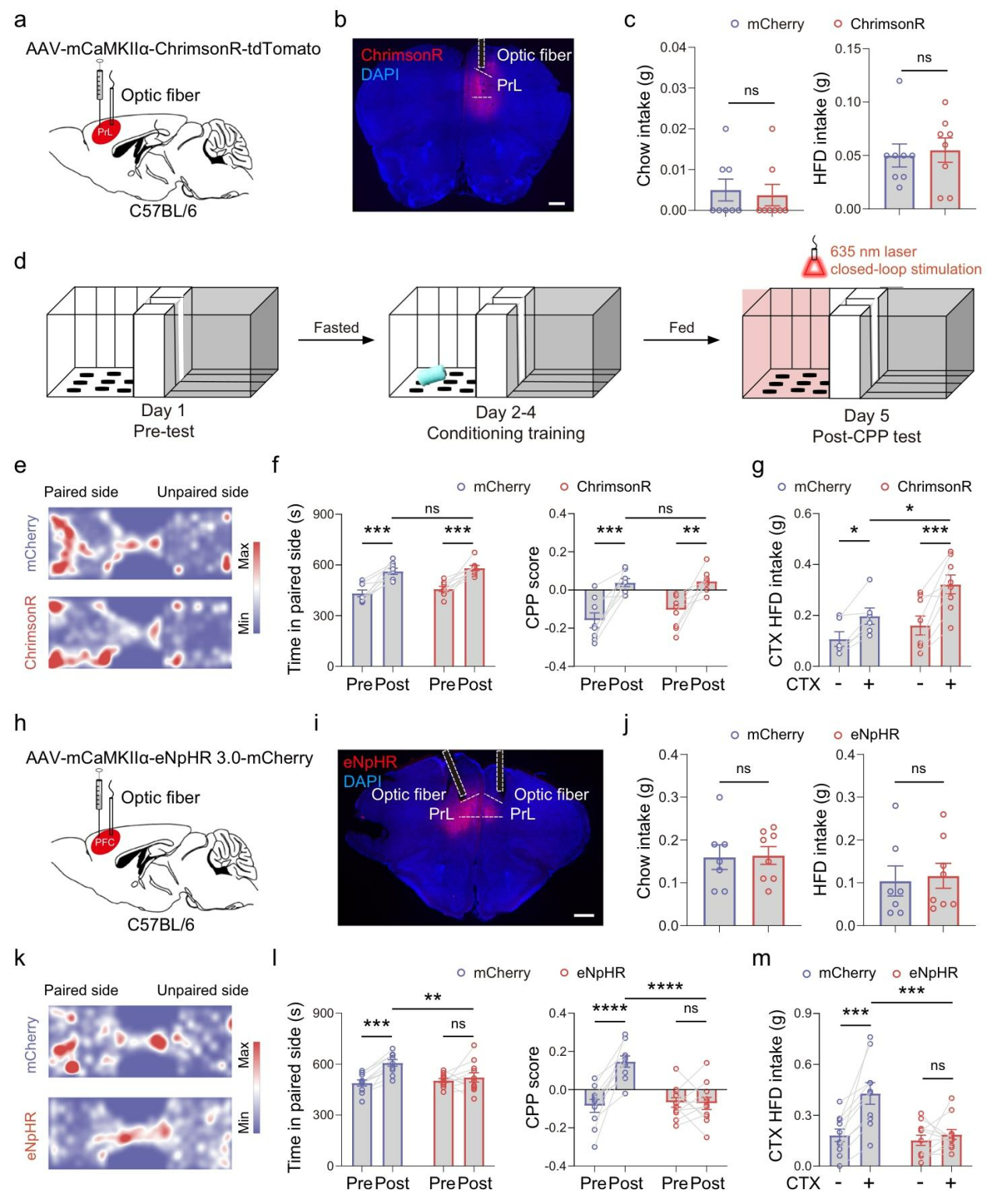
图3 PrLCaMKIIα⁺神经元可双向调控HFD配对情境下的高脂饮食摄入
为解析环境线索诱导HFD过量摄入的分子机制,研究对HFD配对环境(CTX+组)和中性环境(CTX-组)小鼠的PrL区细胞进行RNA测序,发现CTX+组联想学习、ATP代谢通路相关基因显著上调(图4a-c)。在小鼠PrL区注射AAV-GRABATP1.0监测能量动态(图4d),显示进食时细胞外ATP浓度与摄食时长负相关,且CTX+组HFD摄入时ATP降幅更大,ATP外流抑制剂盐酸甲氟喹可逆转该变化(图4e-f),提示信号下降与细胞内ATP降低相关;进一步发现空腹仅上调边缘前皮层AMPKβ1/β2表达,且β2亚基上调更显著(图4g-h)。构建Prkab2flox/flox小鼠并通过PrL区注射AAV-Cre实现AMPKβ2敲除(图4i),微型显微镜钙成像显示,敲除小鼠HFD摄入时PrL区神经元活动降低,线性解码器性能下降(图4j-n)。功能验证表明,AMPKβ2缺失削弱了神经元对条件化环境中HFD摄入的预测能力,大幅降低CTX+组神经元活动依赖性可塑性(图4o-q);采用CRISPR/Cas9技术敲除PrL区AMPKβ2也得到一致结果(图4r-u),表现为小鼠HFD配对箱位置偏好消失,线索诱导的HFD过量摄入被抑制(图4v-x)。综上,PrL区AMPKβ2信号通过调控神经元活动可塑性,介导环境线索与HFD的关联学习,调控线索诱导型HFD过量摄入。
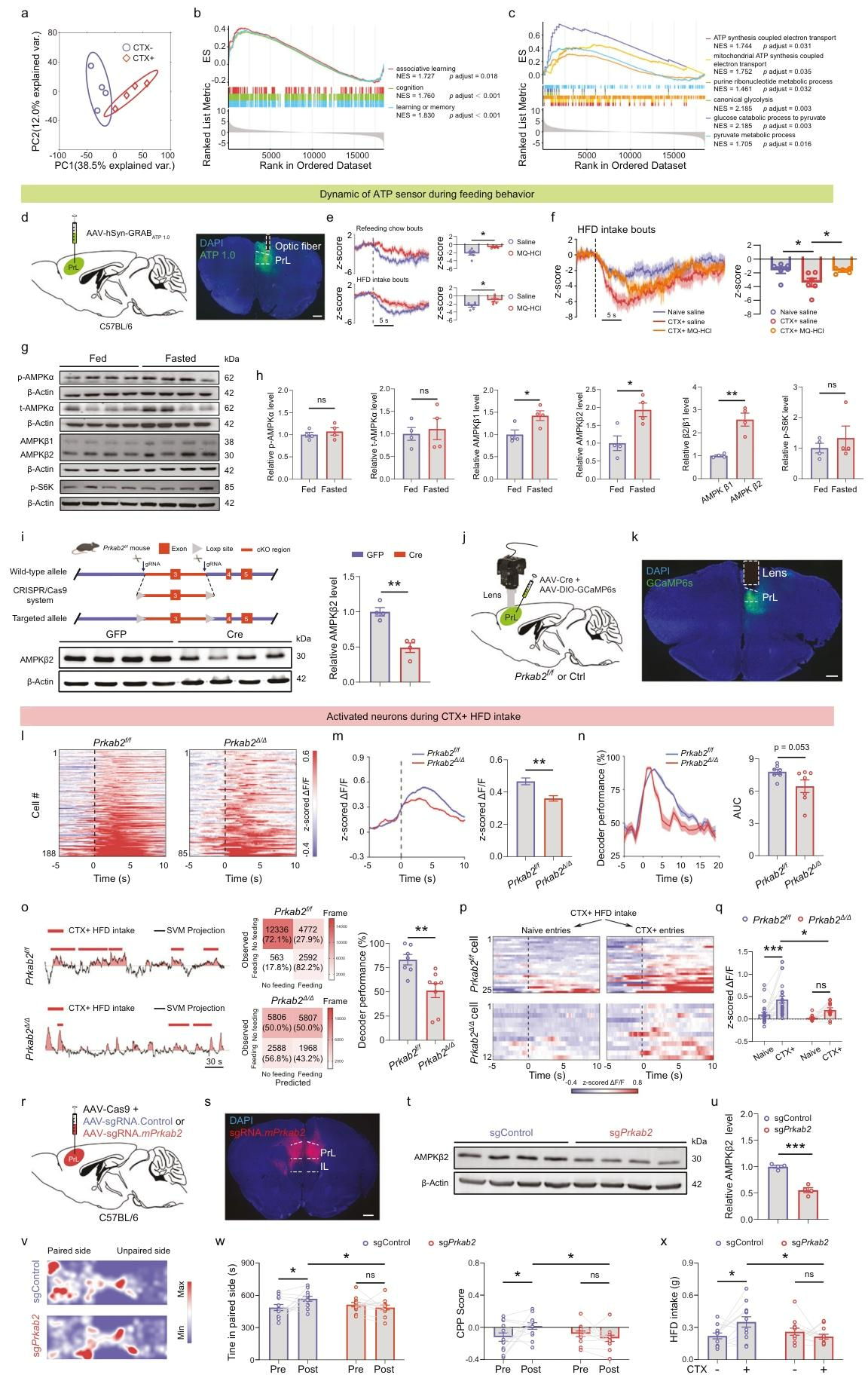
图4 PrL区域AMPKβ2信号调控线索诱导HFD过量摄入
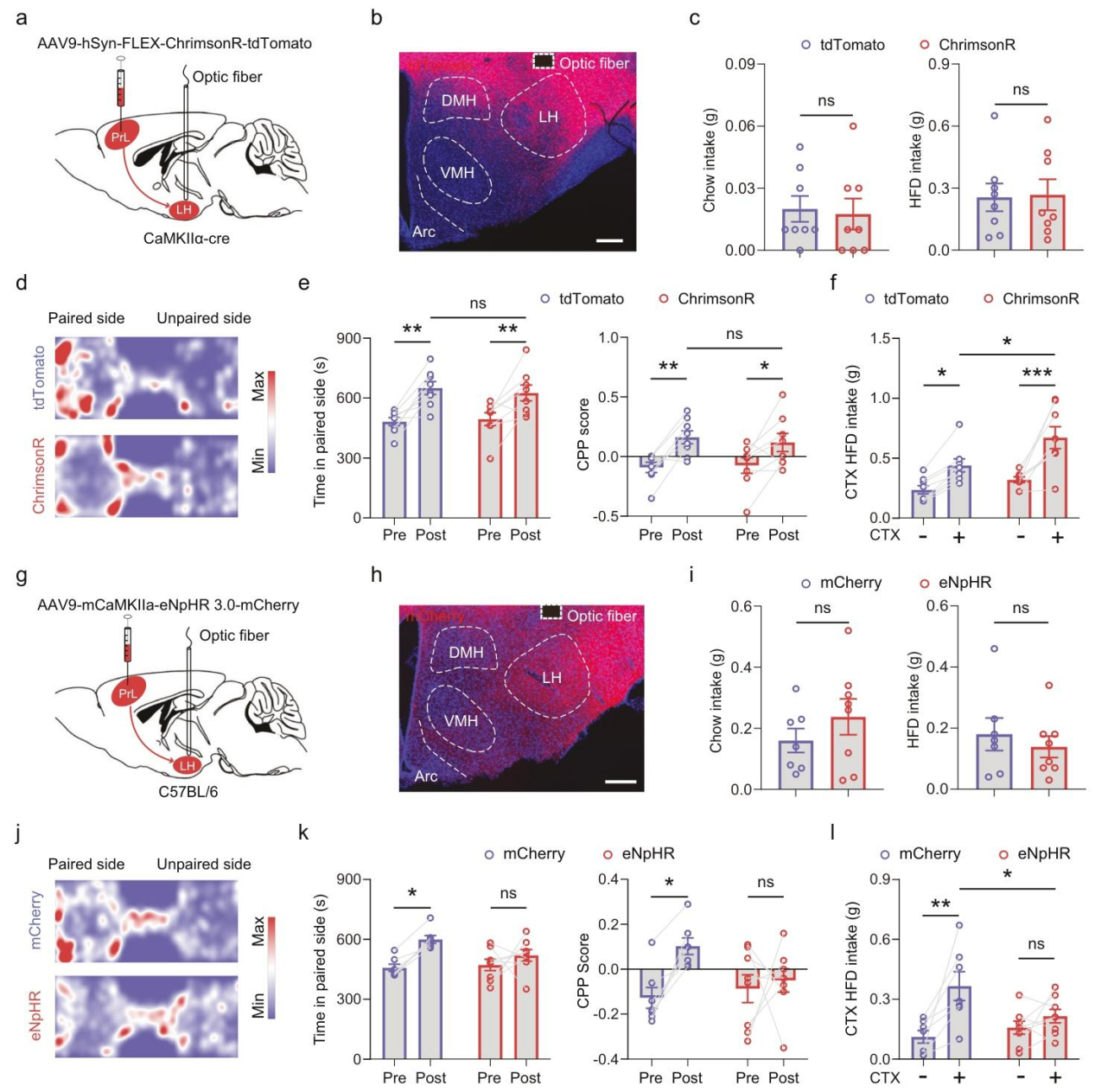
图5 PrL→LH环路活动介导位置偏好,并在配对环境中诱发高脂饮食的过量摄入
进一步探究细胞机制,光激活PrL→LH环路后,LH内63.6%的激活细胞为食欲素神经元(图6a-c)。为证实PrL对LHorexin+神经元的单突触输入,构建Hcrt-cre转基因小鼠(图6d-f),向其LH注射Cre依赖性辅助病毒(AAV-DIO-TVA-mCherry和AAV-DIO-RG),两周后,同一部位注射RV-EnvA-ΔG-EGFP,七天后,注射部位观察到大量双色标记的起始神经元,PrL中出现了大量被狂犬病病毒标记的神经元,证实了PrL对LH食欲素神经元存在单突触输入(图6g-i);利用顺行跨突触AAV1靶向该环路,发现光激活接收PrL投射的LH食欲素神经元可显著增加配对情境下的HFD摄入量(图6j-l)。采用化学遗传学技术抑制该环路(图6m、n),结果显示其不影响饲养笼内的基础摄食量(图6o),但显著削弱小鼠对HFD配对情境的偏好及过量摄入(图6p-r)。综上,PrL→LHorexin+神经元环路是介导环境线索诱导HFD过量摄入的关键通路。
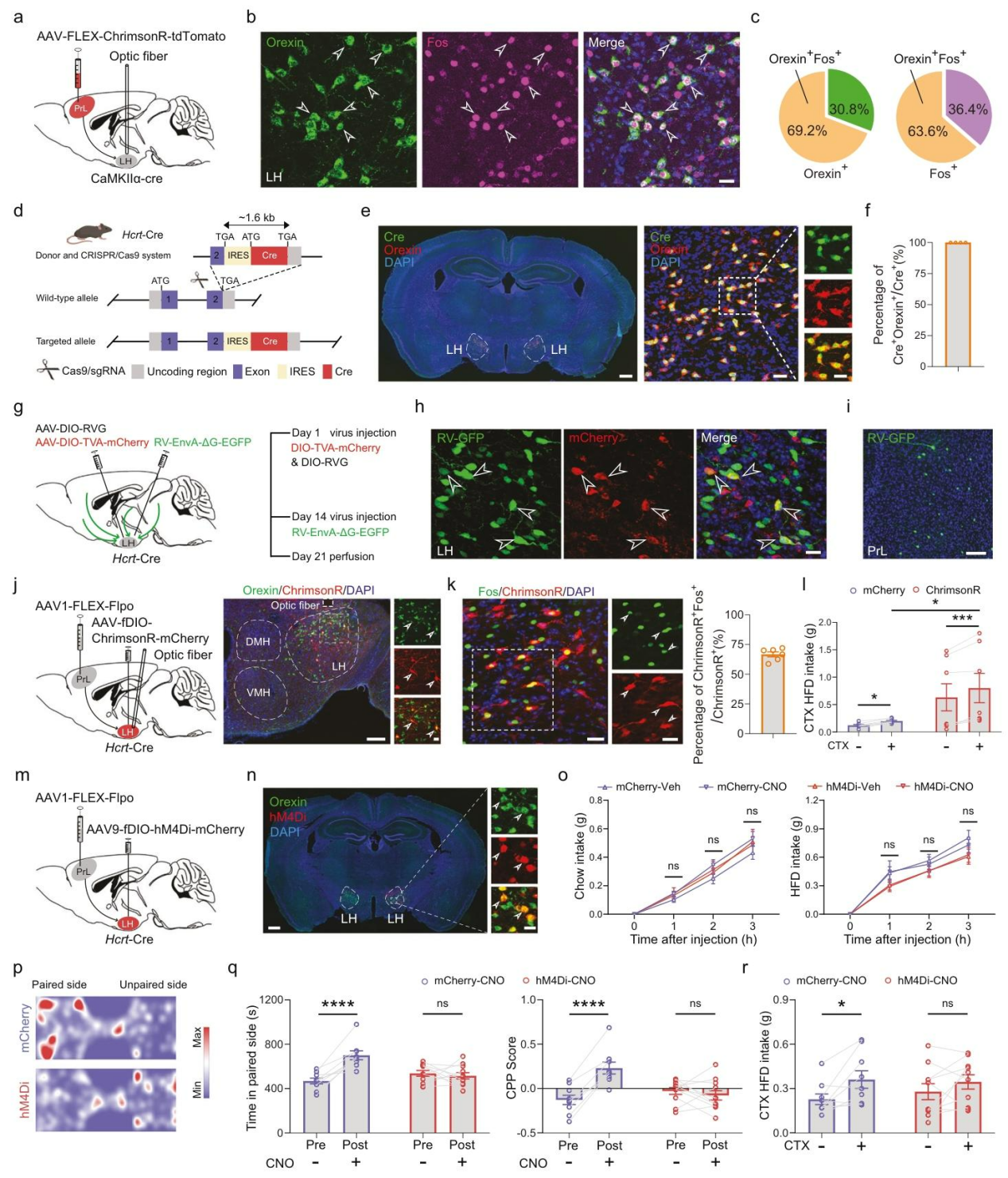
图6 PrL→LHorexin+神经环路调控相关情境下的高脂饮食摄入
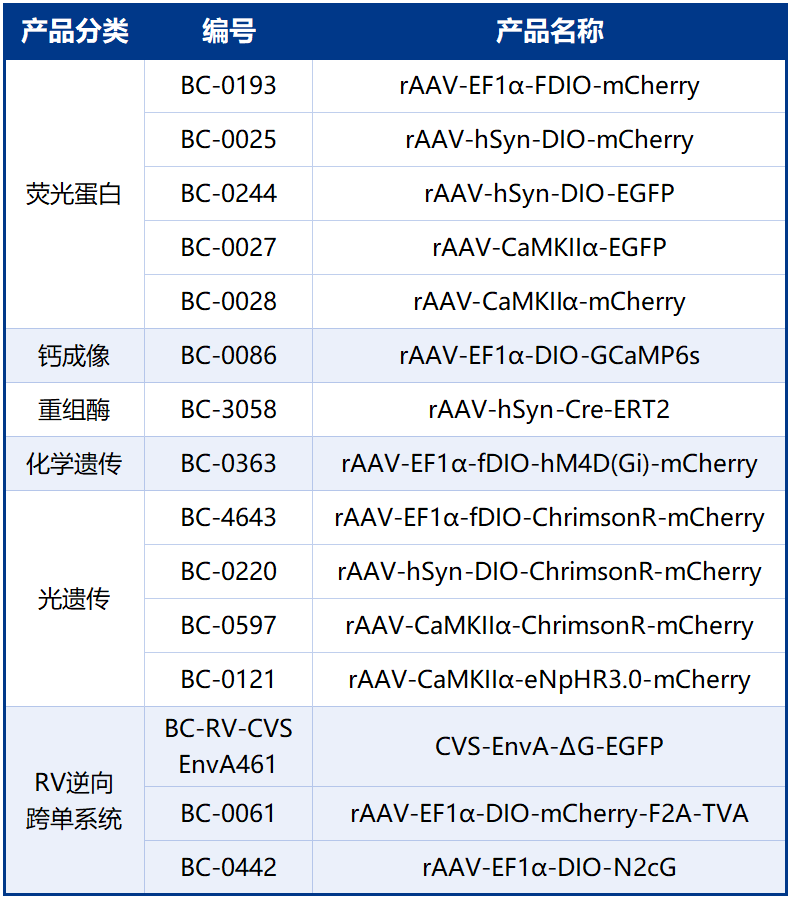
本文使用的工具病毒均由布林凯斯提供如下:
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。