药物暴露形成的药物奖赏关联记忆是药物成瘾及复吸的重要原因,药物关联环境线索提取该记忆可触发药物渴求与复吸。尽管以往研究认为腹侧被盖区(VTA)通过多巴胺能信号在药物奖赏加工中起核心作用,内侧前额叶皮质(mPFC)参与药物关联奖赏记忆加工,目前公认的VTA-mPFC、VTA-伏隔核(NAc)-mPFC环路无法充分解释外部情境信息如何与内部奖赏信号有效整合机制。
2026年1月15日,南京中医药大学医学院的关晓伟/范宇团队在《The Journal of Clinical Investigation》上发表了题为“A midbrain–cortical circuit mediated by claustrum neuronal ensemble orchestrates drug-paired context memory processing”的研究论文。该研究首次发现并证实一条以屏状核CL为中心、负责整合药物奖赏信号与环境线索的关键神经环路—VTA-CL-mPFC,调控该环路或其核心VTA-CL-mPFC神经元集群,能破坏甲基苯丙胺(METH)关联情境记忆提取并阻断雄性小鼠METH条件性位置偏爱(CPP)的获得,且多巴胺(DA)释放及D1R介导的CL神经元激活是该记忆提取的必需条件,揭示了该环路在药物关联环境线索记忆提取中的关键作用。

本研究开展系列实验,向Ai14小鼠CL注射逆标病毒Retro-mTH-Cre(图1A),fMOST成像显示tdTomato阳性胞体主要位于同侧VTA(图1B);向VTA注射Cre系统病毒(图1C),可见VTATH终末分布于CL处CaMKII阳性神经元周围(图1D);CL注射逆行示踪剂CTB555后(图1E),VTA中阳性神经元与TH共标(图1F),证实VTATH-CL通路存在。化学遗传学激活该通路并记录CLDA3h信号,发现激活VTATH神经元可诱导多巴胺释放(图1G、H)。膜片钳记录显示,光遗传学激活VTATH终末可增加CL神经元AP数量(图1I),且该效应被D1R拮抗剂阻断(图1J),证实调控依赖D1R。
向CL注射突触定位病毒(图1K),mPFC内检测到mRuby阳性信号(图1L);向mPFC注射逆行示踪病毒后(图1M),91.8%的阳性CL神经元为CaMKIIα阳性(图1N),证实CL谷氨酸能投射。膜片钳记录显示,蓝光刺激可诱发电信号,TTX抑制、4-AP恢复且NBQX与AP5可阻断该信号(图1O,P),证实单突触功能连接。WT小鼠VTA注射顺行跨单AAV1-Cre病毒(图1Q),CL注射DIO-EGFP病毒,可见CL处EGFP胞体信号、mPFC内见阳性轴突终末(图1R);采用交叉病毒策略向VTA、mPFC及CL分别注射AAV1-Cre,Retro-DIO-FLP和fDIO-EGFP,成功标记了VTA-CL-mPFC神经元群体(图1S、T),初步证实存在VTA-CL-mPFC神经元群体及相关环路。
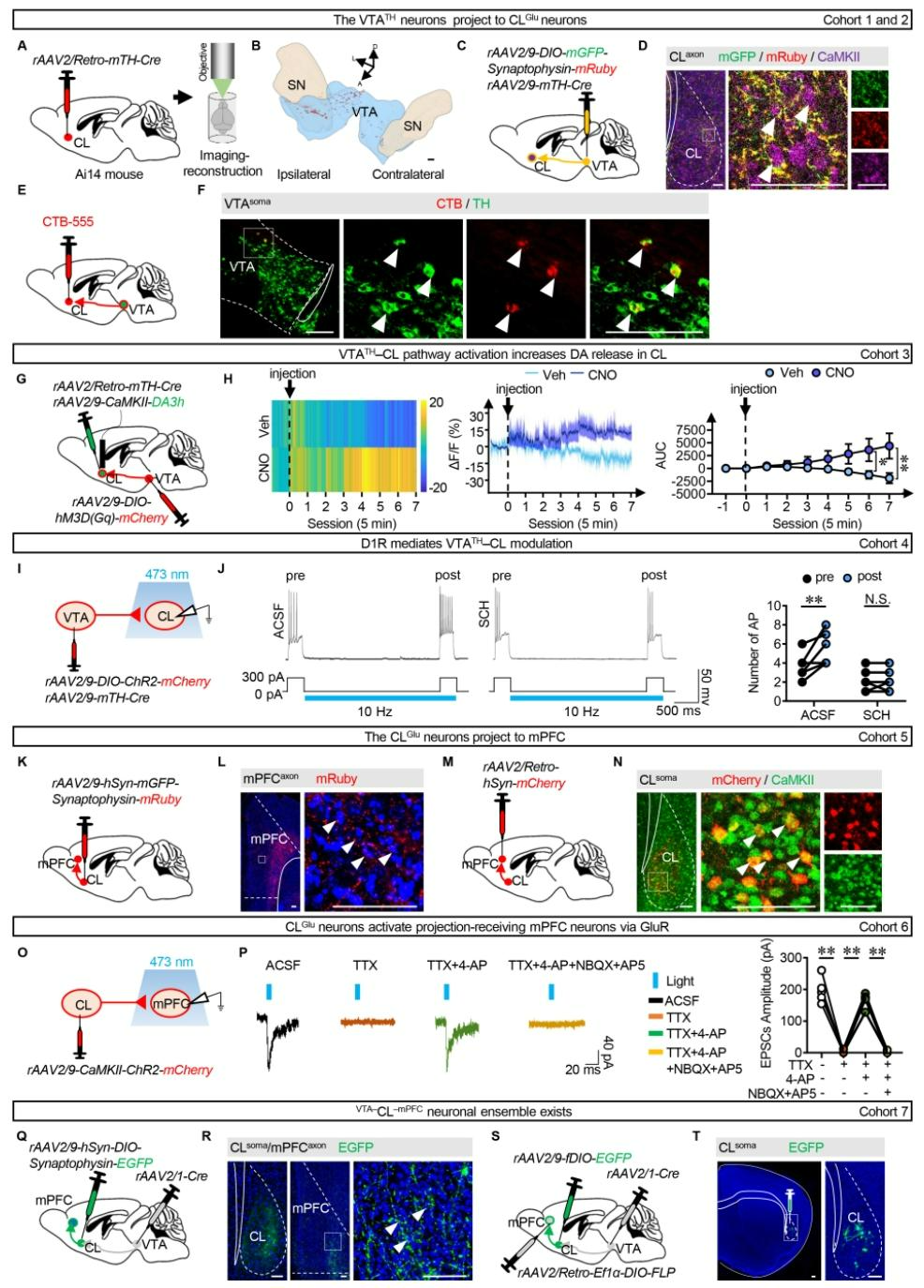
图1 VTATH–CLGlu–mPFC环路及VTA-CL-mPFC神经元集群的存在
为评估CL脑区在METH(一种高成瘾性中枢神经兴奋剂)关联奖赏行为中的作用,对雄性小鼠进行8天METH-CPP(条件性位置偏爱)训练并于第9天测试,结果METH暴露组小鼠的CPP得分显著高于生理盐水组,而两组运动能力无差异,成功构建METH诱导的CPP奖赏记忆模型(图2A-C)。c-Fos及免疫荧光结果显示,METH暴露显著激活CLGlu神经元,而非GABA能神经元(图2D)。在体钙成像记录显示,当小鼠从非药物配对箱进入METH配对箱时,METH组小鼠CLGlu神经元的钙信号在最初4秒内显著升高,证实该神经元在METH奖赏记忆提取阶段被特异性激活(图2E-H);通过化学遗传抑制小鼠CLGlu神经元能够特异性减弱METH-CPP记忆的提取(CPP得分降低),而对生理盐水组无影响,且不影响小鼠的运动能力(图2I-M)。综上,CLGlu神经元在METH关联环境线索触发奖赏记忆提取的过程中被特异性激活,且其活动是该记忆提取的必要条件。
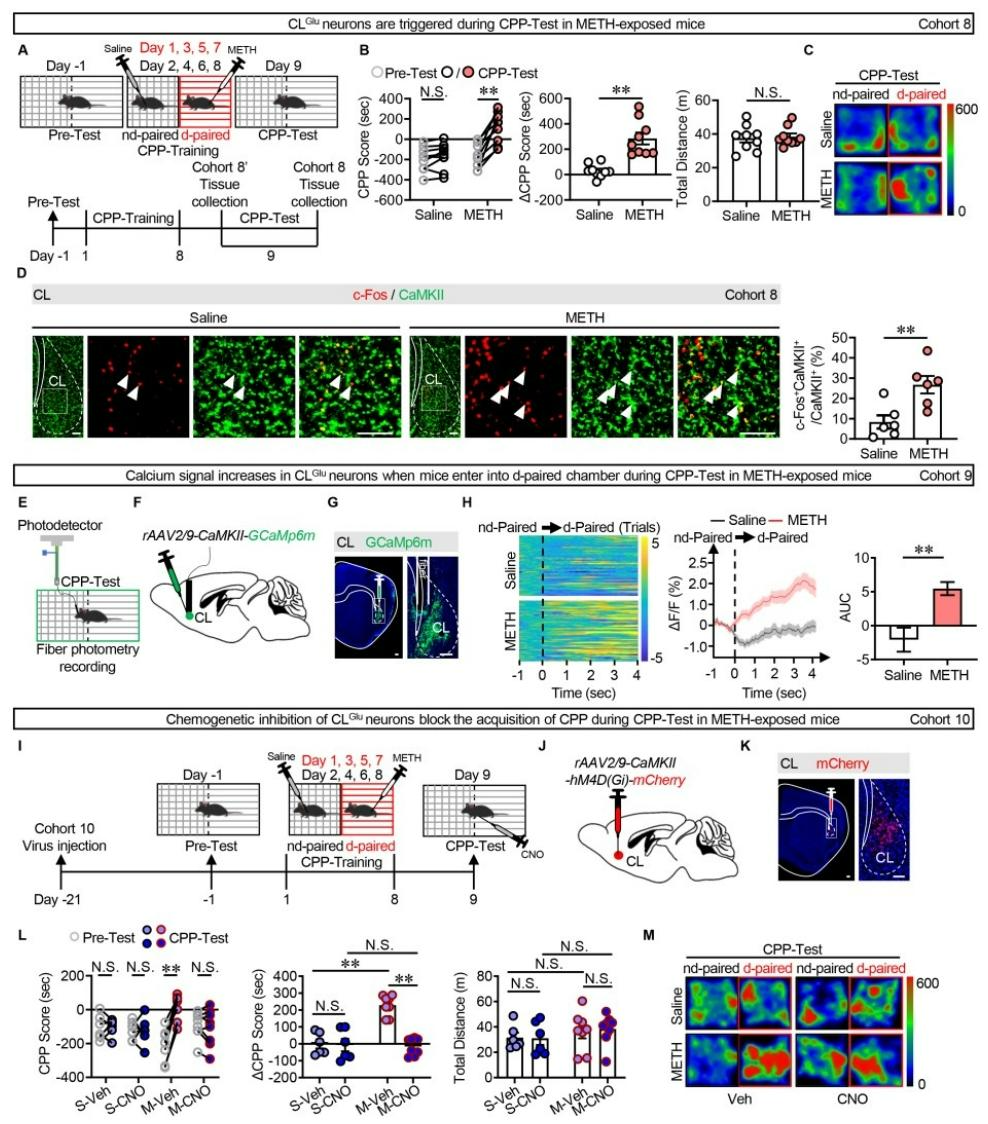
图2 CLGlu神经元参与METH诱导奖赏记忆的提取
为明确VTA-CL-mPFC神经元集群在METH诱导奖赏记忆提取中的作用,采用图1S病毒策略标记雄性小鼠的该神经元集群,结果显示METH暴露的雄性小鼠其VTA-CL-mPFC神经元的树突棘密度和复杂性显著增加(图3A-C),且CPP测试后该神经元集群的AP数量较对照组明显增多(图3D-F),提示METH暴露可激活雄性小鼠的VTA-CL-mPFC神经元。进一步探究该神经元集群在METH-CPP记忆提取中的功能,利用化学遗传病毒策略选择性抑制VTA-CL-mPFC神经元集群(图3G-I),结果发现METH暴露组小鼠表现显著条件性位置偏爱,而CNO介导的神经元抑制可显著减弱药物配对环境的偏好,但不影响运动功能;CNO对生理盐水暴露组则无显著影响(图3J-K)。这一结果证明VTA-CL-mPFC神经元集群参与雄性小鼠METH诱导奖赏记忆的提取。
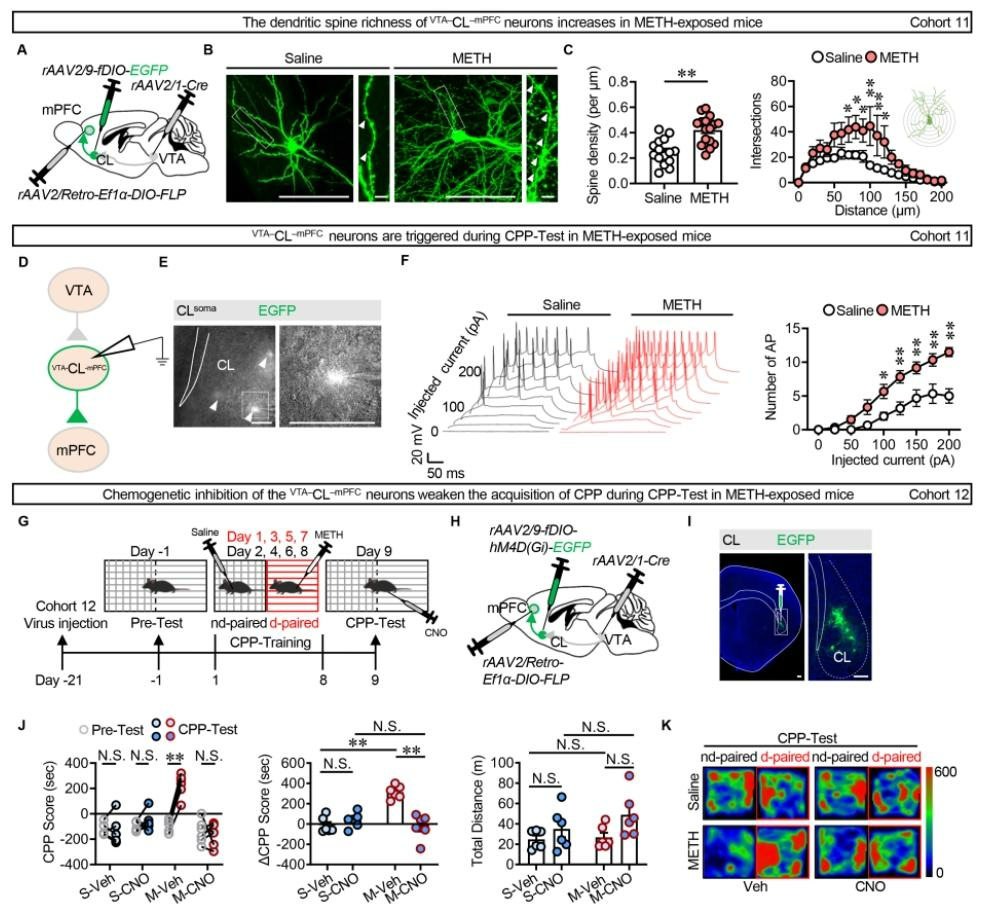
图3 VTA-CL-mPFC神经元集群介导METH诱导奖赏记忆的提取
为探究VTATH-CL通路在METH诱导奖赏记忆提取中的作用,c-Fos免疫荧光结果显示,在METH-CPP测试期间,VTA(而非SN)多巴胺能神经元被特异性激活(图4A)。通过化学遗传学方法选择性抑制投射至CL的VTATH神经元(图4B-F),或在CL局部抑制VTATH神经元末梢的活动(图4G-K),均可有效阻断METH诱导的条件性位置偏爱,显著降低CPP得分,而不影响小鼠的运动能力或生理盐水对照组的偏好行为。综上,VTATH-CL通路活动是提取METH关联环境记忆所必需的。
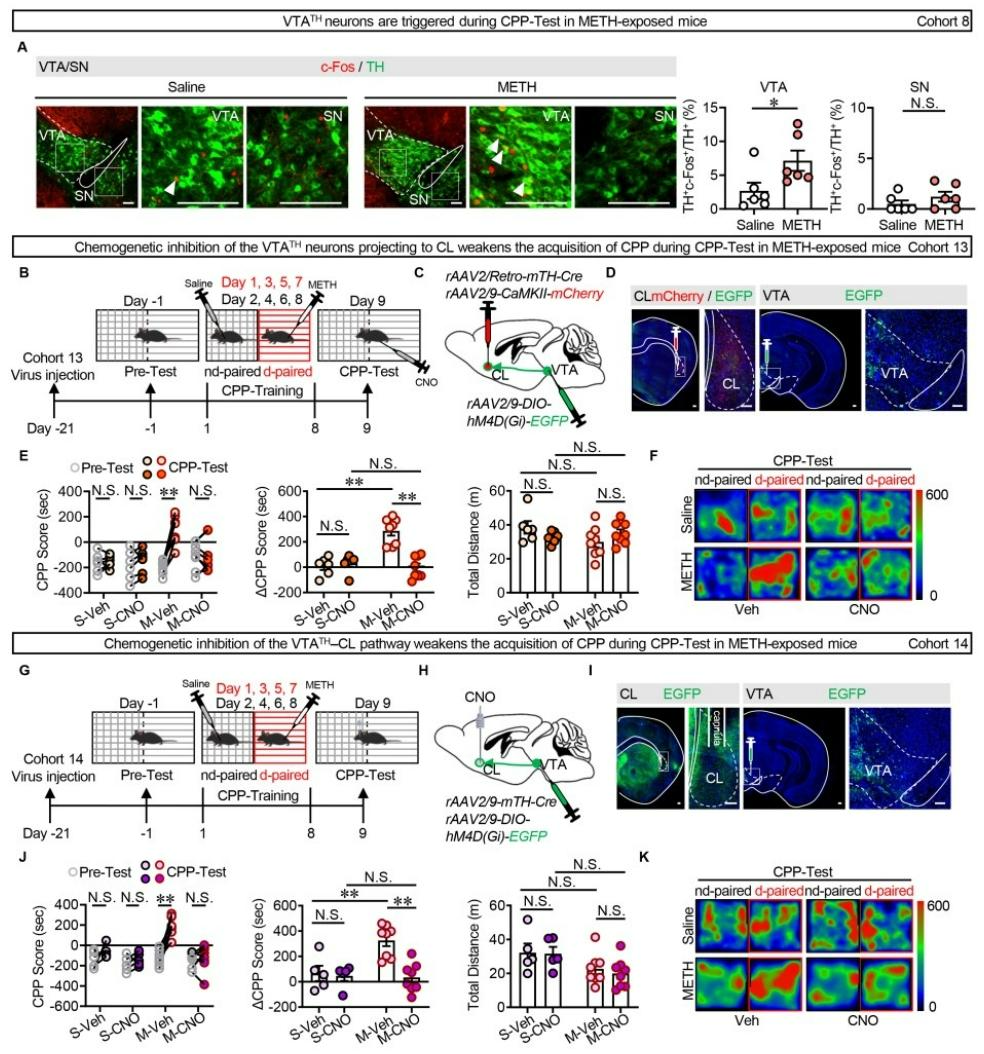
图4 VTATH-CL通路参与METH诱导奖赏记忆的提取
为探究CLGlu-mPFC通路在METH诱导奖赏记忆提取中的作用,c-Fos免疫荧光显示,在METH-CPP测试期间,mPFCGlu神经元的c-Fos含量升高(图5A)。通过化学遗传病毒调选择性抑制投射至mPFC的CL神经元(图5B-D),结果发现CPP测试期间,抑制CLGlu-mPFC通路可有效阻断METH诱导的条件性位置偏爱,显著降低CPP得分(图5E、F),这证实CLGlu-mPFC通路参与METH诱导奖赏记忆的提取。
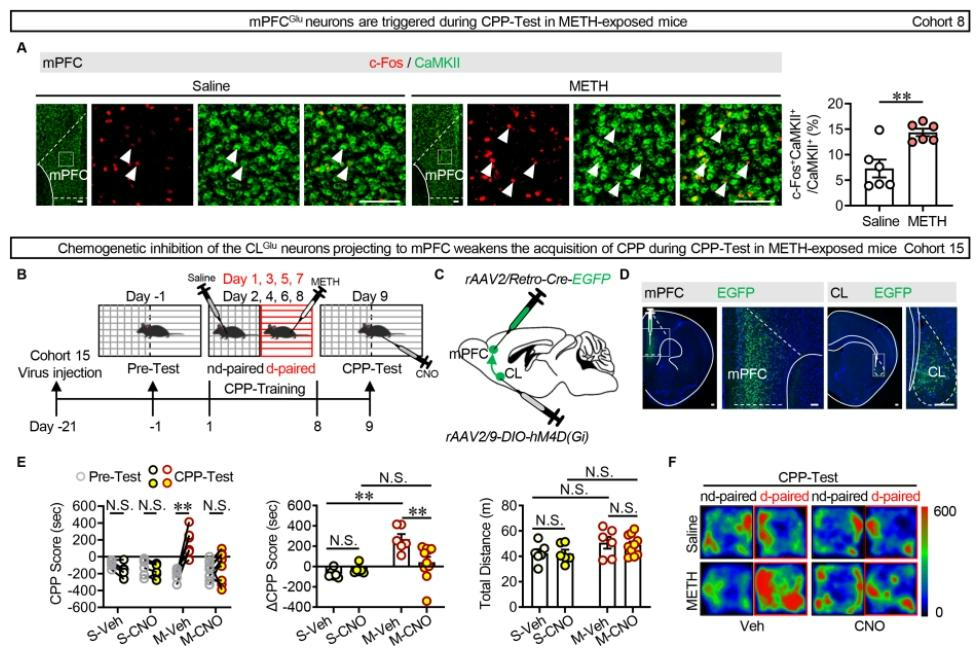
图5 CLGlu-mPFC通路参与METH诱导奖赏记忆的提取
向小鼠CL注射DA3h病毒,光纤光度法实时记录CPP测试期间多巴胺释放(图6A-C)。结果显示METH暴露雄性小鼠完全进入METH配对箱时,CLDA3h信号显著升高(图6D);WB发现METH暴露组D1R蛋白水平升高而D2R无变化(图6E);且METH暴露组CL内c-Fos和CaMKII双阳性(激活的谷氨酸能神经元)上D1R表达平均灰度值高于对照组(图6F),提示METH诱导奖赏记忆提取期间,CL内多巴胺释放增加、D1R水平升高。
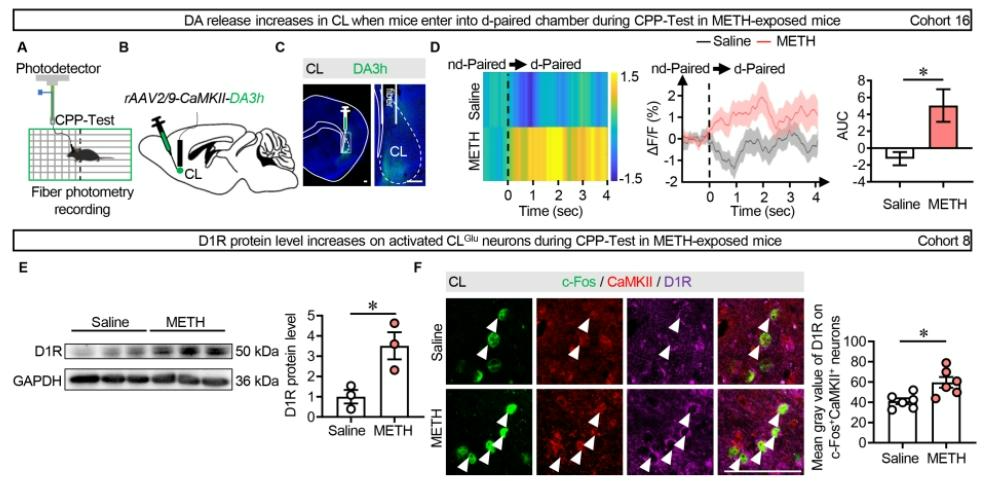
图6 METH诱导奖赏记忆提取期间,CLGlu神经元DA信号及D1R蛋白水平升高
为进一步明确VTATH-CL通路中DA及D1R在METH诱导奖赏记忆提取中的作用,利用化学遗传抑制该通路时,向CL局部补充多巴胺(图7A-E)或D1R激动剂SKF-38393(图7F-J),均可恢复METH暴露小鼠对药物配对环境的的偏好,提示该通路的多巴胺信号参与METH奖赏记忆提取;向CL注射D1R敲低病毒rAAV2/9-CaMKIIα-RNAi-Drd1-EGFP后(图7K-M),METH暴露小鼠CPP得分降低、CLGlu神经元c-Fos阳性比例显著下降,生理盐水组无影响(图7N-P),证实CLGlu神经元上D1R表达上调可促进其激活,参与METH诱导奖赏记忆提取。
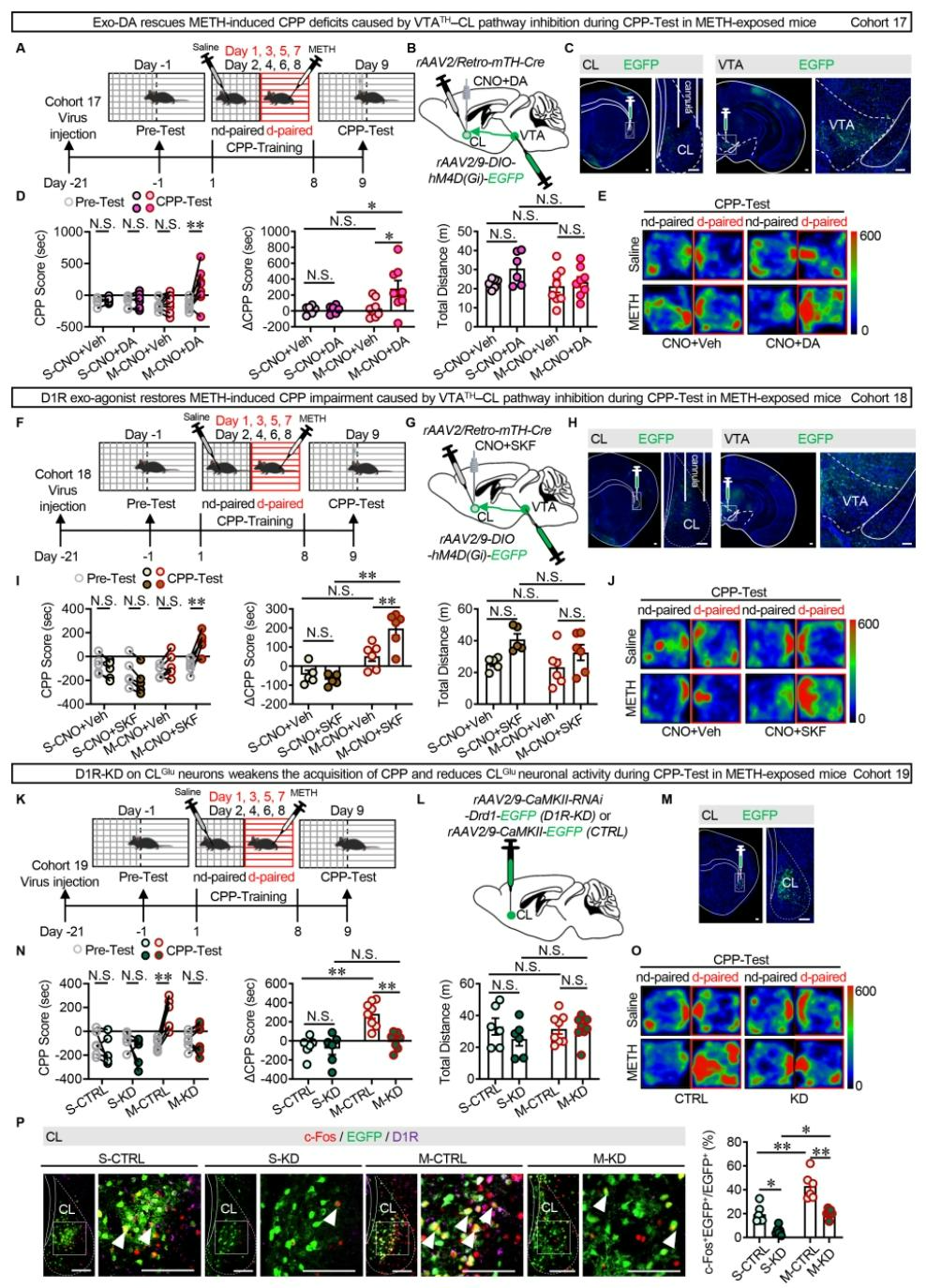
图7 VTATH–CL通路的DA信号传导对METH诱导奖赏记忆的提取至关重要
药物相关记忆可被药物关联线索的再次暴露触发,进而导致觅药行为。本研究以雄性小鼠METH-CPP模型为基础,发现CL为负责整合药物奖赏信号与环境线索的关键枢纽。CL连接VTA与mPFC形成VTA–CL–mPFC环路,调控该环路或VTA-CL-mPFC神经元集群,可破坏METH关联情境记忆的提取。在此过程中,DA信号通路通过CLGlu的D1R介导CLGlu的激活是雄性小鼠METH诱导奖赏记忆提取所必需的。
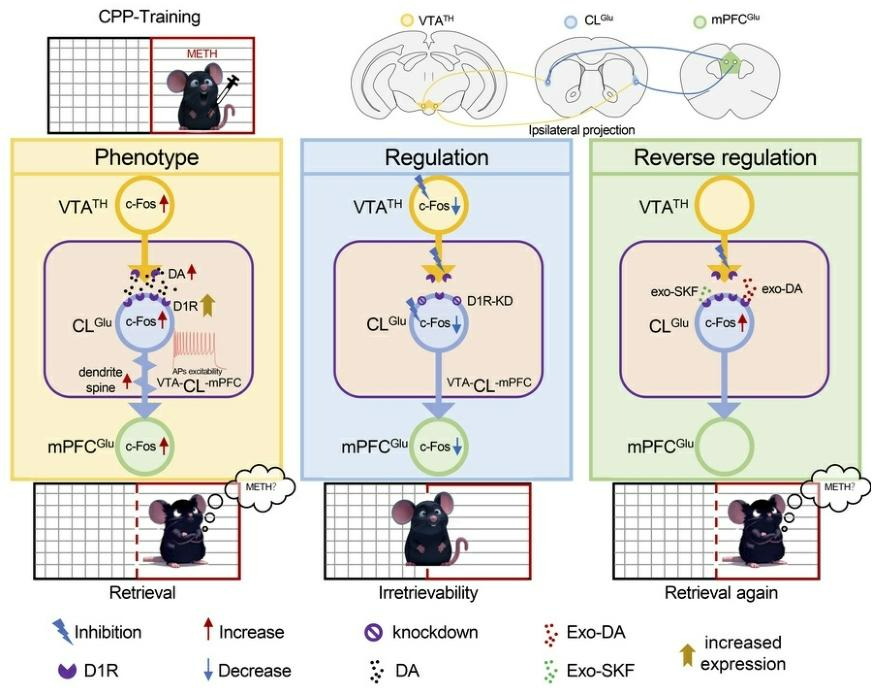
图8 总结图
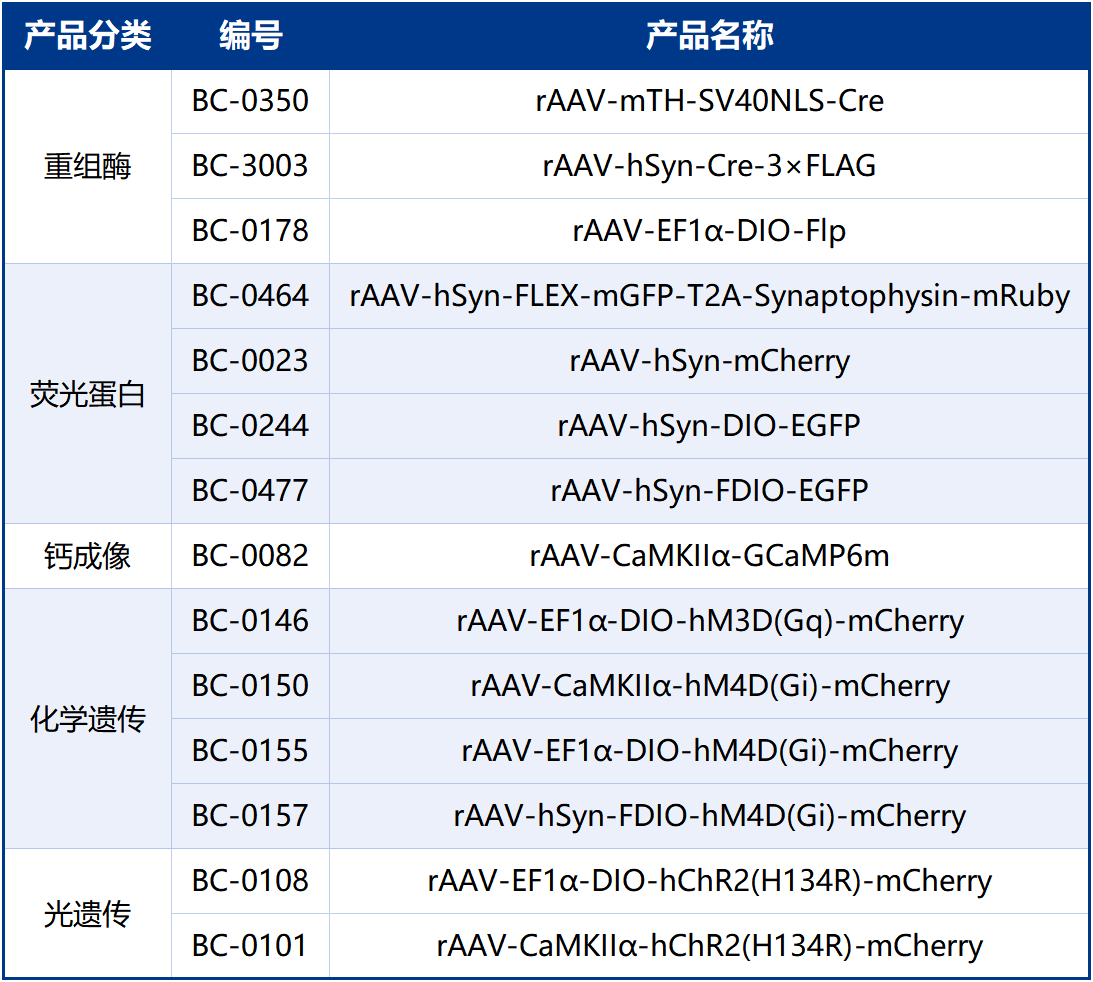
本文使用的工具病毒均由布林凯斯提供如下:
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。