儿童癫痫是常见神经系统疾病,10%-30%发展为难治性癫痫,现有治疗手段存在局限。肠道菌群失调与癫痫相关,但益生菌治疗的疗效和机制尚不明确。
2026年1月16日,深圳先进院脑认知与脑疾病研究所/深港脑科学创新研究院刘欣安副研究员与陈祖昕副研究员团队,联合深圳市儿童医院操德智主任,在国际神经科学权威期刊 Neuron 在线发表题为 “Gut-Brain Cholinergic Signaling Mediates the Antiseizure Effects of Bacteroides fragilis” 的研究论文,揭示脆弱拟杆菌(菌株BF839)通过肠-迷走神经-脑胆碱能信号通路发挥抗癫痫作用,其可激活结肠胆碱乙酰转移酶阳性(ChAT+)细胞、增强乙酰胆碱介导的迷走神经传递,且与肠道乳酸杆菌定植富集相关;临床研究显示,BF839对儿童难治性癫痫治疗有效性。

既往研究表明,癫痫患者肠道菌群存在异常,提示靶向菌群或可为癫痫治疗提供新方向。为了明确癫痫儿童的菌群变化,对114例新诊断儿童癫痫(NDPE)患者及63例健康对照者粪便样本行16S rRNA基因测序(微生物群落分析的核心技术,本质是通过测定细菌中高度保守的16S rRNA基因序列,实现对菌群的分类鉴定、丰度分析和多样性评估)(图1A)。结果显示,两组菌群组成差异显著(图1B、1C),NDPE组α多样性低于对照组(图1D)。NDPE组拟杆菌属丰度显著降低(图1E);大肠埃希菌属、普雷沃菌属、乳酸杆菌属无显著差异,对照组副拟杆菌属水平更高(图1F-1I)。为了验证测序结果并分析难治性癫痫儿童菌群特征,对39例健康对照者和37例难治性癫痫儿童粪便样本进行宏基因组测序(直接对环境样本中全部微生物的总DNA进行高通量测序的技术,无需分离培养单个微生物)。结果与16S rRNA测序一致,两组菌群组成差异显著(图1J、1K),癫痫组脆弱拟杆菌丰度更低(图1L),其他拟杆菌属及乳酸杆菌属无显著差异。上述结果表明,肠道菌群异常(尤其脆弱拟杆菌减少)与儿童癫痫相关,为后续肠-脑轴机制研究及儿童癫痫菌群靶向干预提供了依据。
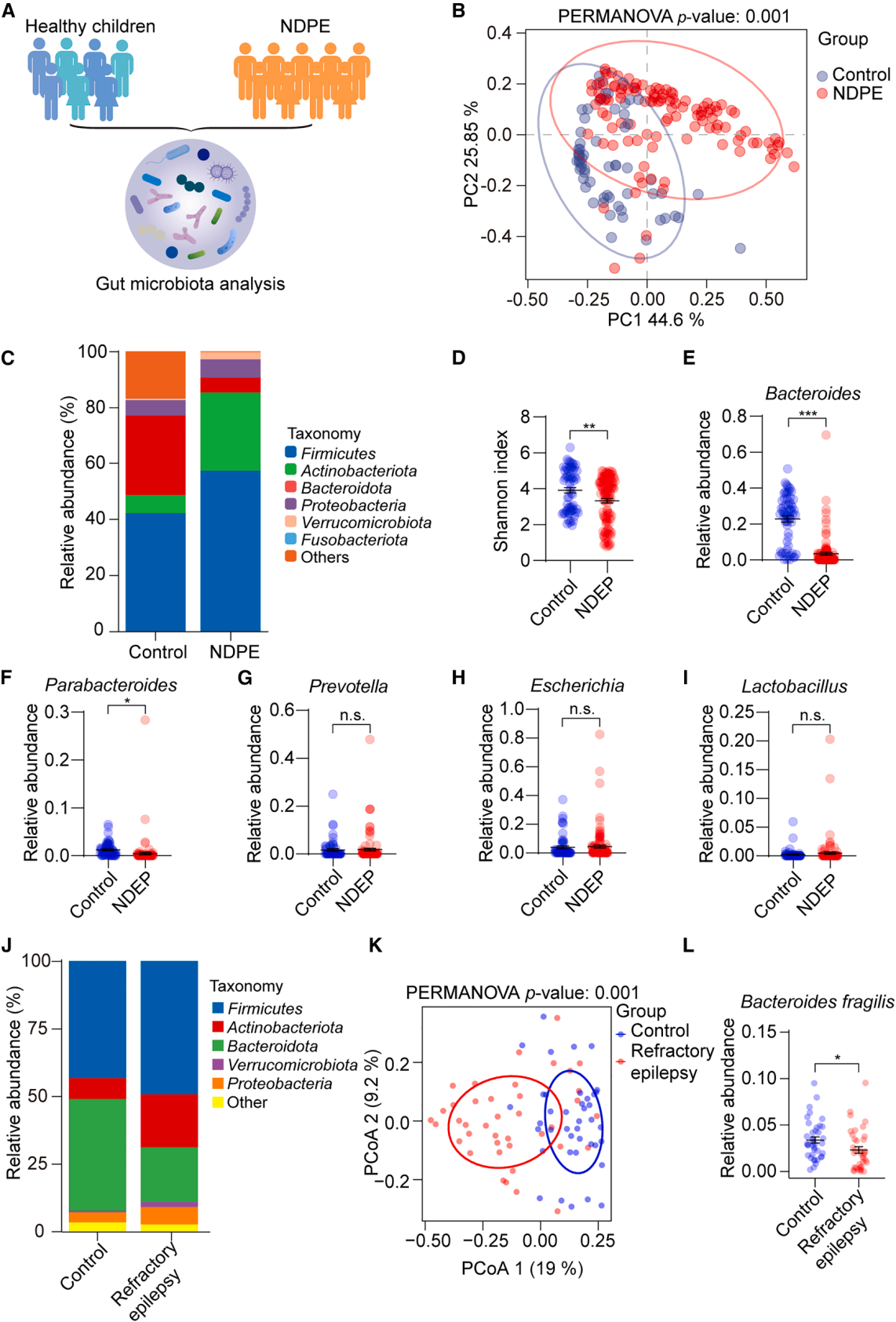
图1. 儿科癫痫患者粪便微生物群组成的改变,包括新诊断和难治性病例
拟杆菌属丰度降低或促癫痫发作,补充该菌属或可干预疾病进展。为了验证其抗癫痫作用,向戊四氮(PTZ)诱导癫痫小鼠施用含脆弱拟杆菌(BF839)的益生菌。4周龄雄性C57BL/6幼鼠灌胃BF839 7天后,用PTZ诱导癫痫(图2A)。菌群分析显示,两组优势菌门均为拟杆菌门和厚壁菌门(图2B),PTZ组拟杆菌属丰度显著低于生理盐水组(图2C),但两组香农指数(Shannon index,衡量样本内微生物群落α多样性的核心指标)无差异(图2D)。BF839组从PTZ注射后第3天起发作频率下降(图2E),第4天起发作程度趋于稳定(图2F),平均发作评分显著低于PTZ组(图2G)。
PTZ点燃模型模拟海马放电异常的难治性颞叶癫痫,本研究通过脑电图(EEG)评估BF839对海马过度兴奋的影响(图2H、2I)。BF839显著降低θ波、α波、β波功率谱密度,对δ波无显著影响。棘波放电(SWDs)是癫痫关键电生理标志(图2J)。BF839组棘波放电密度(图2K)和持续时间(图2L)均显著降低,发作期放电强度减弱。海马神经元过度兴奋伴树突棘形态异常。高尔基染色显示,BF839组树突棘密度显著降低、长度无变化(图2M-2O)。重组腺相关病毒(rAAV-NCSP-YFP-2E5)稀疏标记进一步证实,BF839可降低树突棘密度,不影响长度(图2P)。提示BF839可调控海马树突棘重构,其抗癫痫作用或经肠-脑轴介导。
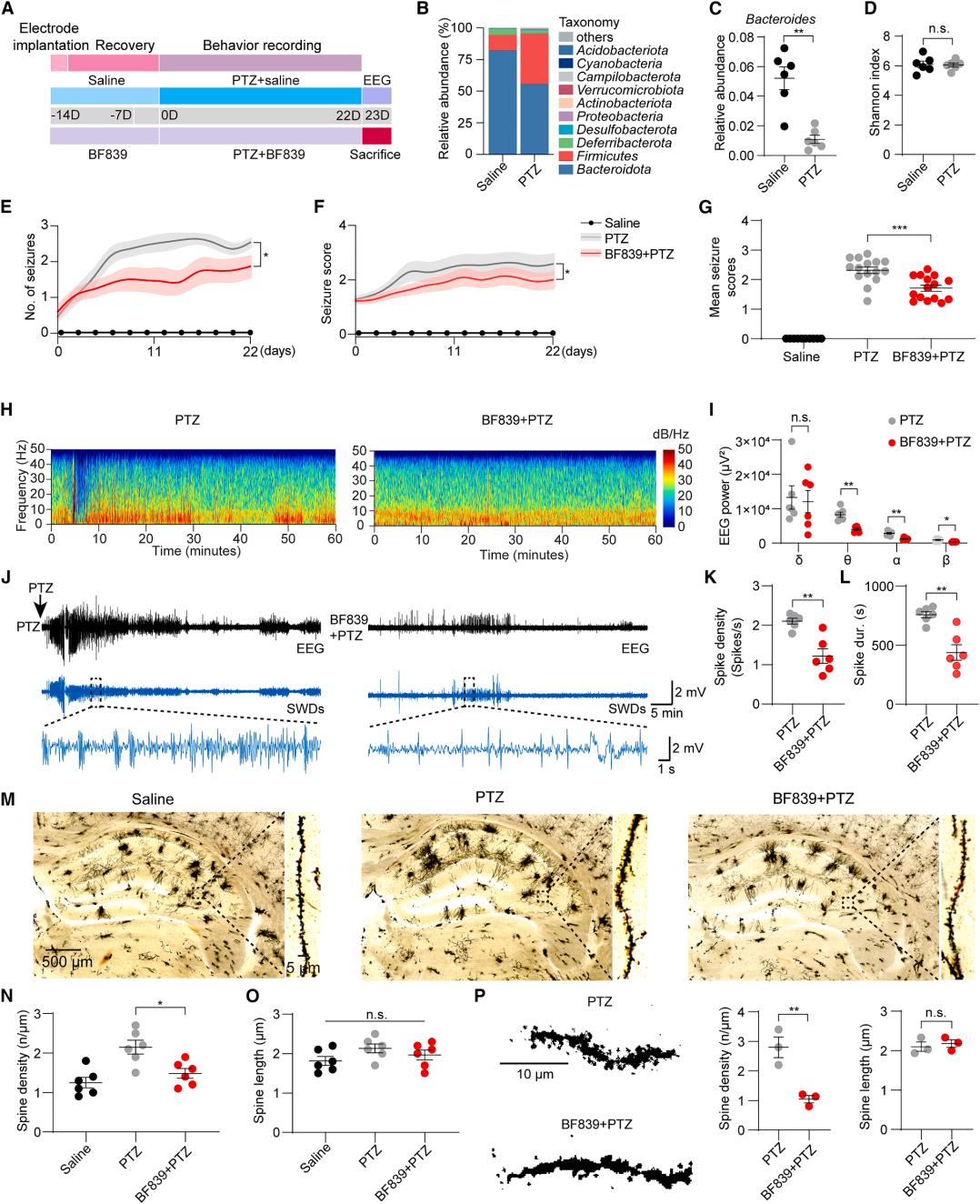
图2. BF839可减轻PTZ诱发的癫痫发作并调节海马神经元的突触活动
迷走神经能介导胃肠与大脑的代谢信号传递,迷走神经刺激(VNS)是难治性癫痫常用疗法,提示二者密切相关。为了验证迷走神经在BF839肠-脑轴抗癫痫效应中的作用,作者记录清醒小鼠自发性迷走神经活动,同时在麻醉小鼠结肠灌注BF839时检测神经节活动以排除运动干扰(图3A)。结果显示,PTZ注射前,BF839处理(BF839+PTZ组)显著增强迷走神经放电频率(图3B、3C);PTZ注射后,其结状神经节活动仍高于PTZ组(图3D、3E)。对比各组PTZ注射前后的迷走神经活动发现,PTZ组迷走神经活动升高显著,BF839组升高温和,提示其增强效应存在阈值上限(图3F)。PTZ注射后用电极刺激迷走神经节(图3G),BF839+PTZ组和联合组(VNS+BF839+PTZ组)发作次数显著少于PTZ组,单独VNS无显著效果(图3H)。联合组发作潜伏期最长,持续时间最短,均优于单独处理组(图3I、3J)。联合组发作评分低于PTZ组,与单独处理组无差异(图3K)。提示VNS与BF839协同增效,为个性化干预提供方向。通过左侧颈迷走神经切断术(LCV)阻断神经传递(图3L),结果显示:LCV显著增加BF839处理小鼠发作次数,PTZ组无显著差异(图3M、3N)。LCV缩短两组发作潜伏期,延长BF839处理组发作持续时间(图3O、3P)。同时,LCV加重BF839+PTZ组发作严重程度,PTZ组无差异(图3Q、3R)。表明LCV削弱BF839抗癫痫效应,迷走神经是其肠-脑信号通路的关键。
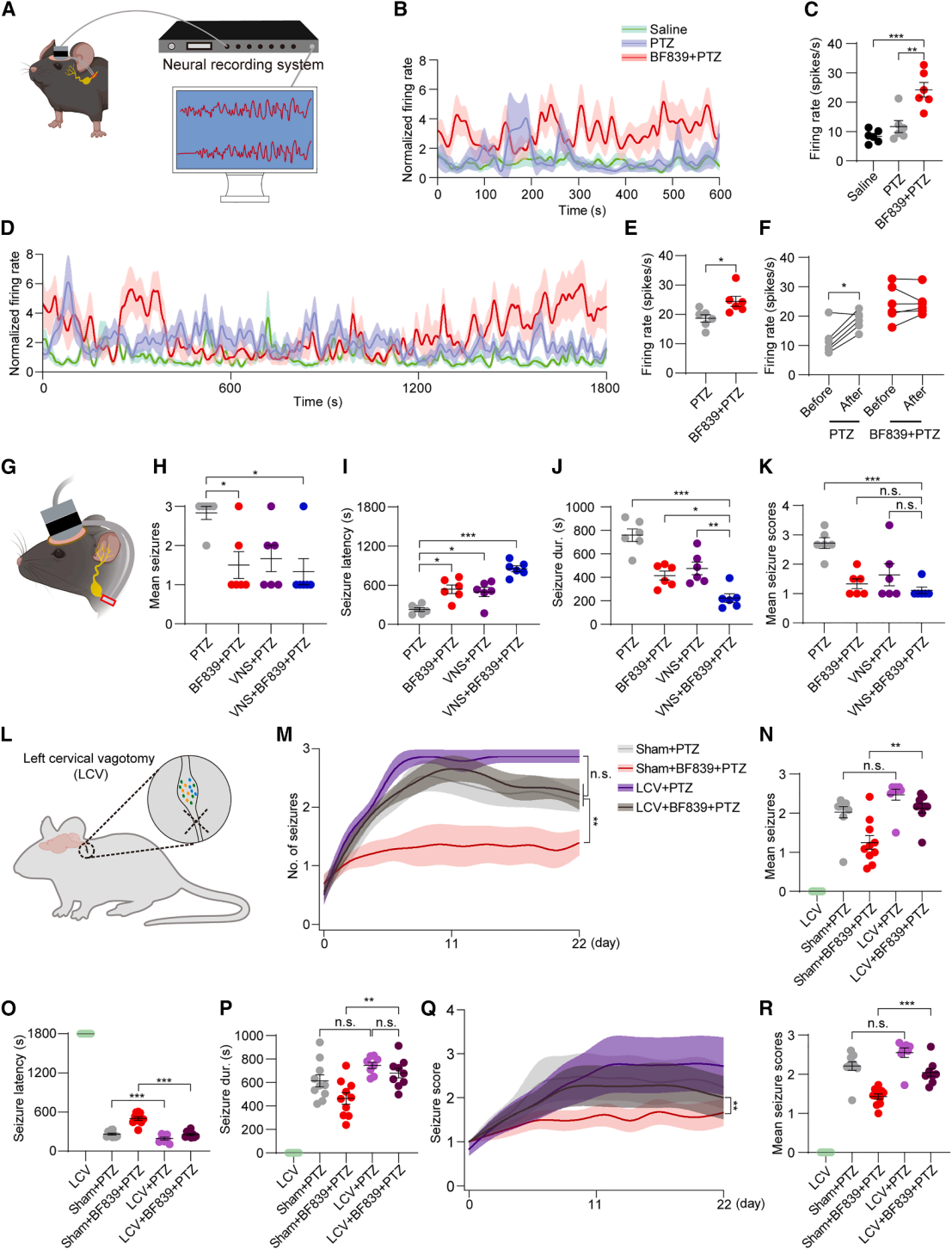
图3. BF839通过激活颈NG增强VNS的抗癫痫作用,而LCV则降低其治疗效果
基于神经通路在BF839抗癫痫肠-脑轴机制中的关键作用,作者对结肠组织神经递质行靶向代谢组学分析。40种神经活性化合物定量显示,PTZ组与BF839组(BF839+PTZ组)差异显著(图4A),其中胆碱代谢物改变明显,提示BF839可能调控结肠胆碱能神经传递(图4A-4C)。结合BF839经迷走神经发挥作用及菌群调控胆碱能通路的研究,作者探究了结肠ChAT介导的肠-脑轴是否参与其抗癫痫效应,结果发现PTZ组小鼠结肠ChAT+细胞数显著低于生理盐水组(图4D),而BF839处理后该细胞数显著增加(图4D)。高效液相色谱(HPLC)检测显示,BF839组结状神经节胆碱水平高于PTZ组(图4E)。pERK-1(结状神经节神经元激活的标志物)免疫染色表明,BF839组激活神经元比例显著高于生理盐水组和PTZ组。后续实验探究BF839对海马神经递质的影响,HPLC结果显示,与PTZ组相比,BF839显著升高海马胆碱和GABA水平(图4F、4G),血清中无显著变化,提示迷走神经通过肠-脑神经通路介导BF839的作用。
为了明确BF839激活的肠-脑轴神经信号是否特异性由ChAT介导,作者探究了肠道ChAT+细胞经迷走神经向大脑传信号的能力。重新分析已发表的单细胞RNA测序数据和迷走神经节数据,结果提示BF839诱导的结肠ChAT信号可突触传递至NG,推测ChAT+簇细胞与迷走神经形成突触连接,通过AChRs传递BF839相关信号(图4H)。抗ChAT与突触素-1抗体共标记实验显示,二者共定位(图4I),证实结肠ChAT+簇细胞的突触特性。PGP95与ChAT共免疫染色进一步验证(图4J),提示该细胞可感知益生菌信号并经迷走神经传至大脑。为了阐明肠-脑神经环路,向结肠近端注射PRV-CAG-EGFP(图4K),追踪发现荧光信号大量存在于NTS(图4L),证实二者神经连接,提示肠道益生菌信号可经迷走神经激活NTS神经元并传至大脑。向NG注射AAV9-Retro-CAG-EGFP(图4M),逆行追踪并三维重建分析显示,结肠迷走感觉纤维与ChAT+细胞间距极近(图4M),提示NG与ChAT+细胞建立密切连接,介导BF839刺激信号的感知与传递。
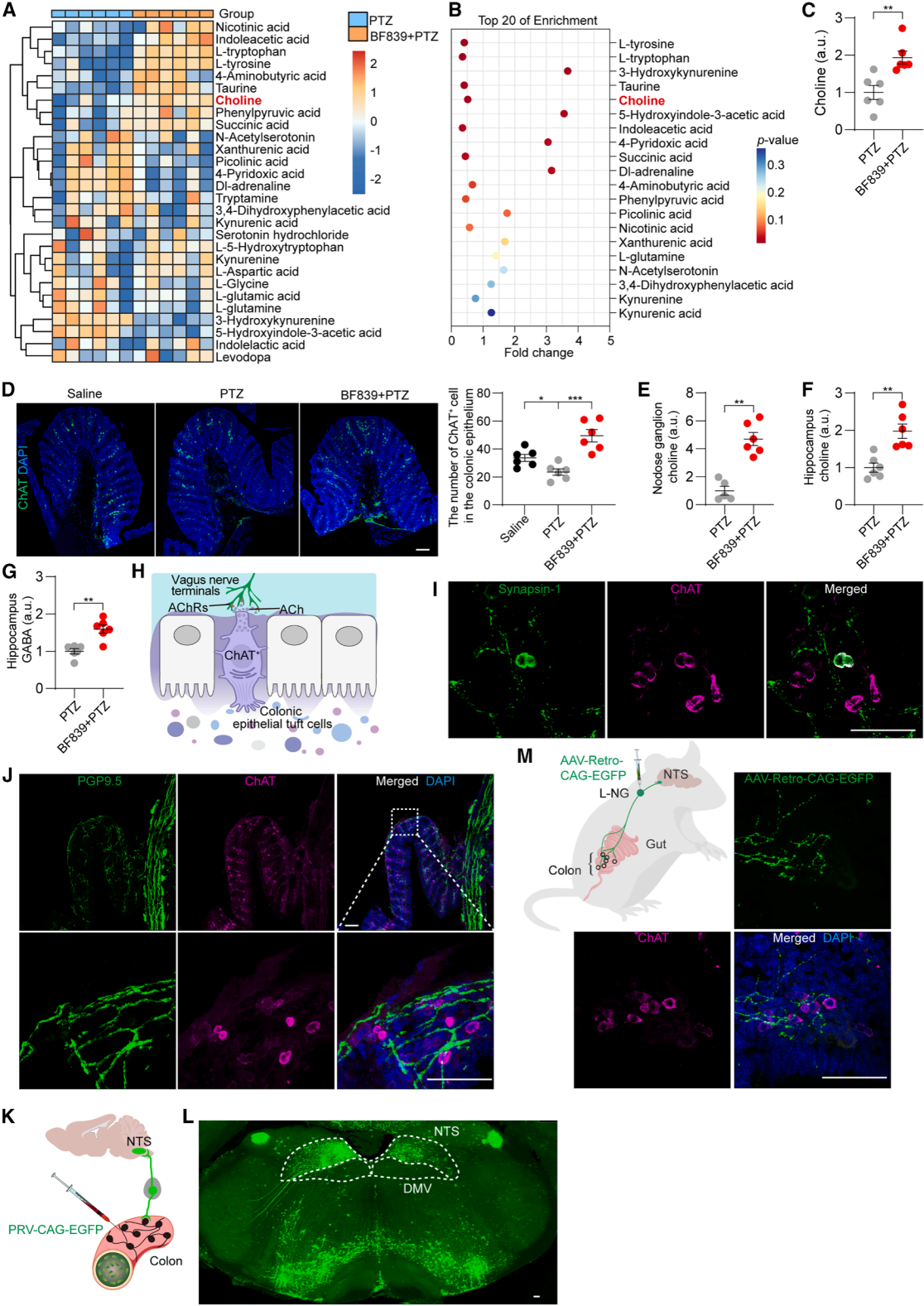
图4. BF839可提高结肠、NG及海马区的ChAT水平
为了验证结肠向NG的胆碱能信号是否参与BF839的抗癫痫作用,作者采用组合病毒策略操控结肠ChAT+-迷走神经传入环路(图5A、5B)。经标记与共染色验证,结肠ChAT+细胞与NG神经元共定位,存在直接神经通路(图5C),AAV转导细胞占肠道ChAT+细胞的29.22%±7.60%(图5C)。PTZ模型中,激活ChAT+细胞显著降低发作频率,消融则削弱BF839作用(图5D)。二者联合可协同降低发作严重程度(图5E),证实结肠ChAT+→NG投射是BF839抗癫痫的必要且充分条件。电生理记录显示,BF839或ChAT+细胞激活均增强迷走神经放电,联合效应最显著(图5F);消融ChAT+细胞则阻断该激活(图5F)。基础放电检测中,taCasp3组放电率低于对照组,hM3Dq组无差异。c-Fos成像显示,BF839或ChAT+细胞激活可升高NTS内侧、中间亚区神经元活性,联合呈协同增强(图5G、5H),背外侧亚区无变化(图5H)。海马CA3区、DG区活性被显著抑制,联合组效果最强(图5I、5J)。综上,结肠ChAT+细胞经迷走神经向NTS传递BF839诱导的胆碱能信号,减弱海马过度兴奋,该通路是BF839抗癫痫的关键。
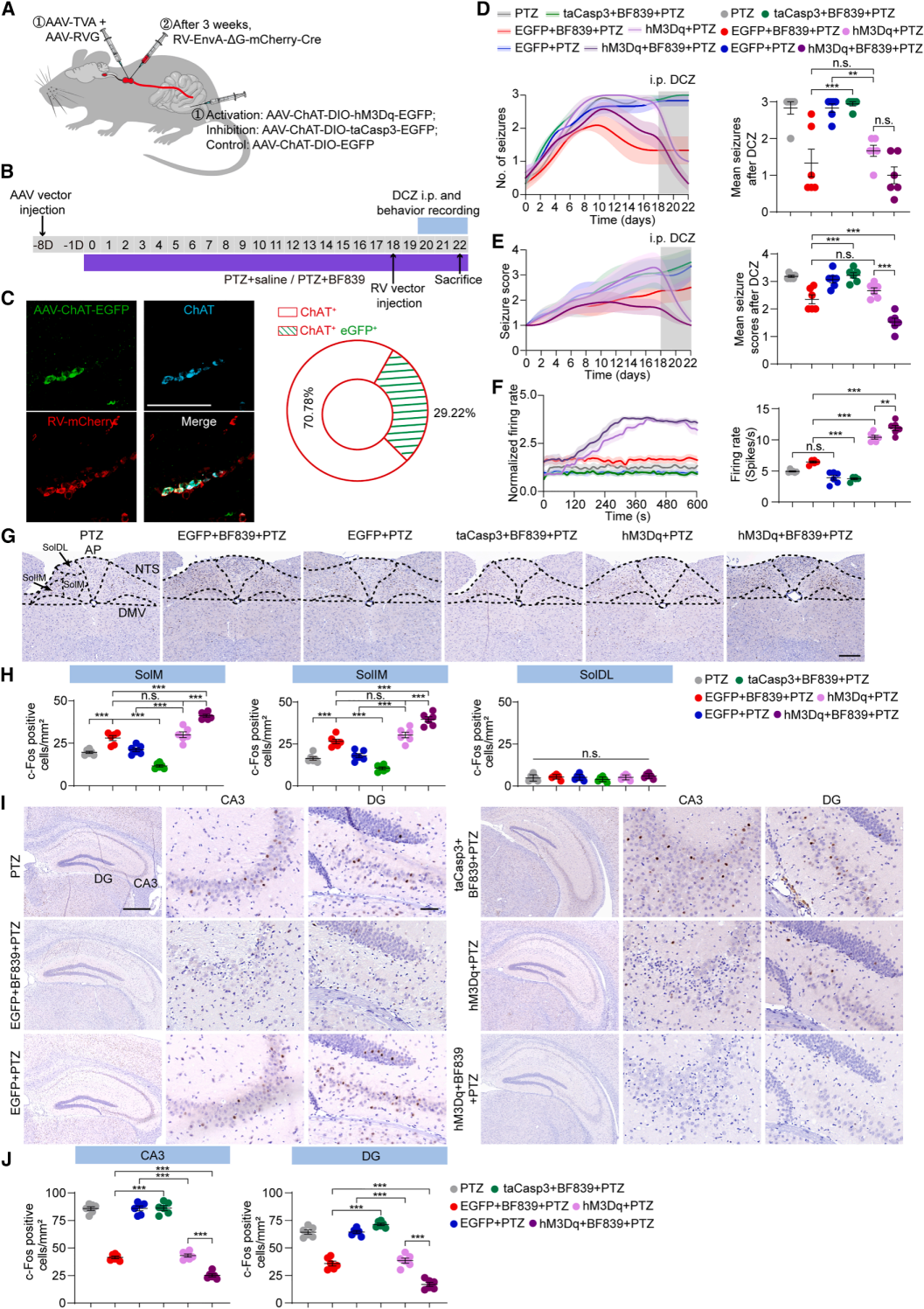
图5. 肠-迷走神经胆碱能通路的激活可抑制癫痫发作并降低海马神经元兴奋性
BF839可缓解PTZ诱导小鼠癫痫发作。干预22天后,BF839+PTZ组发作次数减少、潜伏期延长、持续时间缩短(图6A)。因疗效存在个体差异,将小鼠分为有效组与无效组,有效组发作发生率及评分均显著低于无效组。16S rRNA测序显示,小鼠肠道菌群以拟杆菌门、厚壁菌门为主(图6C),PTZ处理显著改变菌群组成(图6D)。灌胃BF839可显著升高拟杆菌属和乳酸杆菌属丰度(图6E-6G),同时提高菌群α多样性(图6H)。琼脂培养验证,有效组拟杆菌属、乳酸杆菌属丰度均高于无效组(图6I、6J)。斯皮尔曼分析显示,拟杆菌属与乳酸杆菌属丰度呈正相关(图6K),且二者均与发作次数呈负相关(图6L、6M),提示乳酸杆菌生态位影响BF839疗效。此外,乳酸杆菌丰度与结肠ChAT+细胞数、迷走神经节放电率均呈正相关(图6N、6O),二者可能协同激活肠-脑胆碱能信号介导抗癫痫作用。为探究抗生素(ABX)预处理是否通过扩大拟杆菌属生态位促进乳酸杆菌定植,进而增强BF839疗效,结果显示ABX+BF839+PTZ组拟杆菌属和乳酸杆菌属丰度,均显著高于单独BF839组(图6P-S)。厌氧共培养显示,BF839代谢产物可促进罗伊氏乳酸杆菌增殖(图6T)。体内实验中,BF839与罗伊氏乳酸杆菌联合灌胃组,粪便中该菌计数显著高于单独给药组,二者可相邻形成菌落,证实BF839促进罗伊氏乳酸杆菌定植。综上,BF839调控肠道菌群,增加乳酸杆菌生长所需代谢物,促进其结肠扩增,该代谢变化或介导BF839抗癫痫效应。
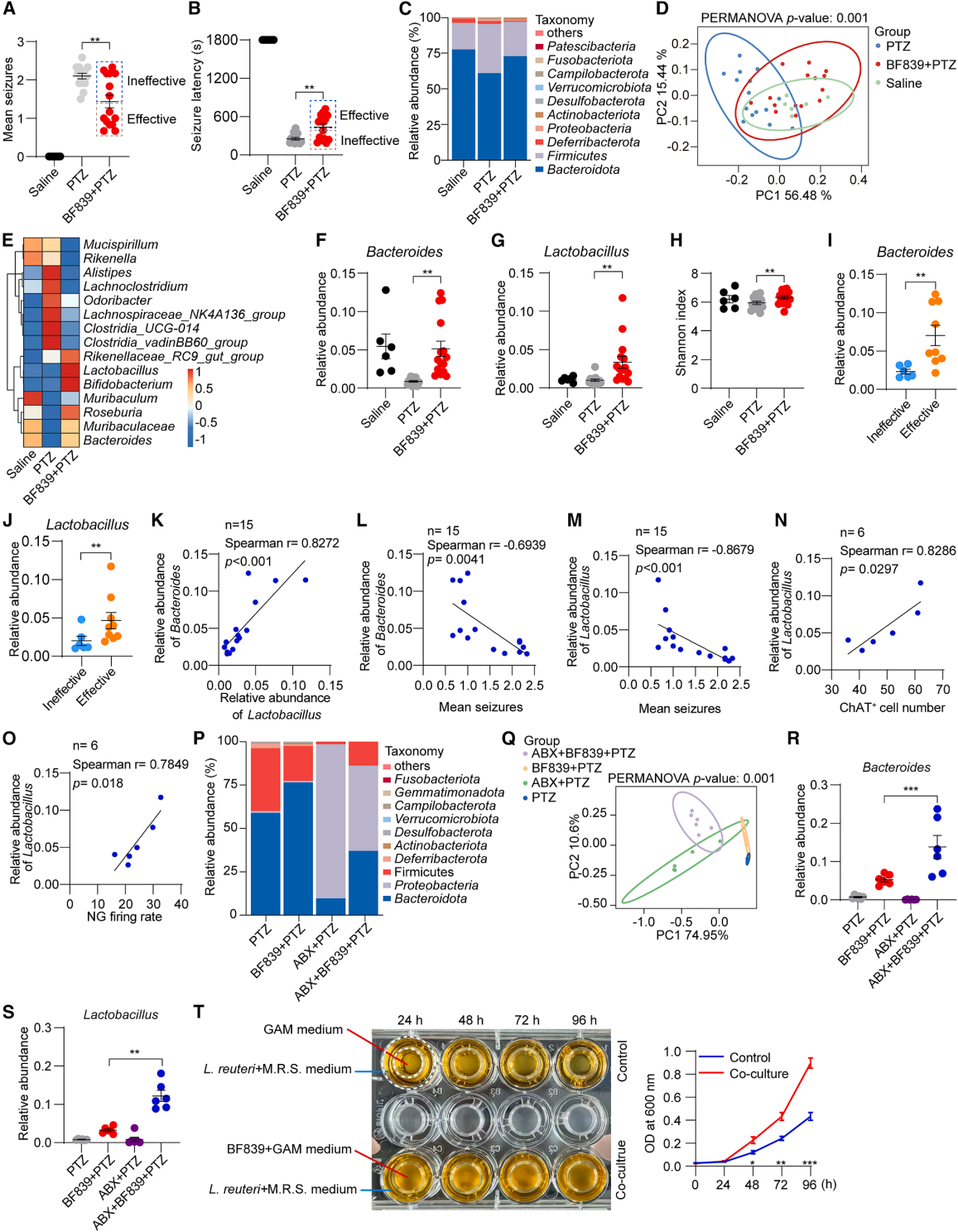
图6. BF839抗癫痫效应不同间差异与乳酸杆菌丰度相关
基于动物实验中BF839可升高结肠乳酸杆菌丰度的结果,作者开展人体验证研究,纳入2021年2月至2022年1月深圳儿童医院60例难治性癫痫患者,评估其抗癫痫效应的转化潜力。受试者随机分两组,维持常规饮食及抗惊厥药治疗3个月(图7A、7B)。BF839组治疗有效率32%,显著高于安慰剂组的5%,且不同年龄组疗效一致(图7C)。标准化发作频率比显示,BF839组显著低于安慰剂组,提示发作频率降低(图7D)。测序显示BF839组拟杆菌属和乳酸杆菌属丰度显著升高,治疗后两菌属丰度亦显著上升(图7E-J)。治疗有效者乳酸杆菌水平显著高于无效者(图7K、7L)。BF839调控肠道菌群,其疗效与两菌属定植呈正相关(图7K),凸显菌群在个体化治疗反应中的介导作用。综上,BF839通过乳酸杆菌协同机制增强胆碱能信号缓解癫痫,临床试验与临床前研究一致,具儿童难治性癫痫治疗潜力。
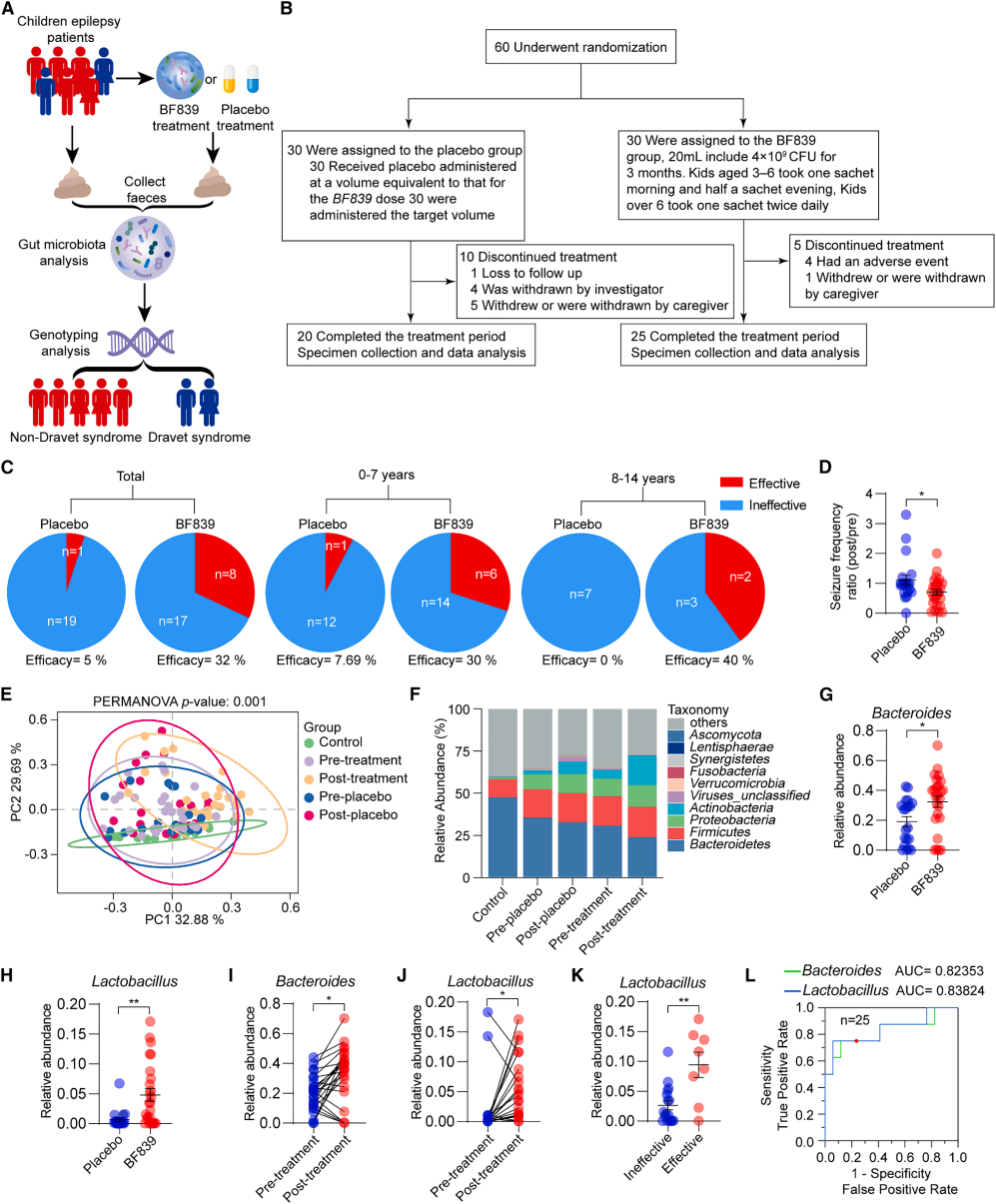
图7. 口服BF839研究中受试者与治疗结局
本文使用的工具病毒布林凯斯均可提供:
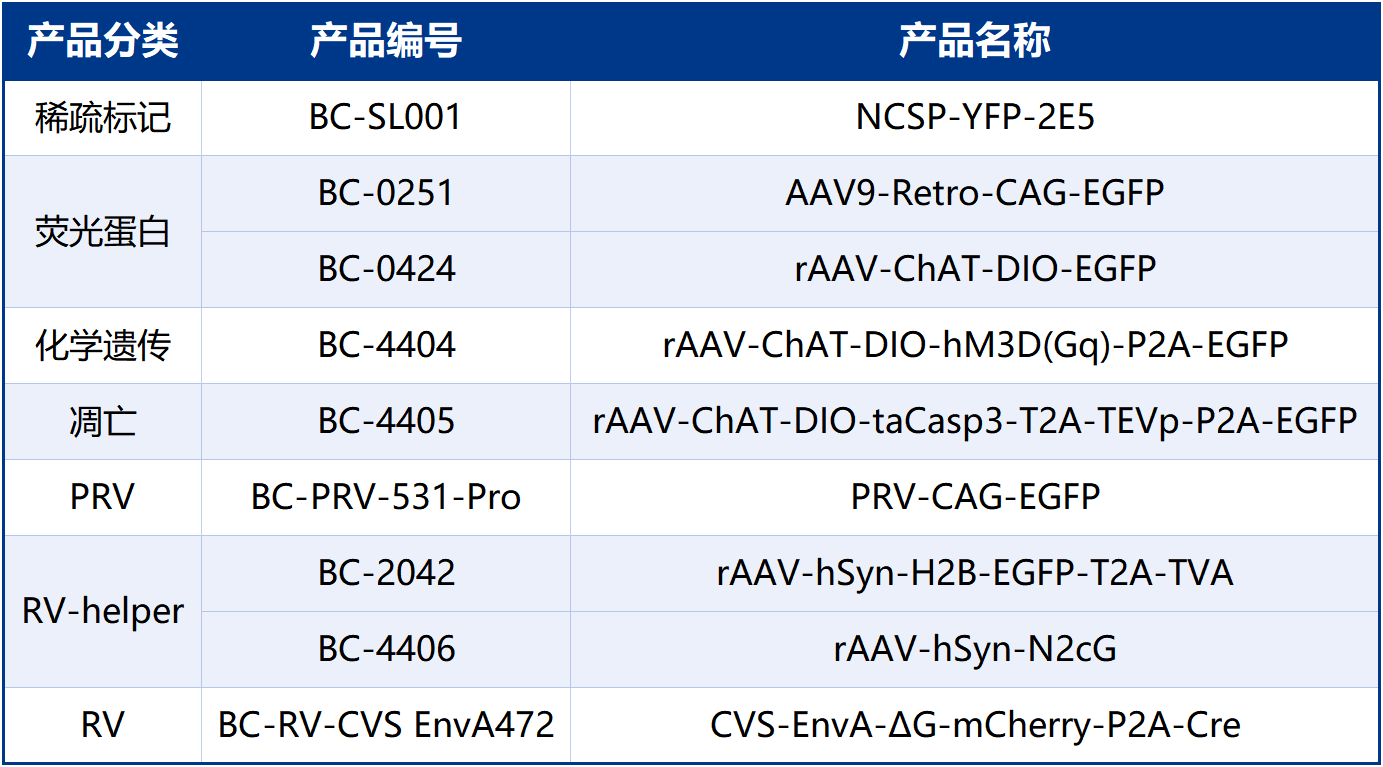
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。