三阴性乳腺癌(TNBC)无雌激素受体、孕激素受体及HER2表达,是最具侵袭性的乳腺癌亚型;免疫检查点阻断(ICB,通过阻断CTLA-4、PD-1/PD-L1等关键免疫检查点,解除肿瘤微环境对T细胞的抑制作用,从而恢复免疫系统识别杀伤肿瘤细胞的能力。)疗法虽有潜力,但仅部分患者获益,肿瘤微环境(TME)紊乱是主要耐药原因。神经支配在肿瘤进展中起关键作用,但感觉神经元在TNBC生态系统中的作用尚未明确。

2026年2月6日,复旦大学附属肿瘤医院江一舟/邵志敏/肖毅团队,联合复旦大学脑科学转化研究院倪金飞研究员团队,在国际顶刊Cell在线发表题为“Sensory neurons drive immune exclusion by stimulating a dense extracellular matrix in the breast cancer tumor microenvironment”相关研究论文,揭示了“肿瘤细胞-神经生长因子(NGF)-感觉神经元-神经肽降钙素基因相关肽(CGRP)-癌相关成纤维细胞(CAFs)-胶原蛋白”的调控轴,阐明感觉神经元驱动TNBC免疫排斥的分子机制。证实CGRP受体RAMP1(受体活性修饰蛋白1)拮抗剂瑞美吉泮(rimegepant)可作为免疫增敏剂,与抗PD-1疗法协同治疗TNBC,为临床药物重定位提供依据。
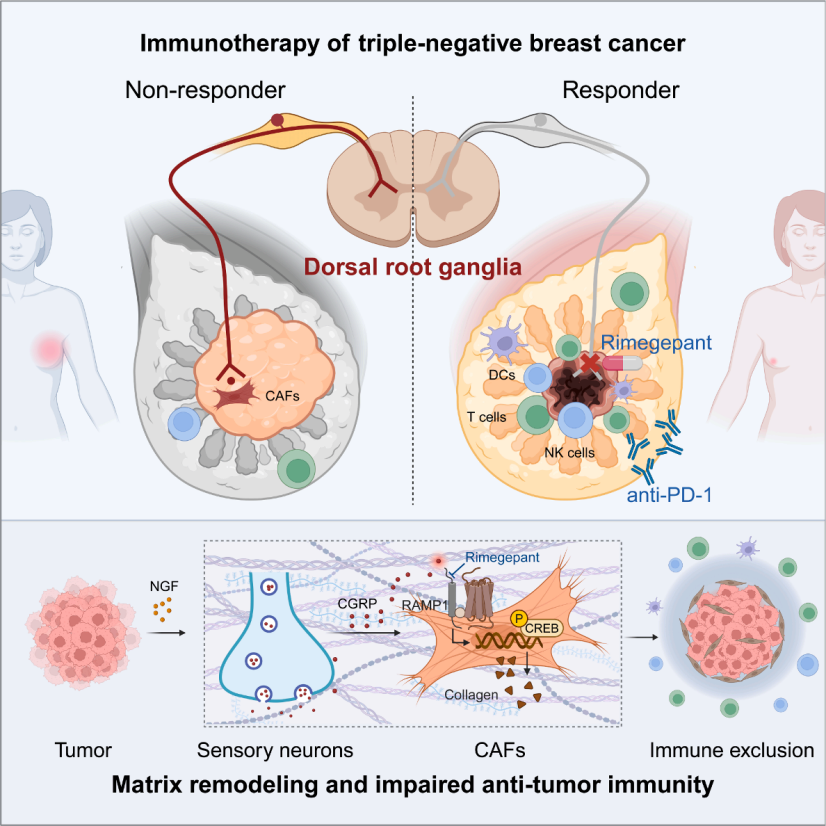
复旦大学附属肿瘤医院邵志敏教授、江一舟教授,复旦大学脑科学转化研究院倪金飞研究员和复旦大学附属肿瘤医院肖毅副研究员为本文共同通讯作者,复旦大学附属肿瘤医院张思维博士、王晗博士、肖毅副研究员和柳络天博士为共同第一作者。
为了探究神经周围浸润(PNI)对TNBC的作用,分析了多组学数据及小鼠模型。复旦大学附属肿瘤医院(FUSCC)-TNBC 队列和癌症基因组图谱(TCGA)队列显示,PNI阳性患者无复发生存期更短,且与晚期淋巴结分期、高骨转移率相关(图1A-E);多因素Cox分析证实PNI是TNBC独立预后不良因素。PNI与基线临床病理特征无关,却显著影响TME:其与免疫浸润负相关、与癌相关成纤维细胞(CAF)丰度正相关,可减少肿瘤浸润淋巴细胞(TILs)、CD4⁺T细胞以及三级淋巴结构(TLSs)/ 淋巴聚集物(LAs)(图1F、1G),同时促进间质活化和纤维化(图1H、1I),表明PNI可能通过破坏TME进而恶化患者生存。多重免疫荧光显示,感觉神经元占TNBC神经突面积约70%(图1J、1K);CTB逆行标记证实其来源于T11-L4背根神经节。此外,PNI仅在TNBC中具有预后意义,在激素受体(HR)⁺/HER2⁻和HER2⁺乳腺癌中无显著关联。综上,PNI是TNBC不良预后因素,与促纤维化、免疫抑制性TME相关,来自T11-L4节段DRGs的感觉神经元是TNBC主要神经元类型。
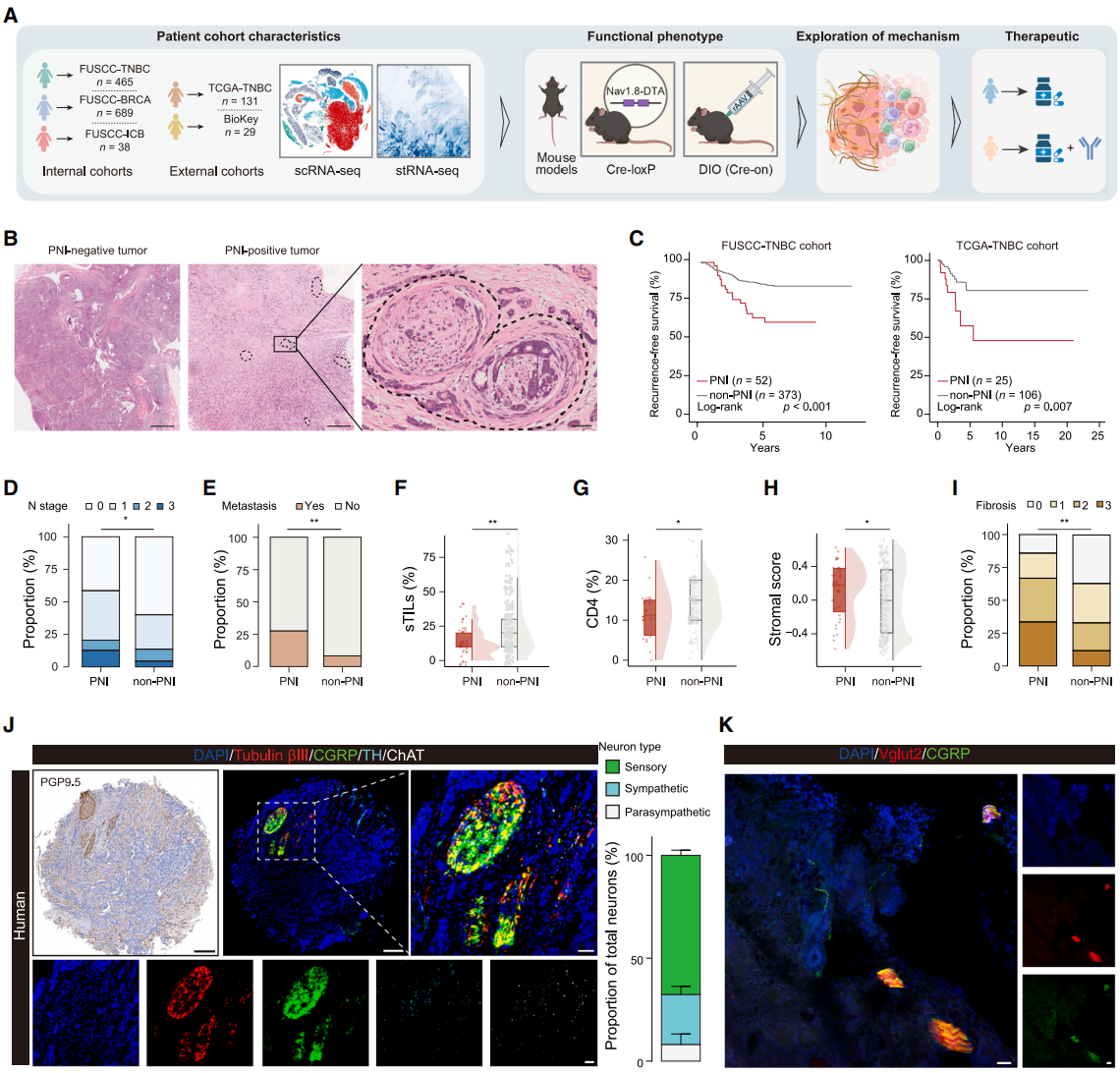
图1. PNI与TME失调相关,且在TNBC中以感觉神经元为主导
采用多种小鼠模型,验证感觉神经元浸润对促结缔组织增生和免疫抑制的驱动作用。低剂量辣椒素饮食构建全身性感觉神经元激活模型,结果显示感觉神经元激活显著加速肿瘤生长和纤维化(图2A-2D),流式细胞术证实辣椒素处理后肿瘤CAFs比例升高,且主要富集肌成纤维细胞型CAFs(myCAFs)(图2E)。进一步检测发现,感觉神经元激活抑制多种免疫细胞浸润(图2F)。构建Nav1.8-DTA全身性感觉神经元消融模型(图2G),与对照相比,该组小鼠肿瘤生长减慢,CAFs(尤其myCAFs)减少,胶原蛋白沉积降低,TME改善,CD4⁺/CD8⁺T免疫细胞浸润增多(图2H-2L)。
采用树脂毒素(RTX,一种强效辣椒素类似物)化学消融感觉神经元,得到类似结果:RTX处理小鼠肿瘤生长减慢、胶原蛋白减少、免疫细胞浸润增加(图2M-2R)。为了排除全身感觉系统影响,向Vglut2-Cre小鼠的腹股沟乳腺脂肪垫注射rAAV-DIO-Caspase3,构建肿瘤内感觉神经元消融模型。结果显示,尽管全身感觉神经元完好,rAAV处理组肿瘤生长仍显著减慢(图2T-2U),CAFs和胶原蛋白沉积减少(尤其myCAFs和I型胶原蛋白)(图2V-2W),免疫细胞功能恢复,凸显局部感觉神经元浸润的关键作用(图2X)。综上,感觉神经元可促进myCAF表型形成,进而驱动TNBC的促结缔组织增生和免疫逃逸。
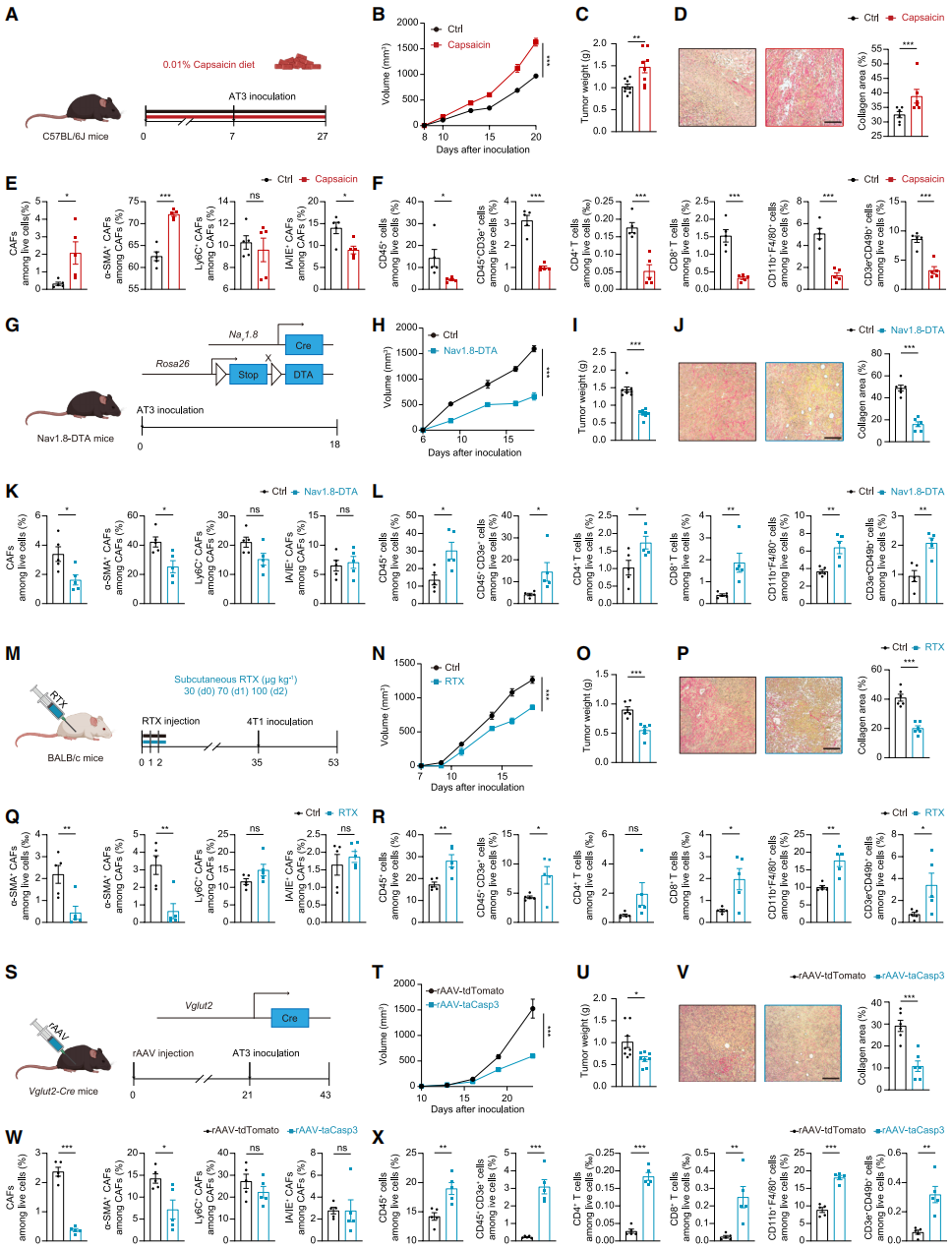
图2. 感觉神经元通过刺激胶原沉积和减少免疫浸润加速肿瘤进展
为了明确TNBC中感觉神经元致敏机制,作者进行单细胞水平空间转录组测序(stRNA-seq),鉴定多种细胞类型并标记PNI区域(图3A)。神经元相关通路在PNI区域显著富集(图3B),空间轨迹分析显示神经生长因子(NGF)在PNI区域附近特异性富集,mIF进一步证实PNI阳性样本NGF水平更高(图3C)。NGF⁺细胞在PNI区域附近富集(图3D),提示NGF促神经浸润作用。既往研究表明癌细胞和CAFs均可分泌NGF,但空间分析及流式细胞术证实,TNBC中NGF主要来源于肿瘤细胞。实验验证显示,AT3肿瘤细胞条件培养基(AT3 CM)中NGF水平升高,其培养的感觉神经元CGRP分泌增加、轴突更密集,此效应可被NGF中和逆转(图3G)。4T1细胞敲低Ngf后,其培养的感觉神经元CGRP分泌减少、轴突缩短,补充重组NGF可逆转该效应(图3H)。体内实验中,shNgf组肿瘤生长受抑(图3I),PNI面积小于shNC组(图3J),TME中胶原蛋白沉积(尤其I型)缓解(图3K),免疫细胞浸润增加(图3L)。综上,肿瘤分泌的NGF可吸引神经元、紊乱TME并促进肿瘤生长。
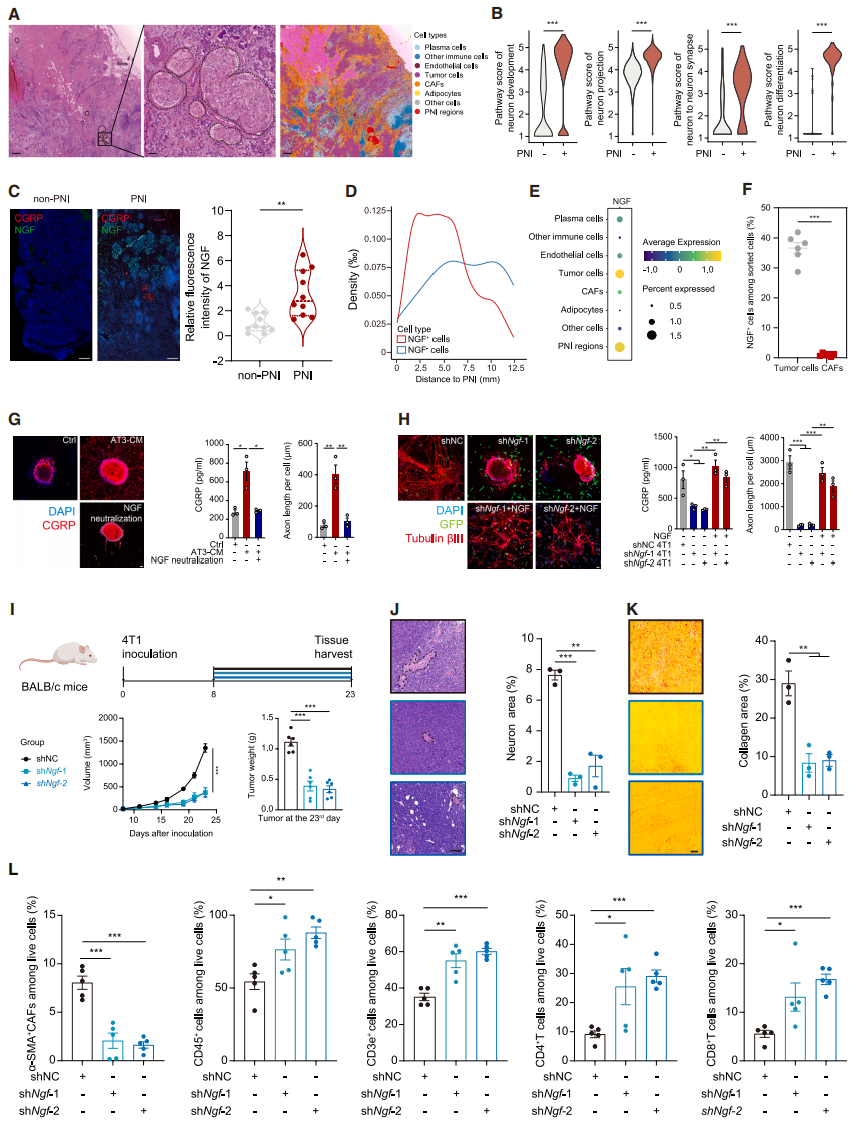
图3. 肿瘤细胞释放的NGF促进感觉神经元的神经突生长及CGRP分泌
作者探究感觉神经元诱导胶原蛋白沉积和免疫抑制的下游机制,采用基于单细胞形态学和拓扑图谱的机器学习框架,分析81例TNBC患者HE图像,发现PNI阳性患者间质细胞聚集明显(图4A、4B),且PNI主要位于间质区(图4C)。mIF证实感觉神经元(CGRP⁺)与CAFs(α-SMA⁺)邻近(图4D)。空间转录组样本分析显示,绝大多数PNI位于间质区,CAFs在PNI紧邻区富集,免疫细胞则被排除(图4E、4F)。上述结果与细胞外基质(ECM)通路和感觉系统发育通路高度共表达一致(图4G),结合感觉神经元消融模型中CAFs显著减少(图2E、2K、2Q、2W),提示CAFs是感觉神经元的作用靶点。
为了明确感觉神经元对CAFs的影响,将CAFs分为myCAFs、炎症型 CAFs(iCAFs)和抗原呈递型 CAFs(apCAFs)三亚型,其中myCAFs与PNI最近(图4H)。从DRGs分离感觉神经元、AT3肿瘤中分选CAFs,2D培养中myCAFs传代4次后稳定在80%左右。感觉神经元条件培养基(neuron CM)可显著激活CAFs(脂滴减少、细胞体积增大)(图4J),提高myCAFs比例。3D培养实验显示,有neuron CM处理后myCAF标志物上调(图4K),且可诱导CAFs大量产生胶原蛋白(图4L、4M)。综上,感觉神经元驱动的myCAFs激活可能参与免疫抑制性TME形成。
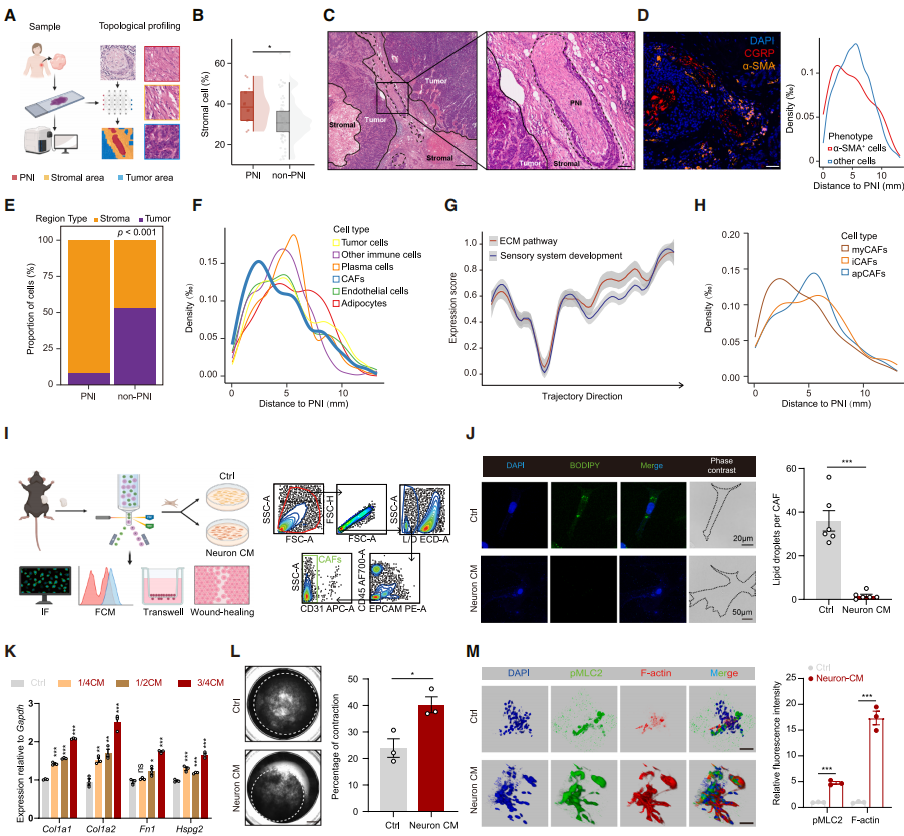
图4. 感觉神经元与CAF相邻并促进胶原沉积
为了探究感觉神经元促进myCAFs激活的机制:对感觉神经元条件培养基(neuron CM)处理后发现,仅小分子多肽可促进α-SMA表达。主要神经肽抑制剂中,仅CGRP抑制剂瑞美吉泮能拮抗neuron CM诱导的CAFs的myCAF表型(图5A)。CGRP不增强CAFs增殖,但可激活静息CAFs、增强myCAFs迁移和胶原收缩功能(图5B)。scRNA-seq数据显示,仅CGRP受体关键组分受体活性修饰蛋白1(RAMP1)在CAFs(尤其myCAFs)高表达(图5C-5F),且与myCAF标志物强正相关。mIF证实RAMP1与α-SMA在TNBC患者及小鼠模型中均共定位(图5G),提示感觉神经元分泌的CGRP是驱动myCAFs激活的关键神经肽。
进一步评估CGRP-RAMP1轴的作用:瑞美吉泮阻断RAMP1,可显著抑制正常及辣椒素饮食小鼠的肿瘤生长(图5H),单独或联合辣椒素使用均能减少myCAFs和I型胶原沉积、增加免疫细胞浸润(图5I-5K)。4T1原位肿瘤模型中,CAFs中敲低Ramp1可抵消辣椒素诱导的肿瘤生长加速(图5L),且减少I型胶原、增加CD8⁺T细胞浸润。在免疫正常的C57BL/6J小鼠中,Ramp1敲低可降低AT3肿瘤负荷、改善TME(图5M),但免疫缺陷B-NDG小鼠中无此现象,凸显RAMP1⁺CAFs响应CGRP调控TME的关键作用。
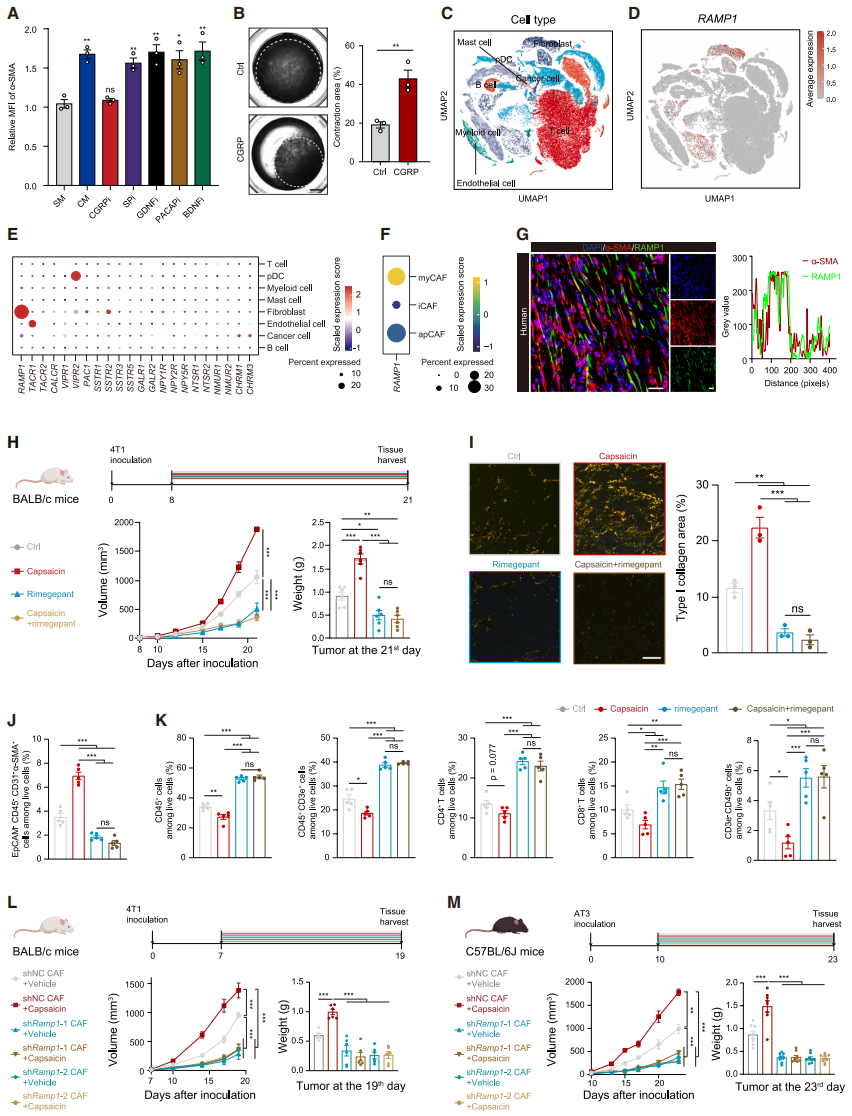
图5. 感觉神经元源性CGRP结合CAF上的RAMP1以促进胶原蛋白分泌
已知RAMP1激活会触发腺苷酸环化酶(AC)产生cAMP,进而促使PKA介导环磷酸腺苷反应元件结合蛋白1(CREB1)磷酸化。CGRP处理后CAFs内cAMP生成增加,效果接近PKA激动剂毛喉素(图6A);PKA抑制剂H89可阻断CGRP和毛喉素诱导的p-PKA、p-CREB1(图6B)。shRamp1 CAFs中p-PKA、p-CREB1水平降低,CGRP处理无法恢复(图6C);CREB1敲低可抑制胶原合成,降低myCAF标志物表达(图6D)。人TNBC组织来源的RAMP1⁺CAFs经CGRP处理后,p-PKA、p-CREB1及FN1水平升高(图6E),证实CGRP通过cAMP/PKA/CREB1通路激活CAFs。
作者探究CREB1调控胶原合成的机制:CREB1作为多效性转录因子,其潜在结合位点(TFBSs)存在于多个ECM相关基因启动子区(图6F)。ChIP-qPCR显示,CREB1在这些TFBSs上显著富集,CGRP处理后更明显(图6G);HEK293T细胞中过表达CREB1可激活相关基因荧光素酶活性,证实其直接调控ECM相关基因转录(图6H)。体内实验中,携带shCreb1 CAFs的4T1肿瘤可缓解感觉神经元激活诱导的肿瘤生长加速,逆转促结缔组织增生和免疫排斥性TME(图6I、6J);AT3细胞与shCreb1 CAFs构建的模型也呈现类似结果(图6K、6L)。综上,CGRP介导的CREB1激活可上调CAFs肌成纤维细胞水平,通过致密胶原基质促进肿瘤进展。
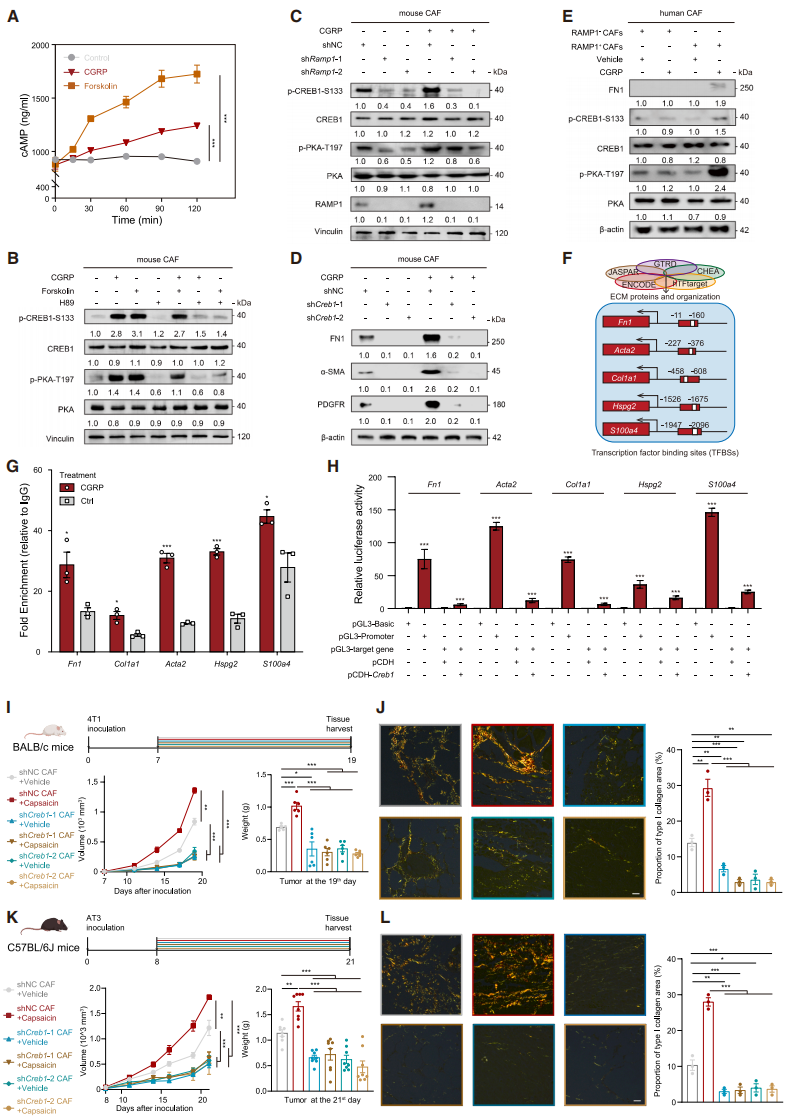
图6. CGRP -RAMP1轴通过cAMP/ PKA /CREB1通路增强CAF中胶原蛋白的生物合成
基于感觉神经元耗竭可改善TME的发现,作者验证其与免疫疗法的协同作用。在Nav1.8-DTA小鼠及其同窝对照中构建AT3异种移植模型并给予抗程序性死亡蛋白1(PD-1)治疗,结果显示,感觉神经元消融联合抗PD-1组肿瘤生长最慢(图7A)。Nav1.8-DTA小鼠CAFs比例更低,联合抗PD-1后免疫细胞浸润增加(图7B)。在C57BL/6J小鼠中,瑞美吉泮与抗PD-1联合治疗可抑制肿瘤生长、减少myCAFs分化及I型胶原沉积,增加肿瘤浸润免疫毒性细胞(图7C、7D),该现象在BALB/c小鼠中也存在(图7E、7F);IHC染色证实联合治疗可增加CD8⁺T细胞浸润。作者探究CGRP的临床意义:采用FUSCC-BRCA队列110例TNBC组织切片,IHC染色证实CGRP是TNBC患者不良预后的可靠生物标志物(图7G)。在FUSCC-ICB新辅助免疫治疗队列中,CGRP阳性患者免疫治疗效果有变差趋势、TILs浸润更少,而化疗效果不受CGRP状态影响(图7H)。综上,CGRP抑制剂与抗PD-1联合使用可能是理想的TNBC免疫治疗策略,CGRP有望成为患者预后及免疫治疗响应的预测生物标志物。
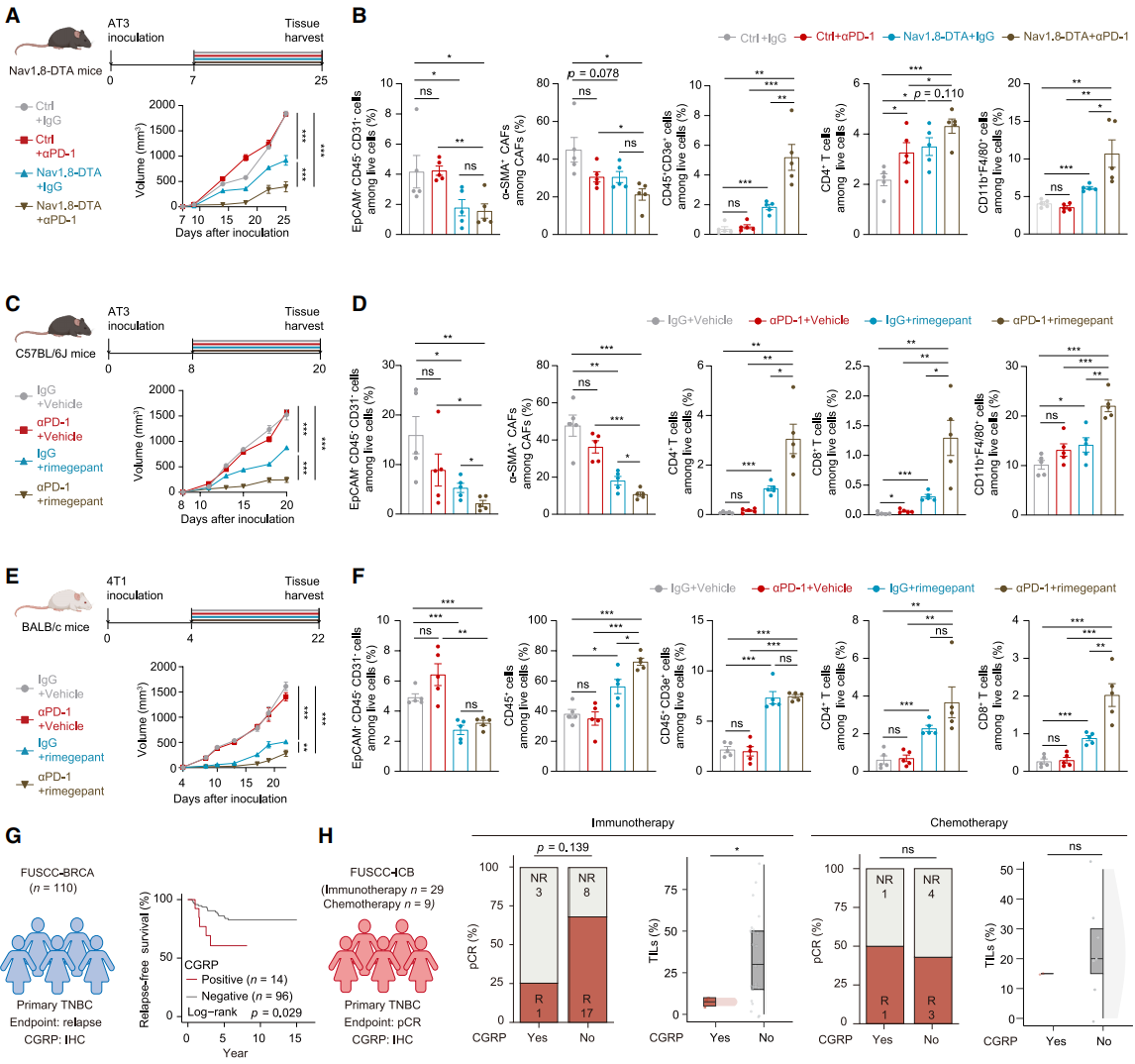
图7. 靶向感觉神经元与ICB在TNBC中的协同作用
本研究发现感觉神经元是三阴性乳腺癌肿瘤微环境(TME)中的主要神经元类型,肿瘤细胞分泌的NGF会激活感觉神经元释放CGRP,CGRP 通过结合癌相关成纤维细胞上的RAMP1受体,经cAMP/PKA/CREB1信号通路促进胶原蛋白沉积,形成致密细胞外基质(ECM)导致免疫排斥;而靶向感觉神经元可重塑 TME,与抗PD-1疗法协同增效,为TNBC免疫治疗提供新策略,且CGRP可作为TNBC预后和免疫治疗反应的生物标志物。
本文使用的工具病毒布林凯斯均可提供:

同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。