腐败食物气味可引发人类呕吐、厌恶等防御反应,避免代谢紊乱,但潜在神经机制不明;传统呕吐研究模型(猫、狗等)缺乏分子/细胞实验资源,小鼠虽无呕吐行为,但存在干呕样行为,适合机制研究。腐败食物气味如何通过嗅觉系统传递至大脑,进而调控干呕样行为和厌恶反应?
中国科学技术大学张智/朱霞教授团队联合中国科学技术大学附属第一医院内分泌科王炜教授团队,以及中国科学院昆明动物研究所周启心副研究员团队,在Nature Communications上发表题为“A nose-to-brain axis for spoiled food odor-triggered defensive responses in male mice”的研究论文,揭示2-甲基丁酸(2MBA) ,可通过两条独立的“鼻—脑轴” 神经通路在雄性小鼠中触发防御反应:一条是鼻→嗅球(OB)→前梨状皮质(aPir)→丘脑背内侧核(MD)→腹外侧导水管周围灰质(VLPAG)→腹侧呼吸组(VRG)→呼吸肌通路,介导干呕样行为;另一条是鼻→OB→aPir→伏隔核(NAc) 通路,介导厌恶反应,且这两条通路分别由aPir区的谷氨酸能神经元(aPirGlu)投射至MD的谷氨酸能神经元(MDGlu)和NAc的γ-氨基丁酸能神经元(NAcGABA)实现。

中国科学技术大学博士后董婉莹,博士生程平凯、苗俊豪,以及中国科学技术大学与临沂市人民医院联合培养博士后石佩,为该论文的共同第一作者;中国科学技术大学/安徽医科大学张智教授、中国科学技术大学内分泌科王炜教授、中国科学院昆明动物研究所周启心副研究员、中国科学技术大学生命科学与医学部特任教授朱霞,为该论文的共同通讯作者。本研究得到科技创新2030—“脑科学与类脑研究”重大项目(中国脑计划)、国家自然科学基金、安徽省中医药攻关专项等项目的资助。
受人类对难闻气味的防御反应启发,建立了气味诱发雄性小鼠干呕样行为的范式。将含不同浓度(双蒸水稀释)难闻气味物质(2MBA、小茴香酮FEN、己醇HEX等)的滤纸片置于盒中挥发,小鼠自由吸入气味20分钟,相机记录行为(图1a)。仅2MBA(腐败食物酸败气味))诱发小鼠类人干呕的张口动作,且动作次数随浓度升高而增加(图1b-d)。
干呕的生理特征是膈肌与腹部肌肉激活。肌电图(EMG)记录显示,2MBA诱发张口动作时,小鼠膈肌、腹外斜肌活动振幅及频率显著升高,其他气味及对照组无此现象(图1e-g),故将该表型定义为干呕样行为。通过条件性位置厌恶(CPA)测试(图1h)探究发现,2MBA配对组小鼠在对应箱体停留时间短、CPA评分高(图1i-j),证实2MBA可诱发小鼠厌恶反应。经鼻腔灌洗硫酸锌构建失嗅模型后,小鼠暴露于2MBA无干呕样行为及厌恶反应,而假手术组有明显反应,表明该防御反应依赖嗅觉感知。
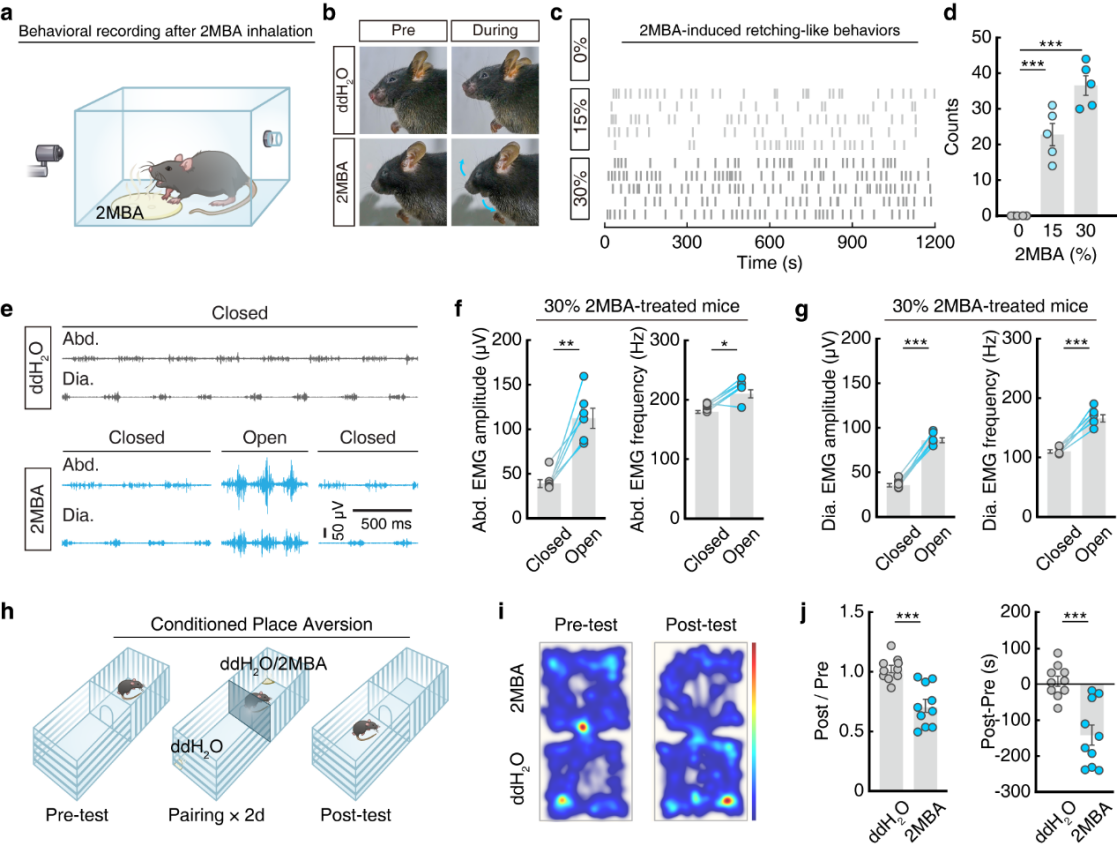
图1 | 2MBA诱发的小鼠类似干呕行为及厌恶反应
已知嗅上皮的嗅觉感觉神经元(OSNs)投射至OB。为了明确OB下游被2MBA激活的脑区,利用FosTRAP2小鼠,通过鼻腔及OB注射特异性AAV标记神经元,腹腔注射4-OHT后让小鼠暴露于2MBA(图2a)。结果显示,OB神经元下游的EGFP⁺纤维在aPir中富集,其他嗅皮质区域(pPir、OT、CoA)则极少(图2b-c),故聚焦aPir的作用。将FosTRAP2与Ai14-tdTomato小鼠杂交,注射4-OHT后标记Fos⁺激活神经元,证实aPir谷氨酸能神经元(aPirGlu)响应2MBA。
通过微内镜及钙指示剂GCaMP6m检测(图2d),发现30%的aPir神经元仅被2MBA单独激活,33.3%可被2MBA与其他气味共同激活(图2e-g)。光纤记录显示,2MBA诱发的aPirGlu钙信号ΔF/F值高于其他气味,且呈浓度依赖性(图2h-k),证实aPirGlu可选择性响应2MBA。通过化学遗传学抑制2MBA激活的aPirGlu(注射AAV-DIO-hM4Di-mCherry,CNO诱导)(图2l-m),结果显示小鼠干呕样行为次数及CPA评分均显著降低(图2n)。c-Fos染色证实TRAP标记效率达92.35%,表明aPirGlu活动增强是2MBA诱发防御反应的关键。
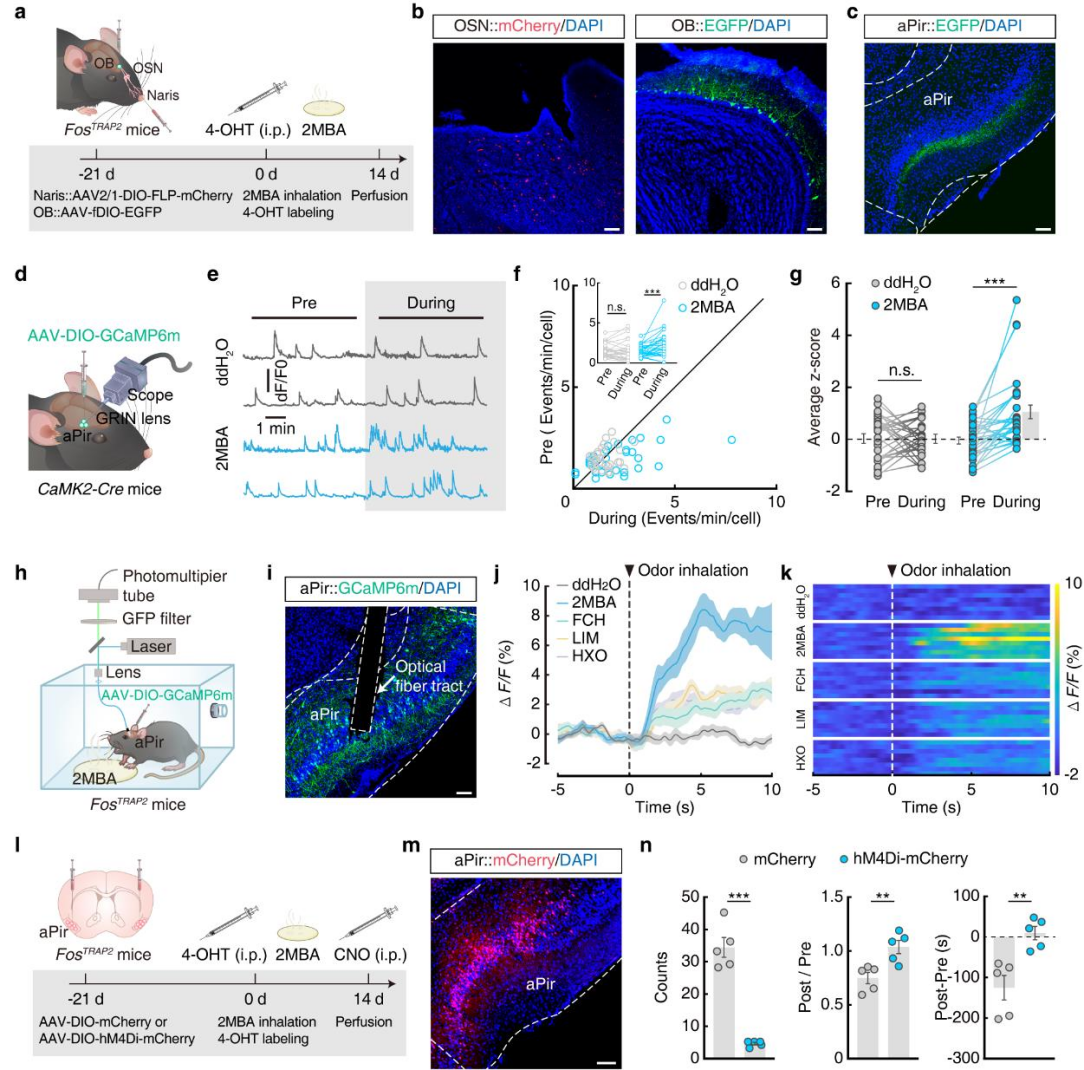
图2 | 2MBA激活aPirGlu神经元活动以触发类似干呕的行为和厌恶反应
为了明确aPirGlu神经元在2MBA诱发防御反应中的下游靶点,向FosTRAP2小鼠aPir注射AAV-DIO-EGFP。三周后腹腔注射4-OHT并让小鼠暴露于2MBA(图3a),两周后在aPir观察到EGFP⁺神经元(图3b),且MD、NAc、LH、PT脑区检测到EGFP⁺纤维(图3c)。监测FosTRAP2:Ai14小鼠脑区活动发现,2MBA暴露后MD(84%共定位谷氨酸抗体)和NAc(93%共定位GABA抗体)的tdTomato表达显著升高,LH、PT无变化。故后续聚焦aPirGlu→MD和aPirGlu→NAc通路。已知MD参与感觉信息传递,通过顺行单突触示踪解析通路:向aPir注射AAV2/1-Cre-mCherry,向MD注射AAV-DIO-EGFP(图3d)。三周后MD的EGFP⁺神经元仅与谷氨酸抗体共定位(图3e,f),证实aPir神经元投射至MD谷氨酸能神经元(MDGlu)。采用逆行跨单突触示踪明确通路结构:向CaMK2-Cre小鼠MD注射辅助病毒,三周后注射EnvA假型RV-ΔG-EGFP(图3g)。一周后在aPir检测到与谷氨酸抗体共定位的EGFP⁺神经元(图3h),确认aPirGlu投射至MDGlu。为了验证功能连接,向FosTRAP2小鼠aPir注射AAV-DIO-ChR2-mCherry,MD注射AAV-CaMK2-EGFP(图3i)。经4-OHT处理及2MBA暴露后,MD可检测到 mCherry⁺纤维和 EGFP⁺神经元(图3j)。光刺激可诱发MDGlu产生EPSCs,AMPA受体拮抗剂DNQX处理后该效应消失(图3k,l),证实aPirGlu与MDGlu存在功能性连接。
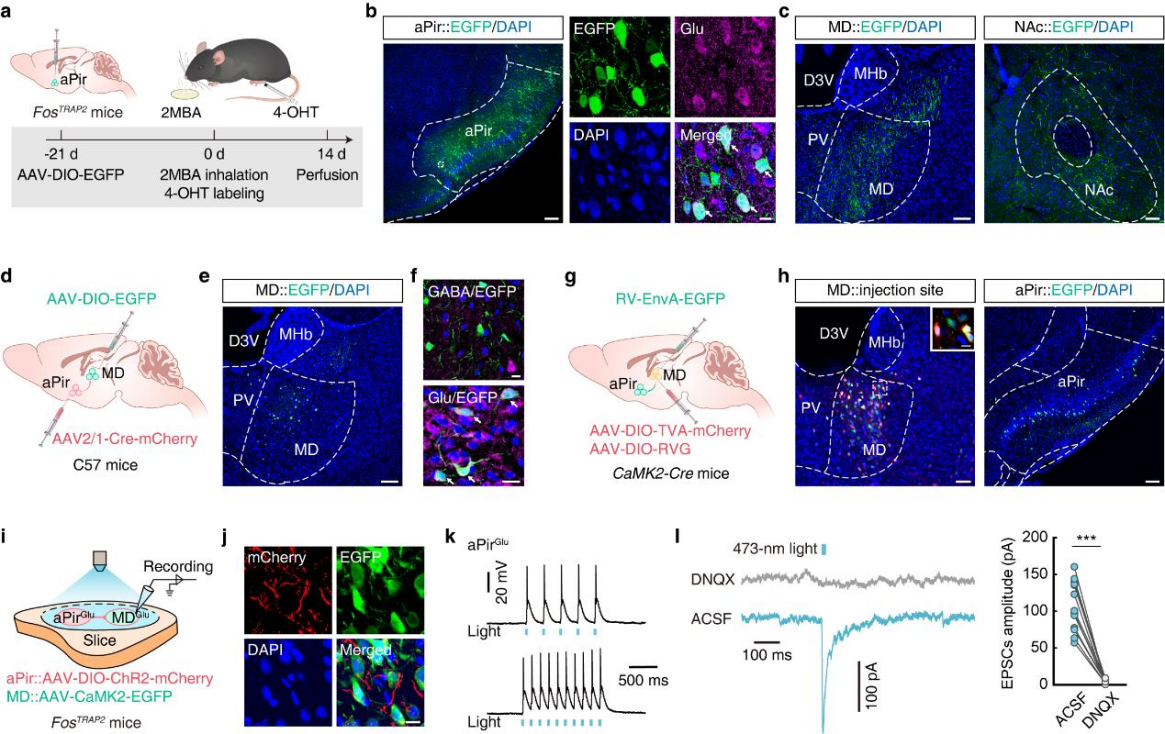
图3 | 2MBA激活的aPirGlu神经元投射至MD
既往研究显示,NAc(95%为GABA能神经元)参与气味加工。为了验证aPirGlu→NAc通路连接,向C57小鼠aPir注射AAV2/1-Cre-mCherry,NAc注射AAV-DIO-EGFP(图4a)。三周后,NAc的EGFP⁺神经元仅与GABA抗体共定位(图4b,c)。向GAD2-Cre小鼠NAc注射辅助病毒后,注射RV-ΔG-EGFP(图4d),一周后在aPir检测到与谷氨酸抗体共定位的EGFP⁺神经元(图4e),证实aPirGlu可投射至NAcGABA神经元。为了明确通路功能连接,向FosTRAP2小鼠aPir注射AAV-DIO-ChR2-mCherry,NAc注射AAV-mDLx-EGFP(图4f)。经4-OHT处理及2MBA暴露后,NAc可见mCherry⁺纤维和 EGFP⁺神经元(图4g)。光刺激可诱发NAcGABA产生EPSCs,DNQX处理后该效应消失(图4h),证实两者存在功能性连接。向C57小鼠MD注射retro-AAV-EGFP,NAc注射retro-AAV-mCherry,结果显示aPir中75.44%的EGFP⁺与mCherry⁺神经元无共定位。表明投射至MD和NAc的aPir神经元为不同亚群,可能介导不同行为。综上,2MBA激活的aPirGlu可投射至MDGlu和NAcGABA(图4i)。
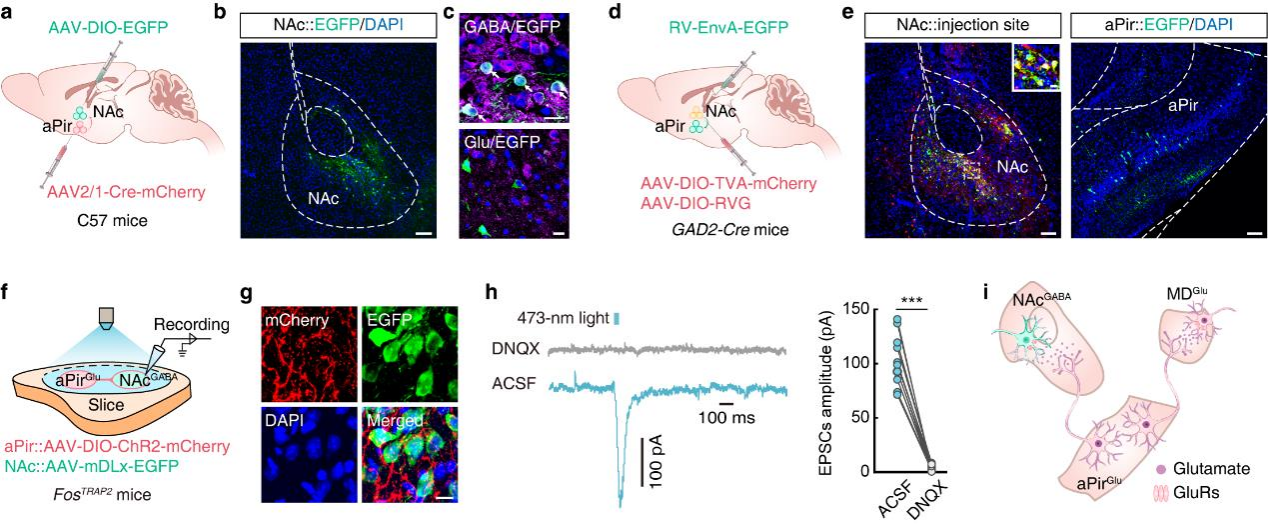
图4 | 2MBA激活的aPirGlu神经元投射至NAc
为了明确aPirGlu→MDGlu与aPirGlu→NAcGABA通路的功能,对自由活动小鼠MD和NAc进行在体多电极电生理记录(图5a)。结果显示,干呕样行为可显著提升MD神经元放电率,NAc无变化(图5b,c);而CPA后测中,小鼠进入2MBA配对箱时NAc放电率升高,MD无变化。据此聚焦MD调控干呕样行为、NAc调控厌恶反应。向CaMK2-Cre小鼠MD注射AAV-DIO-GCaMP6m,光纤记录显示2MBA诱发干呕样行为时,MDGlu钙信号呈时间锁定升高,CPA测试中无此现象(图5d-f)。通过GRIN透镜单细胞监测(图5g),进一步证实aPir支配的MD神经元钙活性仅在干呕样行为时升高(图5h,i),且对其他气味无响应,表明MD神经元特异性响应2MBA诱发的干呕样行为。
通过多部位注射特异性病毒及RV-Flp-DsRed示踪(图5j),在OB观察到EGFP⁺与DsRed⁺共标记神经元(图5k),成功可视化鼻→OB→aPir→MD完整通路。向aPir注射CNO抑制该通路(图5l),结果小鼠干呕样行为显著减少,条件性厌恶无变化(图5m-p),证实鼻→OB→aPir→MD通路是2MBA诱发干呕样行为(非厌恶反应)的必需通路。
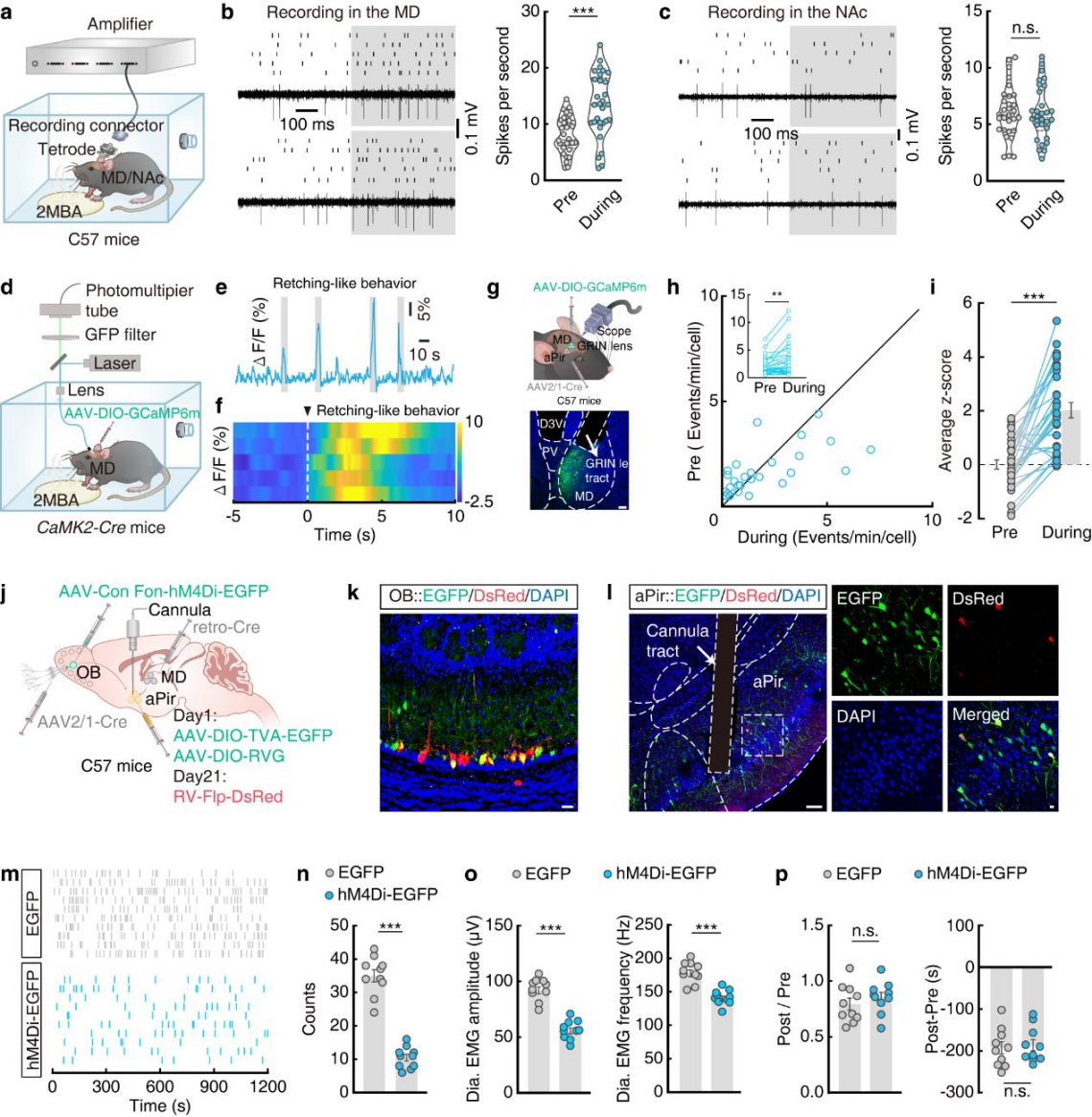
图5 | 鼻→OB→aPir→MD神经环路调控2MBA触发的干呕样行为
为了探究aPirGlu→NAcGABA通路的功能,对NAc表达AAV-DIO-GCaMP6m的GAD2-Cre小鼠,进行光纤记录(图6a)。结果显示,CPA后测中小鼠进入2MBA配对箱时钙活性升高,干呕样行为时无变化(图6b,c)。通过GRIN透镜单细胞监测(图6d),进一步证实该结果(图6e-g),且其他气味暴露时NAc神经元也在厌恶反应中激活,表明NAc神经元参与气味诱发的厌恶反应。通过多部位注射特异性病毒及RV-Flp-DsRed示踪(图6h),在OB观察到EGFP⁺与DsRed⁺共标记神经元,清晰呈现鼻→OB→aPir→NAc通路的解剖学连接(图6i)。向aPir注射CNO抑制该鼻-脑轴(图6j),行为学检测显示,对2MBA的条件性厌恶减轻,干呕样行为无变化(图6k-n),证实其是2MBA诱发厌恶反应的必需通路。
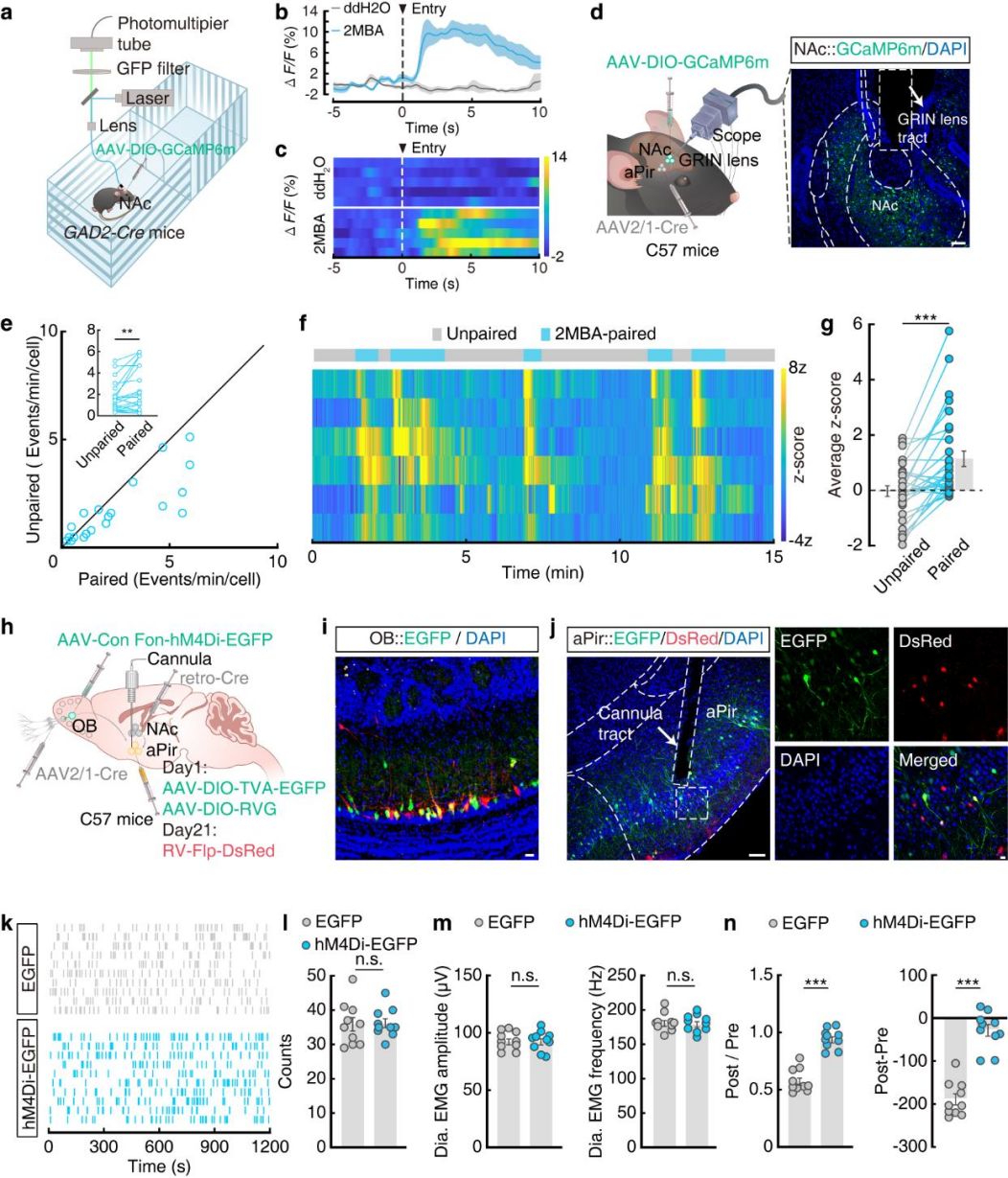
图6 | 鼻→OB→aPir→NAc神经环路调控2MBA触发的厌恶反应
已知“鼻→OB→aPir→MD”通路介导2MBA诱发的干呕样行为,且干呕伴随膈肌、腹部肌肉活动增强,进一步探究MD调控呼吸肌的机制。向C57小鼠腹外斜肌注射PRV-RFP、膈肌注射PRV-EGFP(图7a),四天后在PVN、PAG、VRG等脑区观察到共标记神经元(图7b)。向MD注射AAV-DIO-mCherry、VRG注射逆行EGFP,三周后在VLPAG检测到被mCherry⁺纤维环绕的EGFP⁺神经元(图7c-e),提示MD通过“MD→VLPAG→VRG”通路调控相关肌肉。为了验证“MD→VLPAG”通路功能,向CaMK2-Cre小鼠MD注射AAV-DIO-ChR2-mCherry,VLPAG植入光纤。473nm蓝光激活通路后,干呕样行为增多,腹外斜肌、膈肌活动的频率与振幅升高,对照组无此变化。综上,酸败气味通过两条独立通路介导不同反应:干呕样行为通路为“鼻→OB→aPir→MD→VLPAG→VRG→呼吸肌”,厌恶反应通路为“鼻→OB→aPir→NAc”(图7f)。
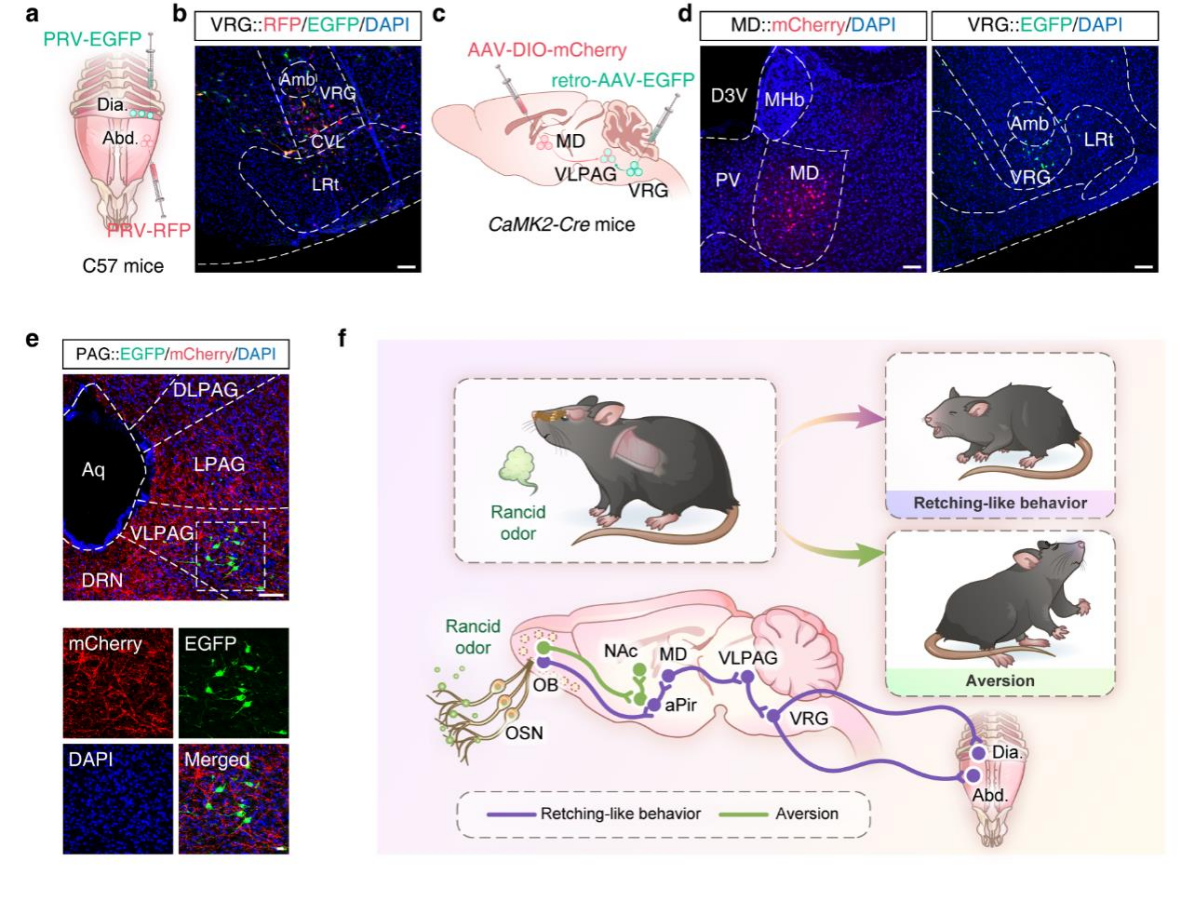
图7 | 定义MD→ VLPAG → VRG →呼吸肌回路
首次阐明腐败食物气味触发防御反应的双重 “鼻—脑轴” 机制,明确 aPirGlu为通路枢纽,揭示了嗅觉信息整合与行为输出的特异性神经编码方式。为开发气味疗法、鼻内神经调节策略提供靶点,可用于维持代谢稳态或治疗代谢紊乱。
本文使用的工具病毒布林凯斯均可提供:
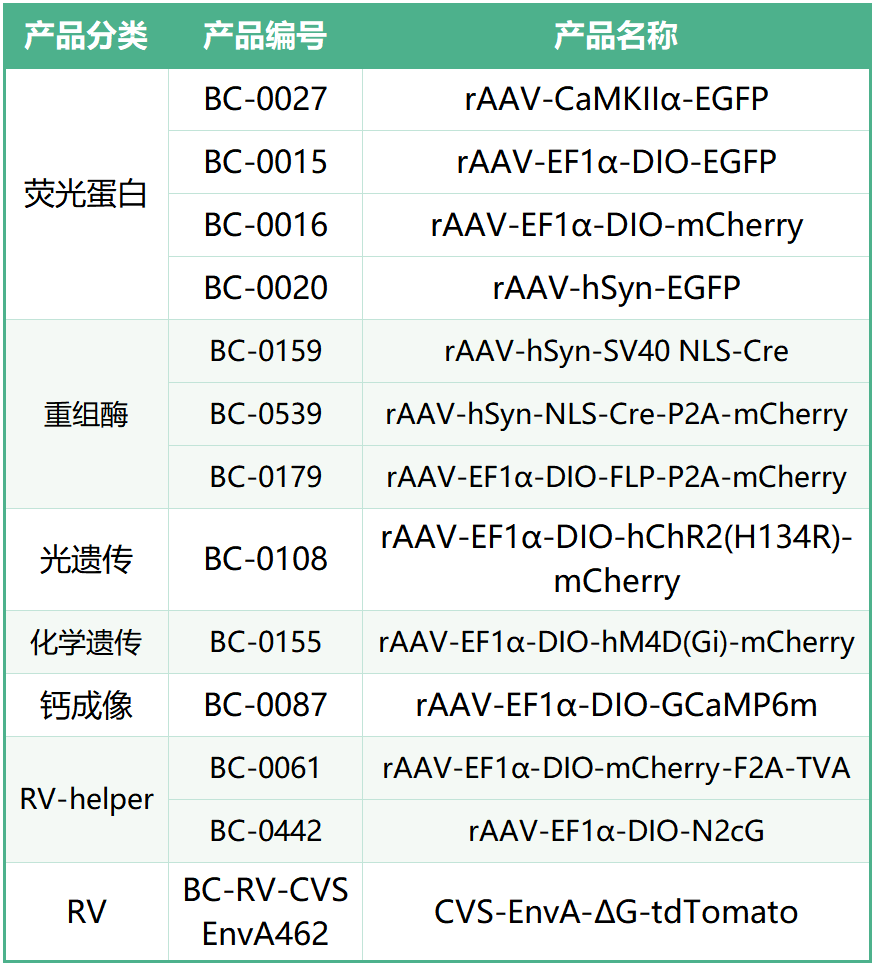
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。