抑郁症(MDD)是全球高发的精神疾病,具有高自杀率、高复发率特点。腹侧海马(vHip)是情绪与应激调控的核心脑区,星形胶质细胞通过维持谷氨酸稳态保护神经元,而铁死亡(铁依赖的脂质过氧化程序性死亡)与抑郁症病理相关。铁分子伴侣蛋白PCBP1调控细胞铁稳态,但其在星形胶质细胞铁死亡及抑郁症中的作用未知。
2025年12月12日,西安交通大学王云鹏、马现仓、魏曙光共同通讯在Advanced Science发表题为“Astrocytic PCBP1 Suppresses Ferroptosis to Restore Glutamatergic Homeostasis and Mitigate Stress-Induced Depression in Male Mice”相关论文,聚焦慢性应激诱导的抑郁症机制,通过蛋白质组学、磷酸化蛋白质组学等多技术手段发现,vHip星形胶质细胞中PCBP1蛋白可通过抑制铁死亡、维持谷氨酸稳态保护谷氨酸能神经元,进而改善小鼠抑郁样行为;PCBP1下调会增强星形胶质细胞铁死亡敏感性,加剧亚阈值应激下的抑郁易感性,而铁死亡抑制剂DFO或星形胶质细胞特异性过表达PCBP1可逆转该效应,揭示PCBP1是应激诱导抑郁症的潜在治疗靶点。

为了探究慢性应激对vHip细胞的影响,采用慢性不可预测温和应激(CUMS)模型评估小鼠抑郁样行为。结果显示,CUMS组小鼠第3-8周体重显著下降,第4周起蔗糖偏好持续降低,悬尾测试(TST)和强迫游泳测试(FST)中不动潜伏期缩短、不动时间延长,成功诱导抑郁样表型;旷场测试(OFT)证实行为改变与运动功能损伤无关(图1a-e)。对两组小鼠vHip组织进行蛋白质组学与磷酸化蛋白质组学分析,CUMS组存在271种差异表达蛋白质(DEPs),其中上调157种、下调114种,凸显vHip蛋白质表达失调(图1f-g)。GO富集分析显示DEPs主要关联突触功能与核糖体活性;KEGG分析表明其参与谷氨酸能突触、神经退行性疾病、凋亡及铁死亡相关通路(图1h-j),其中谷氨酸能突触通路与抑郁症密切相关。免疫印迹验证显示,CUMS组GRIA1、GRIA3、谷氨酰胺合成酶(GS)、14-3-3γ、GPX4下调,DHCR7上调(图1k)。磷酸化蛋白质组学分析有效分组,CUMS组鉴定出345种上调、163种下调磷酸化蛋白质(图1l-n)。KEGG分析显示其富集于铁死亡、胞吞作用等通路,且铁死亡相关蛋白(PCBP1、PCBP2等)磷酸化水平下调(图1o)。综上,CUMS可诱导小鼠vHip产生铁死亡相关的蛋白质组学及磷酸化蛋白质组学特征,后续将进一步探究铁死亡调控vHip功能与抑郁样行为的潜在机制。
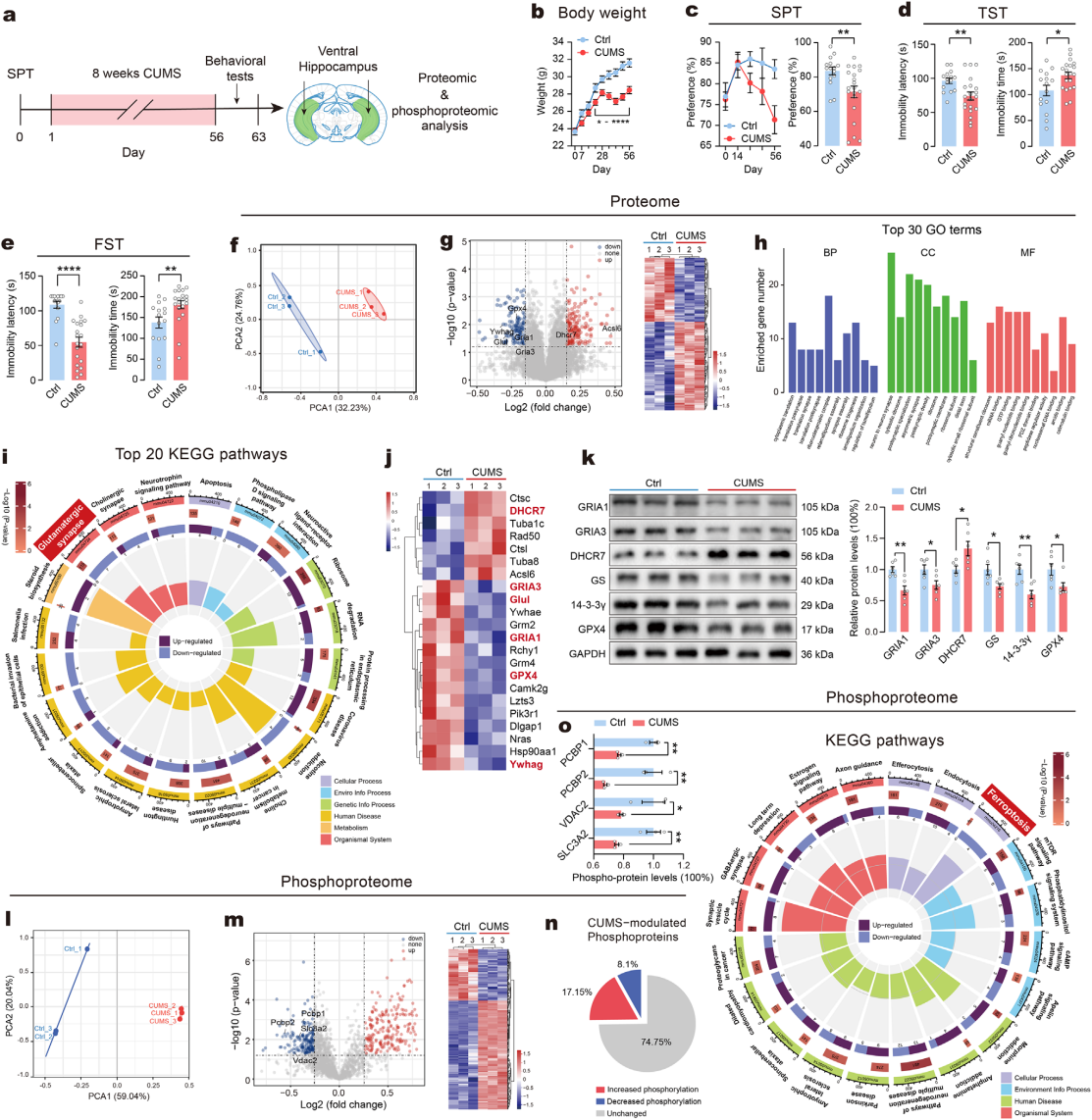
图1 慢性应激影响vHip中的铁死亡
为了验证vHip铁死亡通路与慢性应激诱导抑郁样行为的关联性,检测vHip铁死亡相关病理指标,结果显示慢性应激显著降低vHip谷胱甘肽(GSH)水平,升高丙二醛(MDA)和铁离子浓度,且活性氧(ROS)生成增加(图2a-b)。
免疫荧光染色表明,慢性应激仅导致vHip星形胶质细胞数量显著减少(图2c-d)。CUMS显著减少vHip中GPX4阳性细胞(尤其GPX4⁺-GFAP⁺星形胶质细胞),且DG、CA1、CA3亚区均呈一致趋势;星形胶质细胞形态异常(长度缩短、分支减少),线粒体出现皱缩、嵴减少等铁死亡典型特征(图2e-g)。透射电镜(TEM)和高尔基染色显示,CUMS组vHip突触密度、突触后致密区(PSD)厚度及树突棘数量(主要为分支型)显著降低,突触间隙和PSD长度无影响(图2h-i)。综上,慢性应激可诱导小鼠vHip星形胶质细胞铁死亡,并导致神经元突触损伤。
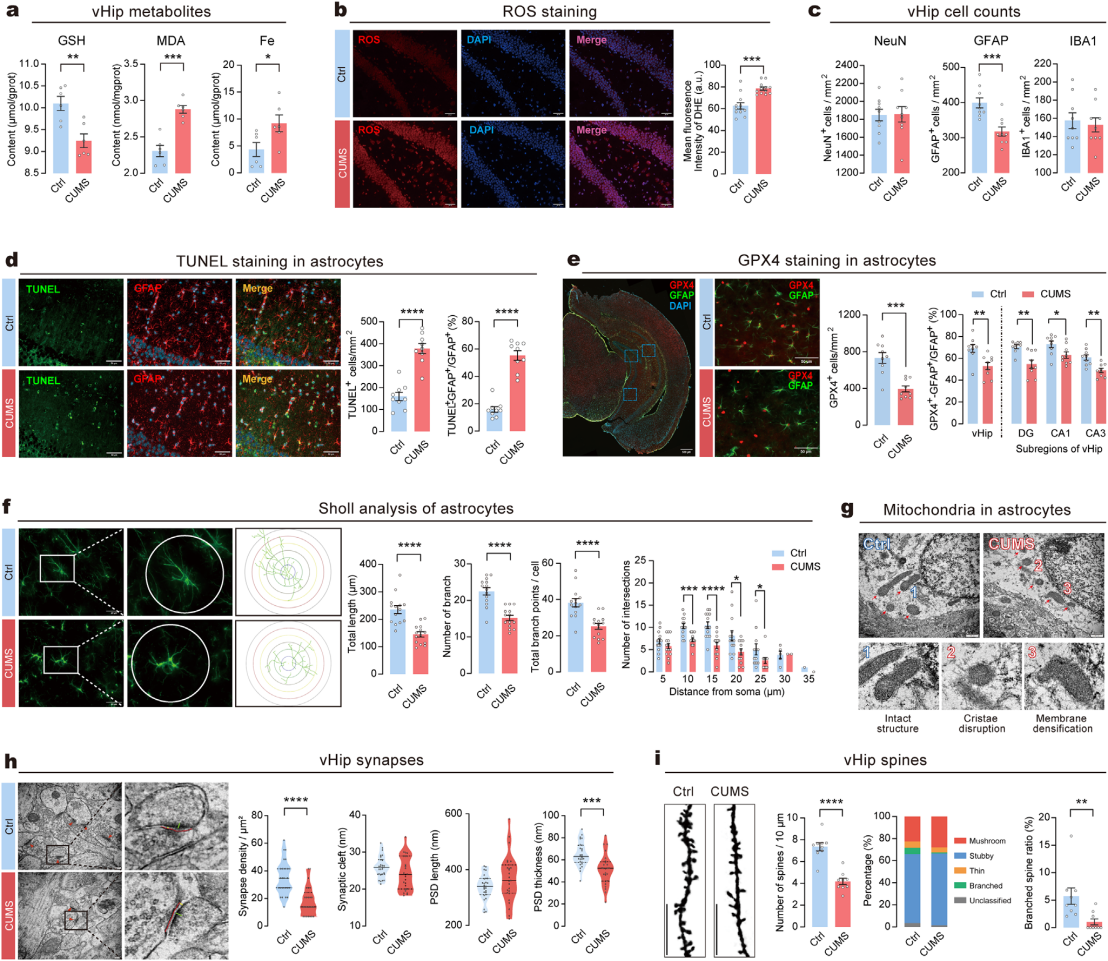
图2 慢性应激诱导vHip中星形胶质细胞铁死亡及神经元功能损伤
为了验证vHip星形胶质细胞铁死亡与慢性应激抑郁样行为的关联,CUMS期间给小鼠施用铁死亡抑制剂DFO(甲磺酸去铁胺)(图3a)。DFO可逆转CUMS小鼠体重下降、恢复蔗糖偏好,改善TST/FST行为学指标(图3b-e),且不影响自发活动,证实抑制铁死亡可改善抑郁样行为。CUMS升高vHip中MDA、铁含量及ROS,降低GSH,DFO可逆转这些铁死亡相关指标异常(图3f-g);同时恢复星形胶质细胞GPX4表达、修复细胞形态及线粒体完整性(图3h-k)。DFO还可逆转CUMS诱导的GS下调,恢复vHip谷氨酸水平至正常(图3l);并修复突触损伤、阻止树突棘密度及分支型比例下降(图3m-n)。综上,DFO通过抑制铁死亡,缓解应激抑郁样行为,恢复星形胶质细胞功能并逆转vHip谷氨酸能神经毒性。
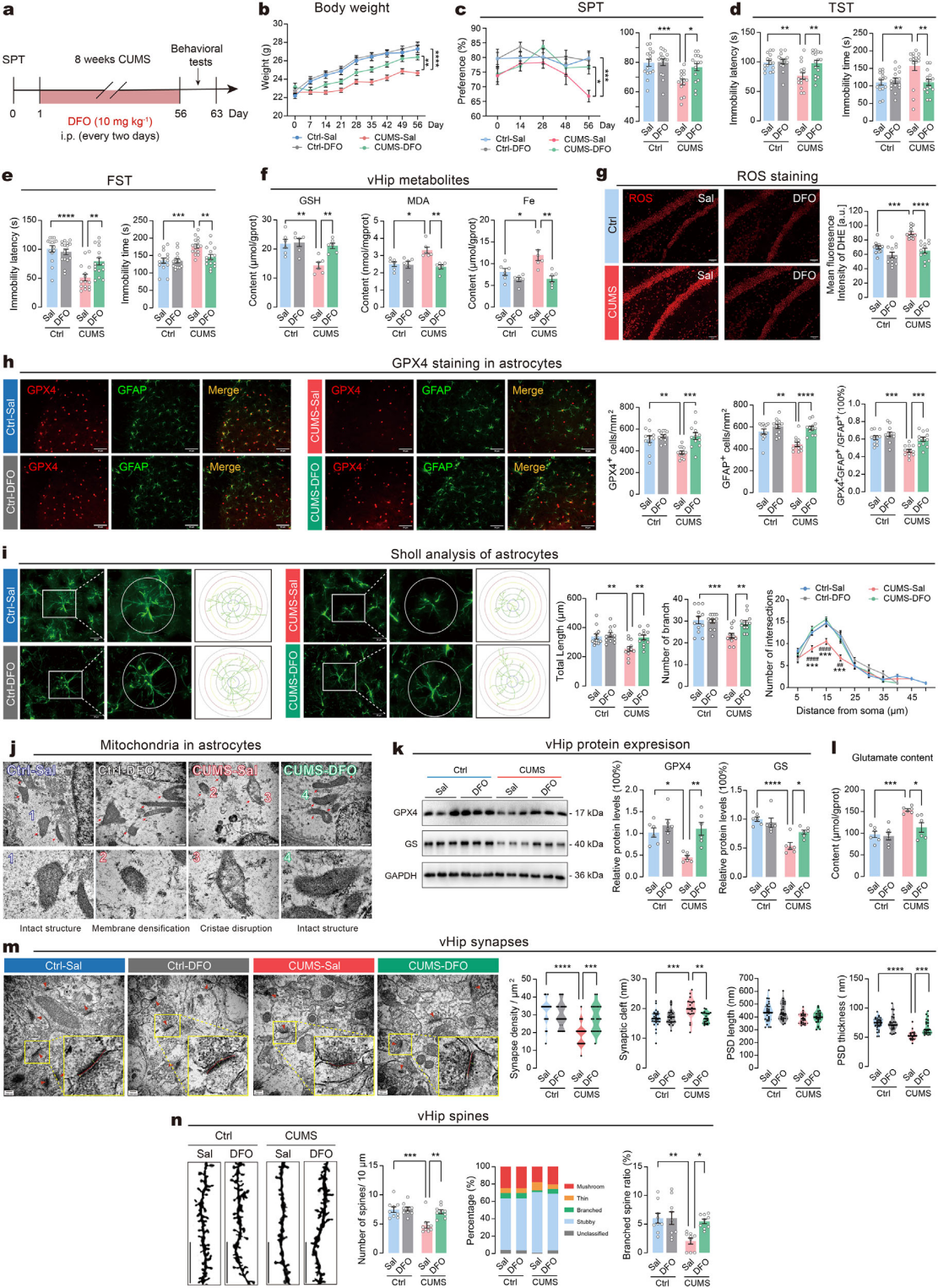
图3 去铁胺通过抑制星形胶质细胞铁死亡改善抑郁行为
细胞外谷氨酸清除主要由星形胶质细胞调控,其功能障碍会导致谷氨酸清除受损、神经元功能缺陷甚至凋亡。本研究建立体外共培养模型(图4a),探究星形胶质细胞铁死亡对海马细胞谷氨酸清除及神经毒性的影响。CCK-8法检测显示,谷氨酸以时间依赖方式降低海马HT22细胞活力(图4b)。与星形胶质细胞GL261细胞共培养可显著降低谷氨酸对HT22细胞的毒性(活力升高、乳酸脱氢酶LDH降低,图4c-d),并挽救谷氨酸诱导的突触标志物PSD95、SYN下调,提示神经毒性减弱(图4e)。向GL261细胞施用铁死亡诱导剂erastin(依拉司汀),其以剂量-时间依赖方式降低GL261活力(图4f)。谷氨酰胺合成酶(GS)是谷氨酸代谢关键酶,erastin可显著降低GL261细胞GS活性,DFO可挽救该效应(图4g),且erastin处理会完全消除GL261对HT22细胞的谷氨酸毒性保护作用(图4h-i)。综上,星形胶质细胞GL261铁死亡会加剧海马HT22细胞的谷氨酸毒性。
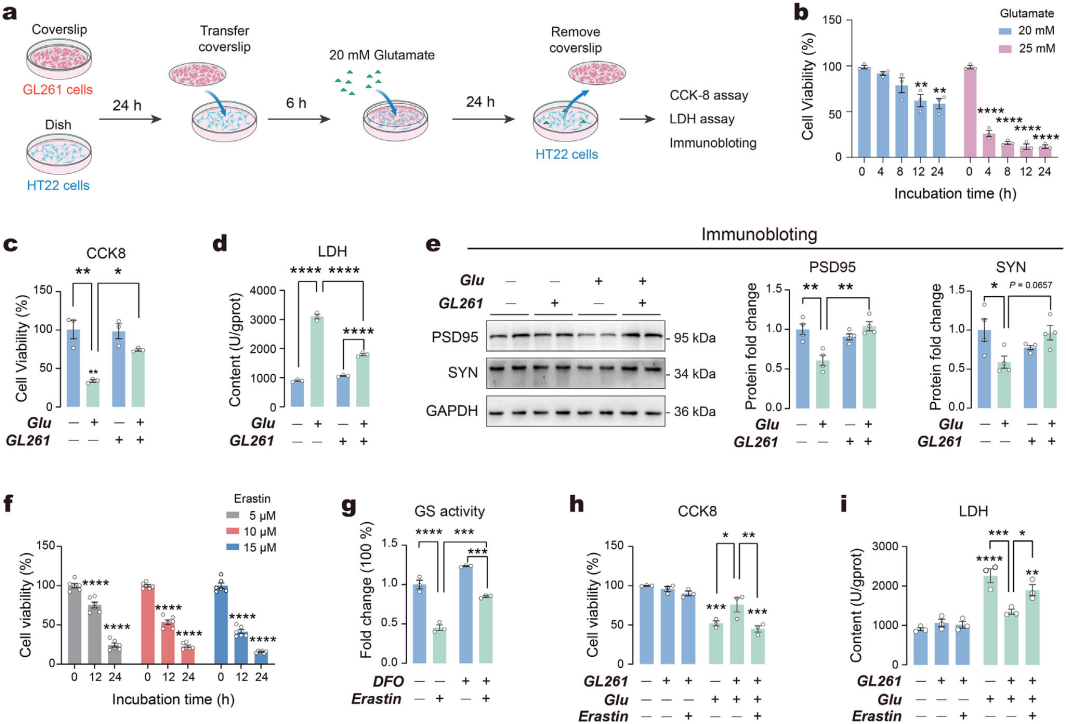
图4 星形胶质细胞GL261中的铁死亡影响海马HT22细胞中的谷氨酸毒性
将靶向PCBP1(shP1)或PCBP2(shP2)的shRNA质粒转染GL261细胞,经10μM erastin处理12h后检测活力及ROS水平(图5a)。结果显示,单独敲低PCBP1/2对细胞活力和ROS无影响;但敲低PCBP1(而非PCBP2)显著加剧erastin诱导的细胞死亡并升高ROS(图5b-c),且转染后相应蛋白表达特异性降低(图5d),erastin处理后各组GPX4表达无差异。C8-D1A星形胶质细胞中重复实验结果一致,提示体外敲低PCBP1增强星形胶质细胞对铁死亡的敏感性。
采用亚阈值CUMS(sCUMS)模型探究vHip星形胶质细胞PCBP1敲低对小鼠抑郁样行为的作用。sCUMS前3周,向小鼠vHip双侧注射星形胶质细胞特异性PCBP1 shRNA腺相关病毒(AAV)(图5e),结果证实eGFP⁺星形胶质细胞中PCBP1有效敲低(图5f-g)。sCUMS结束后评估抑郁样行为:单独敲低PCBP1不影响体重,sCUMS显著降低小鼠体重(图5h);shPCBP1联合sCUMS组小鼠抑郁样行为明显(图5i-k)。铁死亡标志物检测发现单独sCUMS或PCBP1敲低不影响GPX4⁺星形胶质细胞比例及GSH、MDA水平;但二者联合显著降低星形胶质细胞GPX4表达(图5l),降低GSH并升高MDA。综上,PCBP1调控星形胶质细胞对铁死亡的敏感性及小鼠对亚阈值应激的易感性。
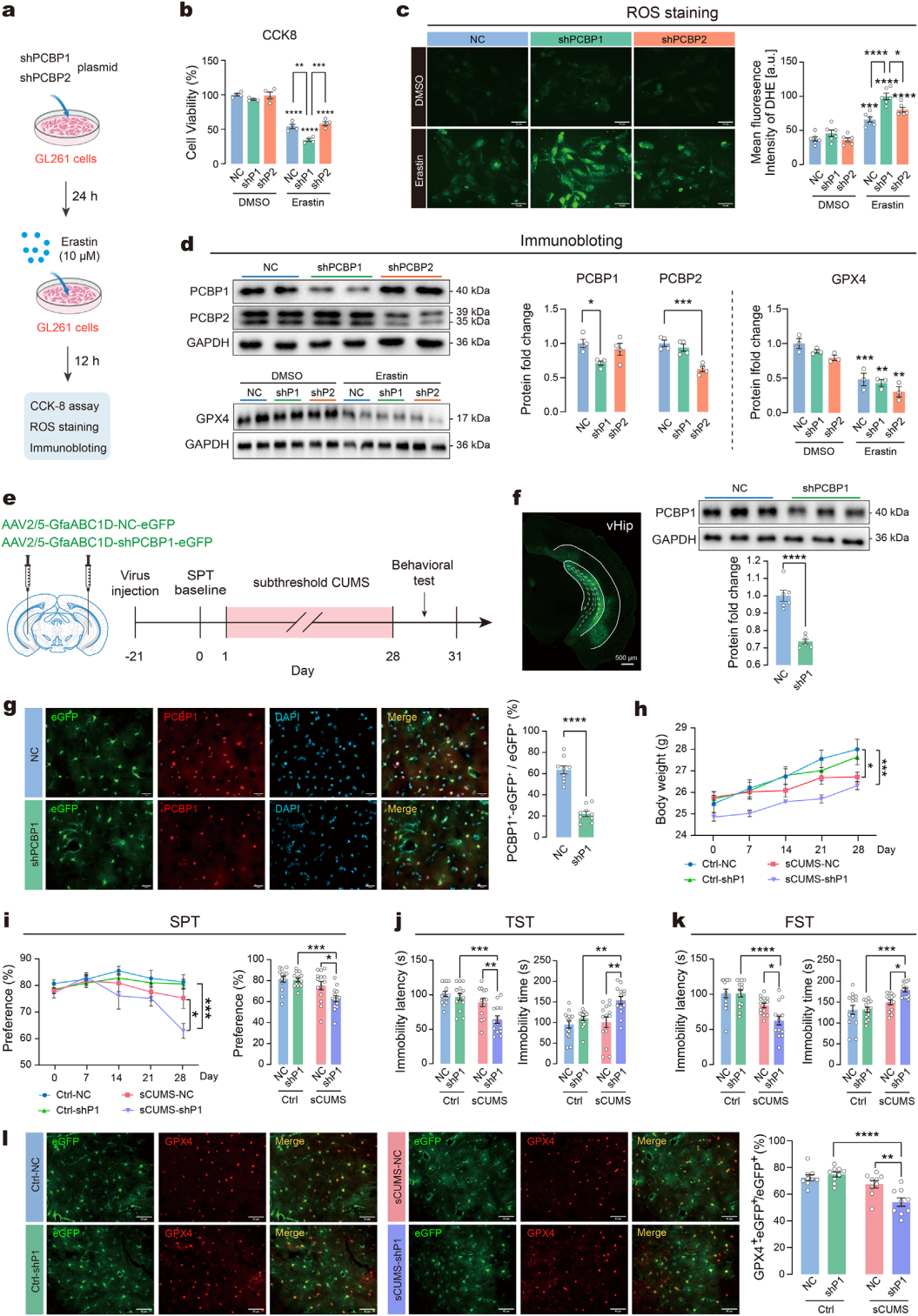
图5 PCBP1负责调控星形胶质细胞铁死亡的敏感性及对阈下应激的易感性
用慢病毒感染星形胶质细胞GL261介导PCBP1过表达,经erastin孵育12小时(图6a)。结果显示,过表达PCBP1可保护GL261细胞免受erastin诱导的细胞死亡,并降低ROS水平(图6b-d),可上调erastin处理组的GPX4表达。这些结果表明,体外上调PCBP1可保护星形胶质细胞免受erastin诱导的铁死亡。
在CUMS处理前3周,向小鼠vHip双侧注射星形胶质细胞特异性过表达PCBP1的腺相关病毒(AAV)(图6e)。过表达PCBP1可显著升高CUMS暴露小鼠的蔗糖偏好(图6f-i);显著延长CUMS组小鼠TST和FST的不动潜伏期,缩短不动时间(图6j-k)。
为进一步验证星形胶质细胞过表达PCBP1在体内对铁死亡和谷氨酸稳态的影响,检测了铁死亡标志物及谷氨酸代谢相关关键蛋白,结果显示过表达PCBP1显著逆转CUMS诱导的GPX4阳性星形胶质细胞比例降低,恢复GSH水平,减轻MDA蓄积(图6l–n);逆转CUMS诱导的GPX4、GLT1和GS表达下调,而谷氨酸-天冬氨酸转运体(GLAST)表达无显著变化(图6o);同时,显著降低谷氨酸含量(图6p)。为了明确PCBP1是否通过调控谷氨酸稳态发挥抗抑郁作用,在行为学测试前3小时向vHip注射GS抑制剂MSO。结果显示MSO处理完全逆转了过表达PCBP1对CUMS小鼠的行为改善效应,表现为蔗糖偏好显著降低(图6s),TST和FST的不动时间显著延长(图6t-u),且达到CUMS对照组水平。这些结果表明PCBP1的抗抑郁效应通过调控vHip星形胶质细胞的谷氨酸稳态介导。综上,这些结果表明,星形胶质细胞PCBP1上调可有效抑制铁死亡、恢复谷氨酸稳态,并改善CUMS诱导的抑郁样行为。
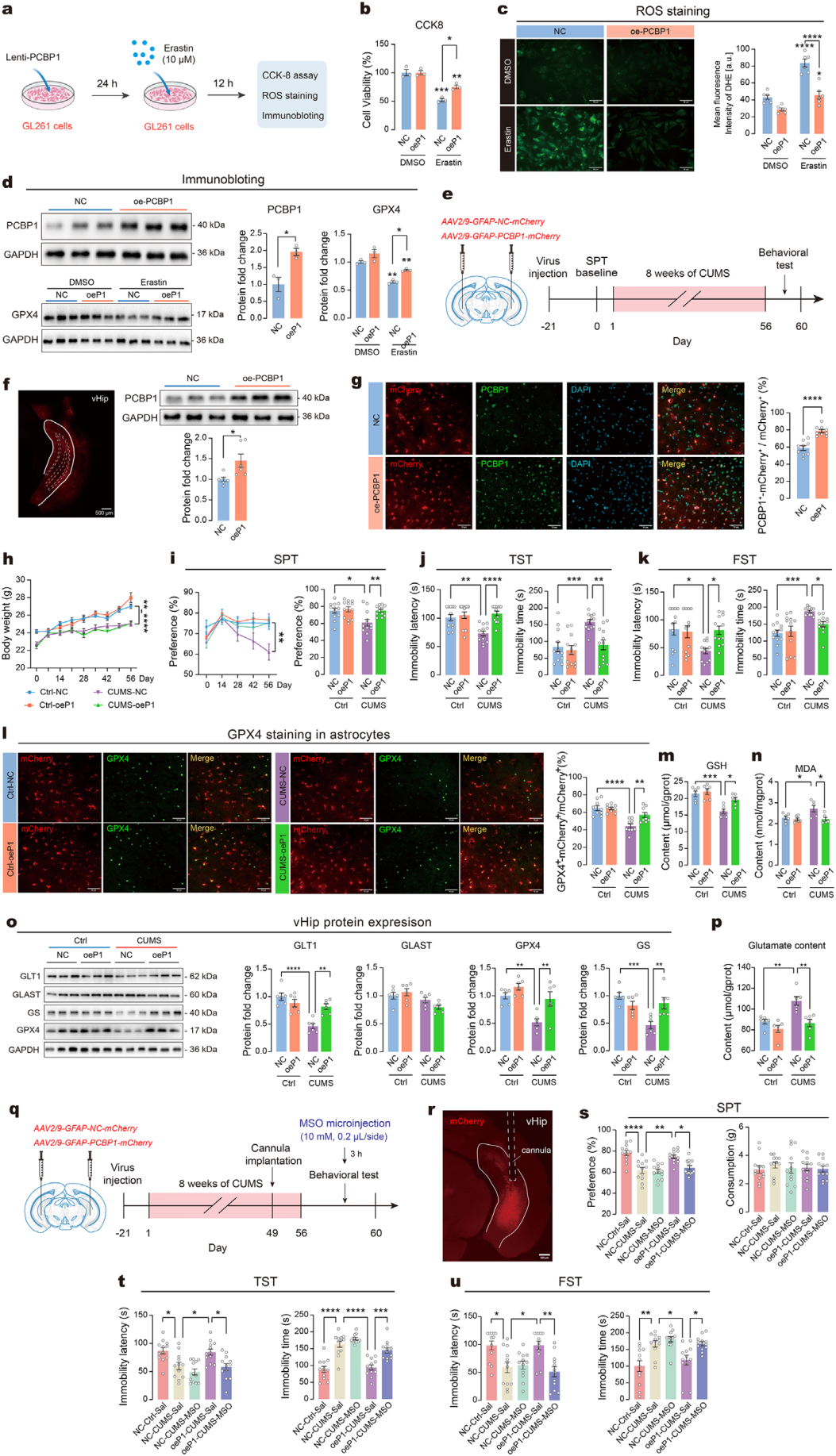
图6 星形胶质细胞PCBP1可保护星形胶质细胞免受铁死亡,并改善慢性应激诱导的抑郁样行为
基于此前星形胶质细胞GL261铁死亡加剧海马HT22细胞谷氨酸毒性的结果,探究星形胶质细胞PCBP1介导的铁死亡抑制是否缓解慢性应激诱导的vHip神经元功能损伤。最后一次FST后,神经元活性标志物c-Fos免疫染色结果显示,强迫游泳诱导Ctrl组vHip c-Fos高表达,CUMS组则降低;c-Fos与CaMKII阳性细胞共定位比例显著下降(图7a),提示应激应答差异主要由谷氨酸能兴奋性神经元介导。在vHip星形胶质细胞过表达PCBP1,采用钙成像GCaMP6s记录CUMS小鼠TST、FST期间神经元活性(图7b-c)。免疫染色显示,PCBP1过表达可增加CUMS小鼠vHip c-Fos阳性细胞总数及其在谷氨酸能神经元中的比例(图7d-e)。TST期间记录显示小鼠挣扎活跃期(高钙信号)与被动不动期(低钙信号)交替出现(图7f);CUMS组随机挣扎后6秒内钙信号强度显著低于Ctrl组,而PCBP1过表达组小鼠钙信号模式与Ctrl组相似(图7g),提示PCBP1过表达可挽救CUMS诱导的vHip谷氨酸能神经元钙活性降低。
采用谷氨酸探针iGluSnFR探究PCBP1对vHip谷氨酸水平的调控(图7b、h),结果显示CUMS组在TST(图7i、j)和FST中谷氨酸事件频率增加、AUC增大、衰减时间延长;PCBP1过表达可将这些异常恢复至Ctrl组水平。vHip脑片全细胞膜片钳记录显示(图7k),CUMS显著降低谷氨酸能神经元mEPSC频率(图7l)和诱发动作电位发放率(图7m),而星形胶质细胞PCBP1过表达可逆转这些损伤。综上,星形胶质细胞过表达PCBP1可有效逆转慢性应激诱导的vHip谷氨酸能神经元低活性及谷氨酸调控异常。
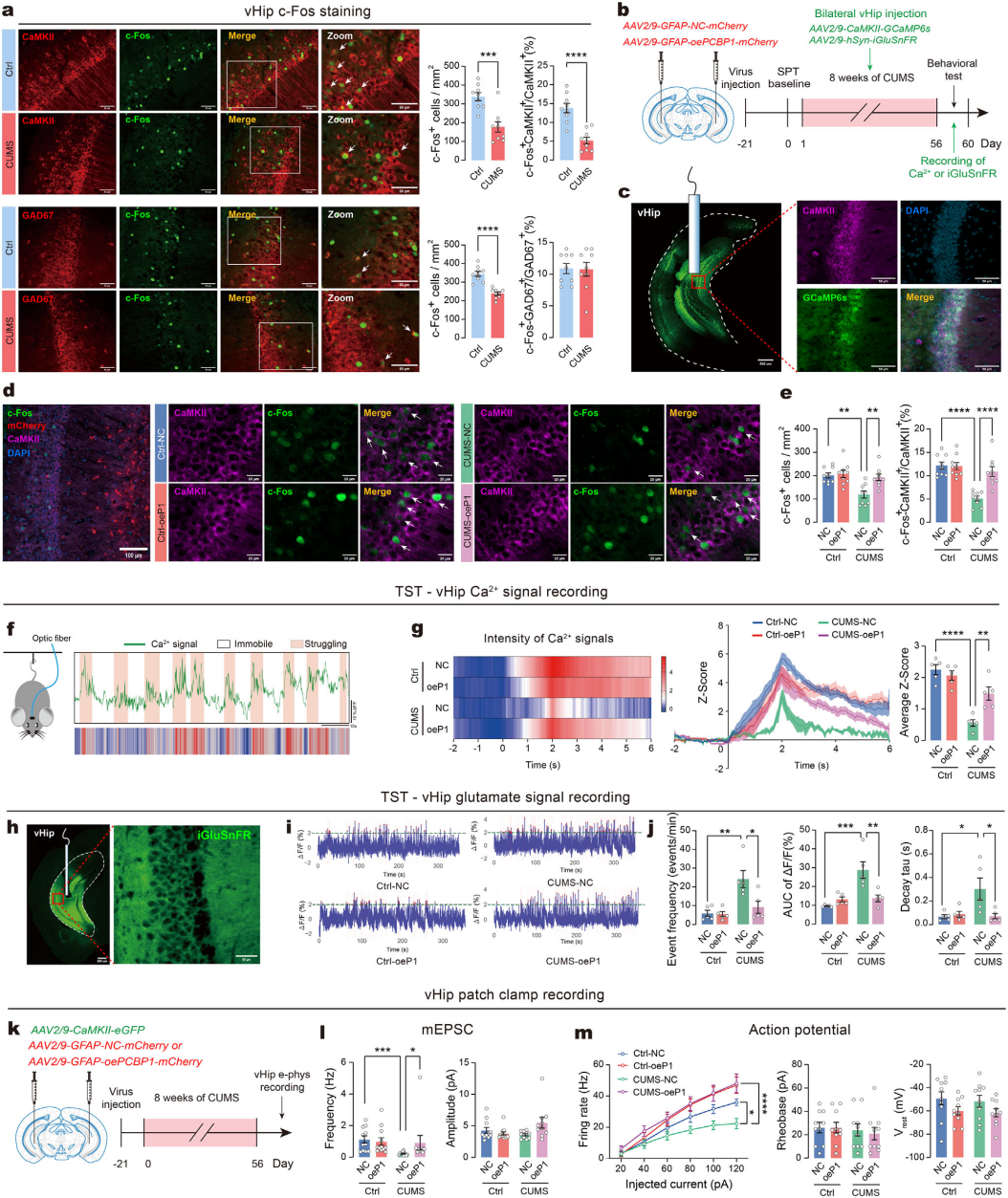
图7 星形胶质细胞PCBP1增强谷氨酸能神经元活动及神经生理学功能
为了探究PCBP1调控星形胶质细胞铁死亡的机制,将shPCBP1质粒转染GL261细胞沉默PCBP1后进行转录组学分析。数据分析显示差异表达基因(DEGs)富集于凋亡、铁死亡及氧化应激相关通路,提示敲低PCBP1影响多细胞通路(图8a-c)。将3093个DEGs与661个铁死亡相关基因(源自FerrDB、KEGG、AmiGO2数据库)交叉比对,鉴定出122个重叠DEGs(图8d)。GO分析显示其富集于氧化应激、铁离子稳态等相关术语(图8e),提示下调PCBP1破坏星形胶质细胞铁平衡与氧化应激状态。KEGG分析表明其富集于铁死亡、HIF-1信号通路等(图8f),核心通路相互作用网络凸显Sat1、Acsl4、Gpx4等铁死亡相关DEGs(图8g)。对122个铁死亡相关DEGs进行蛋白质-蛋白质相互作用(PPI)分析(图8h),Il6、Slc11a2、Hmox1、Gpx4等9个关键枢纽基因连接性显著,在网络中起核心作用。
已知PCBP1可结合基因启动子区富含胞嘧啶基序调控转录。利用MEME套件在枢纽基因上游1kb区域筛选出5个显著富集的PCBP1结合基序(图8i),TomTom工具验证其与已知PCBP1结合基序显著匹配(图8j)。综上,PCBP1通过调控氧化应激和铁稳态相关基因调节铁死亡敏感性,在铁死亡通路中起关键作用。通过RNA免疫沉淀-定量PCR(RIP-qPCR)验证PCBP1对铁死亡相关靶点的直接调控:12个选定基因中11个在PCBP1免疫沉淀复合物中显著富集(图8k),琼脂糖凝胶电泳验证PCR产物(图8l)。PCBP1敲低/过表达分析显示,仅Ftl呈一致双向调控(PCBP1沉默时下调,PCBP1过表达时上调,图8m)。siRNA介导敲低Ftl、Fth、Slc11a2(图8n、o),erastin处理后,敲低Ftl或Fth显著增强铁死亡敏感性(细胞死亡增加、ROS升高),Slc11a2敲低无效应(图8p、q);各组GPX4表达均显著降低(图8r)。综上,Ftl是PCBP1调控星形胶质细胞铁死亡敏感性的主要功能下游靶点。
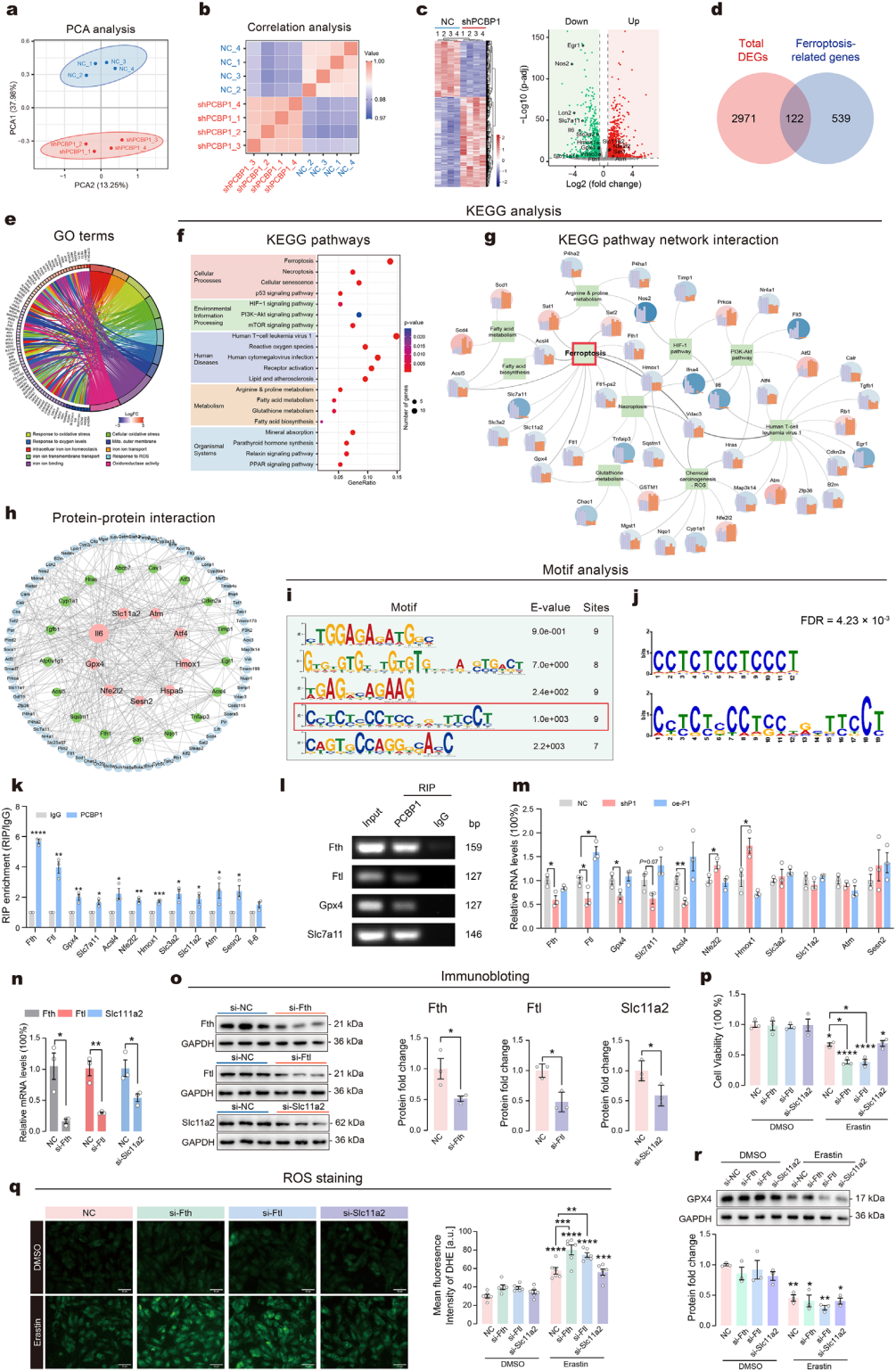
图8 PCBP1调控星形胶质细胞铁死亡敏感性的潜在机制
星形胶质细胞PCBP1通过抑制铁死亡、维持谷氨酸稳态,保护vHip谷氨酸能神经元,改善应激诱导的抑郁样行为,PCBP1是抑郁症潜在治疗靶点。
本文使用的工具病毒布林凯斯均可提供:
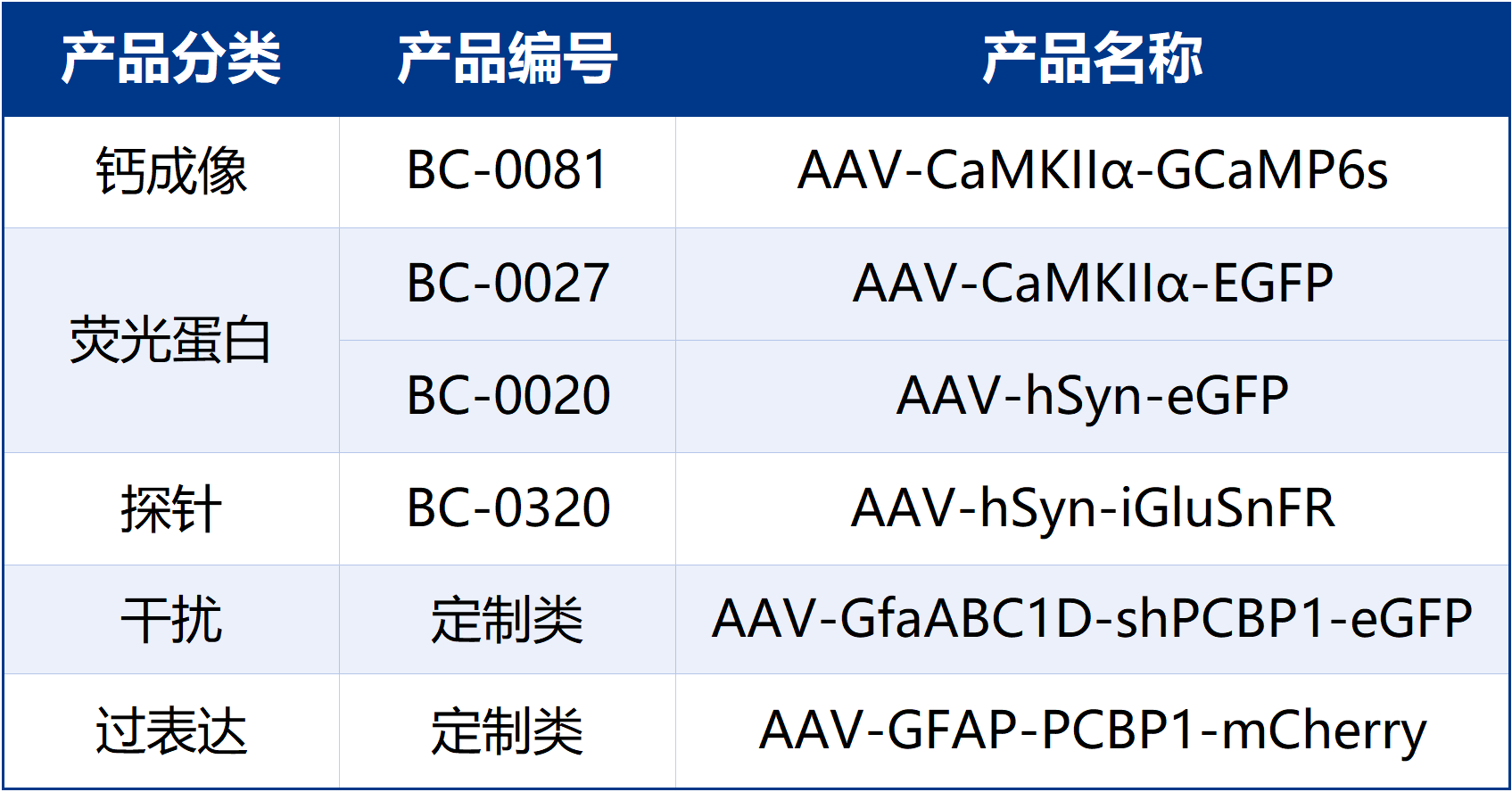
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。