双相情感障碍(BD)是一种以躁狂/轻躁狂与抑郁反复发作为特征的重性精神障碍,全球患病率约2%,临床表现复杂且误诊率高。已有研究表明,内侧前额叶皮层(mPFC)的突触可塑性改变及神经递质紊乱参与BD发病,但其机制尚未阐明。近年来,肠道菌群被视为肠-脑轴调控的关键环节,其失调与精神疾病密切相关,提示菌群可能通过调控神经可塑性及递质系统影响BD的行为表型。
近期,浙江大学医学院附属第一医院精神卫生中心胡少华教授、来建波特聘研究员,联合浙江大学脑科学与脑医学学院,浙江大学极端光学技术与仪器全国重点实验室及良渚实验室龚薇教授、斯科教授团队在Molecular Psychiatry杂志上发表了题为“Gut microbiota modulates synaptic plasticity, connectivity, and dopamine transmission in the VTA-mPFC pathway in bipolar depression”的研究文章。该研究揭示了BD患者肠道菌群通过削弱VTA-mPFC多巴胺能通路的结构连接与功能响应,损害mPFC突触可塑性,进而诱发抑郁样行为,为理解BD的肠-脑轴机制提供了新的实验依据。

研究首先通过抗生素处理(ABX)有效清除了受体小鼠的内源性菌群,随后对小鼠进行了双相障碍患者或健康供体的FMT。16S rRNA 测序显示,两组小鼠肠道菌群结构差异显著:α 多样性分析中 ,BD 组 Chao1、Simpson 指数更高(图1G-H),Shannon 指数和物种丰富度无差异;PCoA 分析表明两组菌群群落明显分离(图1I);LEfSe 分析发现 BD 组富集 6 种炎症相关菌属,部分有益菌属(如柠檬酸杆菌属、肠杆菌属)相对减少(图1L)。进一步分析表明,BD小鼠的菌群特征与人类BD患者的菌群高度重叠,共 259 个细菌物种(图1J、K)。综上,FMT有效构建了具有BD患者菌群特征的小鼠模型。
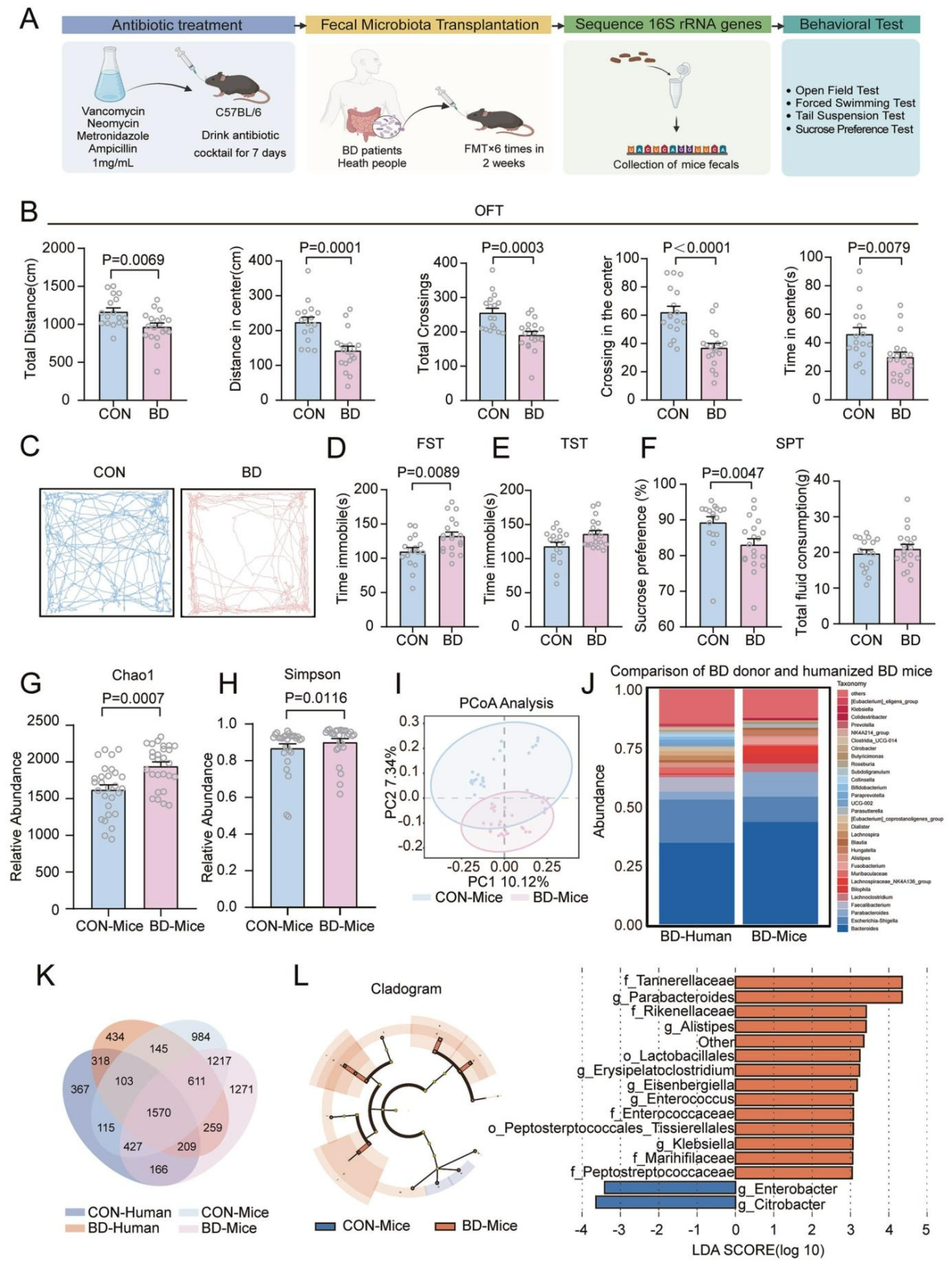
图1 BD患者肠道微生物群定植改变小鼠行为并实现微生物群人源化
为探究微生物-肠-脑轴如何调控双相抑郁样行为,研究聚焦于情绪调节关键脑区——mPFC。RNA测序显示,BD小鼠mPFC中存在202个基因上调和64个基因下调,且两组样本聚类明显分离(图2A-C)。GO富集显示下调基因主要与树突棘可塑性相关,而上调基因主要参与免疫反应(图2D-E)。通过GSEA进一步确认,“突触后翻译”是下调最显著的生物学过程,该过程调控长期突触可塑性(图2FG),同时qPCR实验验证了参与“突触后翻译”的Rpl、Rps、Eef、Uba等相关基因表达降低,这表明移植的微生物群损害了mPFC的长期突触可塑性。
在结构层面,研究向小鼠mPFC注射 SIN-pal-GFP 病毒进行神经元稀疏标记,对mPFC Ⅱ/Ⅲ层和Ⅴ层(主要处理长程输入的层级)神经元的树突棘密度与形态进行分析(图2H)。结果显示,BD小鼠mPFC锥体神经元的总树突棘密度显著降低(图2I-J),且所有树突棘亚型(薄棘、粗短棘、蘑菇棘)密度均呈非显著性降低,其中蘑菇棘的减少尤为明显(图2J),提示突触形成能力受损且存在亚型特异性易感性。综上,来自BD患者的肠道微生物群通过损害mPFC的突触后翻译与长期突触可塑性、降低树突棘密度,进而诱发双相抑郁样行为。
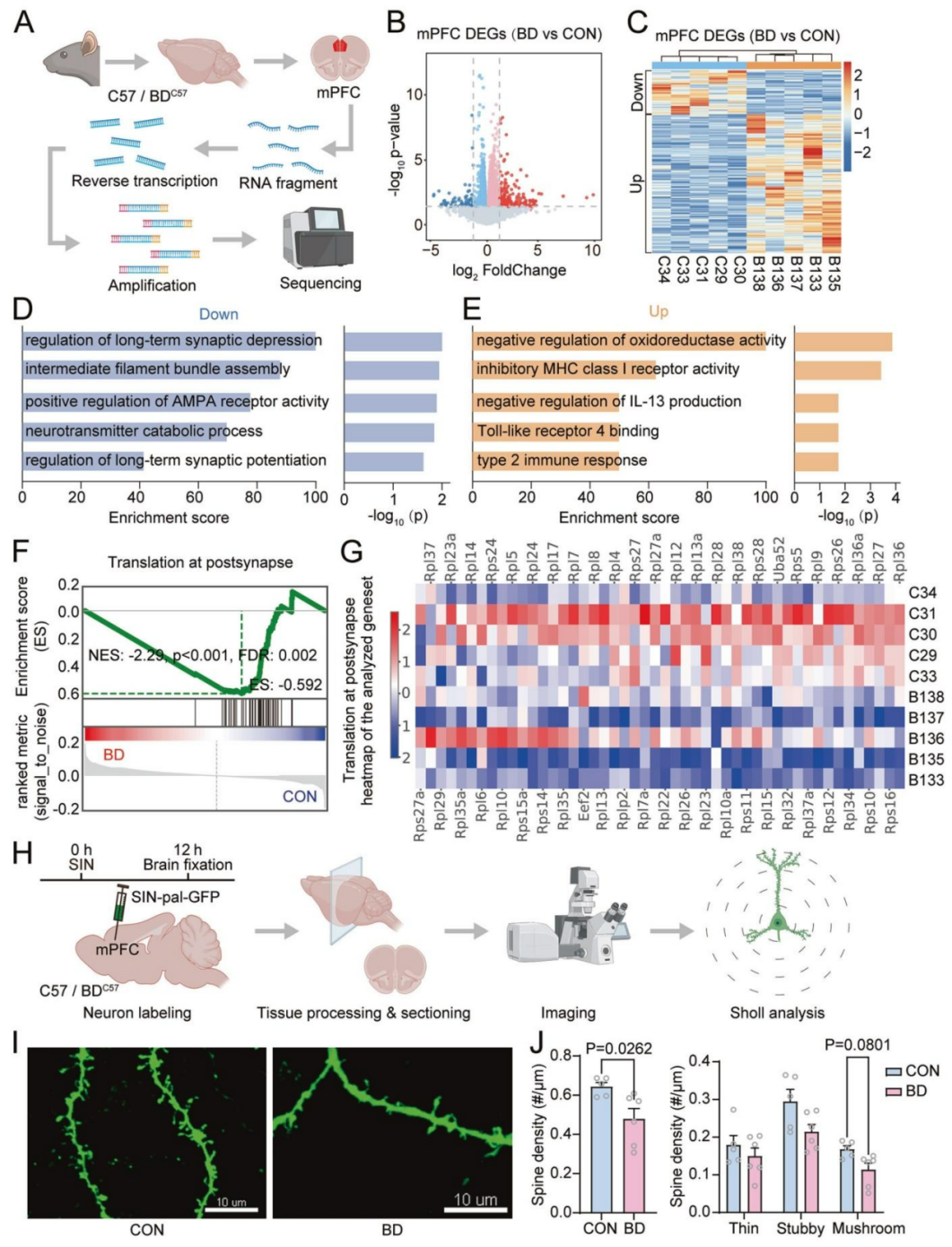
图2 mPFC的转录组和树突棘变化是双相抑郁样行为的潜在机制
为明确FMT对BD小鼠mPFC谷氨酸能神经元神经连接的影响,研究通过狂犬病毒逆向跨单突触追踪技术分析BD小鼠mPFC谷氨酸能神经元的全脑输入连接(图3A)。结果显示,>80%起始细胞集中于mPFC Ⅱ/Ⅲ层和Ⅴ层,两组起始细胞密度无差异(图3B),全脑组织成像显示多个脑区神经元与mPFC谷氨酸能神经元存在单突触连接(图3C)。进一步聚焦与双相情感障碍病理密切相关的神经递质系统,重点分析了具有明确起源核团的四大系统:基底前脑(乙酰胆碱)、中脑VTA/SNc(多巴胺)、中缝背核(5-羟色胺)及蓝斑核(去甲肾上腺素),以及它们向mPFC谷氨酸能神经元的投射变化。结果发现,只有多巴胺系统的病毒标记量在BD组显著低于CON组(图3E),进一步细分脑区分析显示,VTA到mPFC谷氨酸能神经元的连接是减弱的关键通路,来自其他重要脑区的输入在两组间未发现显著差异(图3G-H)。综上,肠道菌群移植可能特异性削弱了VTA-mPFC的多巴胺能通路,这可能是BD抑郁样行为的重要神经环路基础。
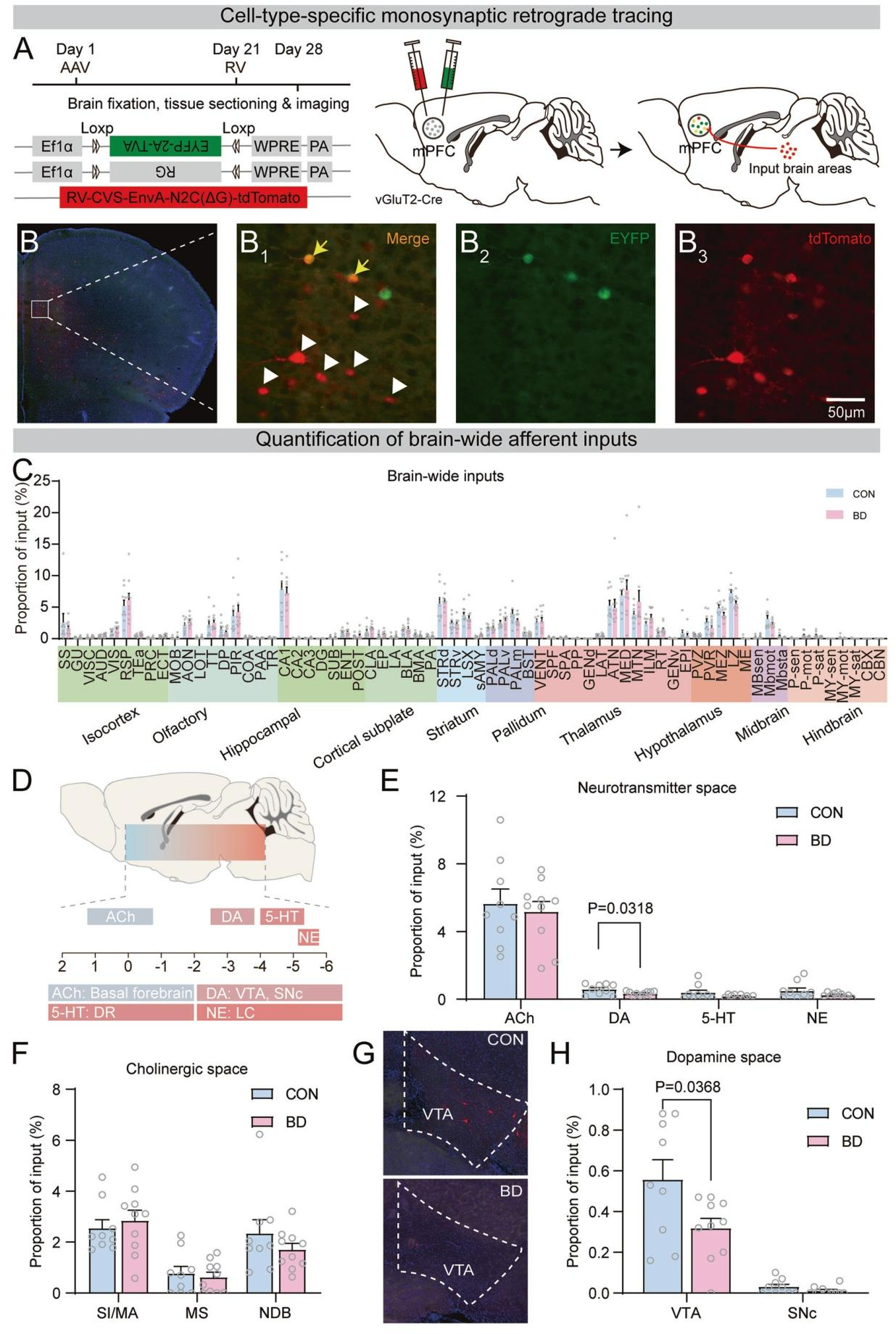
图3 mPFC神经元的多巴胺系统连接减少
鉴于BLA是与双相情感障碍(BD)高度相关的脑区,且mPFC向杏仁核基底外侧核发出密集投射。为探究肠道微生物群移植对BD小鼠投射至BLA的mPFC谷氨酸能神经元神经连接的影响,采用病毒跨突触追踪策略。先向mPFC注射AAV helper混合载体(AAV-EF1α-DIO-EGFP-T2A-TVA和AAV-EF1α-DIO-G),3周后向BLA靶向注射狂犬病病毒(RV-CVS-EnvA-N2C(ΔG)-tdTomato。),经1周表达后对全脑单突触传入进行成像(图4A)。验证结果显示,起始细胞集中于mPFC前边缘-边缘下复合体,约70%集中在Ⅱ/Ⅲ层,两组起始细胞密度无差异(图4B)。全脑组织成像发现,BD组小鼠来自顶盖带(TT)和VTA的输入显著减少和缺失(图4C);进一步分析乙酰胆碱、多巴胺等神经递质系统及丘脑、海马等脑区的输入,显示两组小鼠的输入模式均无显著差异(图4D-H)。综上,BD小鼠投射至BLA的mPFC神经元传入输入重塑具有区域特异性,核心特征为TT和VTA输入缺失。
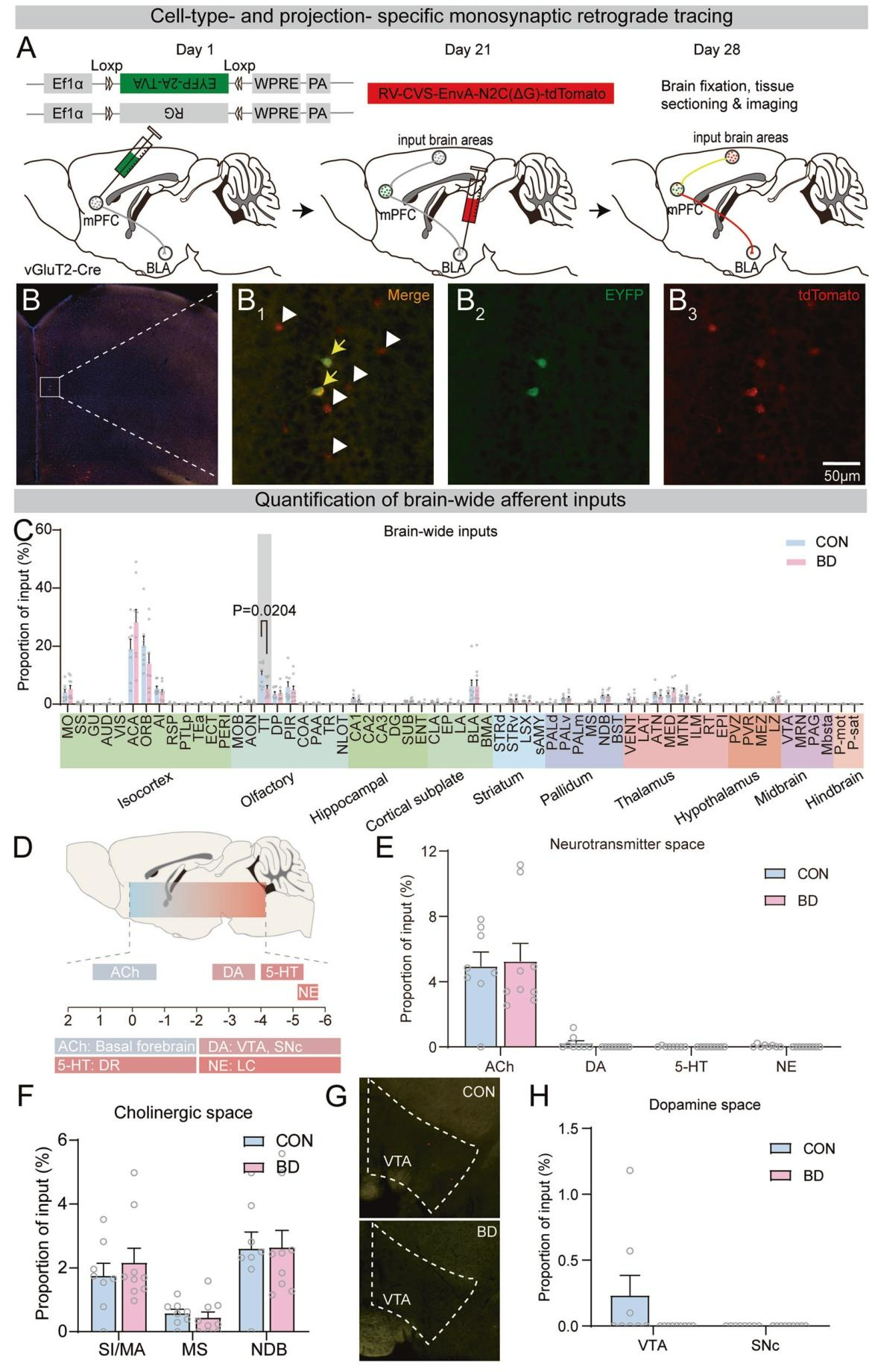
图4 投射至BLA的mPFC神经元的单突触连接
为明确BD小鼠mPFC与VTA连接结构缺陷的功能意义,结合BD患者前额叶-VTA连接改变与奖赏加工、快感缺失相关及VTA为多巴胺主要分泌脑区的背景。研究向小鼠mPFC注射表达多巴胺指示剂AAV-DA2m(图5A),表达一月后,通过光纤光度法结合尾夹刺激实时监测mPFC神经元的多巴胺反应(图5B-D)。结果显示,与对照组相比,BD小鼠mPFC在刺激下的多巴胺释放幅度和整体反应均显著降低(图5F-I)。这表明BD组小鼠mPFC神经元存在功能性多巴胺缺乏。
已证实BD组小鼠的mPFC神经元存在多巴胺结构和功能缺陷。为验证BD组小鼠VTA多巴胺能神经元向mPFC谷氨酸能神经元的投射变化,研究通过mPFC注射逆行示踪剂CTB追踪VTA投射神经元并免疫染色鉴定其多巴胺能属性,发现BD组投射至mPFC的VTA多巴胺能神经元数量呈下降趋势(图5J-L);进一步通过结合狂犬病毒跨单突触追踪与TH免疫染色,研究直接观察到与mPFC谷氨酸能神经元形成突触连接的VTA多巴胺能神经元数量在BD小鼠中显著减少(图5M-O)这些结果从细胞连接层面证实,BD小鼠存在VTA多巴胺能神经元向mPFC谷氨酸能神经元的特异性突触投射损伤,为前述结构与功能的多巴胺异常提供了直接的解剖学证据。
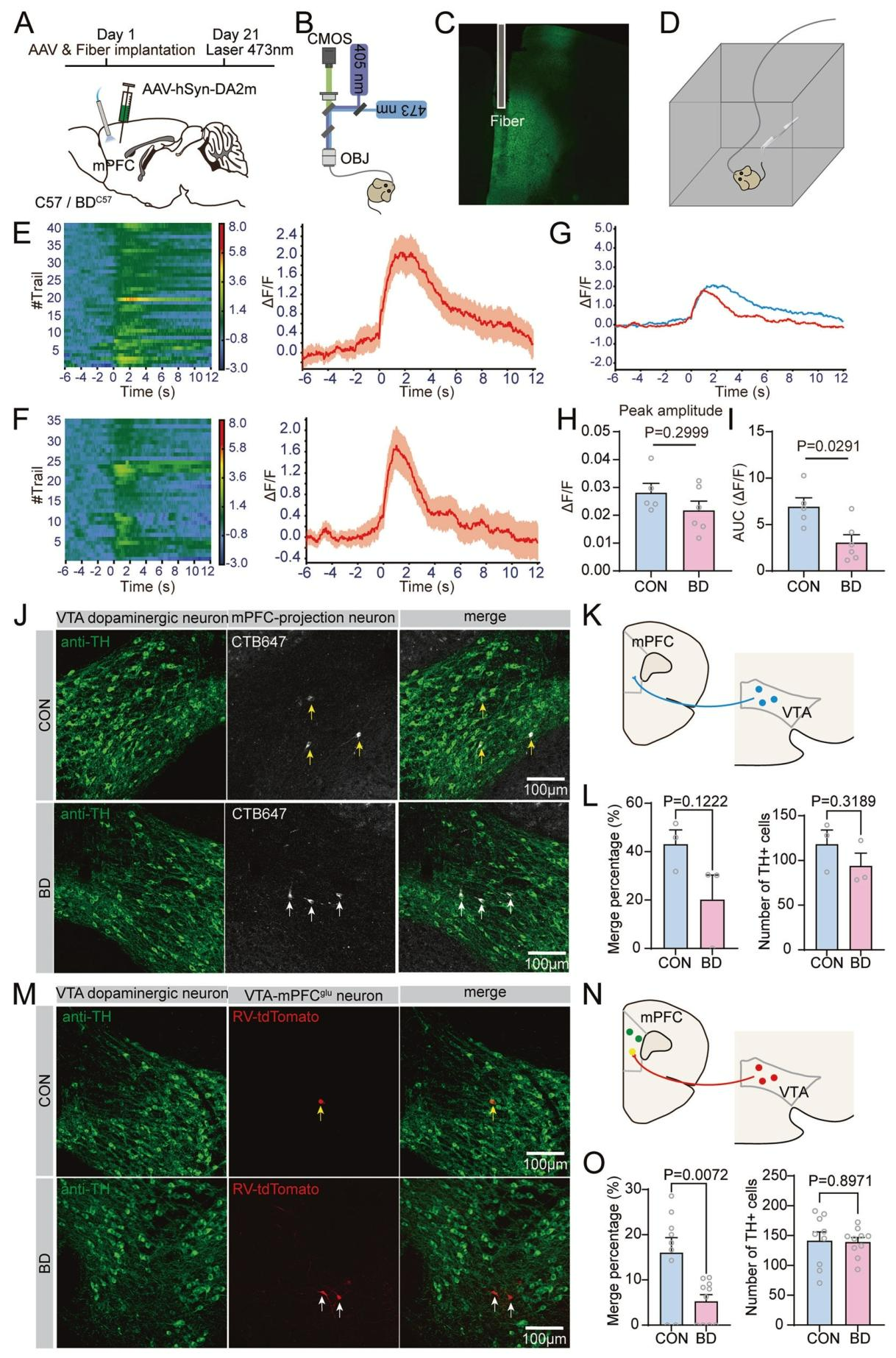
图5 投射至mPFC的VTA多巴胺能神经元的结构和功能性多巴胺缺乏
本研究通过将BD患者的肠道菌群移植给小鼠,成功构建出具有抑郁样行为的小鼠模型。机制上,BD患者的肠道菌群通过肠‑脑轴特异性损害VTA‑mPFC多巴胺能通路的结构连接与功能传递,导致mPFC突触可塑性降低,进而诱发抑郁样行为。该发现为理解双相情感障碍的病理机制提供了新的微生物‑神经环路视角,并提示肠道菌群或可作为该疾病的潜在干预靶点。
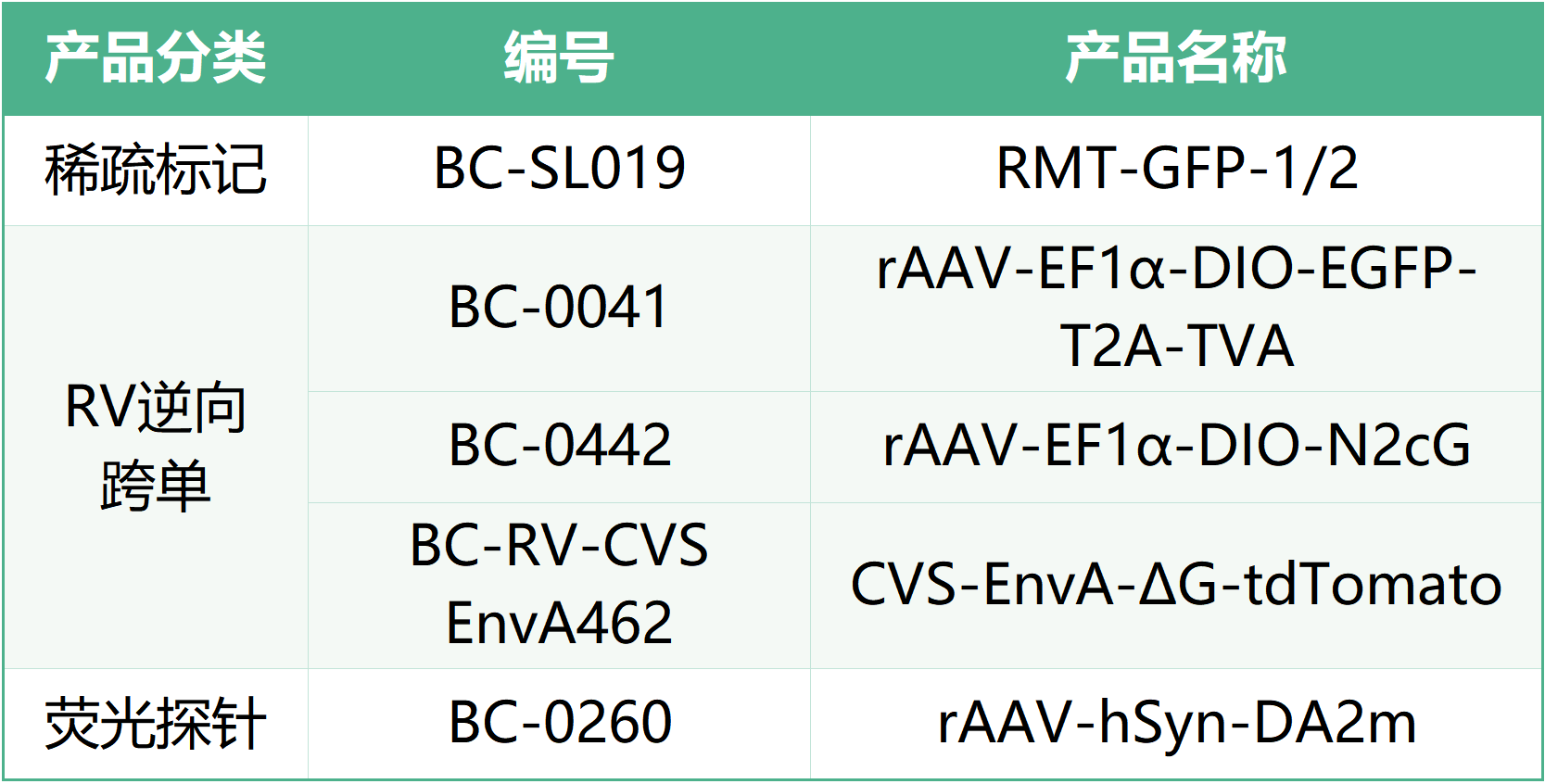
本文使用的工具病毒布林凯斯均可提供: