脂肪凭借独特适口性和高能量密度,成为健康饮食管理的重大挑战,且脂肪偏好与肥胖的关联性强于甜食偏好。现有食欲抑制药物会降低进食愉悦感,还可能引发心理问题,而针对外周脂肪酸受体的干预又会影响脂肪代谢和胰岛素敏感性。同时,糖和脂肪的外周感知机制已明确,但大脑中调控两者偏好的独立机制尚不清晰。

2025年11月26日,浙江中医药大学陈忠教授与郑艳榕研究员团队在Neuron上发表了题为“Biased histamine signaling selectively gates fat preference”的研究,揭示了丘脑室旁核(PVT)中存在分别介导高脂饮食(HFD)和高糖饮食(HSD)摄入的两个不同神经元亚群,其中组胺H3受体(H₃R)是HFD反应性神经元(PVTHFD)的标志性分子,该受体通过G12/13偏向性信号通路调控PVTHFD神经元的兴奋性,且结节乳头核组胺能神经元→PVTHFD神经环路可响应口腔感官线索调节脂肪摄入,此外还发现PVTHFD神经元对模拟脂肪质地的食物有梯度激活反应。
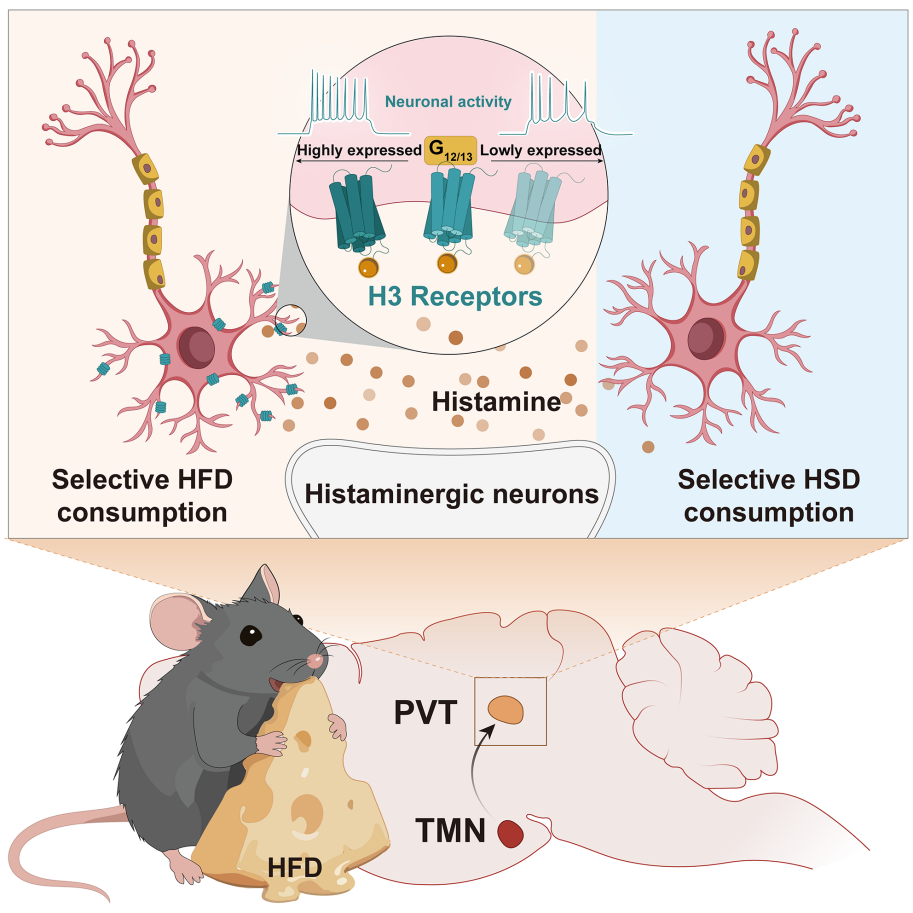
✦ +
+
为了探究独立调控脂肪和甜食摄入的神经环路,研究人员将FosTRAP小鼠与Cre依赖型tdTomato报告基因小鼠杂交,在活性依赖型Fos启动子调控下标记高脂饮食敏感神经元。注射4-羟基他莫昔芬(4-OHT)后,小鼠自由进食高脂饮食诱导tdTomato表达;两周后复喂高脂或高糖饮食,通过c-Fos免疫荧光标记响应神经元(图1A),并量化tdTomato与c-Fos双阳性神经元的占比。复喂高脂饮食时,多数脑区中高脂饮食标记神经元与c-Fos高度共定位,证实其能反映高脂饮食响应神经元(图1B)。更换为高糖饮食后发现,丘脑室旁核(PVT)和孤束核(NTS)中,高脂与高糖饮食响应神经元群显著分离,这与PVT谷氨酸能神经元异质性及NTS区分糖脂刺激的已知功能一致;其他脑区(LH、Arc、PVH、VTA)两类神经元存在明显重叠(图1B)。
研究人员通过光纤记录监测两类神经元的钙离子动态:向PVT共注射SARE-Cre(AAV2/9-E-SARE-ERT2-CreERT2-PEST)与GCaMP6s病毒并植入光纤套管(图1C),发现PVTHFD神经元仅在进食高脂饮食时钙离子信号增强,PVTHSD神经元仅在进食高糖饮食时信号升高(图1D-1G)。此外,CaMKIIα启动子驱动的钙离子传感器实验,进一步证实PVT谷氨酸能神经元可被两类饮食激活。综上所述,丘脑室旁核中存在两个不同神经元亚群,分别对高脂饮食和高糖饮食产生特异性响应。
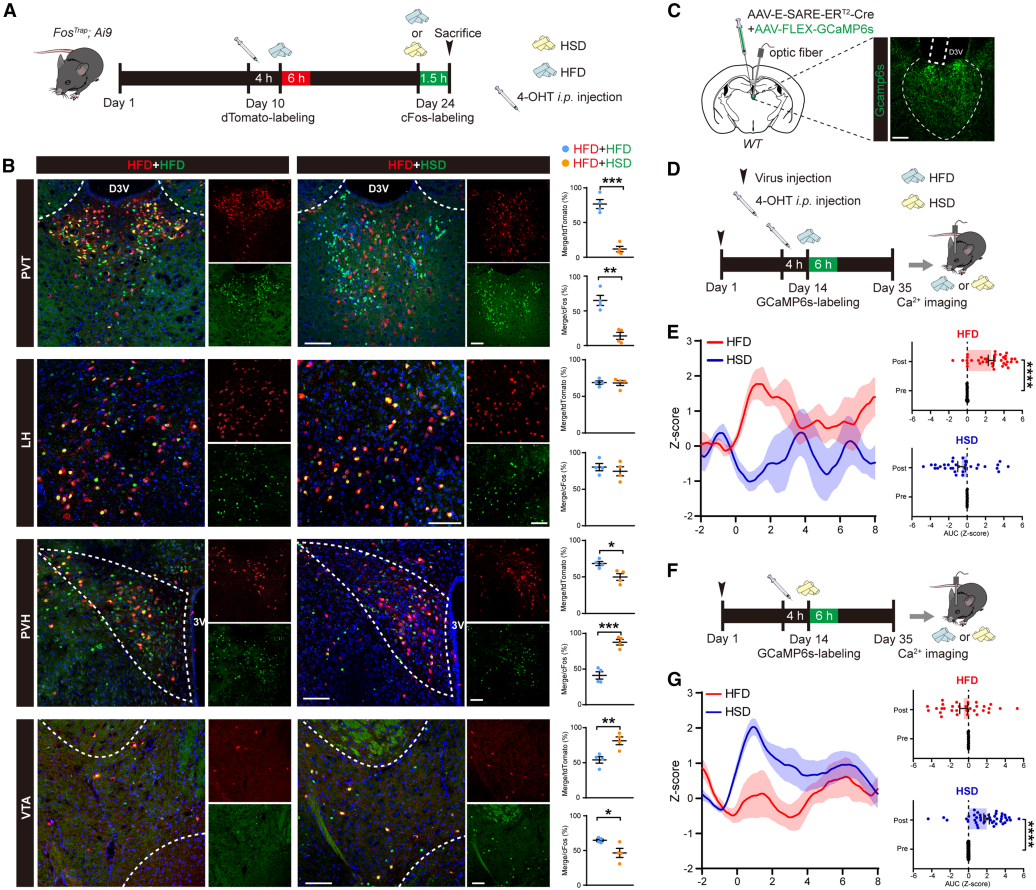
图1 PVT中的两个不同亚群分别对HFD和HSD摄入产生反应
✦ +
+
PVTHSD与PVTHFD神经元对进食的快速响应,提示其具有独特功能。研究人员通过E-SARE启动子调控的设计性药物遗传学受体(DREADD)标记目标神经元亚群后,进行化学遗传学调控(图2A)。神经元标记完成后,复喂HFD和HSD前,向小鼠腹腔注射CNO。结果显示,激活PVTHFD神经元可特异性抑制HFD摄入,对HSD无显著影响(图2B-2D);激活PVTHSD神经元则显著减少HSD摄入,不影响HFD(图2C-2D)。同理,抑制PVTHFD神经元会增加HFD摄入,抑制PVTHSD神经元则选择性增加HSD摄入(图2E-2G)。此外,激活所有PVT谷氨酸能神经元会同时抑制两种饮食摄入,抑制则促进两者摄入。
为了验证两类神经元功能分离特性,研究人员用光纤记录监测小鼠进食类脂肪/类甜食时的神经元活性。将普通饲料粉末与不同浓度黄原胶(模拟脂肪质地的食品添加剂)混合,制备类脂肪质地食物(图2H)。结果显示,随黄原胶浓度升高,PVTHFD神经元激活水平呈梯度增强(图2I);而PVTHFD神经元进食普通饲料或含非营养性甜味剂糖精的饲料时,无显著激活。相反,PVTHSD神经元对纯类脂肪质地食物无响应,仅被添加糖精和黄原胶的甜味类脂肪食物激活。功能上,抑制PVTHFD神经元会增加类脂肪质地食物摄入(图2J),但不影响甜味饲料摄入(图2K)。综上,进一步证实PVTHFD神经元可特异性调控脂肪摄入。
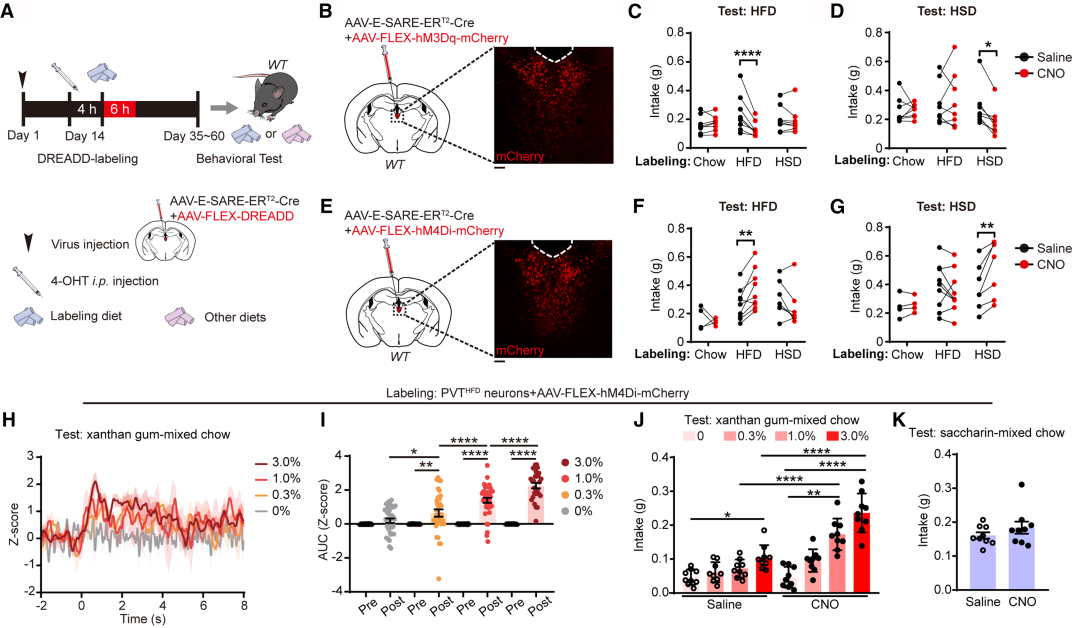
图2 PVTHFD神经元特异性调节脂肪消耗
✦ +
+
鉴于选择性脂肪摄入调控机制尚不明确,研究人员聚焦PVTHFD神经元的功能调控因子。通过神经元活性依赖标记与核糖体亲和纯化技术分离PVTHSD及PVTHFD神经元的mRNA,经单细胞测序(图3A-3B)分析差异表达基因,重点筛选膜相关分子、神经递质相关基因及具药物开发潜力的基因。结果显示,组胺H3受体(H3R,编码基因Hrh3)为PVTHFD神经元高表达的核心候选分子(图3C)。原位杂交实验证实,注射ESARE-Cre病毒的小鼠(图3D-3E)与FosTRAP小鼠(图3F-G)中,PVTHFD神经元的Hrh3表达均显著高于PVTHSD神经元;而其他组胺受体(图3C)及多巴胺受体D2(Drd2)在两类神经元中表达无差异(图3H)。逆行跨单突触示踪,证实组胺能神经元与PVTHFD神经元存在直接相互作用。已有研究表明,三叉神经中脑核(Me5)是组胺能神经元的上游输入源,负责处理口腔本体感觉与机械感觉信号,这与PVTHFD神经元对脂肪食物质地的响应特性契合。利用病毒工作逆行示踪并调控投射至PVT的组胺能神经元(结节乳头核TMN)上游输入。结果显示,示踪的Me5神经元与Me5分子标志物Isl1高度共定位;化学遗传学抑制这些神经元可特异性增加HFD及类脂肪质地食物摄入,对HSD和甜味饲料无显著影响。综上,组胺能输入在PVTHFD神经元的功能调控中起关键作用。
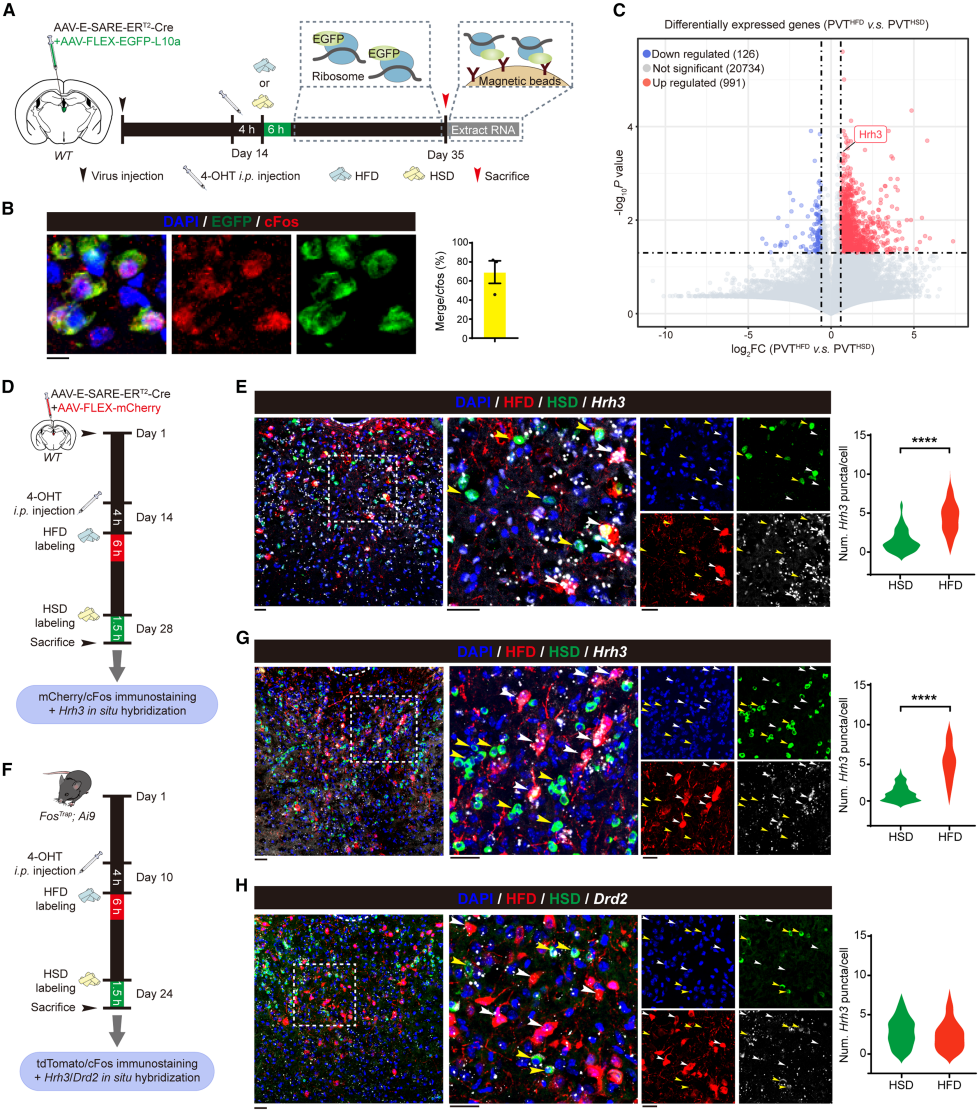
图3 组胺H3受体是PVTHFD神经元的分子标记
✦ +
+
基于明确的神经结构连接,研究人员探究PVT中H3R的功能。向Hrh3^fl/fl小鼠PVT注射AAV2/9-CaMKIIα-EGFP-P2A-Cre,实现PVT谷氨酸能神经元中H3R的非选择性敲除(图4A)。与H3R在PVTHFD神经元的偏向性表达一致,该敲除可选择性增加HFD摄入与偏好度,对HSD无影响(图4B-4D),且该效应在雌雄小鼠中均存在。随后,向Hrh3^fl/fl小鼠PVT注射SARE-Cre与AAV2/9-CAG-FLEX-mCherry病毒混合物(图3E),选择性敲除PVTHFD或PVTHSD神经元中的H3R。结果显示,敲除PVTHFD神经元的H3R可选择性增加HFD摄入与偏好(图4F-4H);敲除PVTHSD神经元的H3R对各类食物摄入无影响(图4I-4K)。
研究人员进一步探究H3R过表达的影响(图4L),在PVT谷氨酸能神经元中过表达H3R,会同时减少HFD和HSD摄入(图4M),可能因H3R在两类神经元中均强制表达;仅在PVTHFD神经元中过表达H3R,可特异性减少HFD摄入(图4N);在PVTHSD神经元中强制表达H3R,仅影响HSD摄入(图4O)。表明正常情况下PVTHSD神经元内源性H3R表达低,限制其功能调控,强制过表达可改变其活性。为了验证结果,向HDC-CreERT2小鼠TMN注射AAV2/9-CAG-FLEX-oChIEF-mCherry病毒,并在PVT植入光纤套管(图4P),光遗传学刺激PVT中的组胺能神经末梢。结果显示,该刺激可选择性减少HFD摄入,与PVTHFD神经元中H3R过表达效果一致(图4R-4T)。此外,局部敲除PVT中组胺H1受体(H1R)对HFD和HSD摄入均无影响。综上,PVT中的H3受体可选择性调控脂肪摄入,且在PVTHFD与PVTHSD神经元中发挥不同作用。
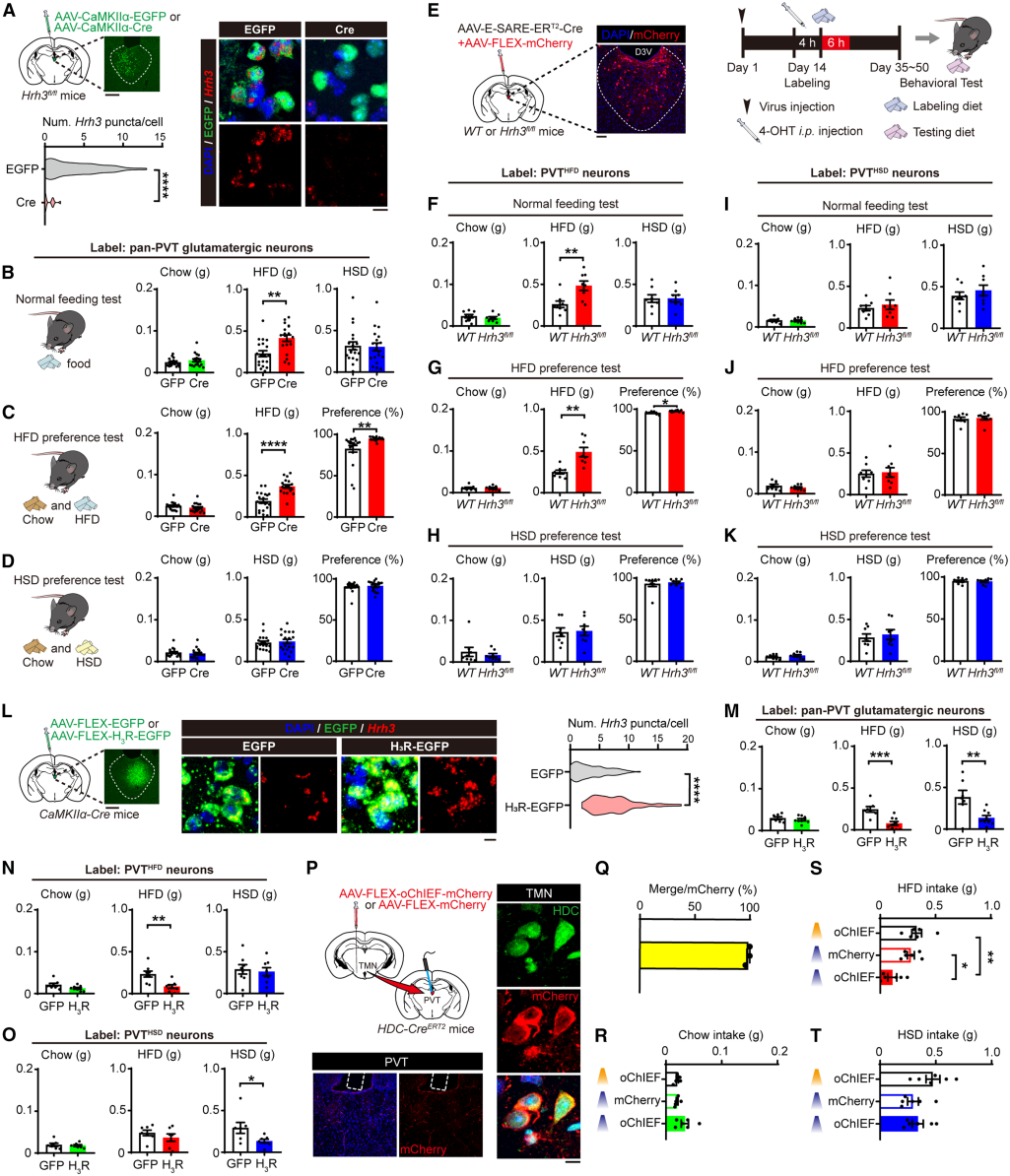
图4 PVT中的H3Rs选择性调控膳食脂肪摄入
✦ +
+
鉴于PVTHSD神经元中强制表达H3R会改变其功能,研究人员探究H3R对PVT谷氨酸能神经元兴奋性的影响。体外电生理实验显示,PVTHFD神经元兴奋性略高于PVTHSD神经元。敲除H3R后,PVTHFD神经元放电频率降低(兴奋性下降),静息膜电位与动作电位幅度无变化(图5A-5C);而PVTHSD神经元放电频率不受影响(图5D-5F)。过表达H3R则可增加PVTHFD神经元放电频率,增强其兴奋性(图5G-5I)。
已知H3R除激活Gi通路外,还可启动多种下游信号通路。研究人员通过纳米荧光素二元技术(NanoBiT)和生物发光共振能量转移(BRET)实验,鉴定出两种人H3R剪接变体:H3R339和H3R365。这两种变体均无法逆转PVTHFD神经元中H3R缺失导致的HFD过量摄入,而全长H3R可有效抑制该现象(图5J-5K),提示G12/13通路可能参与调控。在电生理实验中进一步应用Gq通路抑制剂FR300935和G12/13通路抑制剂Rhosin,并通过蛋白质印迹法验证其对下游蛋白磷酸化的抑制作用(图5L-5M)。结果显示,Rhosin(而非FR300935)可逆转H3R过表达引起的PVTHFD神经元兴奋性升高。此外,在光遗传学激活PVT中组胺能神经末梢介导的HFD摄入抑制实验中,Rhosin可消除该抑制效应,而FR300935与β-抑制蛋白通路抑制剂Barbadin均无此作用(图5N-5O)。综上所述,H3受体通过偏向性G12/13信号调控PVTHFD神经元活性,为其调控脂肪摄入的作用提供了机制解释。
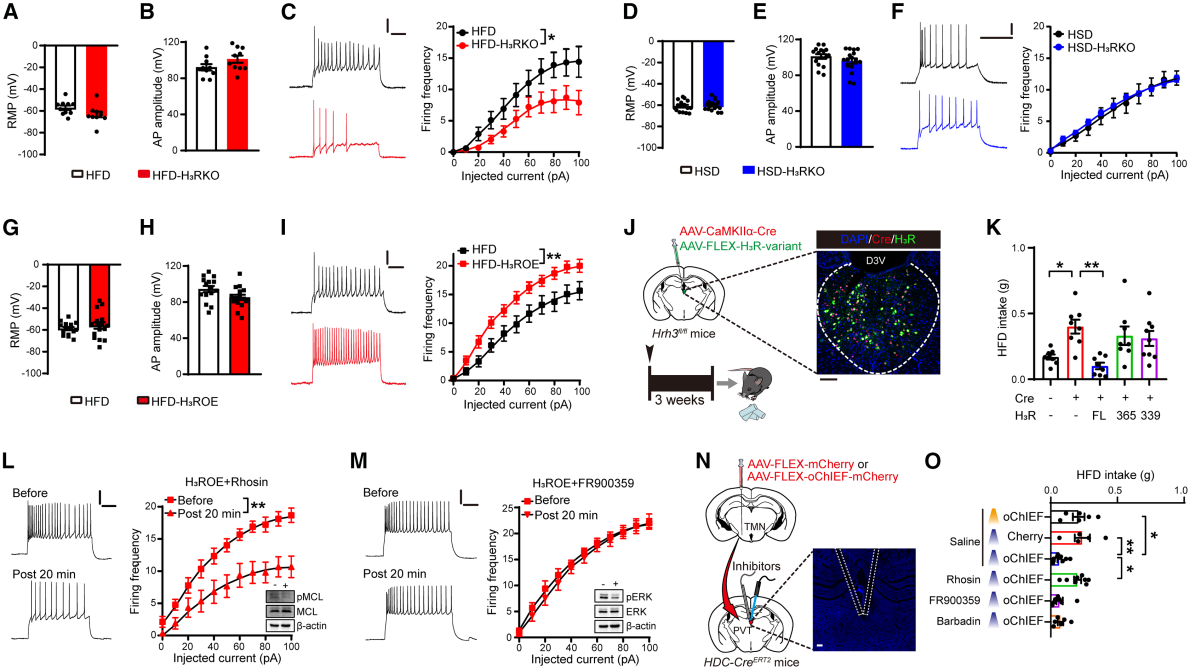
图5 H3R通过偏向性G12/13信号调控PVTHFD神经元活性
本文首次明确了PVT在调控脂肪偏好中的核心作用,揭示了糖和脂肪偏好存在独立的中枢神经调控机制,填补了大脑对不同高热量食物选择性偏好调控的研究空白。确定H₃R-G12/13轴为精准控制脂肪摄入的潜在靶点,为开发副作用小、针对性强的抗肥胖药物提供了新方向,有望解决现有肥胖干预手段的局限性。
本文使用的工具病毒布林凯斯均可提供:
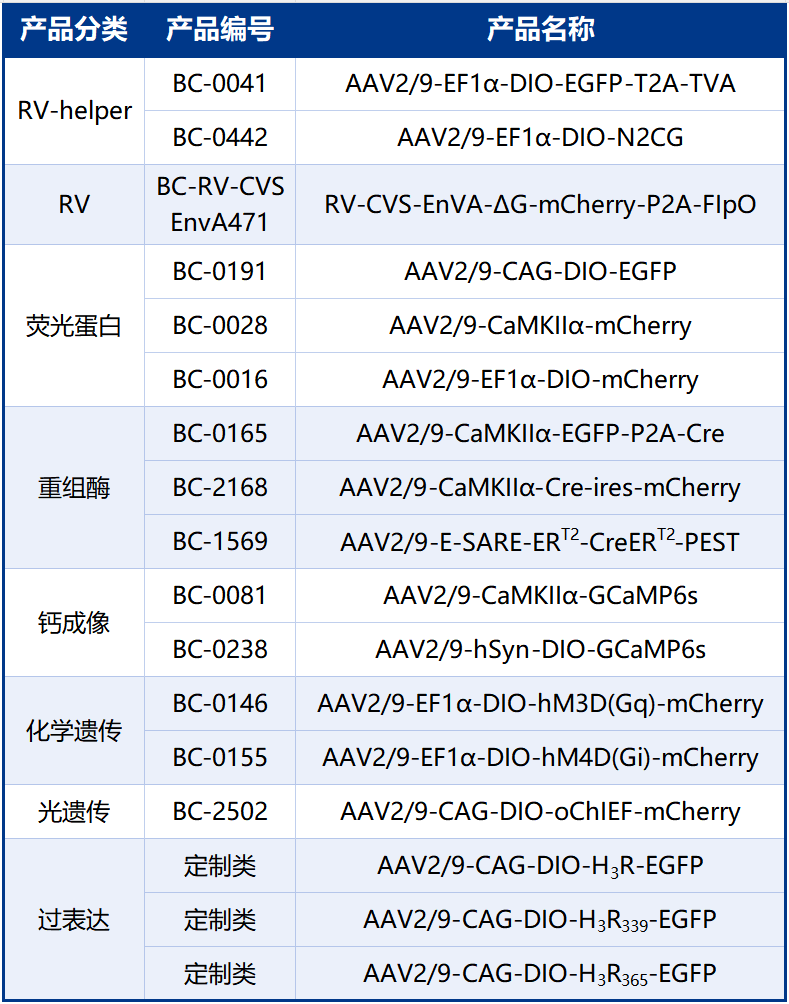
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。