全球约200万人受影响,以骨量减少、骨微结构破坏为特征,脆性骨折风险升高,传统与衰老、绝经相关,但慢性压力导致早发性骨丢失的趋势日益显著。慢性压力可通过交感神经系统(SNS)影响外周器官,但将压力信号转化为骨骼功能障碍的中枢神经环路尚未明确。
2025年12月5日,空军军医大学胡学昱和董玉琳共同通讯在Science Advances上发表题为“A central CeA-LC-PVH circuit mediates stress-induced osteopenia via skeletal sympathetic nerves in male mice”相关研究,揭示了慢性社交挫败压力(CSDS)诱导雄性小鼠骨丢失的核心机制,通过激活CeACRH+-LCNE+-PVHCRH+神经通路,引发CeACRH+神经元向LCNE+神经元的CRH释放增强、GABA能传递抑制的双向失衡,经交感神经传导至骨骼,导致破骨细胞数量增加、骨微结构破坏;而靶向抑制该通路、恢复CRH/GABA平衡或阻断交感神经激活,可有效缓解压力相关性骨质疏松。
为了探究慢性压力对骨代谢的病理生理影响,建立CSDS模型模拟人类慢性社会心理压力(图1A)。小鼠经10天CSDS暴露后,行为学评估显示其出现明显社交回避,社交互动区域活动时间占比显著低于对照组(图1B-D)。干预期间体重持续下降(图1E),去甲肾上腺素(NE)及血清皮质酮水平显著升高(图1F-G)。抗酒石酸酸性磷酸酶染色显示,CSDS小鼠股骨破骨细胞数量(N.OC/BS)显著增加(图1H-I)。显微计算机断层扫描(micro-CT)定量分析表明,小鼠股骨松质骨与皮质骨均出现严重骨结构损伤(图1J-K)。松质骨三维微观结构分析显示,CSDS显著降低骨矿物质密度(g/cm³)、松质骨体积分数(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁数量(Tb.N)及连接密度(Conn.Dn,1/mm³),同时增加骨小梁间距(Tb.Sp)(图1L-Q)。此外,皮质骨定量分析显示,CSDS小鼠的皮质骨厚度(Ct.Th)、皮质骨面积(B.Ar)及皮质骨面积占比(BA/TA)均较对照组显著降低(图1R-T)。
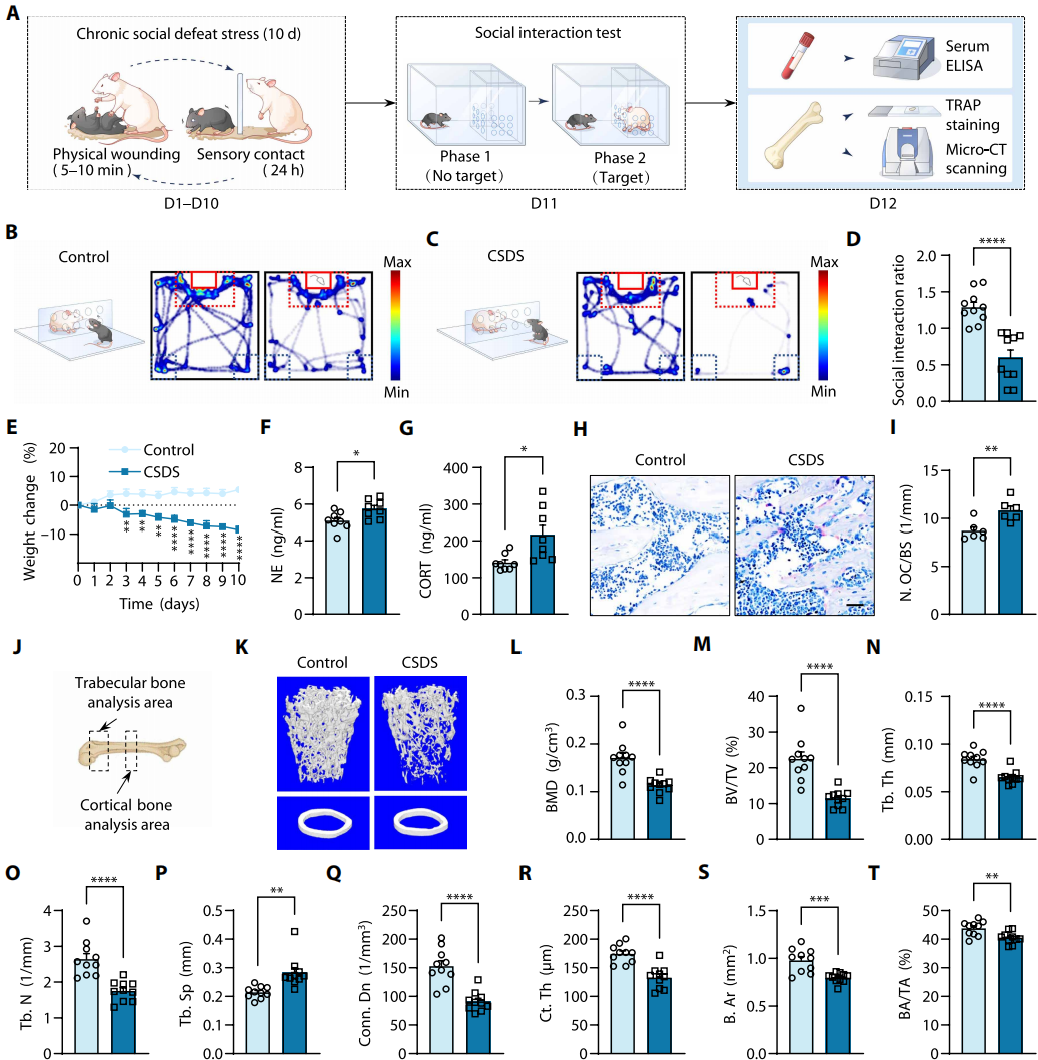
图1 CSDS诱导的雄性小鼠骨质疏松症
尽管流行病学和临床前研究已证实骨质疏松症与交感神经过度激活相关,但骨内去甲肾上腺素能动态的实时监测技术一直受限。采用基因编码G蛋白偶联受体(GPCR)激活型NE传感器(LV-CMV-GRABNE2h)监测骨内交感神经活性(图2A-B)。结果显示,CSDS小鼠骨内交感神经自发活性显著高于对照组,慢病毒(LV-CMV-EGFP)对照组几乎无荧光信号(图2C-D)。施加伤害性刺激后,CSDS小鼠骨内其交感神经活性更高(图2E-I)。为了验证交感神经过度激活对CSDS小鼠骨量的负面影响,每隔一天腹腔注射6-OHDA进行化学交感神经切除(图2J)。TH免疫标记三维成像证实,6-OHDA处理组TH⁺神经纤维几乎完全消融。micro-CT分析表明,6-OHDA处理可预防CSDS诱导的骨损伤,维持松质骨微观结构、皮质骨厚度及骨体积(图2K-T)。此外,区域交感神经切除小鼠对CSDS诱导的骨丢失具有抵抗力。综上,CSDS通过过度激活交感神经系统(SNS)破坏骨代谢平衡。
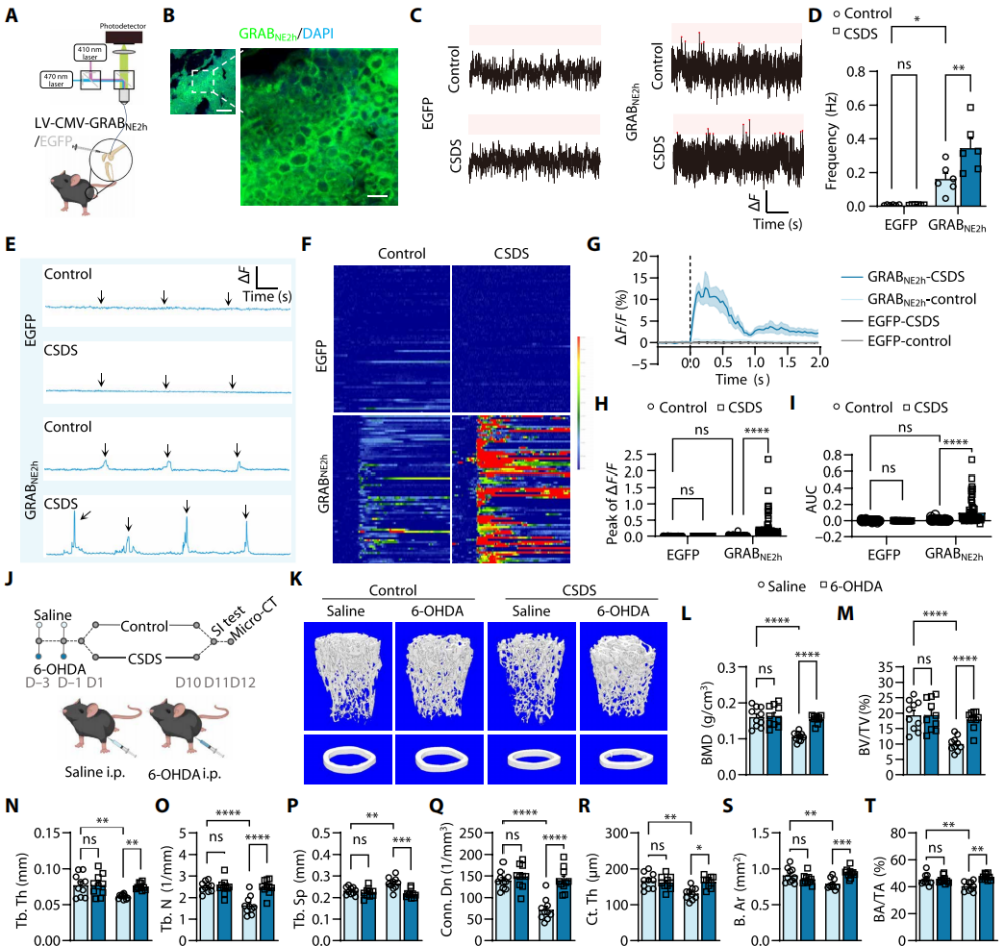
图2 CSDS增强交感神经活性导致骨质流失
为了阐明蓝斑(LC)-交感神经-骨骼轴作用机制,向6-OHDA处理组及生理盐水对照组小鼠股骨骨髓腔注射PRV-CMV-EGFP(图3A),6天后micro-CT证实PRV局限于骨髓腔内(图3B)。对照组双侧蓝斑出现大量EGFP⁺神经元,6-OHDA组几乎无阳性信号(图3C-E);免疫荧光显示PRV标记的LC细胞与TH阳性(TH-ir)神经元共定位,证实LC与骨骼的去甲肾上腺素能神经连接(图3F)。
为了探究选择性激活蓝斑去甲肾上腺素能(LCNE+)神经元对骨内交感神经兴奋性的影响,向双侧LC注射rAAV-DIO-ChR2-EGFP及rAAV-TH-CRE;同时向股骨骨髓腔注射LV-CMV-GRABNE2h(图3G-H)。经5/10/20Hz 473nm激光电生理验证病毒有效性后(图3I-J),发现470nm波长下GRABNE2h荧光信号频率显著升高(图3K-L)。为了明确激活LCNE+神经元对骨量的影响,采用化学遗传学方法:向双侧LC共注射rAAV-Ef1a-DIO-hM3D(Gq)与rAAV-TH-CRE(图3M-O)。病毒表达3周后,小鼠连续10天腹腔注射CNO或生理盐水,结果显示特异性激活LCᴺᴱ⁺神经元导致小鼠松质骨微观结构破坏、皮质骨厚度及股骨体积减少(图3P-Y)。上述结果表明,LCNE+神经元通过神经环路支配骨内交感神经,其特异性激活可引发小鼠骨量下降。
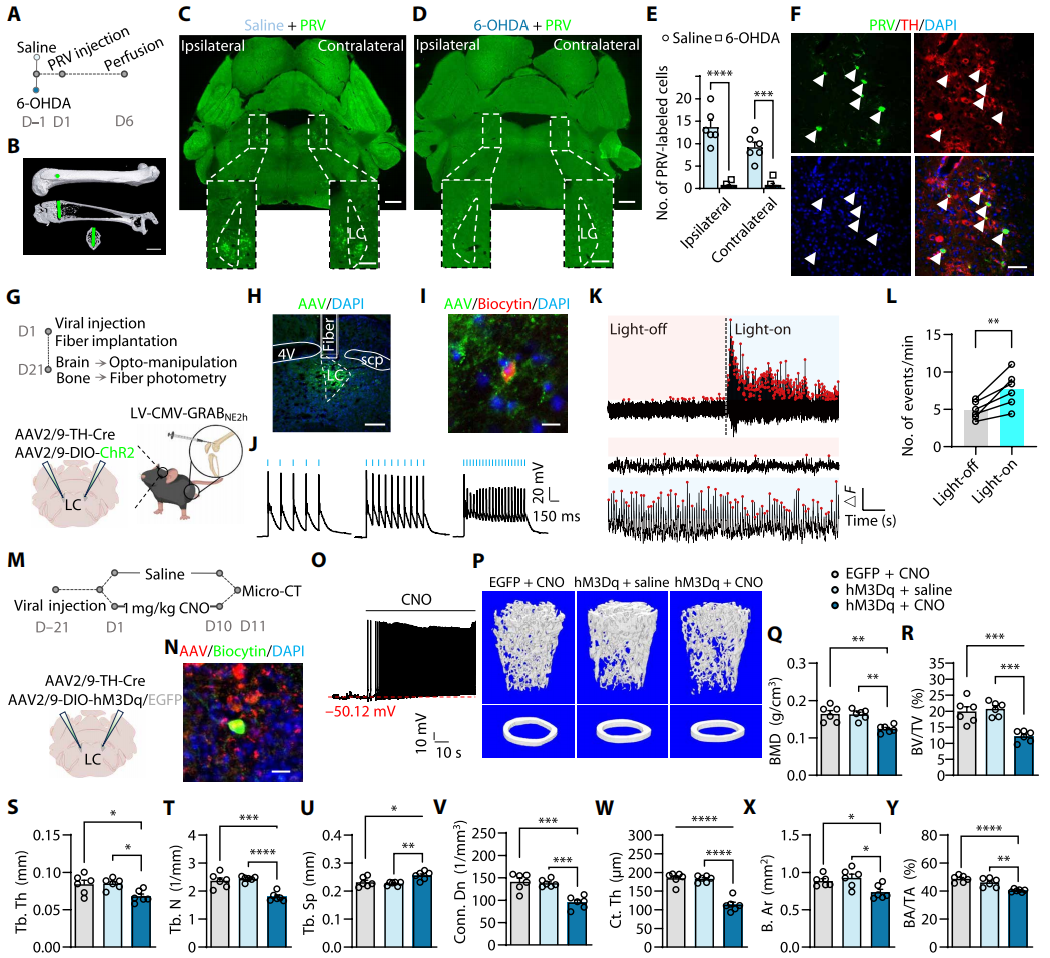
图3 LCNE+神经元激活引发交感神经过度激活导致骨质疏松症
为了在体探究压力暴露期间LCNE+神经元活性,向LC注射Cre依赖型rAAV-Ef1a-DIO-GCaMp6m与rAAV-TH-NLS-CRE病毒(图4A-C)。对CSDS组与对照组小鼠,在三种压力条件下记录:遭遇CD-1攻击性小鼠攻击、社交互动或疼痛夹尾刺激。结果显示,CSDS组小鼠在这些刺激下的群体钙信号显著强于对照组且钙瞬变显著增加(图4F-L),证实CSDS小鼠LCNE+神经元兴奋性升高。基于上述发现,推测特异性抑制该神经元可增加CSDS小鼠骨量。为了验证假设,向双侧LC注射rAAV-Ef1a-DIO-hM4D(Gi)与rAAV-TH-CRE病毒(图4M-O)。CSDS组小鼠连续10天遭遇攻击性小鼠前1小时,腹腔注射CNO抑制LCNE+神经元。micro-CT结果证实与对照组相比,特异性抑制LCNE+神经元可显著缓解CSDS小鼠骨丢失(图4P-Y)。综上,降低LCᴺᴱ⁺神经元兴奋性可缓解CSDS诱导的骨丢失。
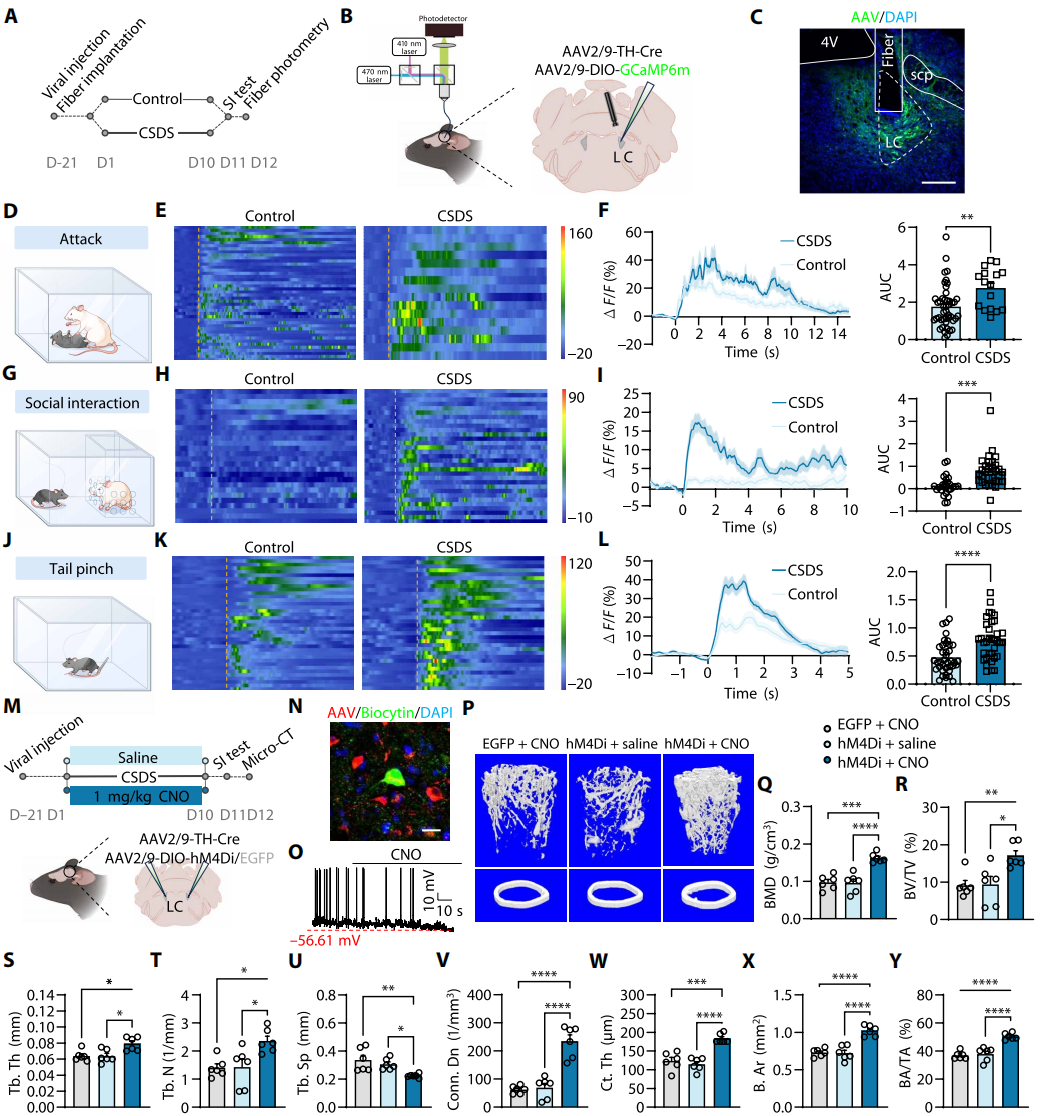
图4 CSDS诱导的LCNE+神经元过度活跃介导骨质流失
为了明确中央杏仁核CeACRH+-LCNE+神经环路是否支配骨骼,向LC注射逆行示踪剂CTB-555(图5A)。组织学结果显示CeA存在CTB标记神经元,且约80%与CRH共定位(图5B);向骨骼注射PRV-CMV-EGFP并向LC注射CTB-555后,CeA检测到PRV/CTB双标记细胞,证实该环路是“脑-骨”轴核心组成。探究慢性压力下环路活性,向CeA注射rAAV-Ef1a-DIO-GCaMp6m,向LC注射AAV2/R-CRH-Cre并植入光纤(图5C)。CSDS组小鼠在遭遇CD-1攻击性小鼠攻击、社交互动及夹尾刺激时,该环路钙活性显著强于对照组(图5D-L)。采用化学遗传学抑制,向双侧CeA注射rAAV-Ef1a-DIO-hM4D(Gi),向双侧LC注射AAV2/R-CRH-Cre(图5M)。CSDS组小鼠每次遭遇攻击前1小时腹腔注射CNO,micro-CT显示其松质骨微观结构改善,皮质骨厚度及体积增加(图5O-W)。综上,CeACRH+-LCNE+神经环路在慢性压力下加剧骨丢失。
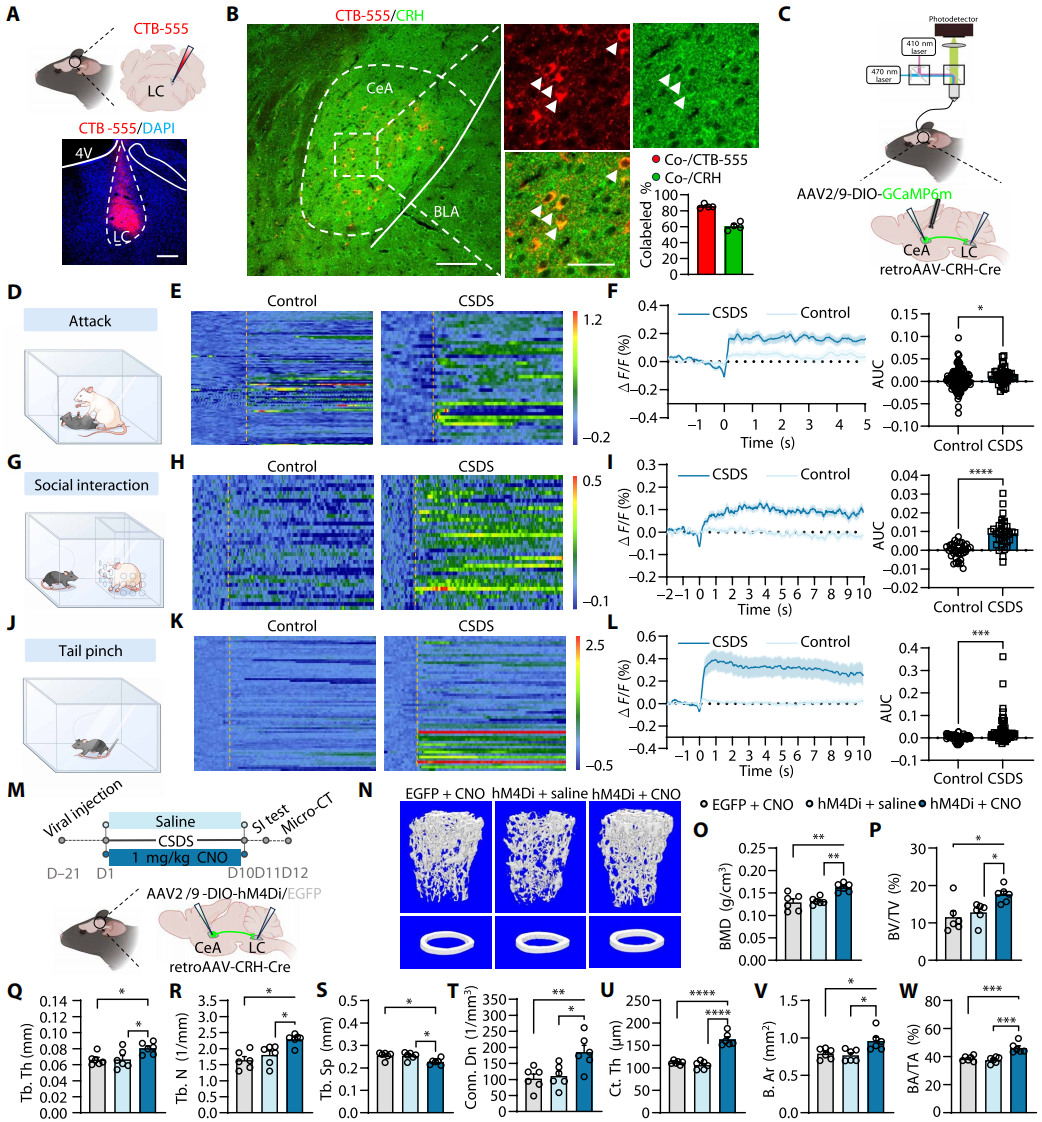
图5 化学遗传学抑制CeACRH+-LCNE+神经环路可减轻CSDS诱导的骨质流失
既往研究表明,CeACRH+γ-氨基丁酸能神经元释放的CRH和GABA在不同状态下存在差异,可导致心理或行为改变。通过AAV在CeACRH+突触表达mRuby,经免疫荧光染色分析CRH和GABA表达模式(图6A)。Manders共定位分析显示,CSDS组小鼠mRuby与CRH共定位显著增加,与GABA共定位显著减少(图6B-C),提示慢性压力导致环路共传递失衡,表现为CRH释放增强、GABA能信号减弱(图6D)。此外,在体光纤记录评估LC内CRH和GABA释放(图6E),结果显示CSDS组CRH荧光信号显著升高(图6F-G),而遭遇攻击时GABA信号相关指标显著降低(图6I),证实CSDS引发环路中CRH与GABA释放失衡。
为了探究CeACRH+投射对LCNE+神经元兴奋性的调控,在CeACRH+神经元表达ChR2并可视化LCNE+神经元(图6J)。在ACSF对照、CRHR1拮抗剂antalarmin、GABAₐ受体拮抗剂picrotoxin三种条件下,向记录神经元注射固定间隔双相电流(图6K)。结果显示,ACSF环境中蓝光刺激不改变锋电位数量;加入antalarmin后,蓝光刺激显著减少锋电位;加入picrotoxin后,光刺激显著增加锋电位(图6L-M),表明CeACRH+神经投射共传递CRH和GABA,其中GABA通过GABAₐ受体抑制LCNE+神经元兴奋性,CRH通过CRHR1发挥兴奋作用。在环路中特异性敲低CRH(图6N),结果证实CRH敲低可显著改善CSDS组小鼠松质骨微观结构,增加皮质骨厚度和体积(图6O-X),表明环路中CRH过度释放是压力诱导骨质疏松的关键驱动因素。用AAV病毒介导靶向vGAT的shRNA降低CeACRH+-LCNE+环路囊泡GABA水平,分析显示该组小鼠松质骨结构破坏、皮质骨厚度及骨体积降低,提示CeACRH+神经元向LCNE+神经元的GABA传递是维持生理骨稳态的必需条件。
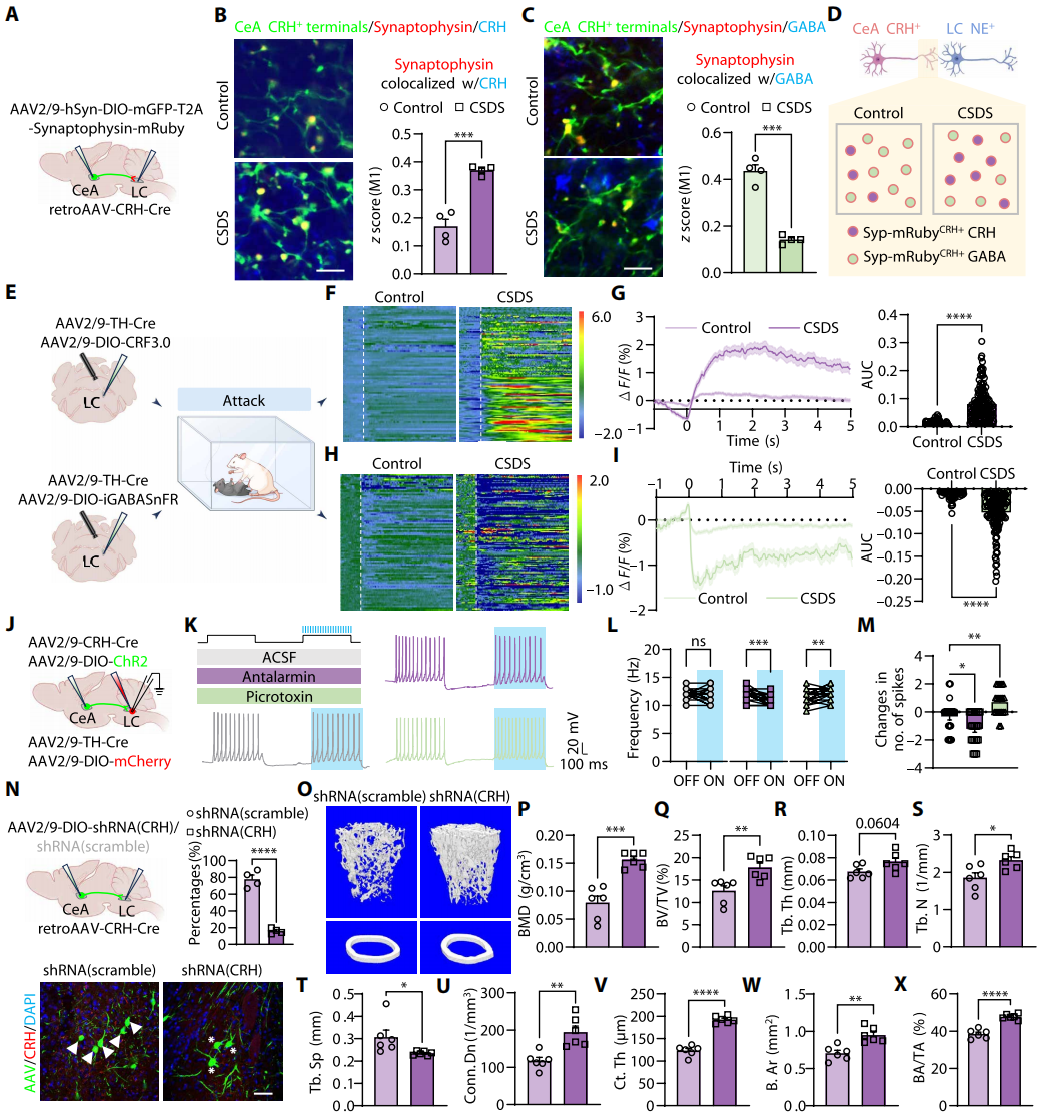
图6 CeA向LC释放CRH可导致CSDS诱导的骨质疏松症
为了明确CeACRH+-LCNE+神经环路的下游靶点,向CeA注射AAV2/1-hSyn-EGFP-Cre病毒同时向LC靶向注射AAV2/9-TH-DIO-EGFP病毒(图7A-B)。结果显示,CeACRH+-LCNE+环路发出的密集投射纤维主要终止于PVH后部(pPVH)(图7C)。通过股骨骨髓注射PRV-CMV-EGFP逆行示踪探究其骨支配情况,结果显示PRV标记细胞主要分布于pPVH,且与CRH共定位。采用顺行与逆行示踪结合策略绘制CeA-LC-PVH环路图谱(图7D-E),结果显示在PVH中观察到“起始细胞”(黄色,图7F),在LC中检测到多个RV标记的突触前神经元(红色);这些RV标记的LC神经元为TH阳性(蓝色),且与EGFP标记的CeACRH+突触终末紧密相邻(图7G)。随后,在CeA-LC-PVH通路中特异性表达ChR2,同时在骨内表达GRABNE2h传感器,蓝光激活该通路可显著增强交感神经活性,提示其参与骨的交感神经介导代谢调控。
为了实现对骨重塑动态的慢性调控与评估,采用无线光遗传学技术,在PVH植入光纤并植入皮下控制器(图7H-K)。全细胞膜片钳记录显示,5~10Hz光刺激可稳定诱导LCNE+神经元产生动作电位(图7L);持续激活10天(每天1小时)后,micro-CT分析显示,小鼠松质骨显著破坏、皮质骨变薄(图7M-V)。综上,CeACRH+-LCNE+环路通过PVH介导的交感神经调控骨代谢。
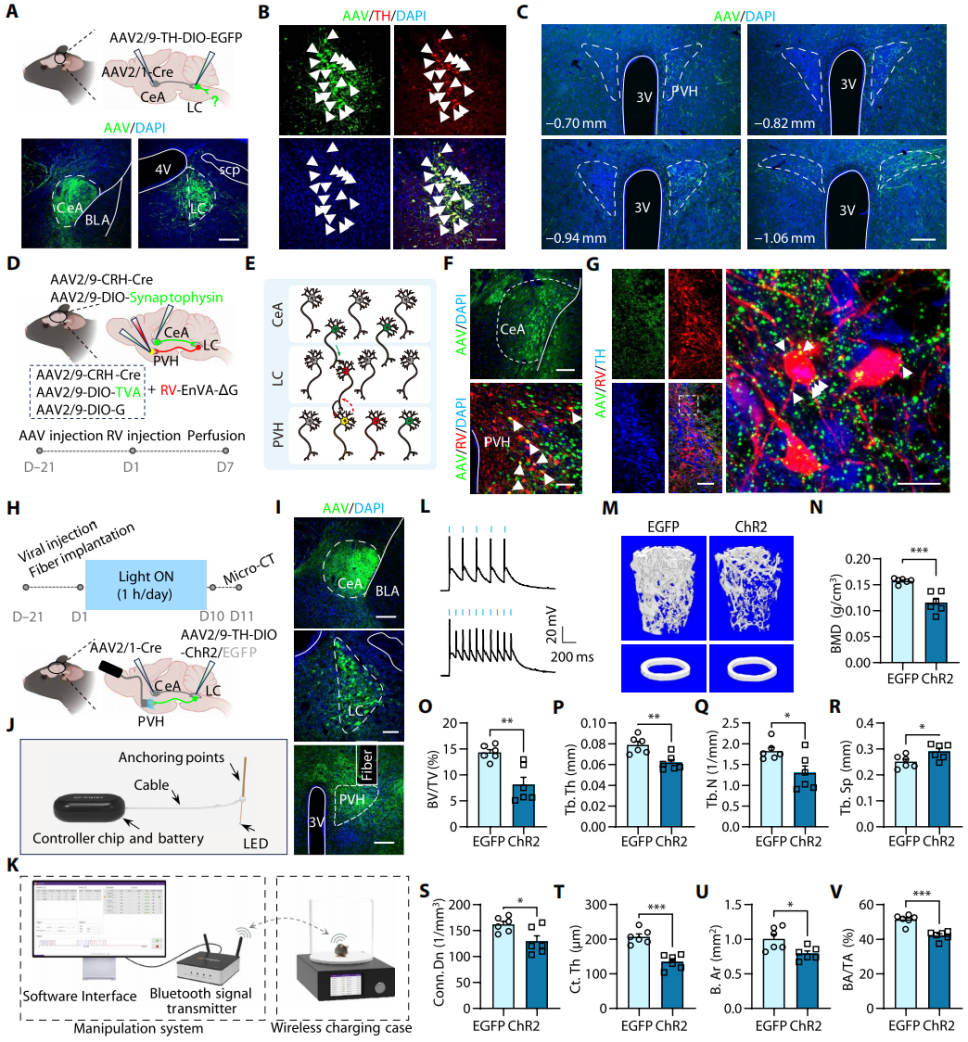
图7 PVH作为CeA-LC神经环路在骨代谢中的潜在下游靶点
慢性压力通过CeACRH+-LCNE+-PVHCRH+神经通路,经交感神经介导骨丢失,其关键机制是CeA-LC环路的CRH/GABA传递失衡;首次明确中枢神经环路调控压力性骨丢失的分子机制,确立 LCᴺᴱ⁺神经元为压力响应核心枢纽;为压力相关性骨质疏松提供神经通路导向的治疗策略。
本文使用的工具病毒布林凯斯均可提供:
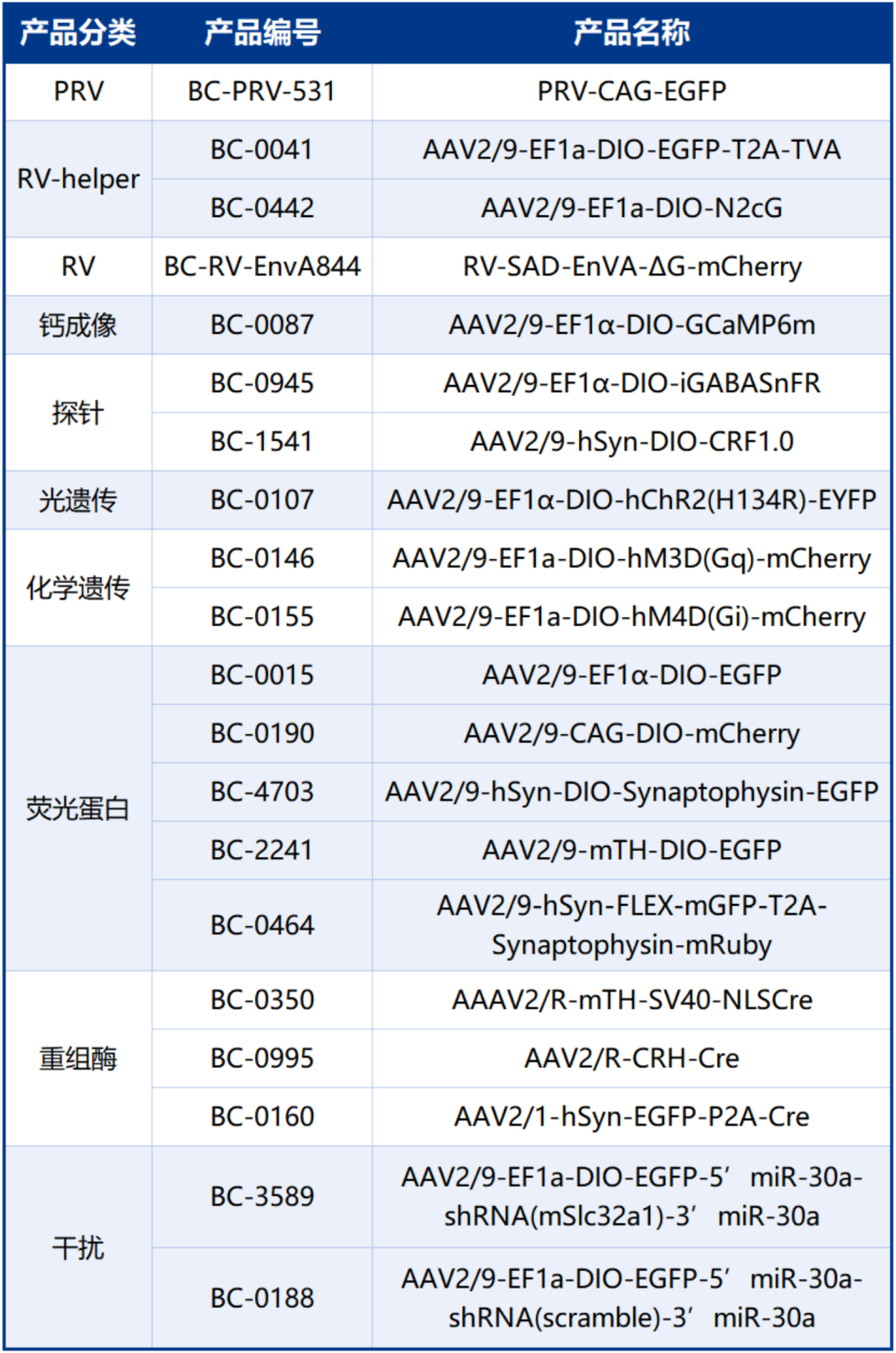
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。