记忆的奥秘始终引人探寻,社会记忆作为动物记住同种个体的关键能力,其缺陷与阿尔茨海默病、自闭症等多种脑部疾病密切相关,而介于短期记忆(秒至分钟级)和长期记忆(数小时以上)之间,那数十分钟至数小时的记忆维持机制,至今仍是尚未破解的谜题。
2025年11月24日,东南大学生命科学与技术学院刘安、谢维团队联合加拿大多伦多大学病童医院加正平团队在 Signal Transduction and Targeted Therapy 期刊上发表题为 Social memory maintenance relies on social interaction-induced proteolytic products of neuroligin 1 的研究论文。该文章表明腹侧海马体(vHPC)的社交活动激活α/γ-分泌酶并切割突触黏附蛋白NLG1,释放出可溶性胞内片段NLG1-CTD,通过其羧基端PDZ结合域(PBD)启动下游cofilin(肌动蛋白结合蛋白)磷酸化信号通路,进而增强树突棘结构,调节突触可塑性,对社会记忆的维持起到至关重要的作用。抑制该切割过程会损害记忆,而补充模拟该片段功能的Tat-PBD肽则能有效挽救记忆缺陷。该机制将细胞外社会信号、细胞内蛋白水解事件与突触结构功能重塑系统性地联系起来,为理解记忆的编码与维持提供了新视角。

为探究分泌酶对社交记忆的作用,研究在vHPC双侧植入套管,恢复一周后,分别注射生理盐水、α-分泌酶抑制剂(GI)和γ-分泌酶抑制剂MRK-560(MRK),一小时后进行三箱社交实验(图1k)。三组小鼠经10分钟适应期后均更多探索陌生小鼠S1,表现出正常的社交偏好(图1m);后续记忆形成测试中,仅GI注射组丧失了对新异小鼠(SFT)的探索偏好,提示α-分泌酶活性对社会记忆形成至关重要(图1n);形成测试后40分钟的记忆维持测试显示,生理盐水组仍能区分熟悉鼠(S1)与新异鼠(SFT’),而GI和MRK注射组均丧失此辨别能力,表明两组均存在社会记忆维持受损(图1o)。综上,社交刺激促进vHPC中α-和γ-分泌酶底物的水解,社会记忆形成依赖α-分泌酶活性,γ-分泌酶专门参与社会记忆维持,且该过程不依赖新蛋白质合成。
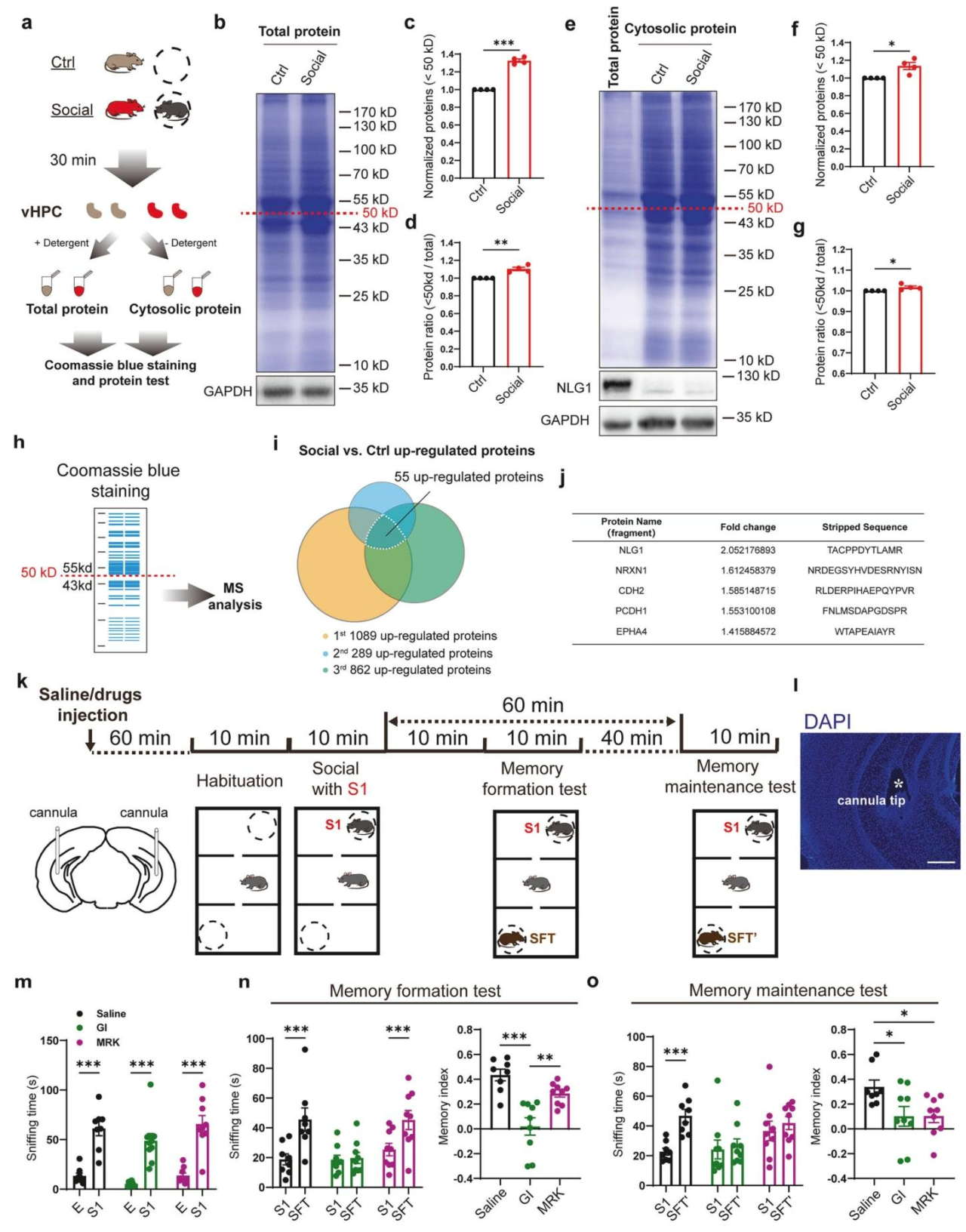
图1 社交互动促进腹侧海马体(vHPC)中的蛋白水解
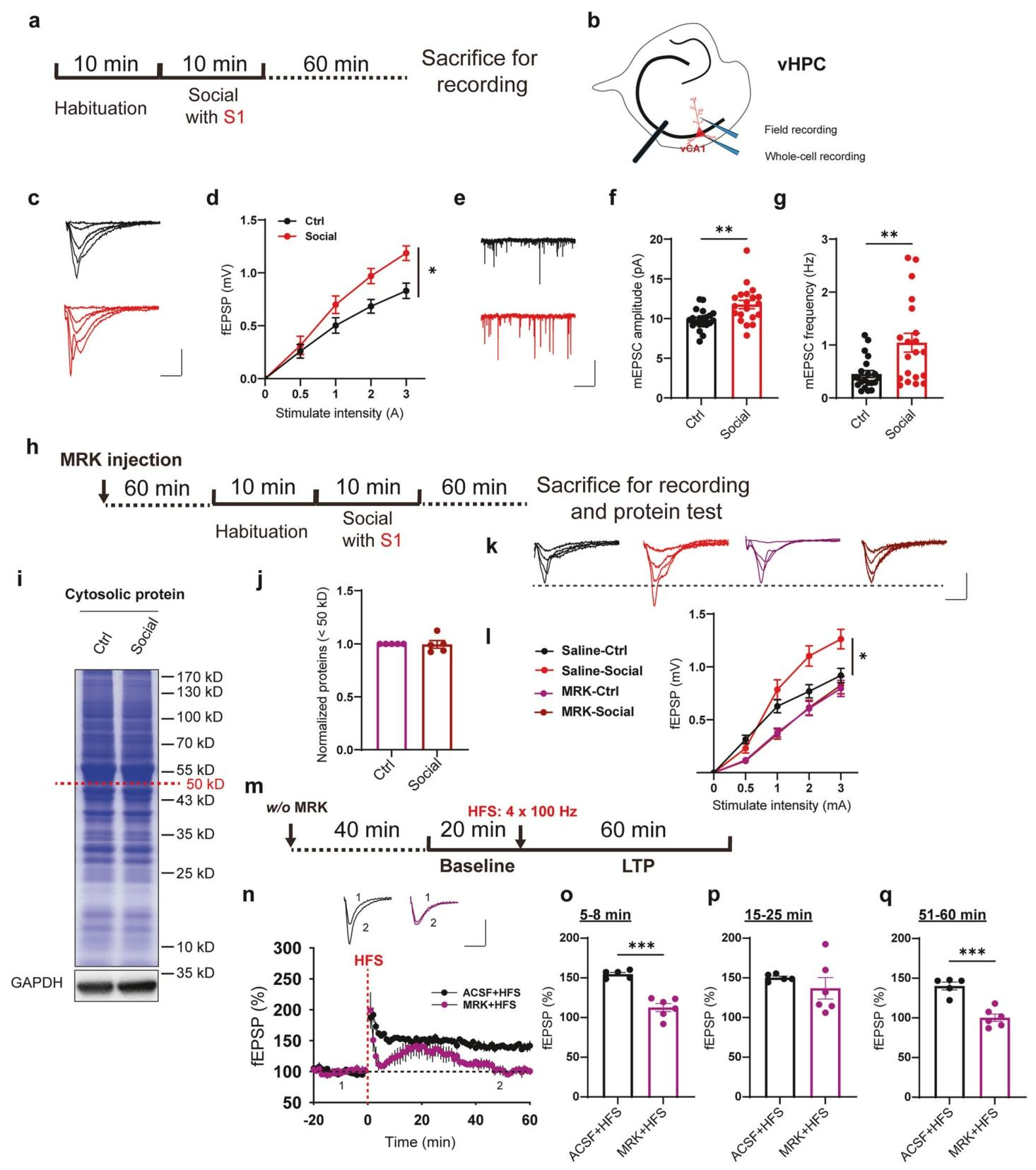
图2 MRK阻断社交诱导的突触传递增强
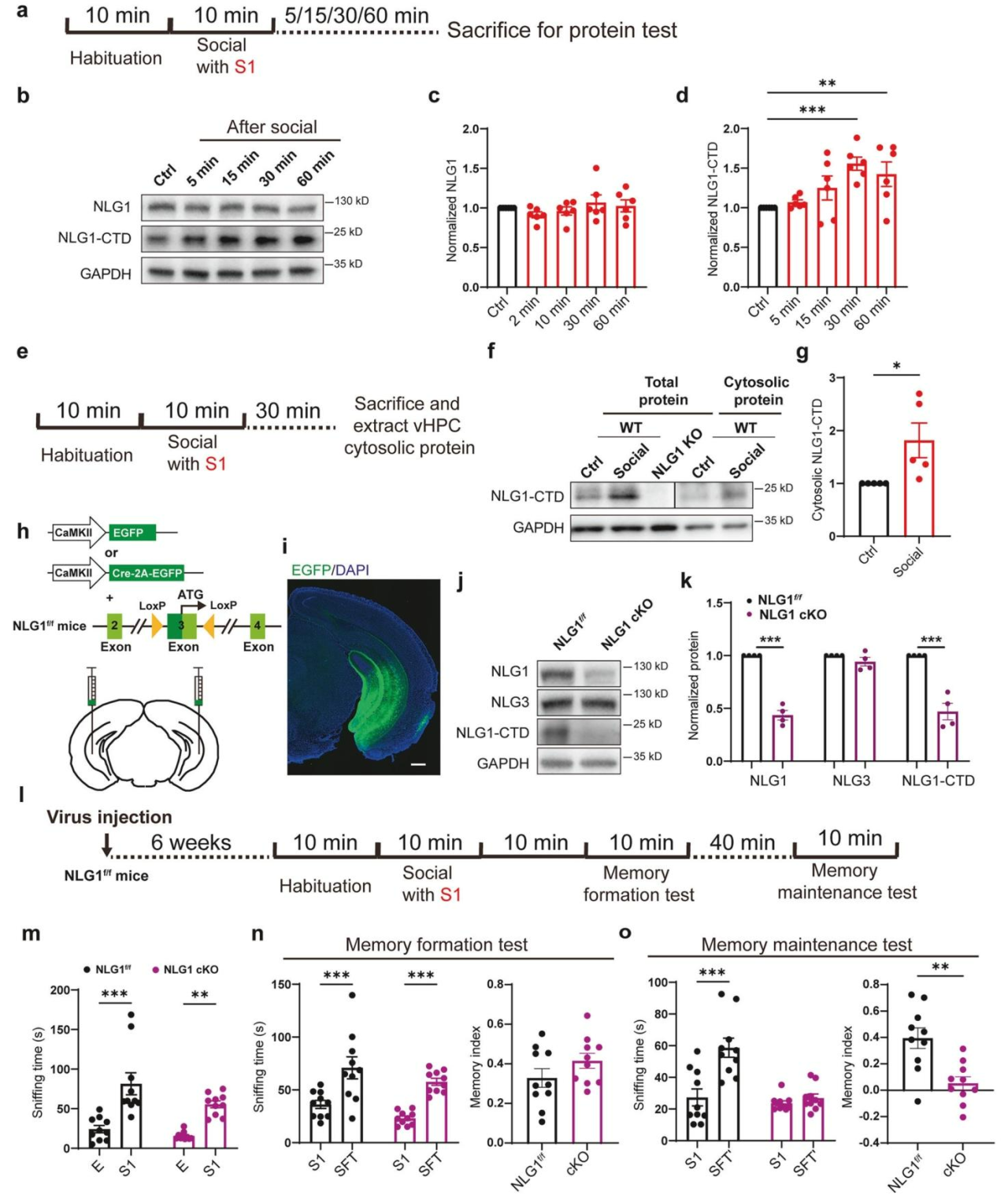
图3 腹侧海马区NLG1发生蛋白水解,且为社会记忆维持所必需
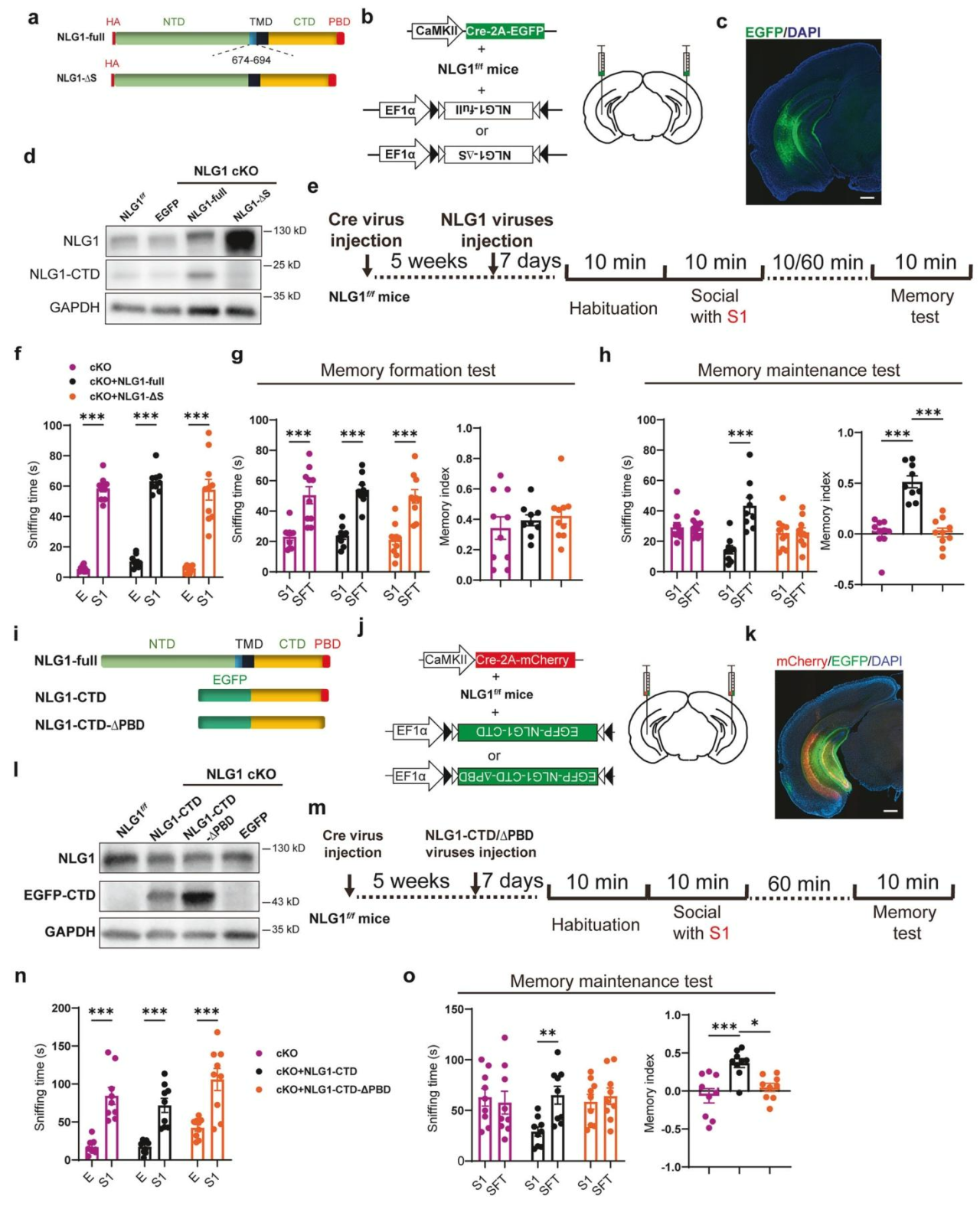
图4 社交记忆维持依赖NLG1的蛋白水解及NLG1-CTD的生成
前期研究证实NLG1-CTD能促进cofilin磷酸化,从而稳定肌动蛋白、增强突触传递。为明确社会记忆维持是否依赖cofilin活性调控,我们检测了社交互动后不同时间点vHPC中cofilin的磷酸化水平(图5i),发现社交后p-cofilin(而非总cofilin)水平显著升高(图5j-l),提示社会记忆维持伴随cofilin磷酸化增加(活性降低)。稀疏标记实验证实社交刺激可通过该机制促进vCA1神经元树突棘成熟与密度增加,提升突触可塑性。向WT小鼠社交后立即注射cofilin激活肽Tat-S3(阻止磷酸化),结果显示社会记忆维持被阻断(图5m、n);同时注射Tat-S3会阻断Tat-PBD对MRK诱导记忆缺陷的挽救作用(图5o、p)。这表明PBD肽参与社会记忆维持的功能依赖cofilin活性降低。
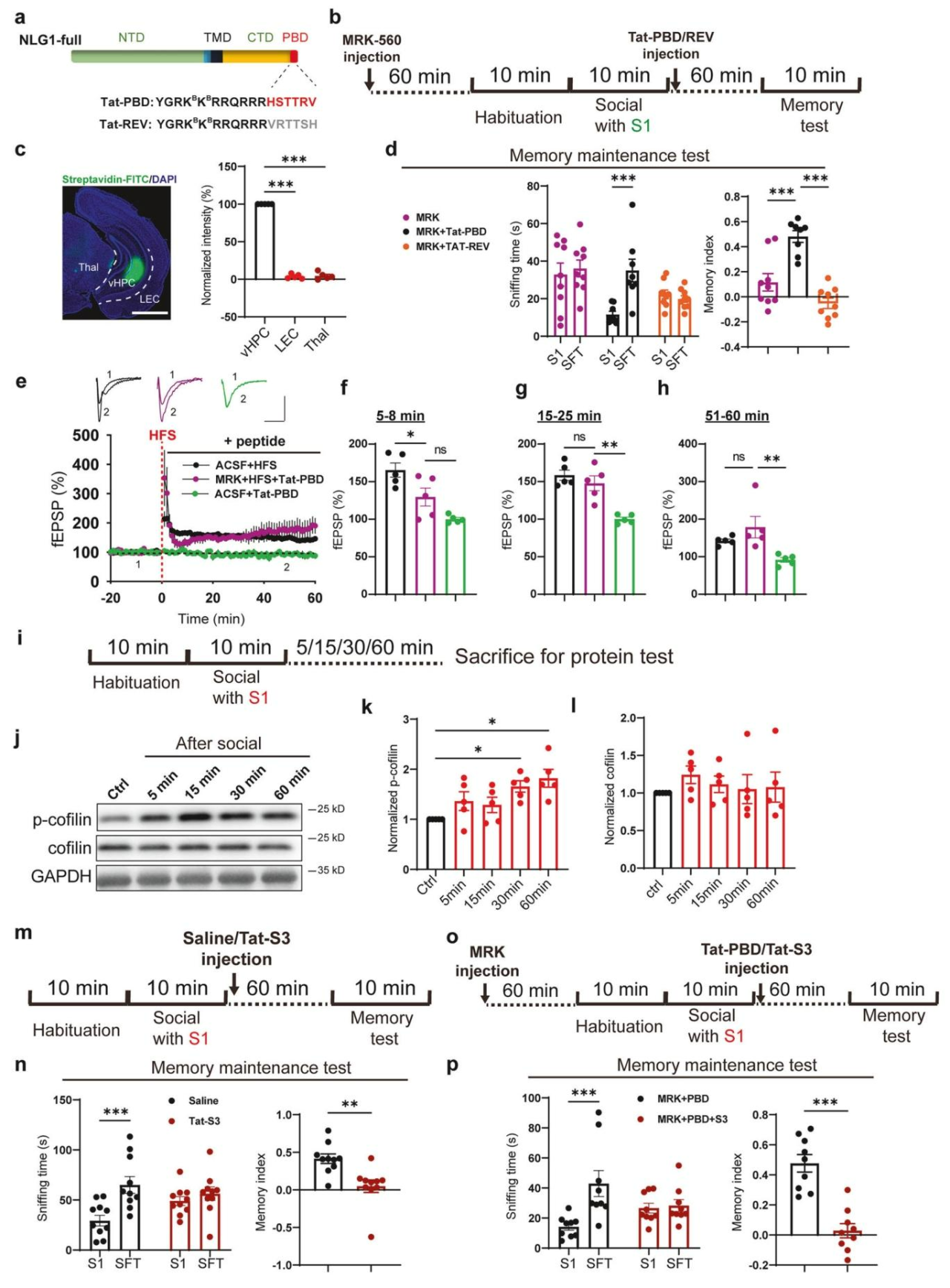
图5 社交记忆维持依赖PDZ结合域(PBD)序列及cofilin的失活
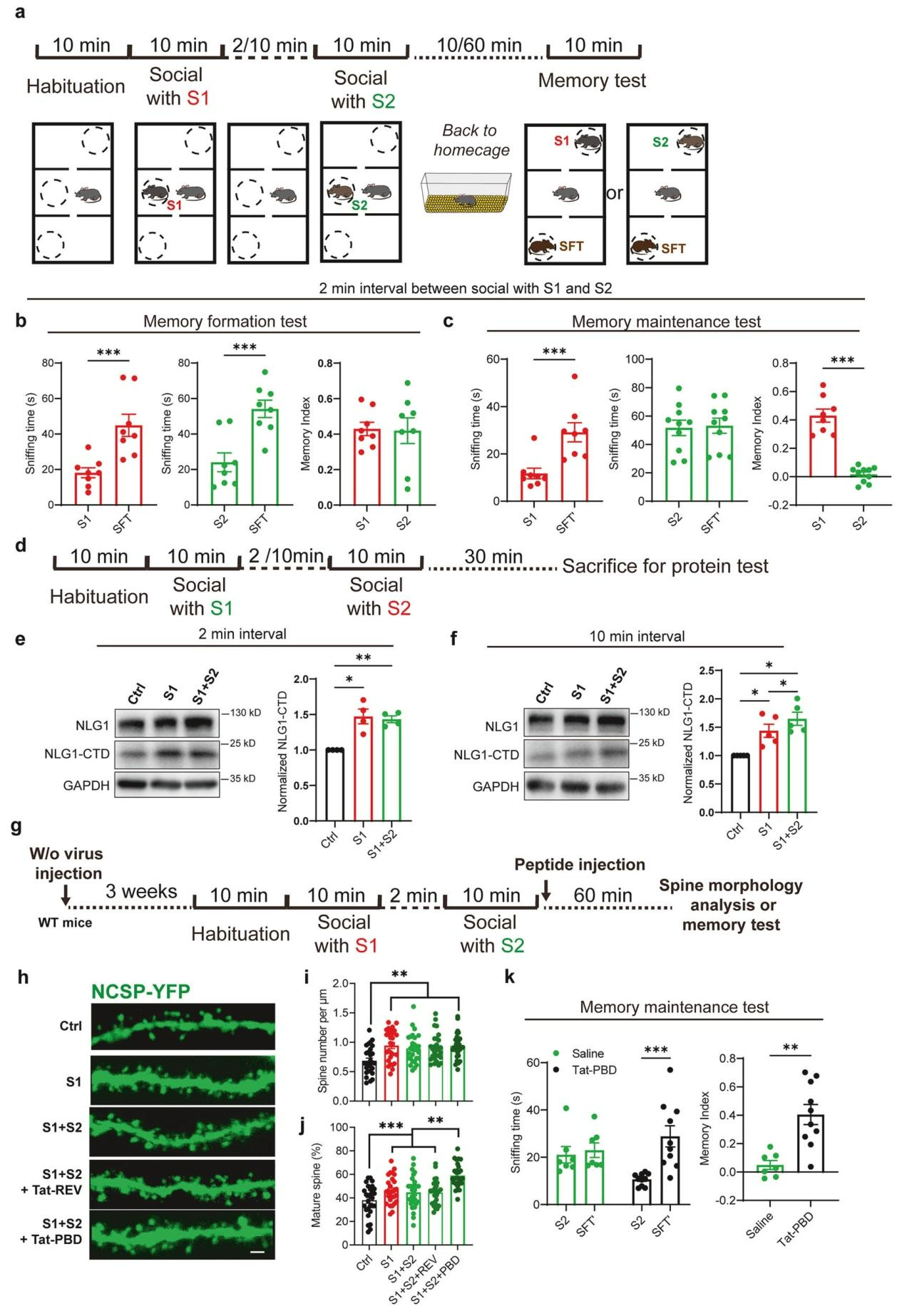
图6 PBD肽挽救短时程连续社交任务中的记忆维持缺陷