高血压是心血管疾病的高风险因素,全球健康负担沉重;尽管降压治疗有进展,但超50%接受治疗的患者血压控制不佳,难治性高血压患者表现出显著的交感神经活性升高,提示中枢交感过度激活机制是潜在治疗方向。脑干(如延髓)的血管运动中枢是交感激活和动脉血压控制的核心,高血压患者存在脑干结构和功能异常,脑干损伤可诱发神经源性高血压,但安全且高效的中枢降压靶点仍稀缺。

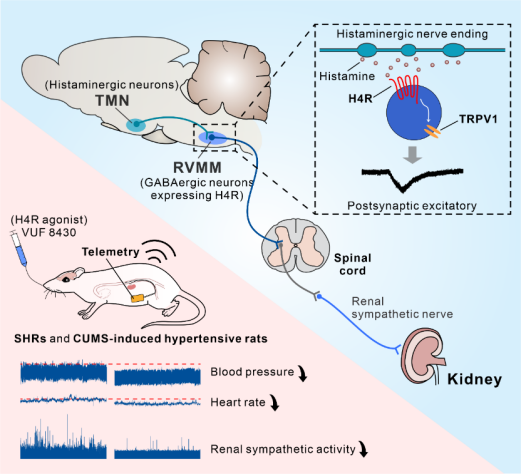
2025年9月29日,南京大学生命科学学院、医药生物技术全国重点实验室和脑科学研究院朱景宁教授团队在Advanced Science(IF=14.1)上发表题为“Targeting Histamine H4 Receptor in the Rostral Ventromedial Medulla to Relieve Hypertension”相关文章,该研究聚焦难治性高血压的中枢调控机制,首次发现组胺受体家族H4R在人和大鼠的延髓头端腹内侧区(RVMM)保守表达,RVMM是关键的交感心血管调节中枢;激活RVMM中H4R可通过瞬时受体电位香草酸1(TRPV1)通道兴奋GABA能交感前神经元,进而引发降压和心动过缓反应,同时抑制肾交感神经活动(RSNA);在自由活动的自发性高血压大鼠(SHRs)和应激诱导高血压大鼠(CUMS大鼠)中,经鼻递送H4R激动剂能产生持续降压效果。
生命科学学院石莹博士、张洋浔博士、硕士研究生陈俊毅和博士研究生马赛为该论文的共同第一作者。生命科学学院朱景宁教授、张潇洋特聘研究员和江苏第二师范大学于雷博士为本文的共同通讯作者。南京大学王建军教授、张骑鹏副教授、陈迪俊教授、李红召高级工程师,以及河北医科大学马会杰教授等对本工作提供了指导和重要帮助。该工作受到“科技创新2030—脑科学与类脑研究”重大项目课题,国家自然科学基金重点项目、青年科学基金项目(B类),江苏省杰出/优秀青年基金,以及南京大学中央高校基本科研业务费和AI & AI for Science专项项目等的资助。
利用人类脑细胞图谱1.0版的单核RNA测序(snRNA-seq)数据集分析人类延髓(含心率与血压调控中枢)中H4R表达:对203472个细胞经卢万聚类(scikit-network)得到13个细胞群(图1A),神经元细胞群中H4R基因(HRH4)表达相对较高(图1B-C)。采用RNA原位杂交(RNAscope)结合免疫荧光,检测大鼠延髓交感心血管中枢RVMM与RVLM的H4R分布,两区域均检测到Hrh4荧光信号,且与NeuN阳性神经元共定位(图1E-D);RT-qPCR显示两区域Hrh4表达水平相当(图1F)。结合人类延髓转录组数据,提示H4R在哺乳动物延髓表达具有保守性。
接下来探究了RVMM与RVLM中H4R的心血管调节作用。向RVMM注射H4R选择性激动剂VUF 8430,平均动脉压(MAP)显著下降(图1G、H),平均峰值心率(HR)显著降低(图1G、I),肾交感神经活性(RSNA)显著降低(图1G、J),提示激活RVMM-H4R可抑制中枢交感传出;而向RVLM注射VUF 8430对MAP、HR、RSNA均无影响。综上,激活RVMM而非RVLM中的H4R可诱导降压和心动过缓反应。

图1 H4R在正常大鼠体内RVMM中表达,可诱导MAP、HR和RSNA水平降低
为了明确RVMM组胺能传入纤维的心血管调节作用,参照既往研究构建HDC(内源性组胺合成关键酶)启动子调控Cre重组酶的转基因大鼠,在其TMN组胺能神经元中选择性表达ChR2-EYFP病毒,探究光遗传学激活TMN-RVMM投射的影响(图2A)。结果显示ChR2-EYFP及对照病毒在TMN选择性表达且与HDC阳性神经元共定位(图2A);全细胞膜片钳证实5Hz蓝光脉冲(10ms)可诱导神经元高保真发放动作电位(图2A);EYFP标记的组胺能传入纤维在RVMM可见曲张体(神经纤维上的串珠状膨大结构,其本质是神经末梢的“递质储存与释放位点”)(图2A),直接证明TMN神经元可通过纤维投射到RVMM并释放组胺。
与ChR2阴性对照相比,光遗传学激活TMN-RVMM组胺能末梢,可显著降低MAP(图2B)与HR(图2C),提示TMN组胺能神经元直接投射至RVMM并引发降压、心动过缓。向RVMM微注射H4R拮抗剂JNJ 10191584,几乎完全消除光遗传学诱导的降压(图2D)与心动过缓(图2E)反应。综上,TMN-RVMM组胺能投射可能通过激活H4R,在心血管活动内源性负向调节中起关键作用。
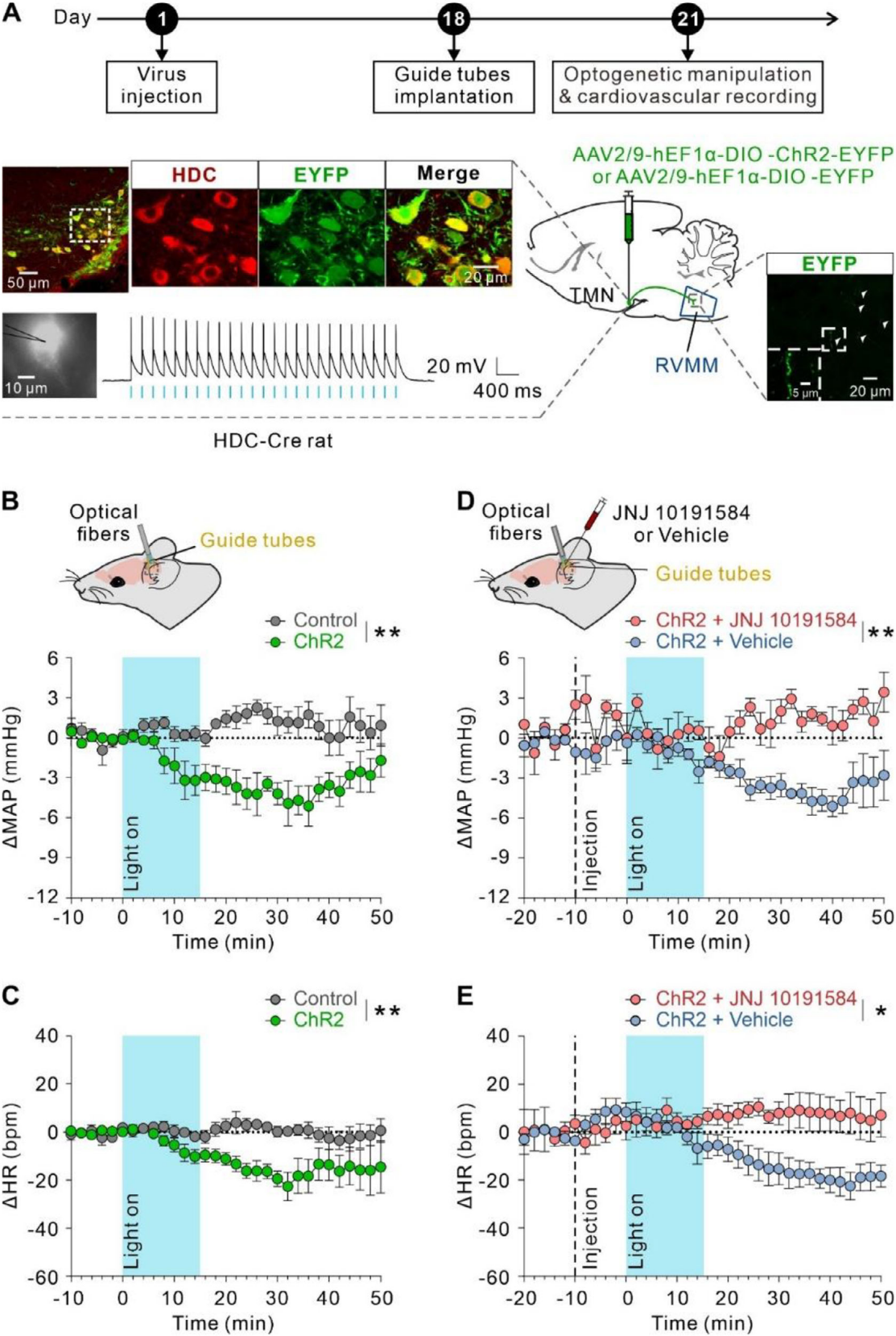
图2 TMN-RVMM组胺能回路通过H4R介导降压和心动过缓反应
为了明确H4R介导心血管效应的细胞机制,本研究采用全细胞膜片钳记录技术,探究H4R激活对RVMM神经元电生理活动的影响,结果发现选择性H4R激动剂VUF 8430以浓度依赖方式兴奋RVMM神经元,均可诱导内向电流(图3A-B),拟合浓度-反应曲线得EC₅₀=37.63μM(图3B)。野生型小鼠中VUF 8430呈浓度依赖性反应;进一步在Hrh4-KO小鼠(Hrh4表达完全缺失,图3C-D)中验证VUF 8430特异性,即使300μM VUF 8430也无法激活RVMM神经元(图3E-F),证实VUF 8430对RVMM神经元的兴奋效应由H4R特异性介导。此外,VUF 8430对RVLM神经元无显著影响,与“RVLM中H4R激活无心血管反应”结果一致,提示H4R激活仅兴奋RVMM神经元,不兴奋RVLM神经元。
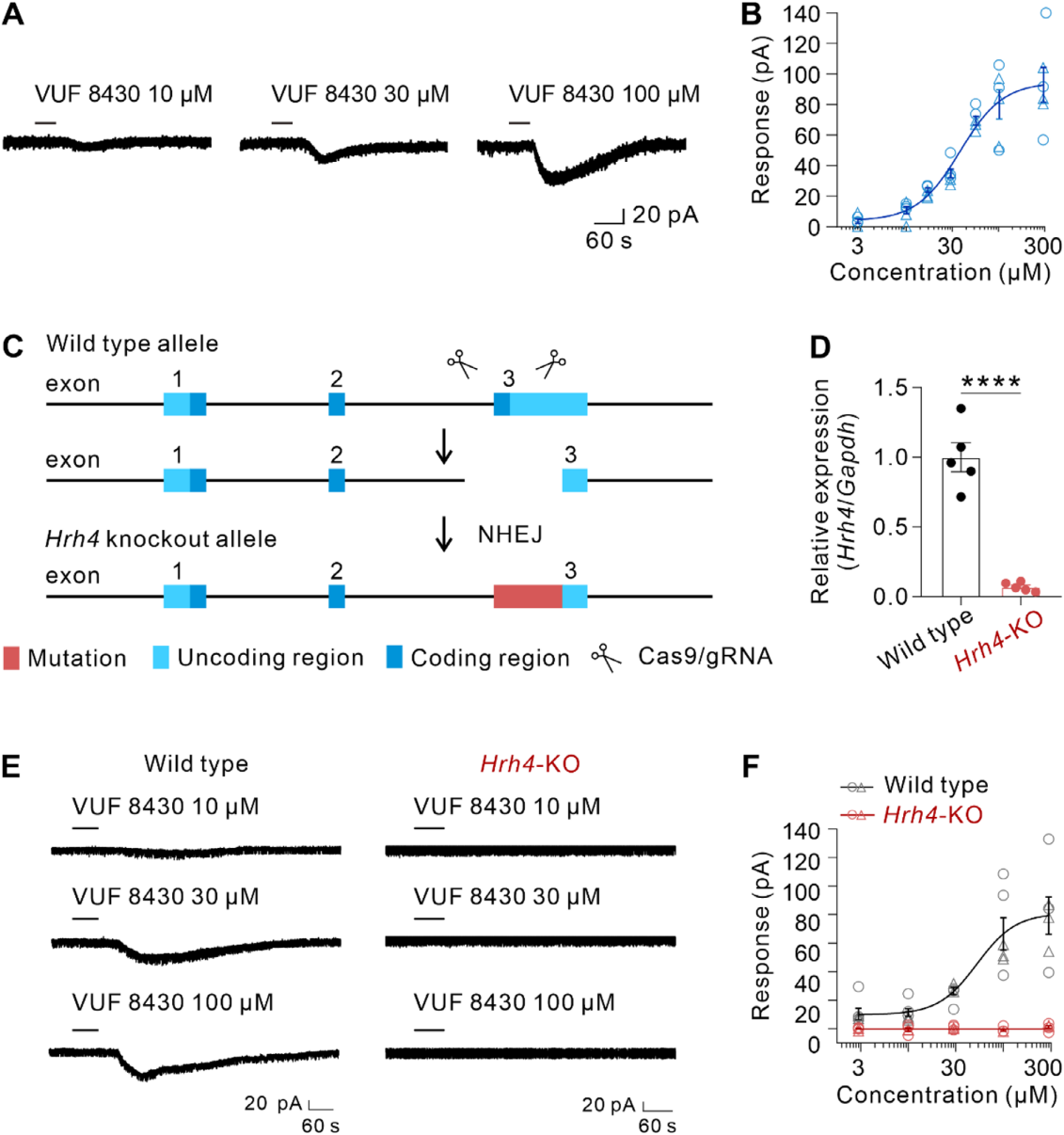
图3 选择性H4R激动剂VUF 8430在RVMM神经元上以浓度依赖的方式诱发内向电流
为了探究H4R在组胺对RVMM神经元作用中的贡献,实验使用高选择性H4R拮抗剂JNJ 10191584。结果显示,组胺以浓度依赖方式诱导RVMM神经元产生内向电流,EC₅₀=1.80μM(图4A-B);JNJ 10191584可浓度依赖抑制3μM组胺(接近EC₅₀)的兴奋效应,灌流JNJ 10191584后,组胺诱导的内向电流均降低(图4C-D),证实H4R参与组胺对RVMM神经元的兴奋效应。此外,JNJ 10191584还能浓度依赖阻断30μM H4R激动剂VUF 8430诱导的内向电流(图4E-F),进一步佐证H4R激活对RVMM神经元的兴奋作用。
鉴于H4R为突触后受体,实验探究其兴奋效应是否为直接突触后作用,电流钳模式下加0.3μM TTX(选择性电压敏感性钠通道阻滞剂),30μM VUF 8430仍诱导RVMM神经元5.62±0.63mV去极化(图4G-H);电压钳模式下联合使用TTX、SR 95531(选择性GABAA受体拮抗剂)、NBQX(选择性AMPA受体拮抗剂)和AP5(选择性NMDA受体拮抗剂)阻断突触传递,VUF 8430诱导的内向电流未受影响(图4I-J)。综上,组胺H4R激活对RVMM神经元具有直接突触后兴奋效应。
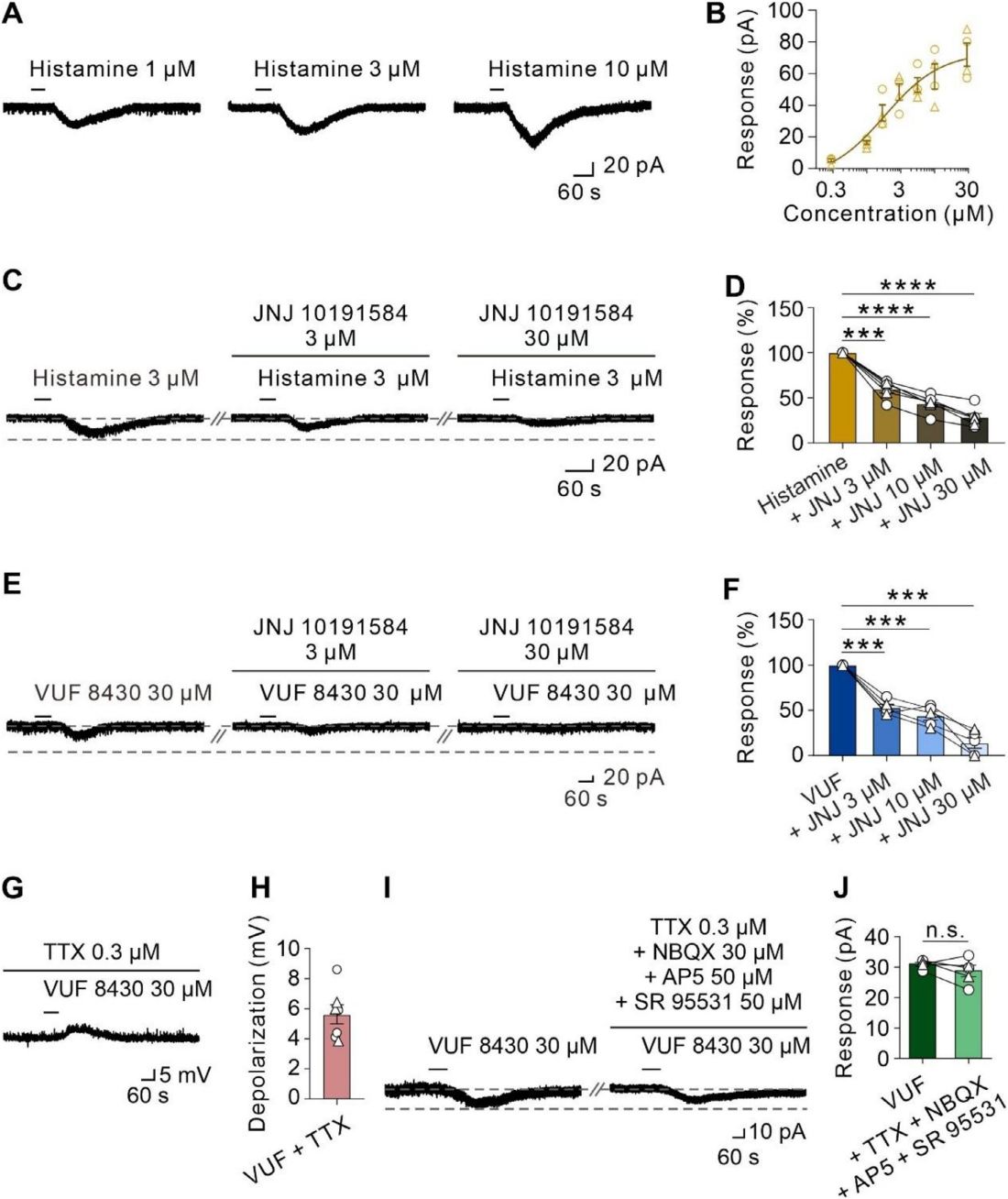
图4 选择性H4R拮抗剂JNJ 10191584可阻断组胺和VUF 8430诱发的内向电流
H4R激活介导兴奋效应的中枢离子机制不明,已知TRPV1参与外周DRG神经元中H4R诱发的兴奋,故用含TRPV1拮抗剂AMG 9810的ACSF(人工脑脊液)灌流脑片,探究其对H4R激活诱导RVMM神经元兴奋的介导作用。结果显示,30μM AMG 9810几乎完全阻断3μM组胺诱导的RVMM神经元内向电流(图5A-B),也完全阻断30μM VUF 8430诱导的内向电流(图5A、C),表明H4R激活通过开放TRPV1兴奋RVMM神经元。还检测了TRPV1在RVMM中的分布情况,RVMM中89.83%±3.51%含H4R阳性的神经元共表达TRPV1(图5D-E);RVLM虽有TRPV1表达,但H4R与TRPV1无共定位(图5D-E),进一步佐证TRPV1介导H4R对RVMM神经元的兴奋效应。体内实验中,向RVMM微注射AMG 9810,可完全阻断光遗传学激活TMN-RVMM组胺能投射(图5F)诱导的降压(图5G)和心动过缓(图5H)反应。综上,H4R及其下游TRPV1通道共同介导RVMM组胺能传入信号诱导的RVMM神经元兴奋,以及后续降压和心动过缓反应。
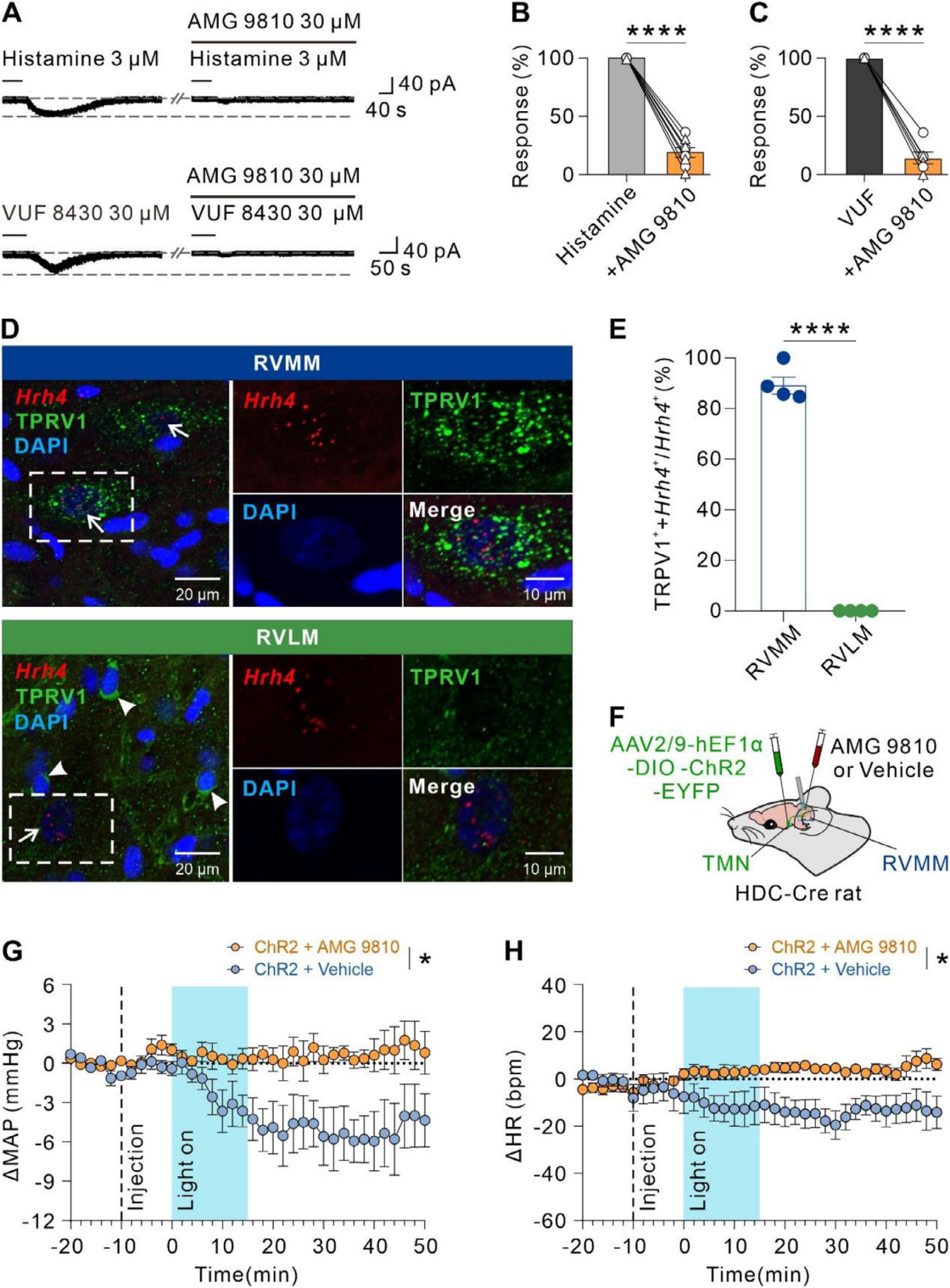
图5 H4R激活通过TRPV1通道的开放来兴奋RVMM神经元
已知降压、心动过缓常由肾交感神经活性(RSNA)抑制引发,且RVMM含兴奋性与抑制性交感前神经元,故探究H4R介导交感传出抑制的机制。采用电极记录RVMM神经元全细胞电流,发现经H4R激动剂VUF 8430灌流后被兴奋的RVMM神经元,均呈GAD65/67免疫阳性(图6A-C),提示H4R激活可兴奋RVMM的GABA能神经元。为了验证该GABA能神经元是否为交感抑制性神经元,将逆行跨多突触示踪剂伪狂犬病病毒(PRV)注射至肾实质,标记RVMM内谷氨酸阳性交感兴奋性神经元与GAD65/67阳性交感抑制性神经元(图6D)。RNA原位杂交显示,Hrh4信号定位于PRV标记的RVMM GABA能神经元(图6E-6G);而投射至肾的谷氨酸能交感兴奋性神经元中,未检测到Hrh4 mRNA(图6F-G)。综上,H4R激活可直接兴奋RVMM 的GABA能交感前神经元,进而抑制肾交感神经传出,诱导降压、心动过缓反应。
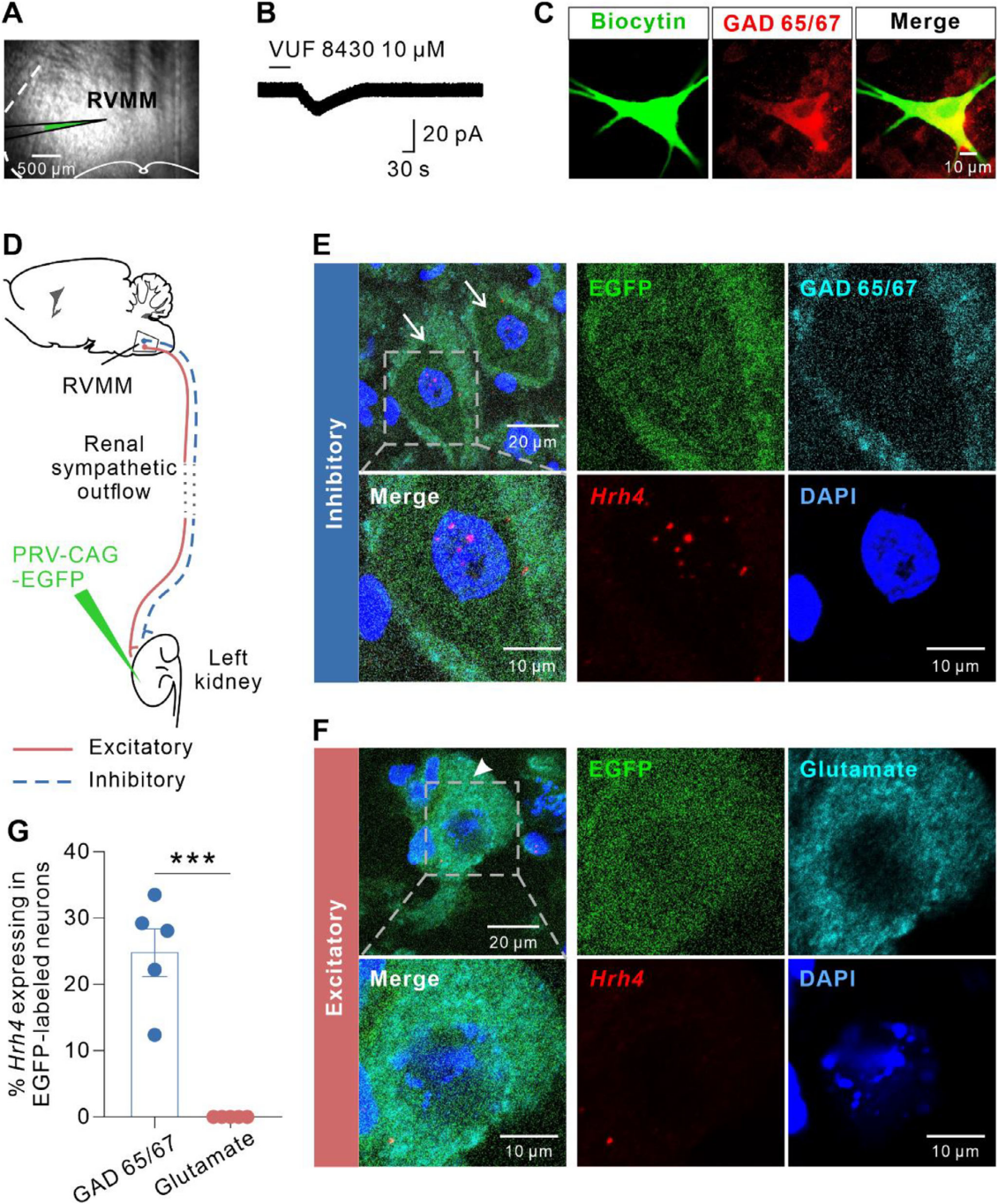
图6 RVMM-Hrh4神经元诱导抑制性肾交感神经流出
采用自发性高血压大鼠(SHRs)和慢性不可预测轻度应激(CUMS)诱导高血压大鼠(两种原发性高血压模型),探究RVMM-H4R的降压治疗潜力,已知过度交感活性是两类模型高血压的关键诱因。在SHRs的RVMM局部注射 H4R激动剂VUF 8430:与对照组比,MAP、HR和RSNA均显著降低(图7A-G),雌雄效应一致;H4R激活的降压效应在高血压与正常血压大鼠中无差异。全身给药实验,经鼻递送VUF 8430在高血压与正常血压大鼠中降压、心动过缓效应相当(图7H-J);分子水平上,高血压大鼠(SHRs、CUMS)RVMM 中H4R mRNA表达及组胺含量与正常大鼠无差异,提示高血压状态下H4R介导的神经调节功能完整,且H4R是稳定调节系统,非高血压致病因素。
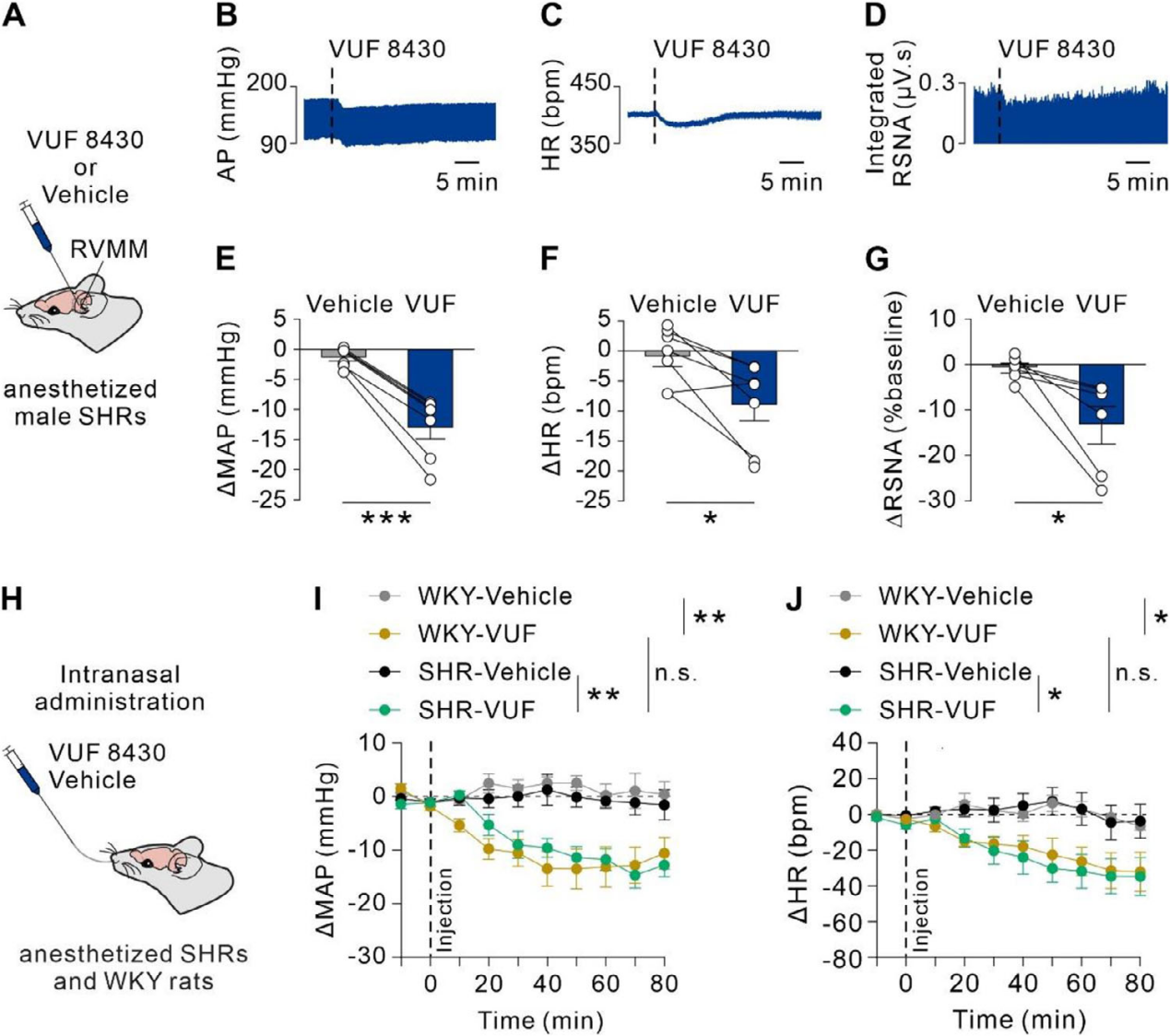
图7 在麻醉SHR大鼠和正常血压大鼠中,RVMM中H4R的激活均能产生相似的降压作用
为了评估慢性组胺H4受体激活的治疗潜力,用无线电遥测监测自由活动SHRs(图8A),单次经鼻VUF 8430可降SBP、MAP、HR并抑制RSNA,与麻醉状态一致(图8B-F);连续3天每日经鼻给药,SHRs血压、心率持续下降,停药后恢复(图8G-J)。鉴于长期应激是高血压高发诱因,进一步探究经鼻VUF 8430对7周慢性不可预测轻度应激(CUMS)诱导高血压大鼠的影响(图8K)。与既往研究一致CUMS大鼠SBP、MAP显著升高且维持高位(图8L-M),连续5天每日经鼻给药,可逐步持续降低其SBP、MAP、HR(图8N-Q)。综上,组胺H4R或为治疗神经源性高血压的潜在中枢靶点。
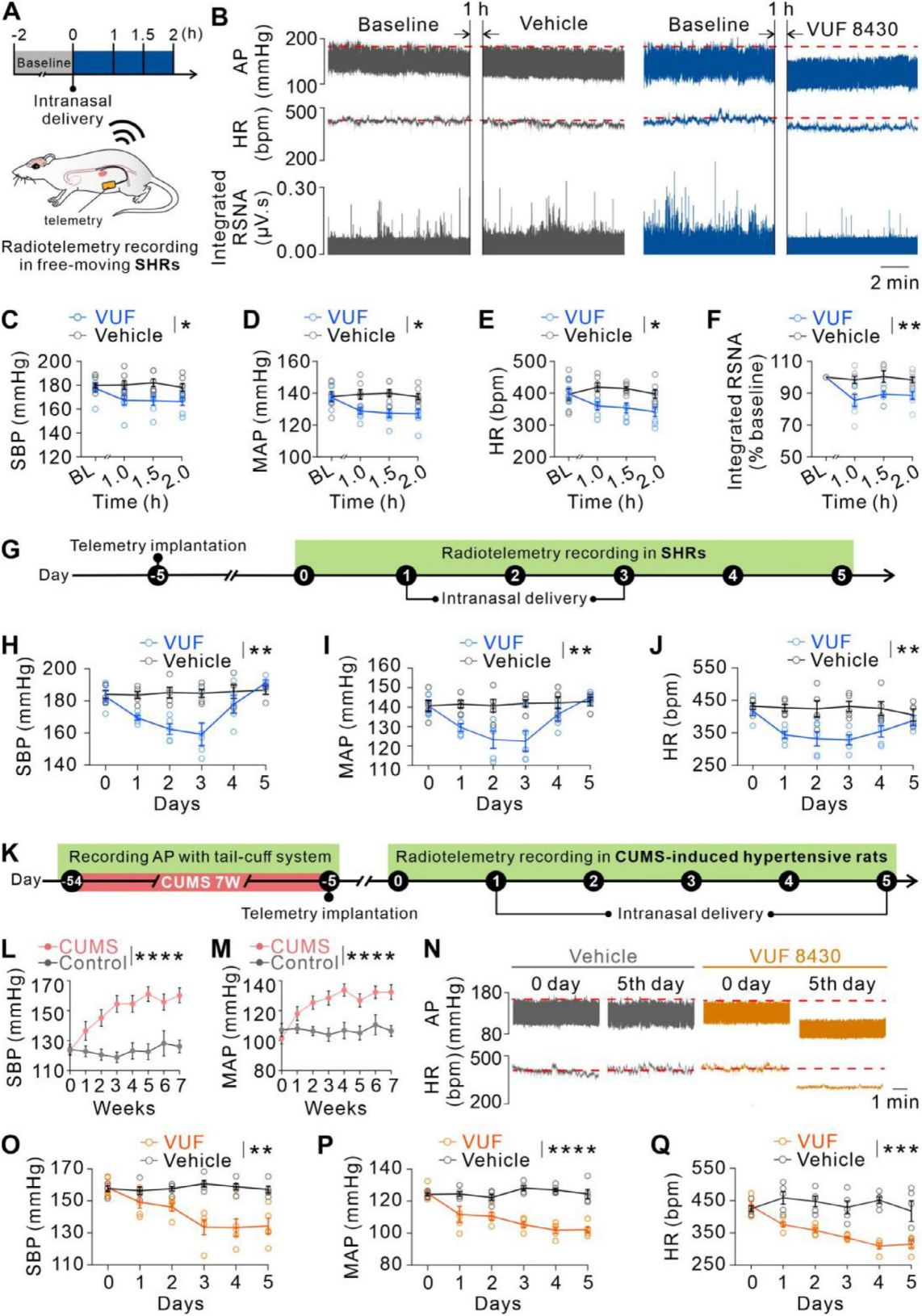
图8 鼻内注射VUF 8430可改善自由运动SHR和CUMS诱导高血压大鼠的高血压
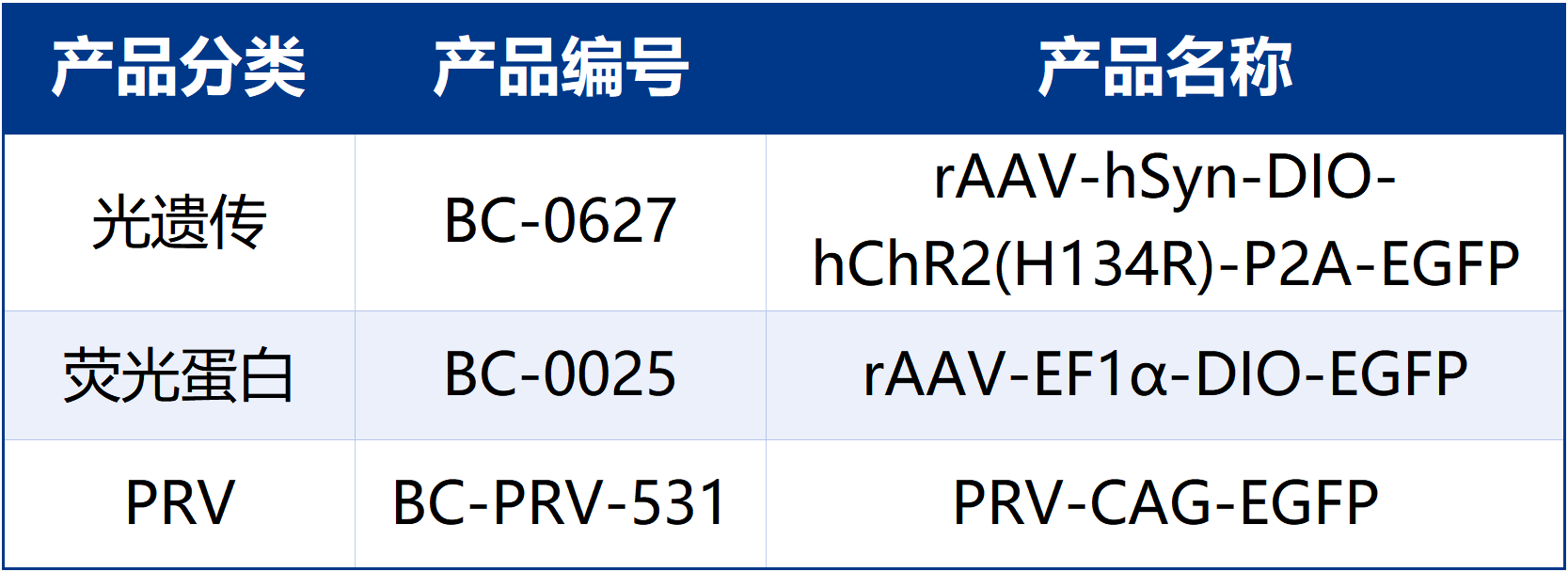
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。