现有乳酸探针检测工具可体内检测,但空间分辨率低(无法单细胞水平)且有创(破坏组织)。绿色荧光传感器(如eLACCO2.1)虽实现微创成像,但光谱与GCaMP钙离子传感器重叠,无法多标监测乳酸与神经活动。
2025年发表于《Nature Communications》的研究文章“A red fluorescent genetically encoded biosensor for in vivo imaging of extracellular L-lactate dynamics”,开发出红色荧光基因编码的细胞外L-乳酸探针R-eLACCO2.1,其通过定向进化优化(从R-eLACCO0.1经多轮进化获得,含25个突变)及Igκ leader与COBRA anchor的膜定位优化,在体内对细胞外L-乳酸升高的敏感性和光谱正交性上优于此前绿色荧光探针。

研究人员先通过将绿色探针eLACCO1的环形排列绿色荧光蛋白(cpGFP)替换为环形排列红色荧光蛋白(cpmApple),构建出红色荧光L-乳酸探针原型R-eLACCO0.1(ΔF/F=0.2),随后经定向进化获得ΔF/F=4.3的R-eLACCO1,引入Leu79Ile突变得到低亲和力变体R-eLACCO1.1(ΔF/F=3.9,Kd=1.4 mM),但该变体细胞表面表达荧光暗淡、响应有限(ΔF/F≈1);进而以R-eLACCO1为模板,经1轮定点优化和11轮全基因随机突变定向进化得到ΔF/F=18的R-eLACCO1.93,引入Ile191Val突变后获得含25个突变的高度优化变体R-eLACCO2,表征发现其变体可作荧光寿命成像显微镜(FLIM,通过监测探针分子的“荧光寿命(τ)变化”实现检测,荧光寿命是荧光分子的固有属性,不受浓度、激发功率等外界因素影响)探针,冷冻电镜解析其2.7Å乳酸结合态结构,揭示发色团与Lys211的静电相互作用及Lys211对荧光的关键调节作用。在细胞表面定位优化上,基于此前eLACCO2.1研究经验,筛选发现GPI类锚定结构域(如CD59、COBRA、GFRA1)能实现低亲和力变体R-eLACCO2.1高效膜定位,14种N端引导序列中HA、Igκ、pat-3荧光最强,进一步组合筛选得出Igκ引导序列+COBRA锚定结构域为最佳组合,该组合下R-eLACCO2.1的ΔF/F约为5,是R-eLACCO1.1(CD59引导-锚定组合)的5倍。
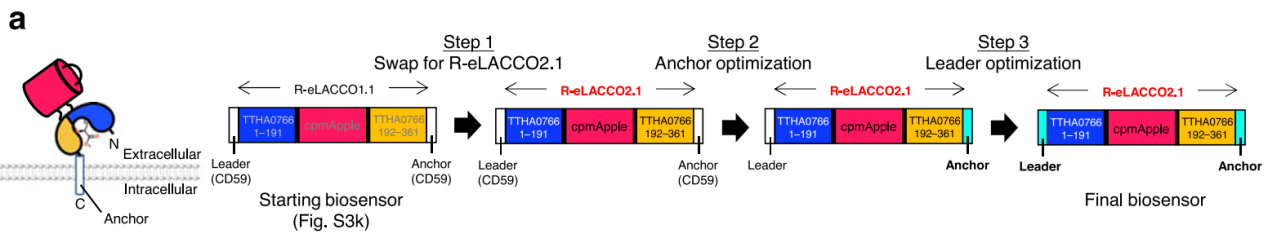
图1 L-乳酸探针细胞表面定位优化概述
对带优化引导序列(Igκ)和锚定结构域(COBRA)的R-eLACCO2变体进行表征(图2a),HeLa细胞表面表达的R-eLACCO2、R-eLACCO2.1经10 mM L-乳酸处理后,ΔF/F分别为4.5±0.1、6.2±0.2(图2b-c);对照R-deLACCOctrl膜定位正常,但对L-乳酸无响应(图2a-d)。二者对L-乳酸的原位表观Kd分别为560 μM、5.1 mM(图2d),对Ca²+的原位表观Kd为310 μM、610 μM(图2e),均低于脑内胞外Ca²+浓度;结合速率(τon)均为61±5 s/61±3 s,解离速率(τoff)为72±4 s/35±3 s(图2f)。基于cpmApple的探针蓝光下易光激活且光稳定性复杂,HeLa细胞中R-eLACCO变体经470 nm蓝光(~4 mW/cm²)照射,荧光轻微升高(图2g),其光激活ΔF/F远小于乳酸响应,动力学更快(图2c-f)。无乳酸时,R-eLACCO2、R-eLACCO2.1的积分荧光(IF,量化荧光信号的整体强度与稳定性)为1251±18、1485±32,高于mApple;有乳酸时,两者的光稳定性有所下降,IF降至702±5、731±9(图2h);R-deLACCOctrl光稳定性始终高于mApple。
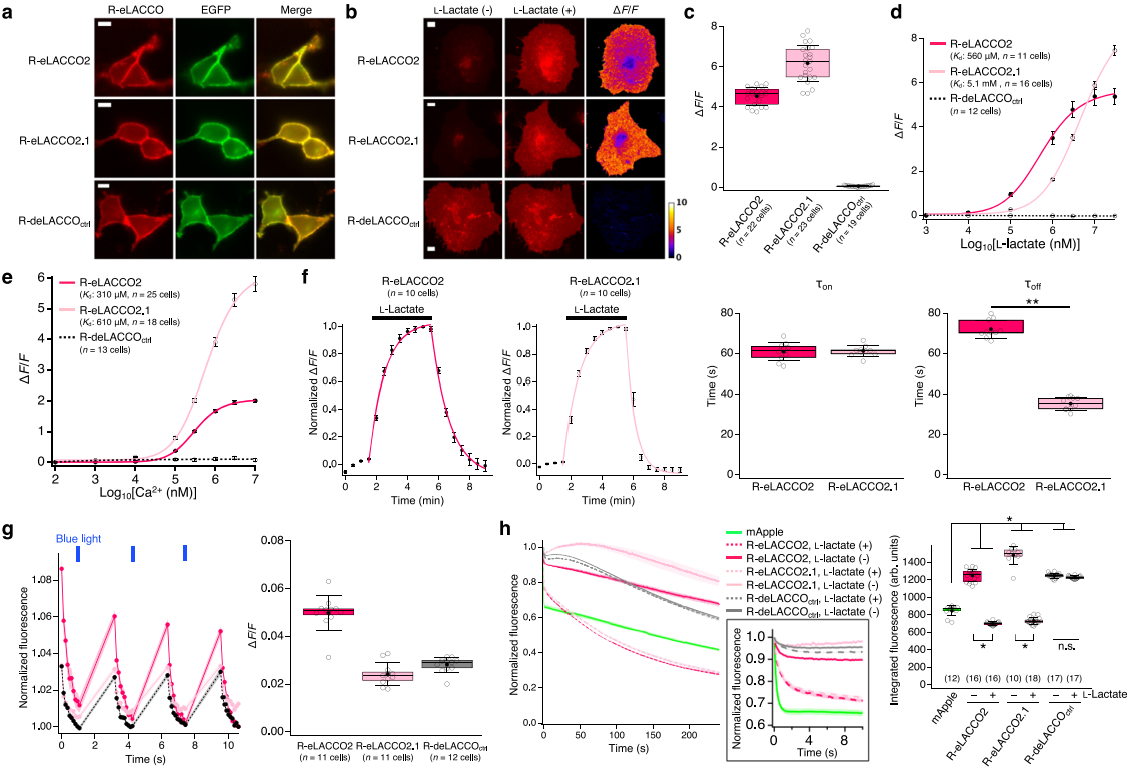
图2 活体哺乳动物细胞中R-eLACCO2变体的表征
观察L-乳酸时空动态,饥饿胶质母细胞瘤细胞(T98G)共表达R-eLACCO2.1(胞外)与iLACCO1(胞内)(图3i),葡萄糖刺激后二者荧光同步升高(图3j-k),R-deLACCOctrl荧光下降(推测因乳酸升高伴随pH降低,图3k)。HeLa细胞中R-eLACCO2与笼状L-乳酸(MNI-L-乳酸,紫光照射下会释放L-乳酸)共孵育,405 nm光照射后,R-eLACCO2荧光先降(质子释放致pH降低)后升(图3m-n),R-deLACCOctrl仅短暂下降无后续响应,表明其可与绿色荧光探针、紫光激活工具联用。FLIM检测中,HeLa细胞表面的R-eLACCO2、R-eLACCO2.1经10 mM L-乳酸处理,两者的荧光寿命显著延长(图3o-p)。胶质母细胞瘤细胞(T98G)共表达R-eLACCO2.1与LiLac(胞内乳酸FLIM探针),葡萄糖刺激后R-eLACCO2.1荧光寿命如预期升高,LiLac如预期降低(图3q-s),证明其可作为FLIM探针检测活细胞胞外L-乳酸。
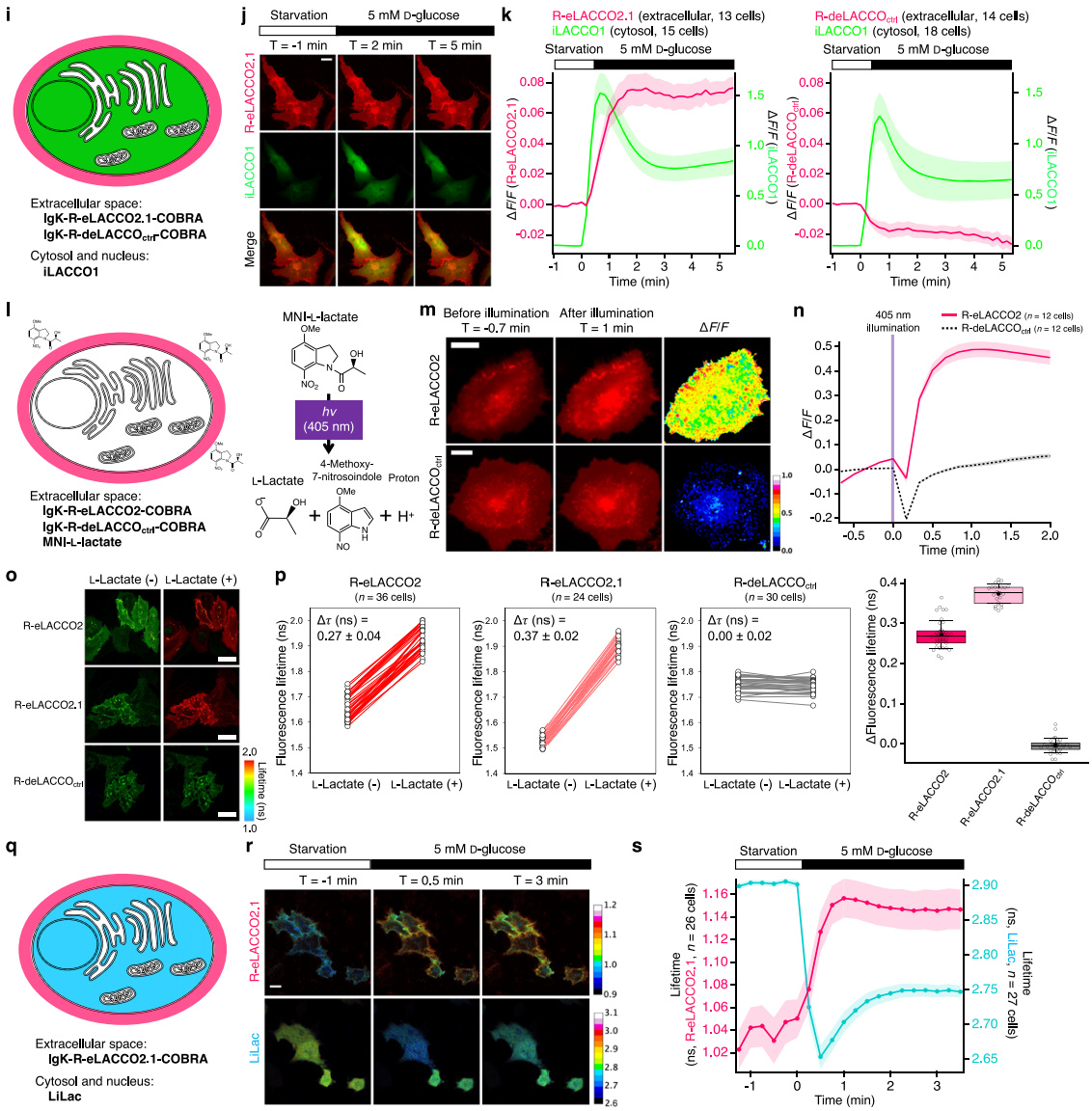
图3 用R-eLACCO2变体直接观测L-乳酸的时空动态变化
为了表征R-eLACCO变体在神经元表面性能,将其构建于神经元特异性启动子hSyn调控表达的质粒中并转染大鼠原代皮质神经元,表达R-eLACCO2的神经元呈明亮膜定位荧光(图4a);浴槽加10 mM L-乳酸后,R-eLACCO2、R-eLACCO2.1的ΔF/F分别为4.3±0.3、4.5±0.2,R-deLACCOctrl无响应(图4b-c)。将探针构建到星形胶质细胞特异性启动子gfaABC1D调控表达的质粒,在大鼠原代皮质星形胶质细胞表面可正确表达(图4d);浴槽加10 mM L-乳酸后,R-eLACCO2、R-eLACCO2.1的ΔF/F分别为4.7±0.4、3.9±0.4(图4e-f),R-deLACCOctrl无响应。
为了验证R-eLACCO2.1检测完整组织乳酸的能力,对AAV介导表达该探针的小鼠脑SCN切片进行检测(图4g),虽然培养基15 mM葡萄糖可能升高基础胞外乳酸,但浴槽加乳酸后,R-eLACCO2.1荧光显著高于R-deLACCOctrl(图4h-j)。综上,带优化引导序列与锚定结构域的R-eLACCO变体,可用于培养神经元、星形胶质细胞表面及脑切片中细胞外L-乳酸的成像检测。
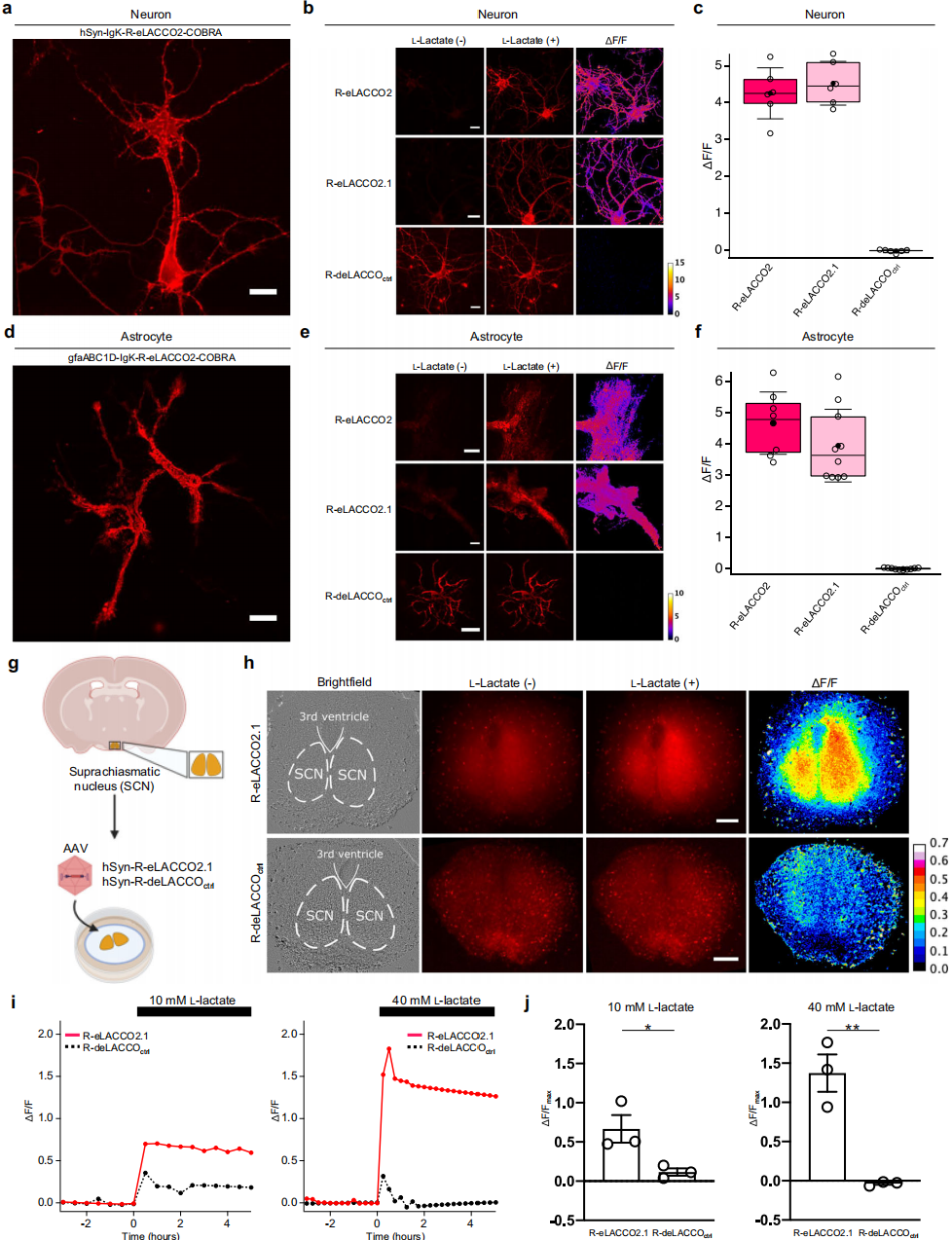
图4 R-eLACCO2变体在脑细胞与脑组织中的验证
为了验证R-eLACCO2.1体内性能,研究人员向成年小鼠注射编码hSyn-R-eLACCO2.1的AAV,使其在vS1皮层表达(图5a)。已知静脉注射的L-乳酸可穿过血脑屏障,向清醒小鼠尾静脉注射后,通过双光子激光扫描显微镜(AO2P)观察到,100 μm和400 μm深度处R-eLACCO2.1荧光显著升高(图5b)。为了进一步证实其监测胞外L-乳酸动态的能力,研究人员同步记录R-eLACCO2.1荧光信号与体外校准后植入vS1的电化学(EC)L-乳酸探针电信号(图5c-d),结果显示二者信号均随乳酸浓度变化而增减;生理盐水注射会引发R-eLACCO2.1微弱荧光响应,原因未明(图5d)。成像表明,R-eLACCO2.1与EC探针信号高度相关(图5e),证实其胞外L-乳酸探针功能。活体成像中,静脉注射L-乳酸后,R-eLACCO2.1的荧光响应高于GFP基探针eLACCO2.1(图5f)。综上,R-eLACCO2.1作为胞外L-乳酸探针,在体内功能良好。
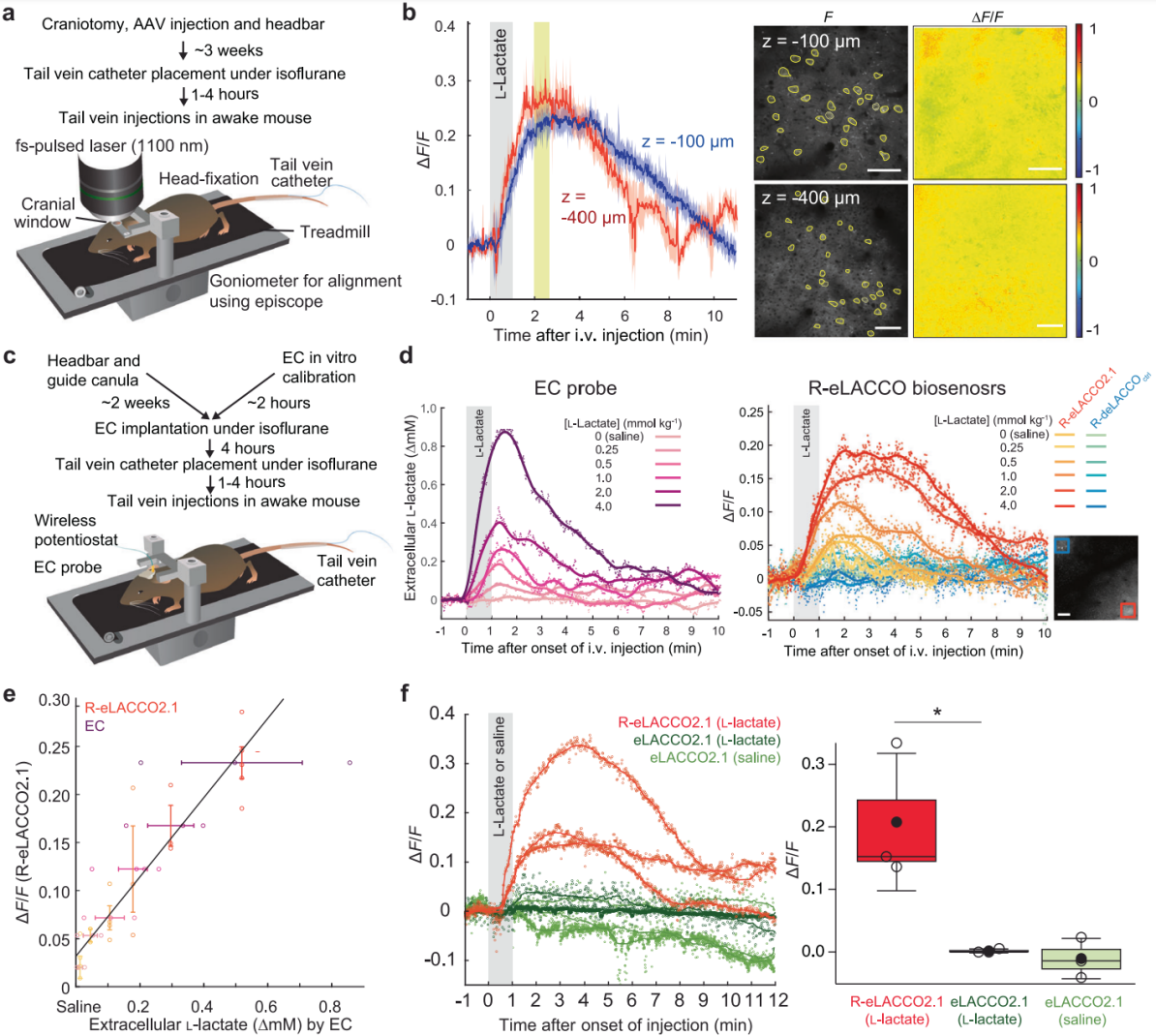
图5 R-eLACCO2.1在清醒小鼠中的验证
为了监测清醒小鼠内源性胞外L-乳酸动态,研究人员在其vS1皮层神经元表达R-eLACCO2.1,记录荧光响应与气流触须刺激下的运动速度(图6a)。vS1皮层Ⅱ/Ⅲ层神经元中,触须刺激既使R-eLACCO2.1荧光升高,也诱导小鼠运动(图6b);长期成像显示该探针荧光稳定,证明荧光变化由乳酸浓度驱动,非光漂白。小鼠30秒静息后自发运动,R-eLACCO2.1荧光升高幅度与20秒触须刺激时相当(图6c),提示触须刺激下的荧光响应主要源于运动;未诱导运动的触须刺激仅引发微弱荧光响应。需注意,触须刺激诱导血管舒张与功能性充血,因激发光、发射光吸收增加导致探针实测荧光降低(图6b-c)。体内成像还证实,R-eLACCO2.1可检测运动后静息期胞外乳酸降至基础水平的过程,表明其能以细胞分辨率检测清醒小鼠内源性胞外L-乳酸动态。
最后,研究人员通过多通道AO2P成像探究清醒小鼠神经活动与代谢关联,向FLEX-GCaMP6f的转基因小鼠注射含hSyn-R-eLACCO2.1与hSyn-cre的AAV混合物(图6d)。单光子宽场成像与AO2P成像显示,vS1区域Ⅱ/Ⅲ层神经元中,R-eLACCO2.1定位于细胞膜,GCaMP6f定位于胞体(除细胞核),证实体内表达定位(图6e)。无明显运动时,自发神经激活后胞外乳酸先降后恢复(图6f-g)。综上,R-eLACCO2.1可同步监测清醒小鼠内源性胞外L-乳酸动态与神经活动。
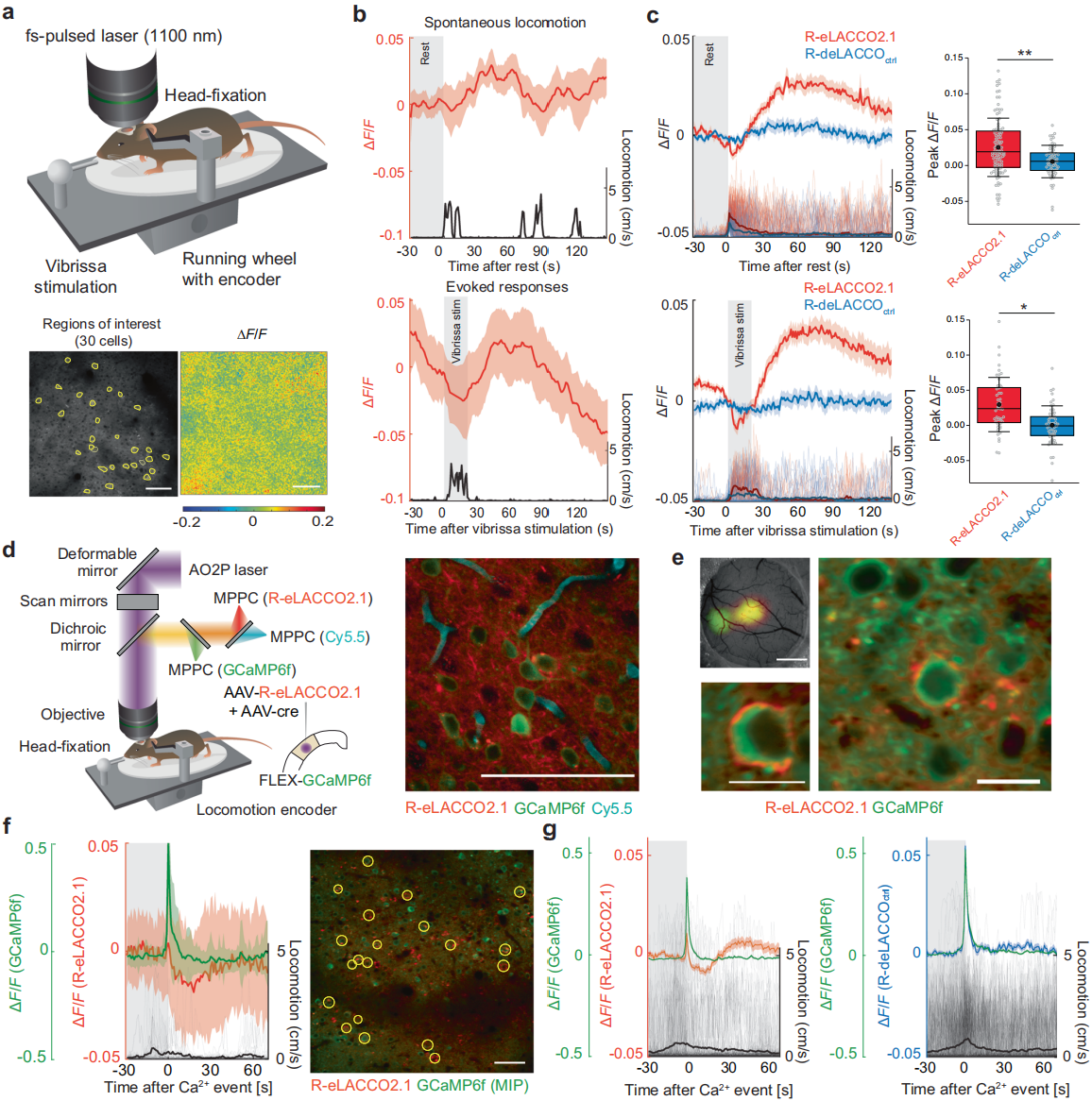
图6 神经活动期间体内L-乳酸动态变化
R-eLACCO2.1探针红色荧光可与绿色指示剂(如GCaMP)同时使用,实现“乳酸-神经活动” 多标成像;体内对乳酸升高的响应优于绿色探针,且能检测基线以下的乳酸下降,兼具荧光强度成像与FLIM功能。