脑血管系统作为维持大脑高代谢活动的关键枢纽,其结构或功能异常可引发多种严重神经系统疾病。其中,由脑内皮细胞体细胞突变驱动的脑血管畸形,特别是具有高出血风险的脑动静脉畸形(bAVM)和脑海绵状畸形(CCM),已成为神经科学领域的重要研究焦点。然而,现有AAV载体难以在脑发育关键阶段实现高效特异的基因递送,同时传统建模方法周期长、效率低,且受限于病毒载体容量而无法满足大型基因递送需求,严重阻碍了疾病机制研究和治疗开发。
2025年10月29日,北京脑科学与类脑研究所戈鹉平团队和孙文智团队联合在Nature Biomedical Engineering期刊上发表题为“A targeted vector for brain endothelial cell gene delivery and cerebrovascular malformation modelling”的研究论文。该研究成功开发了一种rAAV-miniBEND系统,可实现高效、特异性地靶向脑血管内皮细胞的基因递送;并利用该系统成功构建了MAP3K3I441M介导的CCM模型以及BrafV600E介导的AVM模型,为脑血管疾病建模与脑内皮细胞特异性基因递送提供了有力工具。

北京脑科学与类脑研究所(CIBR)的李军为第一作者,毕湛迎与陈行军为共同第一作者,北京脑科学与类脑研究所戈鹉平教授与孙文智教授为共同通讯作者。
为开发脑内皮细胞特异性重组腺相关病毒(rAAV)载体,研究借助内皮细胞特异性标志物Tek基因的内源性表达调控系统。经多物种Tek基因组序列比对,筛选出第1内含子、5'非翻译区(5'UTR)及转录起始位点上游2.5kb的保守区域。为评估不同截短版本启动子/顺式元件的功能,将其与Cre重组酶构建至rAAV-PHP.eB-miniBENDs载体,通过眶后注射Ai报告小鼠进行系统性验证(图1a)。结果发现,截短5'非翻译区(5'UTR)明显减弱启动子活性,优化版mPro723启动子活性最高(图1b-d);顺式元件可抑制非内皮细胞中的转录,mCis700效果最佳(图1e–g)。免疫染色结果显示,GFP信号与内皮细胞标志GLUT1和CD31高度共定位,且不与周细胞、平滑肌细胞重叠(图1h–j),这证实rAAV-miniBEND可实现脑内皮细胞的精准靶向。
进一步静脉注射AAV-PHP.eB-miniBENDs,除小脑外,几乎所有脑区内皮细胞均被高效标记,其中mPro723启动子可最大限度减少神经元的非特异性标记(图1k–m)。综上,rAAV-miniBEND系统通过Tek基因调控元件的优化组合实现对脑内皮细胞的高效、特异性基因递送。
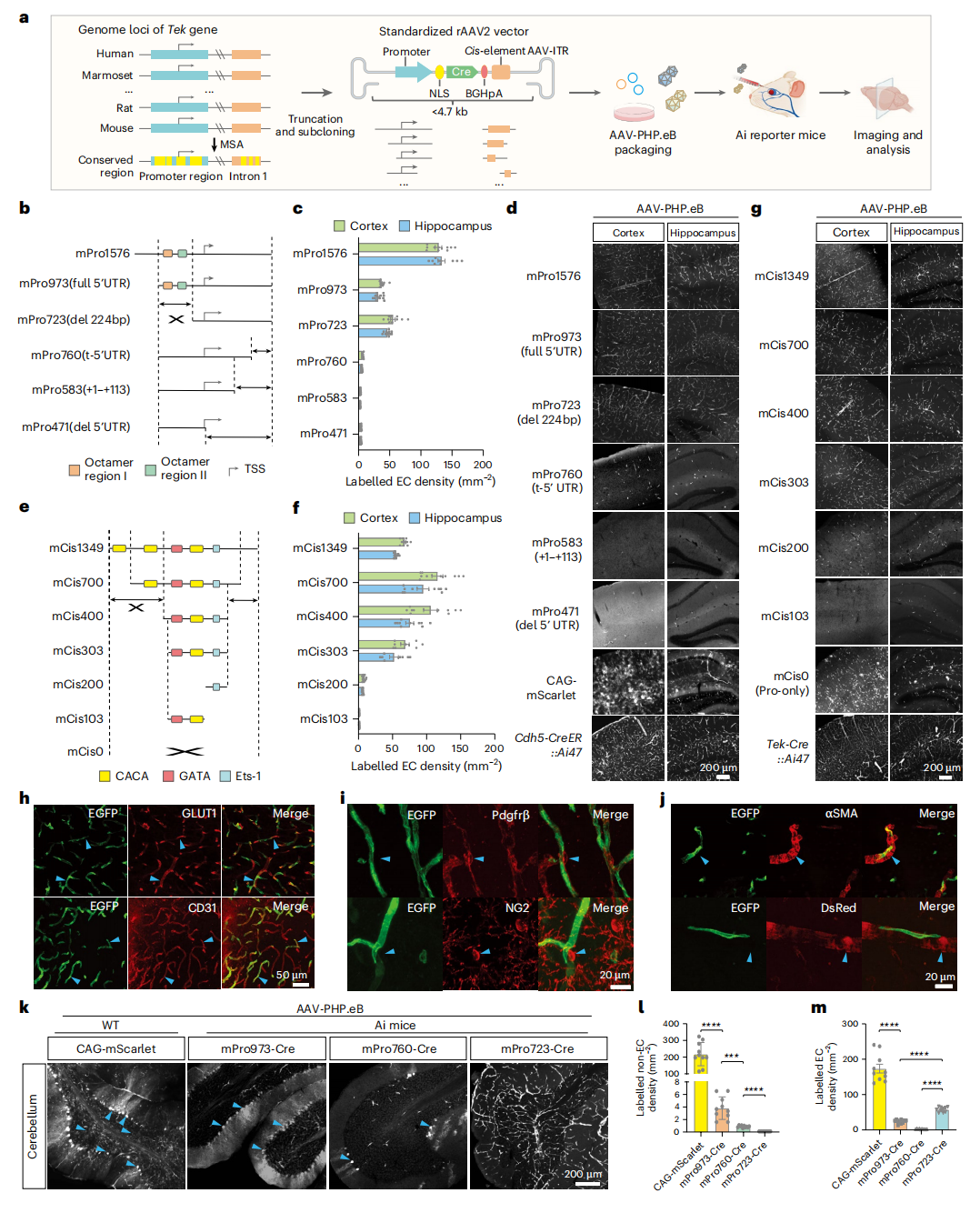
图1特异性靶向脑EC的rAAV-miniBEND系统开发
发育中大脑的细胞类型特异性基因操作是模拟相关脑畸形动物模型的关键。为研究rAAV- miniBEND系统对发育中大脑脑内皮细胞的基因递送能力,选取不同发育阶段(胚胎期、出生后早期及青春期)小鼠进行验证(图2a–d)。结果显示,AAV-BR1在青春期小鼠中大量标记非脑内皮细胞,AAV-BI30虽改善但仍有神经元标记,而rAAV-miniBEND系统(AAV-PHP.eB-miniBEND)可显著提高脑内皮细胞的标记特异性和效率(图2e–g)。
现有rAAV载体无法经颅内注射实现脑内皮细胞的高效标记,AAV-BR1、AAV-BI30局部注射会标记大量非内皮细胞,而rAAV-miniBEND-Cre结合AAV-PHP.eB或AAV-9P13可在青春期及成年小鼠中实现脑内皮细胞高效标记,仅存在少量神经元被标记(图2h,i)。向Glut1fl/fl小鼠脑皮层局部注射AAV-PHP.eB-miniBEND-Cre病毒,可实现脑血管内皮细胞Glut1的高效敲除,敲除效率61.65±14.89%(图2j–m)。这些结果表明,通过颅内注射方式,rAAV-miniBEND系统能够实现外源基因在脑内皮细胞中的有效递送。
在胚胎期局部注射/新生期小鼠侧脑室注射实验中,单独AAV-BR1、BI30、PHP.eB无法高效转导脑内皮细胞且多标记非靶细胞,而AAV-BI30-miniBEND和AAV-PHP.eB-miniBEND均能特异性标记脑内皮细胞(图2o–r)。AAV-BI30-miniBEND对大鼠脑内皮细胞也表现出高转导效率与特异性,这表明,rAAV-miniBEND系统在小鼠与大鼠中具有优异的脑内皮靶向特异性。另外,研究证实rAAV-miniBEND系统可与多种AAV血清型(PHP.eB、BI30、BR1及9P13)兼容,显著提升脑内皮细胞的标记特异性;且有效避免外周器官脱靶效应。
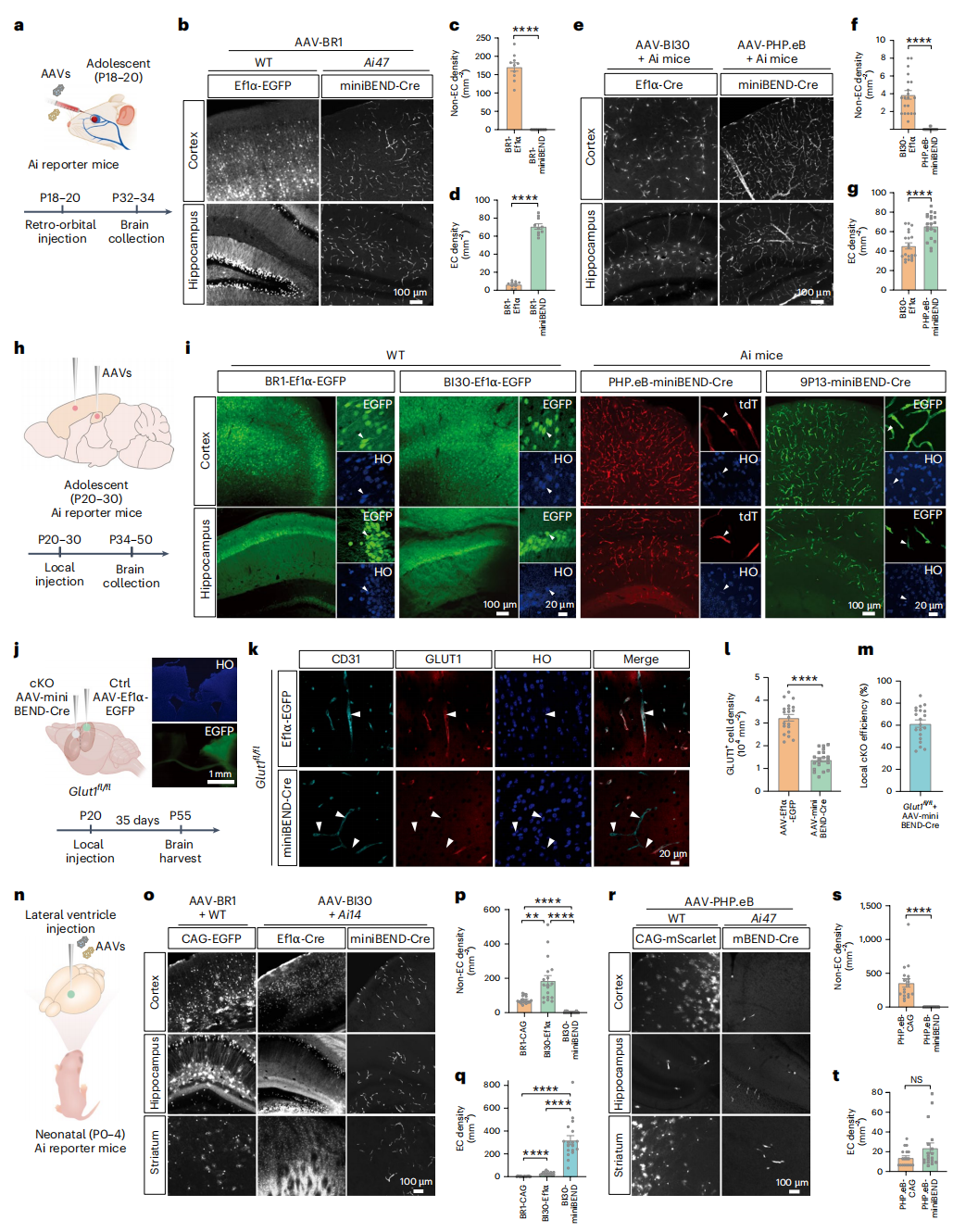
图2 rAAV-miniBEND系统向脑内皮细胞递送基因的特性分析
为增强miniBEND启动子的启动强度,研究引入内含子调控序列构建嵌合启动子(mPro1576-glo566、mPro723-glo566、mPro723-glo228),显著提高了启动强度和内皮细胞特异性,其截短版嵌合启动子(mPro723-glo566或glo228)对脑内皮细胞的标记强度不受影响,mPro723-glo228嵌合体启动子大小951bp(<1kb)(图3a-c)。经实验验证,miniBEND系统可实现外源基因持续至少3个月的稳定表达。这表明经优化的miniBEND元件(mPro723+glo228)总长仅951bp,可容纳较大外源基因并支持长期稳定的基因表达。
基于在皮肤血管畸形和CCM患者中发现MAP3K3I441M体细胞突变——该突变已被证实是小鼠模型中散发性CCM形成的关键因素,研究将突变的人源基因MAP3K3I441M克隆至rAAV-miniBEND载体,通过静脉或局部注射后(图3d),诱导出与临床散发性CCM相似的“爆米花状”脑出血,并伴随血脑屏障破坏和血管扩张(图3e–l),同时MRI检测发现小鼠出现了类似临床IV级CCM的表型(图3h)。这表明rAAV-miniBEND系统可成功用于构建小鼠散发性CCM模型。
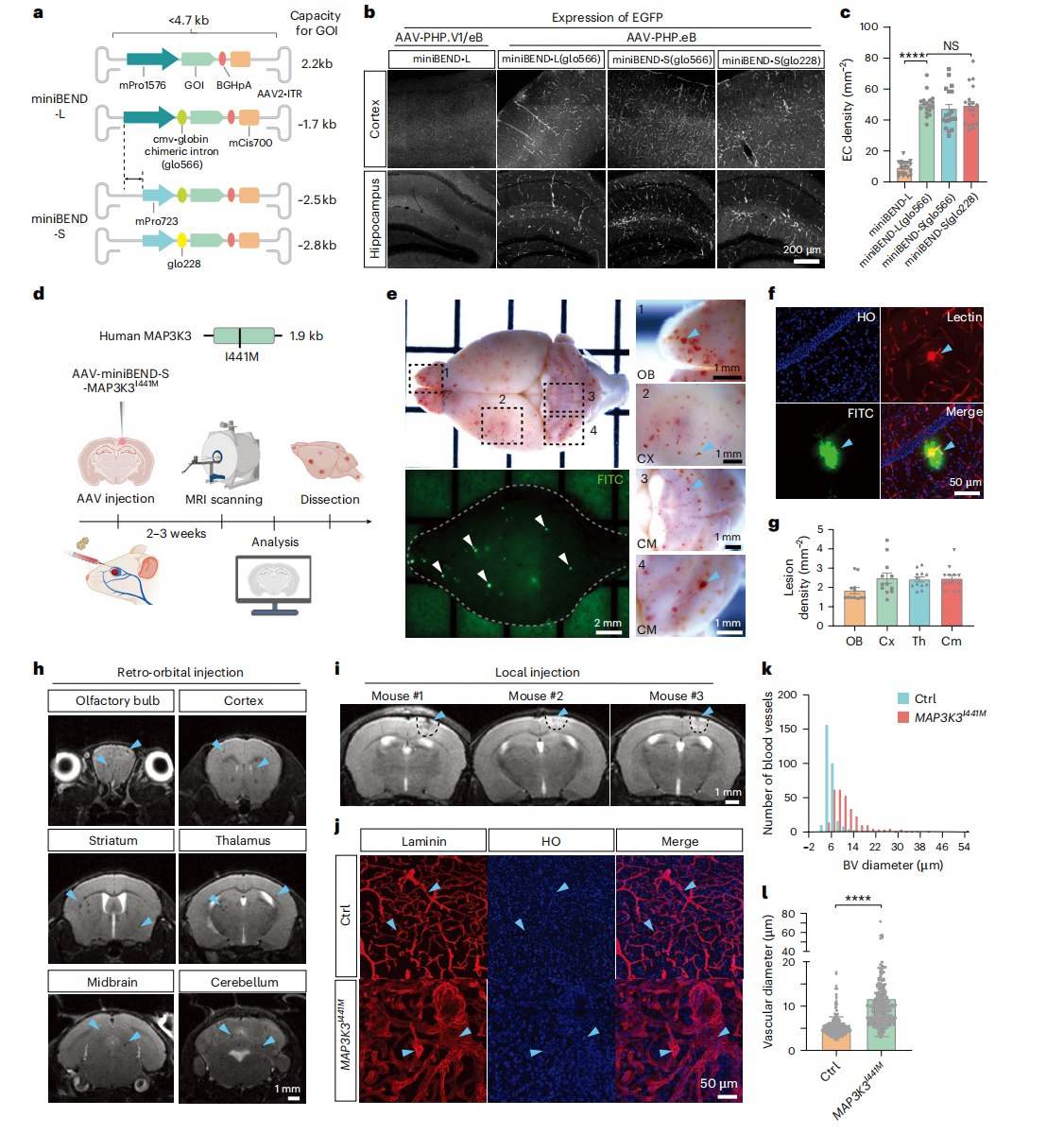
图3 利用rAAV-miniBEND系统建立脑海绵状血管畸形(CCM)模型
为利用rAAV-miniBEND系统建立bAVM模型,研究选取在bAVM患者中发现但功能未明的BrafV600E突变为研究对象。向30-50日龄Braf-CAfl/fl小鼠脑皮层/海马体局部注射AAV-PHP.eB-miniBEND-Cre病毒,诱导脑内皮细胞表达BRAFV600E突变蛋白(图4a)。结果显示该模型在数周内快速出现了脑出血、水肿、畸形血管团、组织坏死等一系列典型bAVM病理特征;另外模型小鼠出现偏瘫和癫痫等症状,3个月存活率不足50%(图4c-f)。
TUNEL和血管染色及在体实时成像显示,bAVM病变区主要由异常扩张的畸形血管主导,缺乏正常毛细血管,且血管直径随时间逐渐增大,导致局部血流动力学改变(图4g-l)。双光子成像揭示血脑屏障破坏(表现为血浆泄漏)和内皮-间充质转化(EndMT)的细胞簇,提示EndMT可能是bAVM形成的细胞学基础(图4j–n)。最后,通过乳胶灌注与PEGASOS透明成像直接证实大脑中出现动静脉分流这一bAVM最核心的病理结构(图4o,p)。
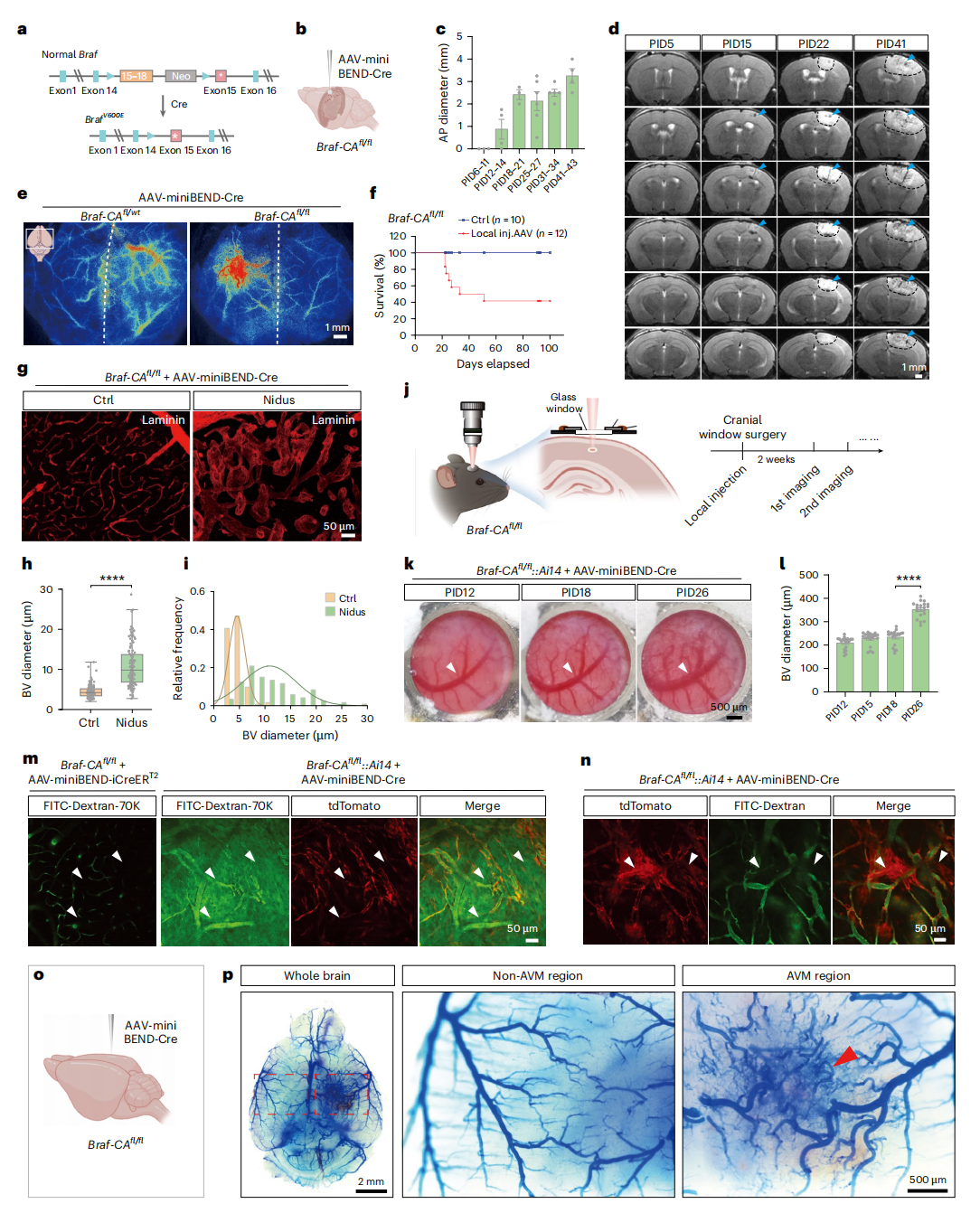
图4 利用rAAV-miniBEND系统建模bAVM
为验证该模型的治疗应用潜力,研究在诱导bAVM后使用了BRAFV600E抑制剂PLX4032(维莫非尼)进行干预。结果显示,与对照组相比,药物治疗显著减小了bAVM病变的尺寸和畸形血管的密度与直径(图5a-g)。这表明BRAF及其下游通路激活驱动bAVM发病。
综上,rAAV-miniBEND系统成功建立了BrafV600E介导的bAVM小鼠模型,该模型为脑血管畸形机制研究及药物筛选提供了新平台。
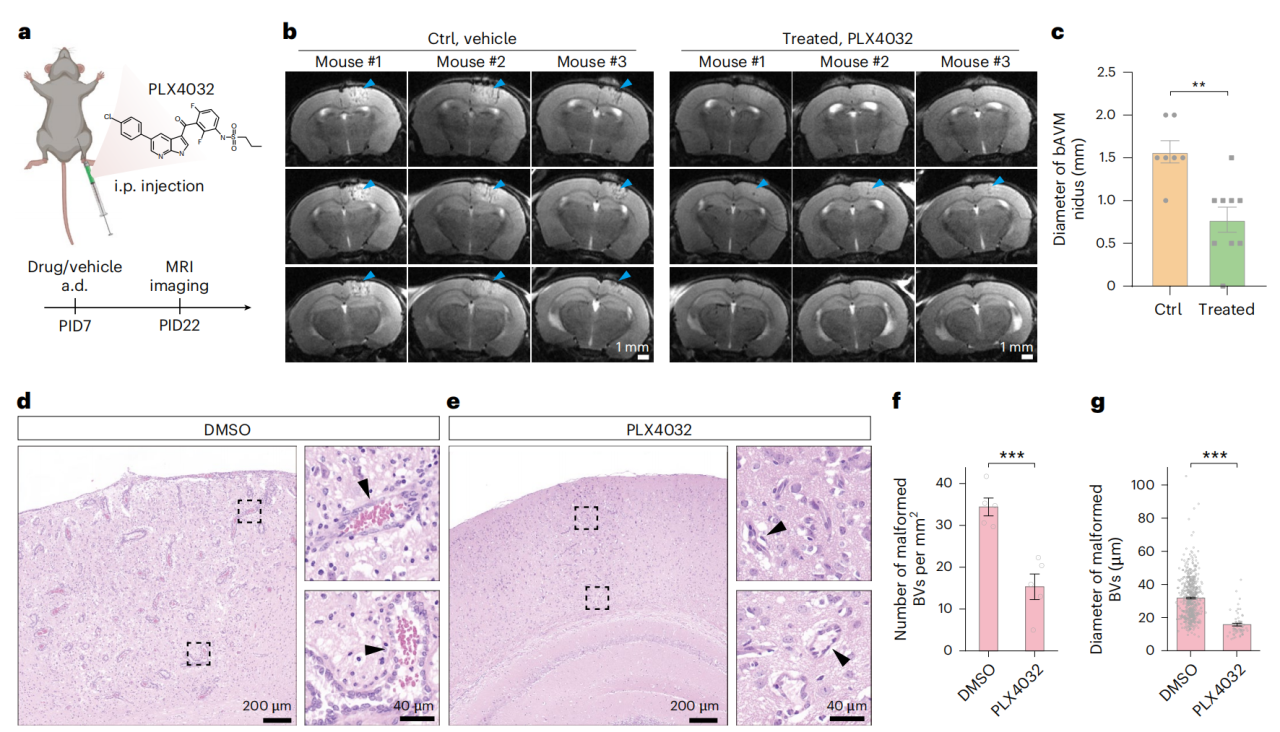
图5 PLX4032用于治疗bAVM
为阐明bAVM的分子机制,研究在Braf-CAAᶠˡ/ᶠˡ小鼠局部注射AAV-miniBEND-Cre病毒后15天(早期)和27天(晚期)后,对病变组织进行了单核RNA测序(snRNA-seq)。聚类分析发现病变区有多个阶段特异性细胞簇(图6a-c),且存在系列差异表达基因(如Slco1a4、Spock2的下调和Tll1、Ackr1的上调),这些基因的表达变化与人类bAVM患者内皮细胞转录组结果高度一致(图6d-i、7b)。
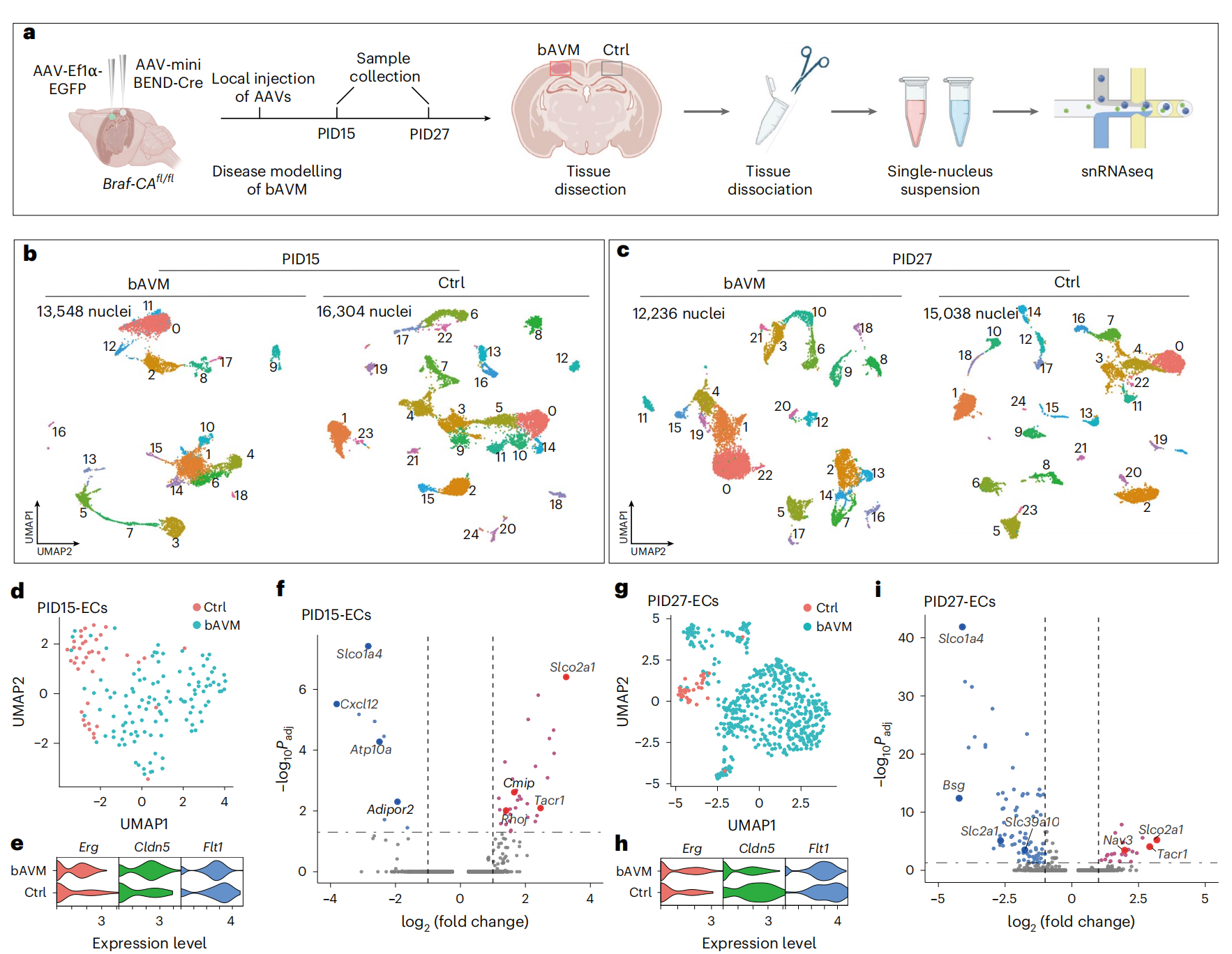
图6 单核苷酸RNA测序(snRNAseq)揭示了脑血管异常血管(bAVM)形成与发展的分子机制
随后,通过GO富集分析发现,Braf-bAVM模型中与人类患者重叠的上调基因显著富集于血管生成和上皮/内皮细胞迁移等过程(图7a);同时检测到病变内皮细胞中增殖相关基因(Mki67、Cdk1、Cdk6、Ccnd3、Gse1和Nrp2)均上调(图7b),Ki67染色证实病变区增殖细胞数量显著增多(图7c-g)。同时,病变内皮细胞的尖端细胞(Flt4、Dll4、Robo4、Kdr、Nrp2和Nrp1)和茎细胞(Notch1、Jag1和Rhoa)相关标志物基因均上调(图7h-i)这揭示bAVM病变中存在一个异常活跃的、由BRAFV600E突变驱动的病理性血管生成过程。
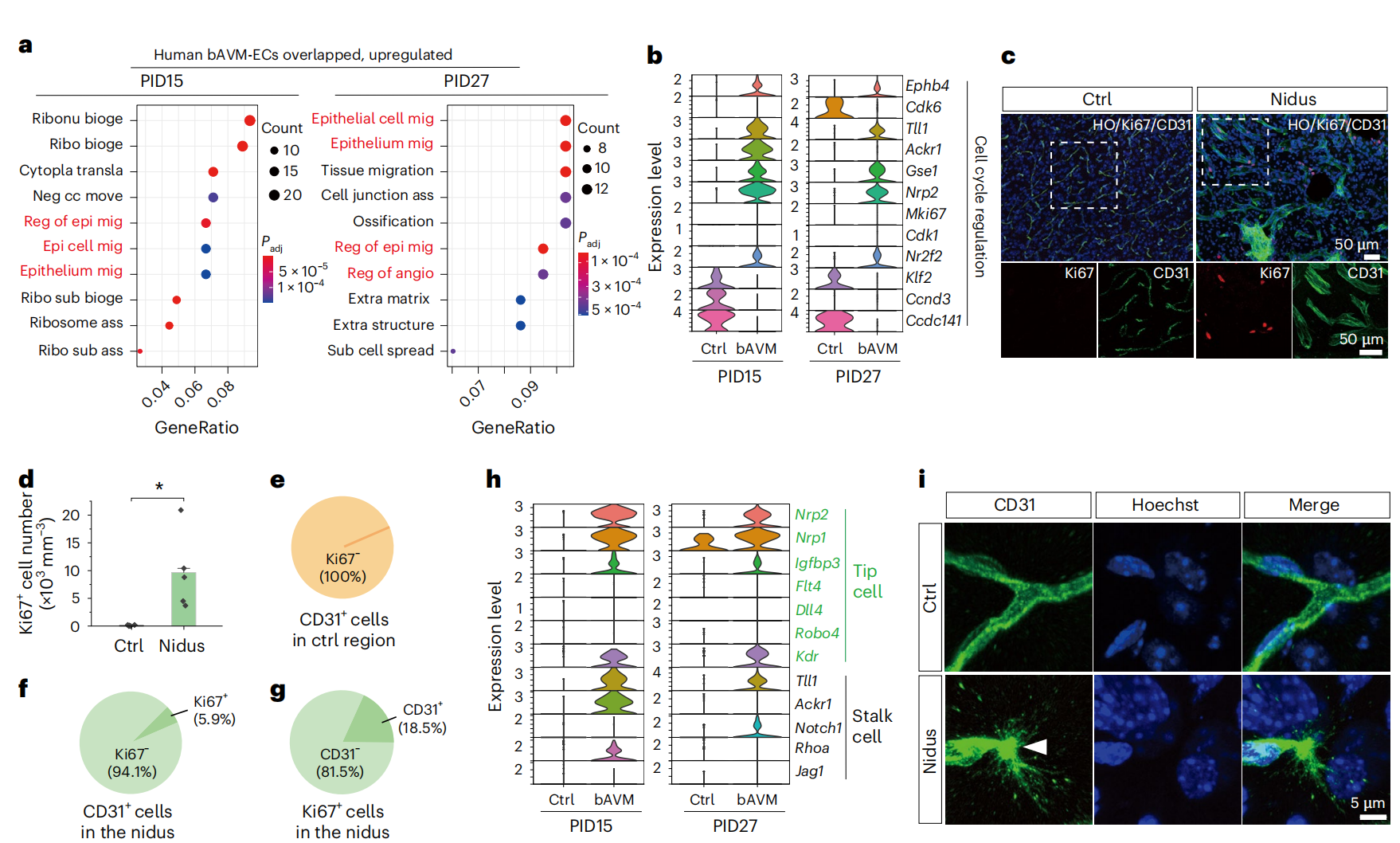
图7 鉴定脑动静脉畸形(bAVM)发病及进展的关键通路和相关基因
进一步对AAV-miniBEND-Cre处理后小鼠大脑皮层内皮细胞进行单细胞测序(scRNA-seq)(图8a),共获得5646个内皮细胞(bAVM组2624个、对照组3022个);聚类分析识别出动脉、静脉、毛细血管内皮细胞三类亚群(图8b–d),且静脉内皮细胞(vECs)比例在bAVM组中显著增加(图8e–g),其差异基因主要涉及血管炎症、内皮增殖与功能异常(图8h)。GSEA分析显示vECs中血管生成调控及ERK1/2通路正向调控显著激活(图8i–l)。这表明静脉内皮细胞在bAVM发展中起着更为关键的作用。
综上,rAAV-miniBEND介导的BrafV600E模型重现了bAVM患者的关键分子特征,揭示静脉内皮细胞在bAVM形成与进展中的核心作用。
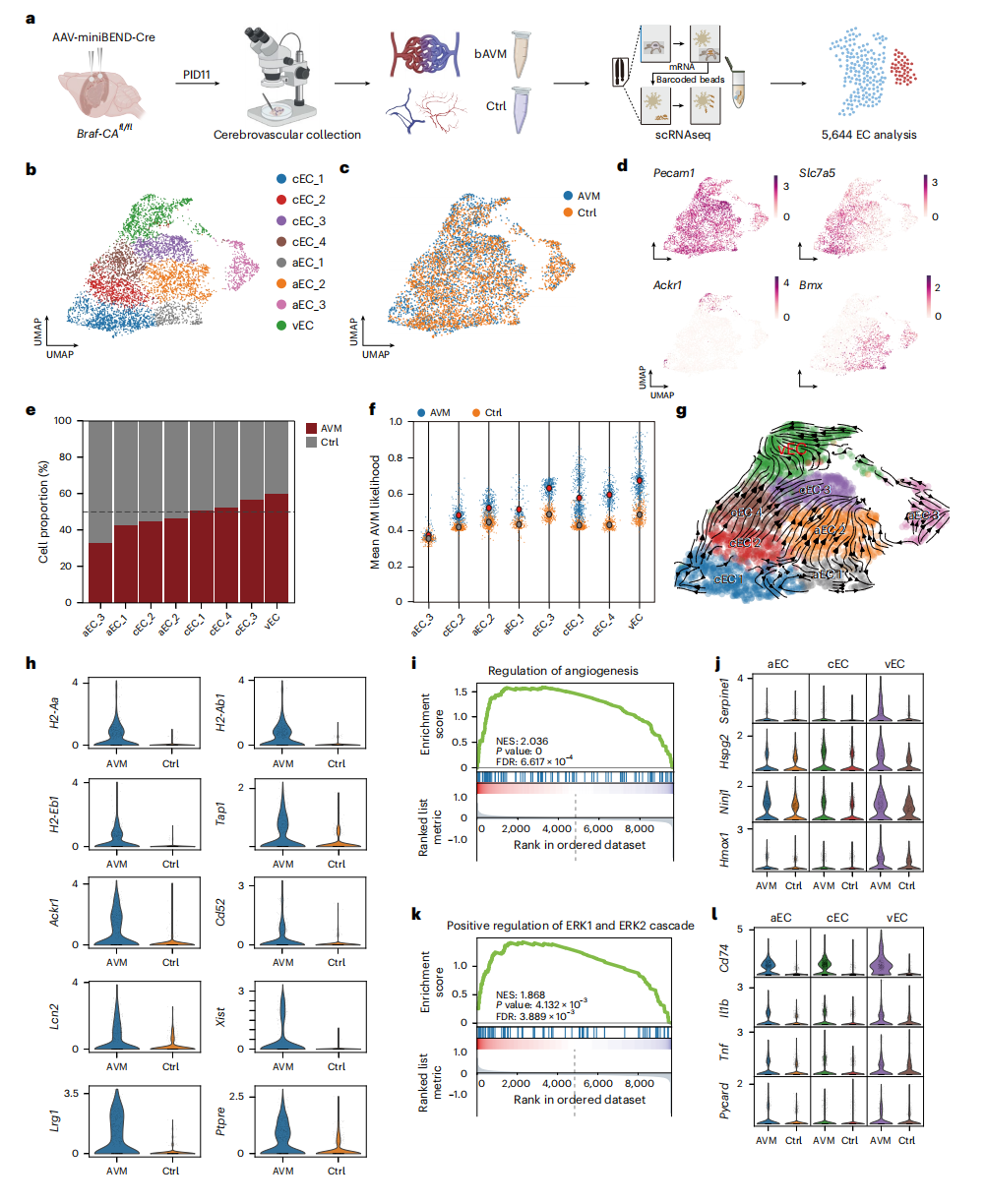
图8 BrafV600E介导的脑动静脉畸形(AVM)中脑内皮细胞的单细胞RNA测序分析
本研究基于Tek基因调控元件优化,成功开发了rAAV-miniBEND系统,实现了脑内皮细胞的高效特异性基因递送,并具有2.8kb大容量外源基因的装载能力。rAAV-miniBEND系统可支持多种注射方式(颅内/系统注射),在小鼠和大鼠的不同发育阶段实现脑内皮细胞的高效特异性靶向递送,且有效避免外周器官脱靶效应。该系统成功构建了MAP3K3I441M介导的脑海绵状血管畸形(CCM)模型以及BrafV600E介导的脑动静脉畸形(AVM)模型,可在两周内快速诱导典型病变,支持多模态实时观测,有效克服了传统模型周期长、效率低的技术瓶颈,为脑血管疾病研究提供了强大的实验工具,更有望为脑血管畸形的机制研究与治疗药物开发注入新动力。
本文使用的rAAV-miniBEND系统工具病毒,布林凯斯均可提供:

同时布林凯斯也可提供各类定制(如基因过表达、干扰等)服务,请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。