在神经科学研究中,传统石蜡切片或冰冻切片技术长期面临“碎片化”困境 —— 不仅难以完整保留神经元的长程投射路径及神经环路的复杂连接网络,还可能因机械切割导致样本结构破坏与信息丢失。而组织透明化技术的突破性发展,通过化学手段降低组织光散射、均质化折射率,实现了样本的三维成像,为神经科学从局部观察迈向系统解析提供了革命性工具。
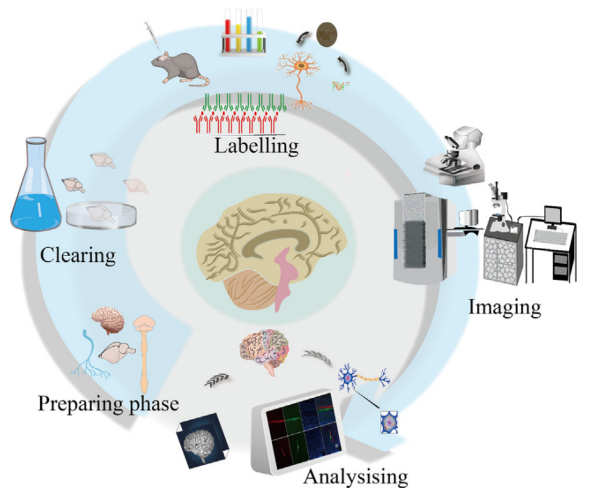
图1 组织透明化技术实现神经系统三维成像示意图
组织透明化的核心原理是通过脱脂、脱色素、脱钙等化学处理去除组织中导致光散射与光吸收的物质,同时调节样本与成像介质的折射率匹配,减少光线传播干扰以实现组织透明。目前主流技术分为三大类:①疏水性(有机溶剂)组织透明化方法依赖有机溶剂实现快速高效的大样本透明与成像,如vDISCO;②亲水性(水溶剂)组织透明化方法采用水溶性试剂兼具生物相容性与荧光保留优势,如CUBIC;③水凝胶组织透明化通过水凝胶包埋固定生物分子,最大程度保留组织结构与成分完整性,如CLARITY。
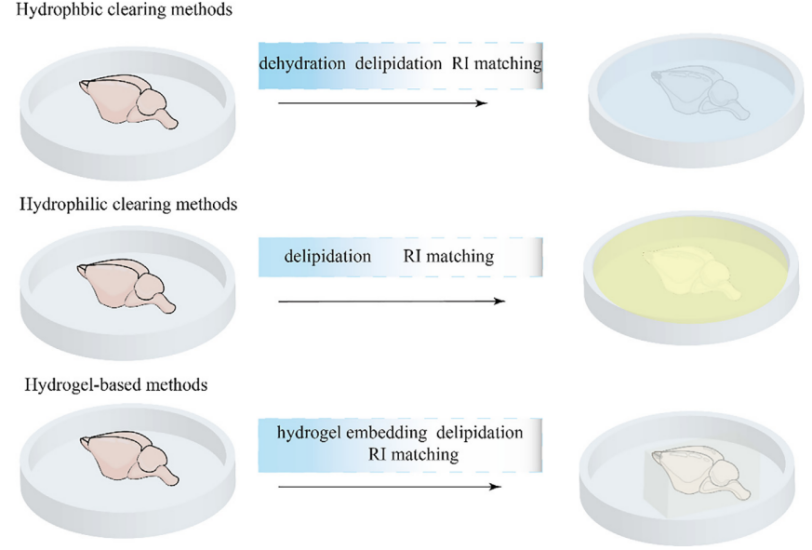
图2 三种组织透明化方法的示意图
组织透明化技术与光片显微镜(快速大体积成像)、单细胞标记技术(如病毒介导的荧光标记)、AI数据分析(如BigStitcher图像拼接、iLastik细胞分割)结合,可以实现海量成像数据的高效解析。这种技术协同模式,使组织透明化技术在神经科学领域实现了多维度突破性应用,覆盖了从大脑、脊髓等中枢神经组织到肝脏、肾脏、心脏等外周器官,从基础神经环路绘制到临床疾病机制解析的广泛场景。
研究团队采用AdipoClear透明化方法,将固定后的小鼠整脑经抗体标记和DBE折射率匹配处理,结合光片显微镜实现全脑FOS信号的三维成像与定量分析。结果显示,脂多糖(LPS)处理后小鼠孤束核与最后区(NTS-AP)FOS阳性神经元显著增多,通过三维重构技术可清晰呈现脑干迷走背侧复合体内激活细胞的密集分布,并动态追踪到全脑多个脑区在免疫刺激下的神经元活动变化。该透明化成像策略首次实现了免疫应激状态下全脑神经元激活的时空动态图谱绘制,精准定位了NTS-AP区域为免疫-脑互作的关键中枢节点,为后续深入解析相关神经环路调控机制提供了重要的结构基础。
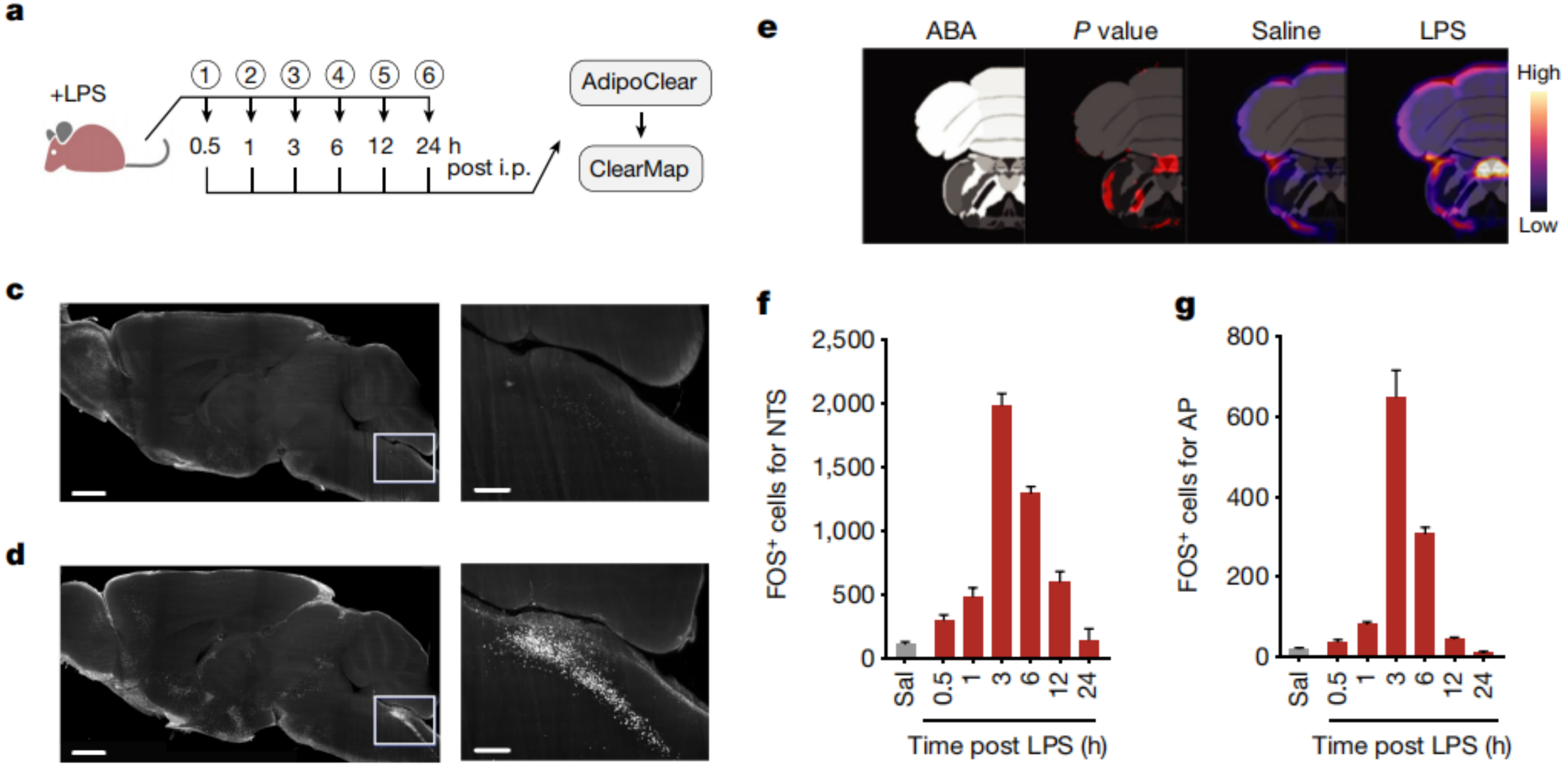
图3 疾病行为期间全脑活动变化[4]
研究人员将AAV-flex-tdTomato与多病毒交叉标记策略联用,对完整脊髓标本进行脱钙-透明化处理后,采用光片显微镜完成纵向连续成像,实现脊髓内特定神经元亚群轴突投射的三维可视化。研究结果在单细胞分辨率下完整呈现了胸段Vsx2+神经元向腰段步行中枢的密集长程投射轨迹,并直观验证了损伤-再生轴突与自然投射模式的高度重叠。该透明化-光片成像体系不仅系统描绘了分子定义神经元亚群的自然连接组,也为后续判定“靶向腰段再生即可重建步行功能”提供了直观而全面的解剖学证据。
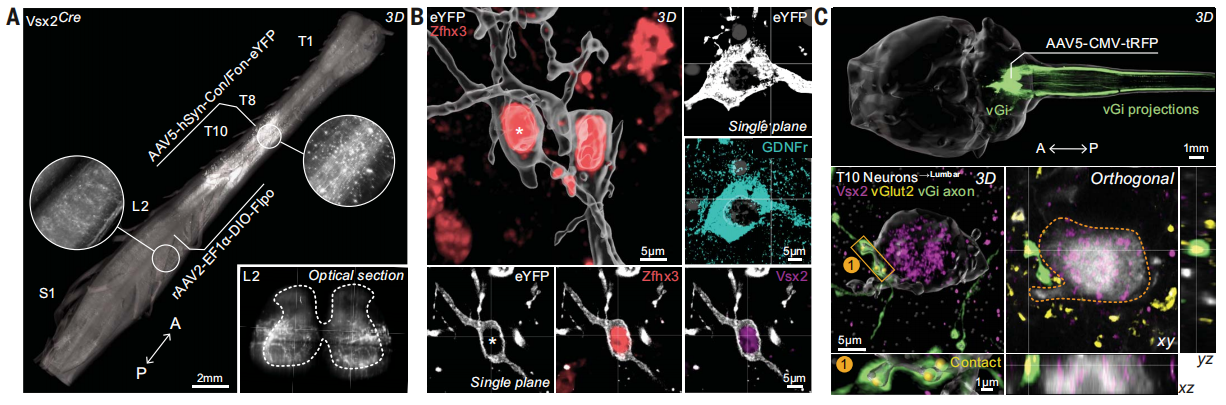
图4 神经元连接与投射特征[5]
研究团队采用优化后的iDISCO+全组织免疫标记-光片成像流程,对小鼠、非人灵长类及人类肝脏进行透明化处理,通过高效脱脂与折射率匹配实现光学均质。透明化肝脏在光片显微镜下三维扫描,结合Imaris重建分析,首次在单轴突水平获得肝内交感神经纤维的完整空间图谱。结果显示,肝实质内TH阳性交感轴突沿门三联呈树状分支,密度高且与血管紧密并行,而副交感纤维几乎缺失,证实肝脏神经支配以交感为主的核心特征。进一步研究发现,高脂饮食(HFD)干预20周后,肝内交感轴突密度下降超过50%,形成“交感神经病变”,而该病变可通过肿瘤坏死因子-α(TNF-α)中和抗体处理或Sarm1基因敲除实现逆转;同时,热量限制或瘦素替代治疗4周可使轴突密度完全恢复,这也为代谢性疾病的治疗提供了新的靶点。
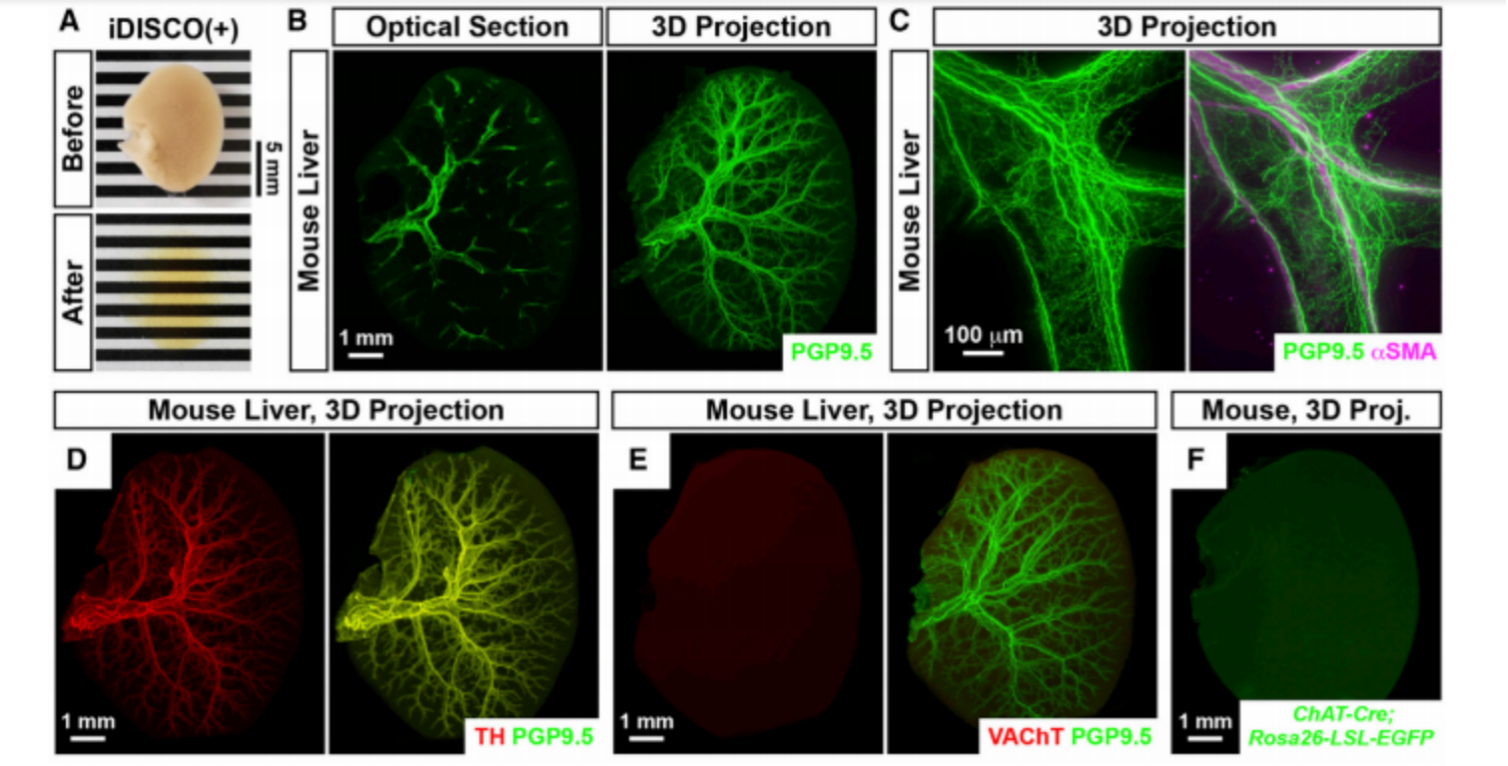
图5 小鼠和灵长类动物肝脏的三维神经解剖学[6]
研究团队采用CLARITY-SHIELD主动透明化技术结合光片荧光显微镜,对0-75岁人类肾脏厚切片样本进行多标记免疫染色与多尺度三维成像,快速构建覆盖皮质-髓质轴的神经-血管-肾单位连接图谱。结果显示,肾小球随发育呈极性朝向并聚集成“社区”,通过“母肾小球”节点形成可重复的中心-辐射神经网络,实现跨肾单位信息同步;同时,肾脏神经网络呈现显著的动态变化,新生儿肾脏神经网络分布稀疏,成年期达到峰值,而老年或者糖尿病、积水患者肾脏则出现神经连接减少、硬化单元过度连接或全域神经退行性变三种病态重构。揭示人肾神经-肾单位社区的发育规律与疾病相关重塑,为理解肾脏协同调控和干预慢性肾病提供三维结构基础。
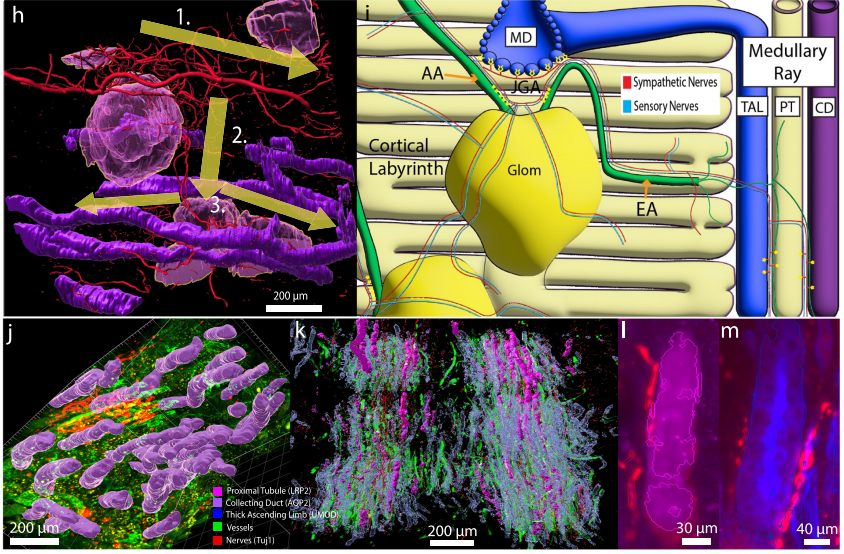
图6 三维形态计量学分析[7]
案例5
外周-中枢连接研究:脑-肝神经调控环路的完整解析
研究团队利用PRV-CAG-mRuby3病毒示踪结合vDISCO透明化技术,首次实现从肝脏到大脑的全脑-肝脏神经回路的三维可视化,突破了跨器官神经环路成像的技术瓶颈。研究结果清晰揭示了从肝脏到侧旁巨细胞核(LPGi)、再到下丘脑室旁核(PVH)以及腹内侧下丘脑(VMH)的神经投射路径,明确了该环路的层级结构与关键节点。这一发现为深入探究肝脏与大脑之间的神经调控机制提供了完整的解剖学基础,比如该环路可能参与肝脏代谢(如糖脂代谢)、免疫功能的中枢调控,为理解代谢性疾病(如糖尿病、肥胖)的中枢调控机制提供了全新视角。
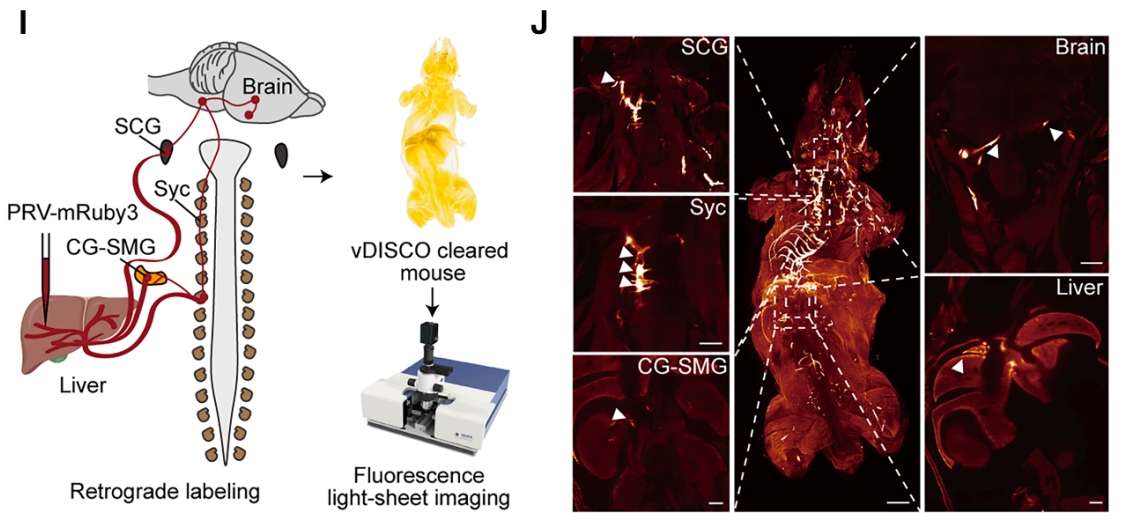
图7 PRV标记脑-肝神经回路的示踪方案和整体成像[8]
组织透明化技术通过疏水性、亲水性、水凝胶三大主流技术路径,成功实现了神经组织从单细胞到全器官尺度的无损伤三维成像,其技术本质是通过化学与物理手段重构组织光学特性,同时最大限度保留生物结构与分子信息,彻底突破了传统切片技术的碎片化局限。该技术与光片显微镜、单细胞标记、AI数据分析等技术的深度融合,在神经环路绘制、神经退行性疾病机制解析、外周神经-器官交互作用研究及临床病理样本分析等多个领域展现出强大的应用价值,为神经科学研究从局部观察向系统解析的跨越提供了核心技术支撑。
布林凯斯公司可提供专业的组织透明化服务,涵盖大脑、肝脏、脊髓等多种样本类型,为科研人员提供一站式技术支持。
参考文献
[1] Ueda HR, Ertürk A, Chung K, et al. Tissue clearing and its applications in neuroscience. Nat Rev Neurosci. 2020;21(2):61-79. doi:10.1038/s41583-019-0250-1
[2] H. Mai, D. Lu. Tissue clearing and its applications in human tissues: A review. VIEW. 2024, 5, 20230046. https://doi.org/10.1002/VIW.20230046.
[3] He C, Yuan Y, Gong C, Wang X, Lyu G. Applications of Tissue Clearing in Central and Peripheral Nerves. Neuroscience. 2024;546:104-117. doi:10.1016/j.neuroscience.2024.03.030
[4] Ilanges A, Shiao R, Shaked J, Luo JD, Yu X, Friedman JM. Brainstem ADCYAP1+ neurons control multiple aspects of sickness behaviour. Nature. 2022;609(7928):761-771. doi:10.1038/s41586-022-05161-7
[5] Squair JW, Milano M, de Coucy A, et al. Recovery of walking after paralysis by regenerating characterized neurons to their natural target region. Science. 2023;381(6664):1338-1345. doi:10.1126/science.adi6412
[6] Liu K, Yang L, Wang G, et al. Metabolic stress drives sympathetic neuropathy within the liver. Cell Metab. 2021;33(3):666-675.e4. doi:10.1016/j.cmet.2021.01.012
[7] McLaughlin L, Zhang B, Sharma S, et al. Three dimensional multiscalar neurovascular nephron connectivity map of the human kidney across the lifespan. Nat Commun. 2025;16(1):5161. Published 2025 Jun 3. doi:10.1038/s41467-025-60435-8
[8] Wang J, Sun X, Gong X, et al. Galnt2 neurons in the ventromedial hypothalamus counterregulate hypoglycemia via a brain-liver neurocircuit. Cell Metab. 2025;37(11):2264-2279.e10. doi:10.1016/j.cmet.2025.09.006