膜片钳技术是现代电生理学的革命性突破,凭借对细胞膜电信号的超高精度捕捉能力,成为解析细胞生理功能的核心工具。其原理是通过电极拉制仪将玻璃微电极尖端拉制成直径 1.5~3.0μm 的细微端口,利用负压吸引使端口与细胞膜形成千兆欧姆级高阻封接,将端口内的细胞膜区域与周围电隔离,再通过人工钳制该区域膜电位,实现对膜片上离子通道电流的精准监测与记录。
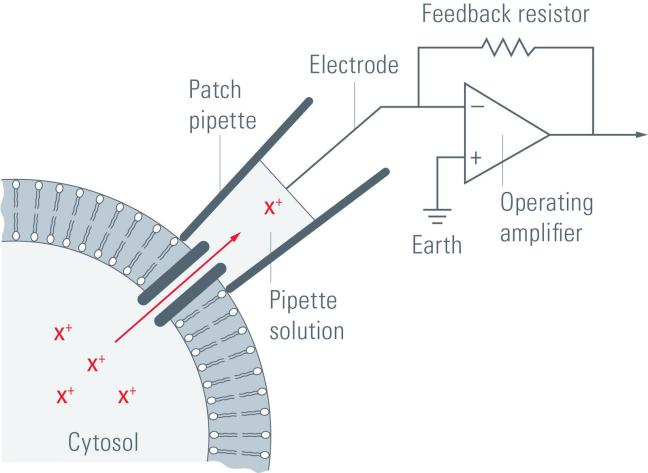
图1 膜片钳的技术原理
膜片钳技术有 4 种经典记录模式,包括细胞贴附模式(cell-attached mode)、膜内面向外模式(inside-out mode)、膜外面向外模式(outside-out mode)、全细胞模式(conventional whole-cell mode)。
可针对不同研究目标灵活选择:细胞贴附模式为非侵入式,保留细胞原生微环境,用于记录单离子通道自发活动;膜内面向外模式使胞质侧暴露,可调控胞内因子,解析胞内信号依赖型通道机制;膜外面向外模式让膜片胞外侧接触灌流环境,模拟胞外信号刺激,检测配体门控通道药物敏感性;全细胞模式突破封接膜片,记录神经元整合性电活动,用于动作电位、突触后电流及神经元兴奋性研究 。
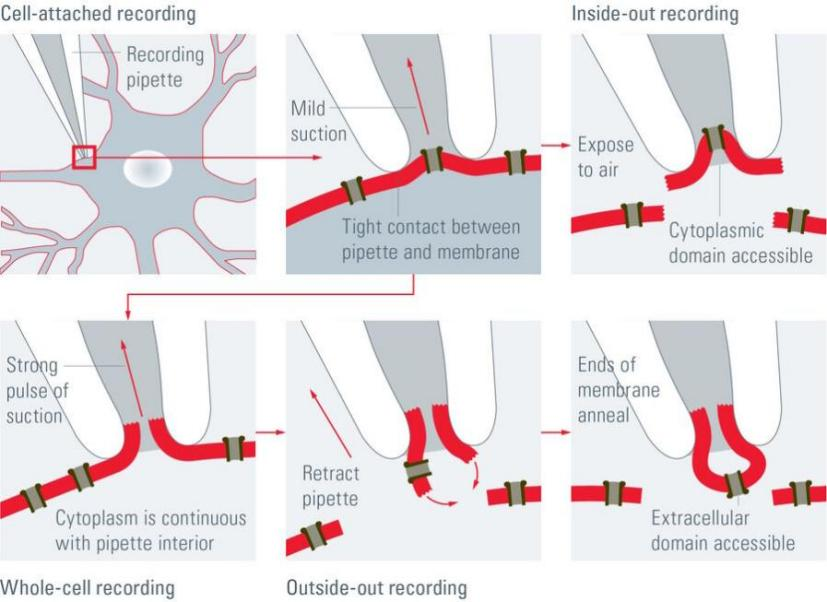
图2 膜片钳的4种基本记录模式
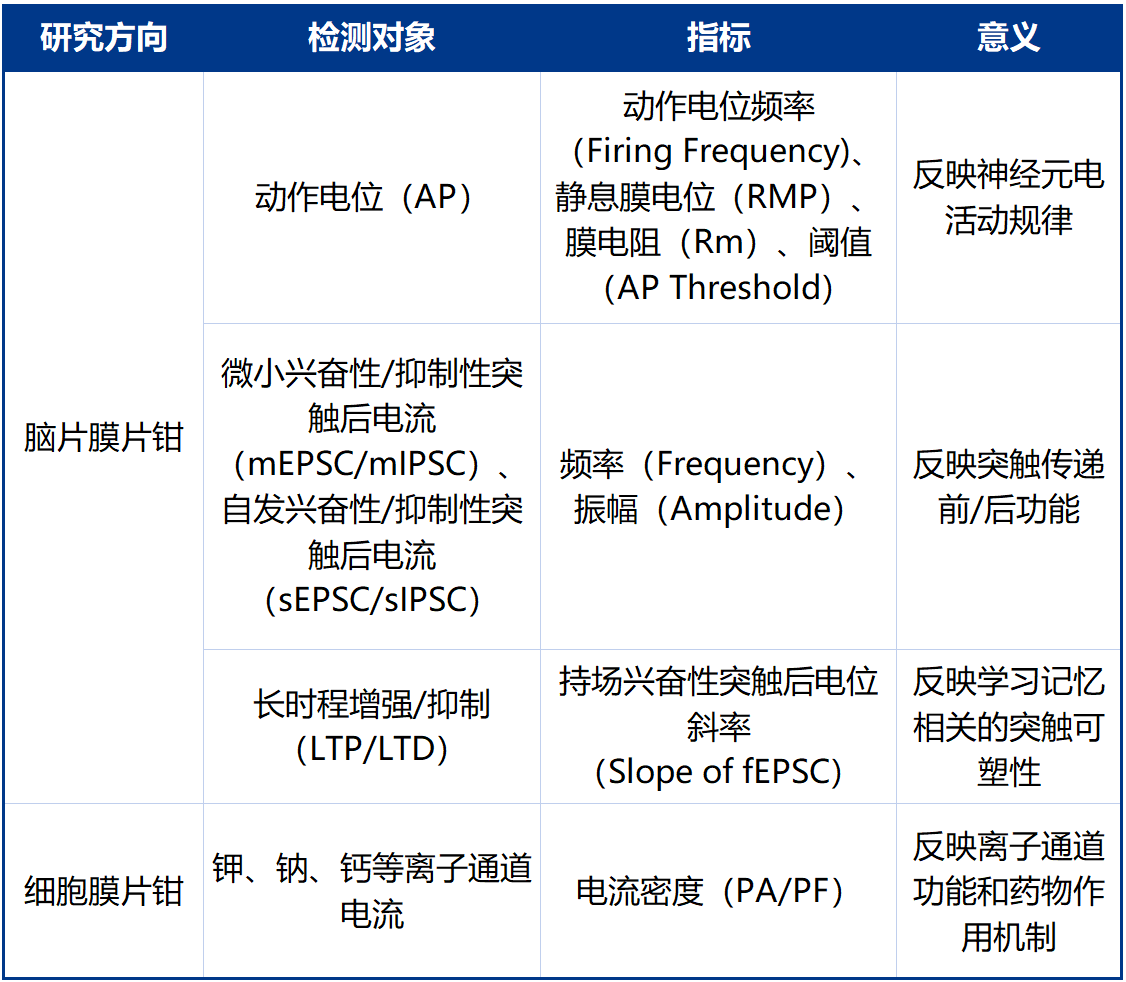
服务类型涵盖神经细胞、心肌细胞、肌肉细胞、干细胞与免疫细胞等,可精准记录单细胞膜电流、动作电位及受体-通道动力学,用于阐明离子通道在细胞兴奋性、信号转导及药物作用中的关键角色。
服务以不同脑区的急性脑片为对象,既可在单细胞水平解析突触传递,又能保留局部微环路,支持 LTP/LTD、网络振荡及神经药理学研究,为脑功能与疾病机制提供高保真数据。
01、需求沟通:明确研究目标、细胞类型和组织样本类型及检测指标;
02、方案定制:根据需求设计实验方案,包括记录模式选择、刺激范式优化、样本量确定;
03、细胞培养/组织样本制备:包含实验细胞系的前期培养以及小鼠脑片切片、预处理,确保样本符合实验要求;
04、信号记录:采用高精度膜片钳系统完成电信号采集,全程监控数据质量;
05、数据分析:通过 pClamp 等专业软件进行数据统计分析;
06、结果交付:提供原始数据、分析结果及完整实验报告。
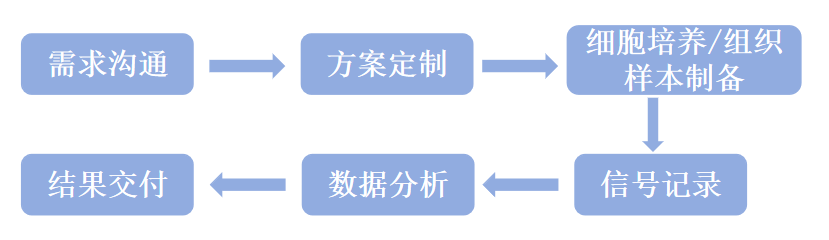
实验周期通常约 1个月,具体周期将根据实验方案的复杂程度确定。
• 原始数据:信号记录原始 pClamp 文件;
• 分析结果:有效数据统计结果、组间统计学分析表格;
• 项目报告:含实验方法、分析图表及结论,完整呈现实验过程与结果。
案例一:
为阐明慢性束缚压力对成本–收益决策的相关机制,实验将成年 C57BL/6J 雄鼠随机分为对照组(Control)与实验组(Exp,慢性束缚压力组),实验组每日束缚 6h,持续 14d 以模拟人类慢性应激,对照组无束缚处理。随后制备含腹内侧前额叶皮层(PL)的冠状脑片(厚度 300 μm),脑片置于 32°C、持续氧合的人工脑脊液(aCSF)中孵育。采用全细胞电流钳模式在 PL 脑区第 Ⅴ 层锥体神经元记录动作电位(AP)发放,以 - 70mV 为起始静息电位,给予 0~140pA、步阶 20pA、时长 600ms 的去极化电流刺激。结果显示当刺激强度为 100、120、140pA 时,实验组 AP 发放个数显著高于对照组(P<0.01),而两组的静息膜电位(RMP)、膜电阻(Rm)无统计学差异,这表明慢性束缚压力通过上调 PL 锥体神经元增益,使决策相关微环路对同等输入产生过度放电,从而干扰价值编码、诱发短视决策偏向。
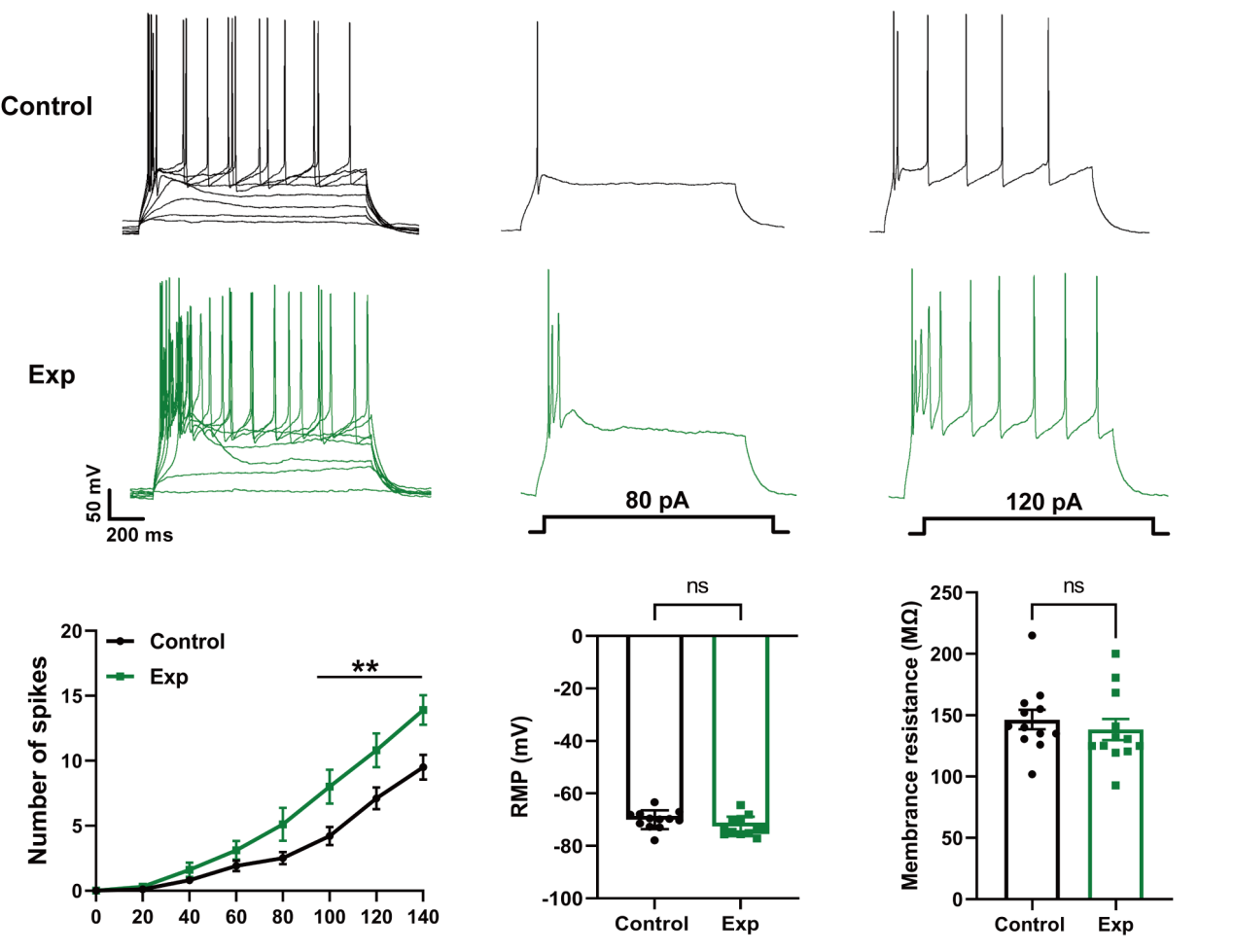
图3 AP记录结果展示:不同刺激强度下的 AP 原始记录图,AP 发放个数、静息膜电位、膜电阻的组间对比统计图。
案例二:
为阐明高脂饮食(high-fat diet, HFD)诱导的肥胖对记忆灵活性的突触机制,实验将 8 周龄 C57BL/6J 雄鼠随机分为对照组(Control)与实验组(Exp),对照组给予标准饲料喂养,实验组给予高脂饲料喂养,连续 12 周建立饮食性肥胖模型。制备含背侧海马 CA1 区的水平脑片(厚度 300 μm),脑片在 32°C、aCSF中维持活性,采用全细胞电压钳模式,分别以 - 70mV、0mV 为钳制电位,记录自发兴奋性突触后电流(sEPSC)与自发抑制性突触后电流(sIPSC),每组记录 10 个有效神经元,每个神经元连续采集 5min 数据。结果显示与对照组相比,实验组 sEPSC 的频率与振幅显著升高(P<0.001),sIPSC 的频率与振幅也显著升高(P<0.01),提示长期高脂摄入通过协同上调 CA1 锥体神经元的兴奋-抑制突触强度,从而影响海马脑区与记忆相关环路。
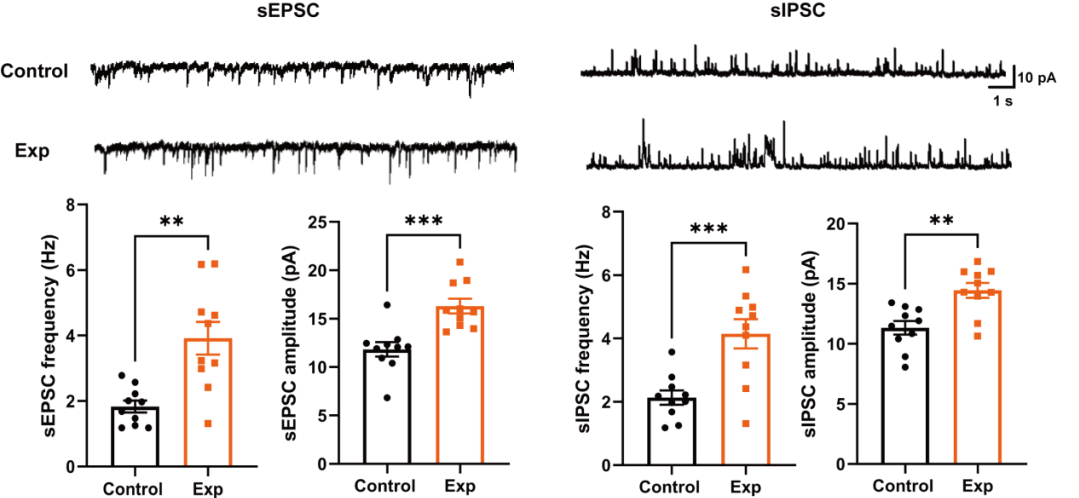
图4 sEPSC和sIPSC记录结果展示:sEPSC、sIPSC 原始记录图,两类电流频率、振幅的组间对比统计图。
案例三:
为阐明早期社交隔离(isolation rearing,ISO)提升成年攻击性的前额叶兴奋-抑制失衡机制,实验将C57BL/6J雄性小鼠随机分为群居对照(Control,5只/笼)与社交隔离组(ISO,单笼饲养P21-P63),于P63 时急性分离内侧前额叶皮层(mPFC)原代锥体神经元,神经元分离后4h 内完成记录。实验采用全细胞电压钳模式,电压协议设定以 - 100mV 为钳制电位,阶跃至 -60~+60mV(步阶 20mV,持续 50ms,间隔 5s),采用 P/4 在线漏减技术校正漏电流,专一记录电压门控钠通道电流(Nav 电流)。结果显示当钳制电位为 - 40mV 与 - 20mV 时,实验组的 Nav 电流峰值密度显著高于对照组(P<0.05),表明早期社交隔离通过上调 mPFC 锥体神经元的 Nav 电流密度,增强前额叶神经元的兴奋性,打破兴奋 - 抑制平衡,最终导致成年期攻击性升高。
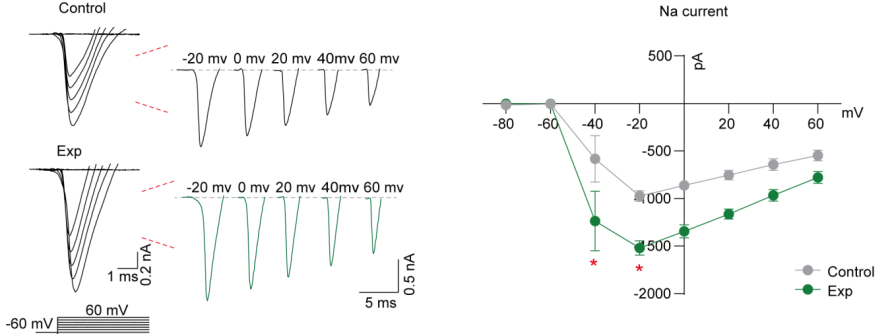
图5 钠离子通道记录结果展示:不同钳制电位下的 Nav 电流原始记录图,电流密度的组间对比统计图。