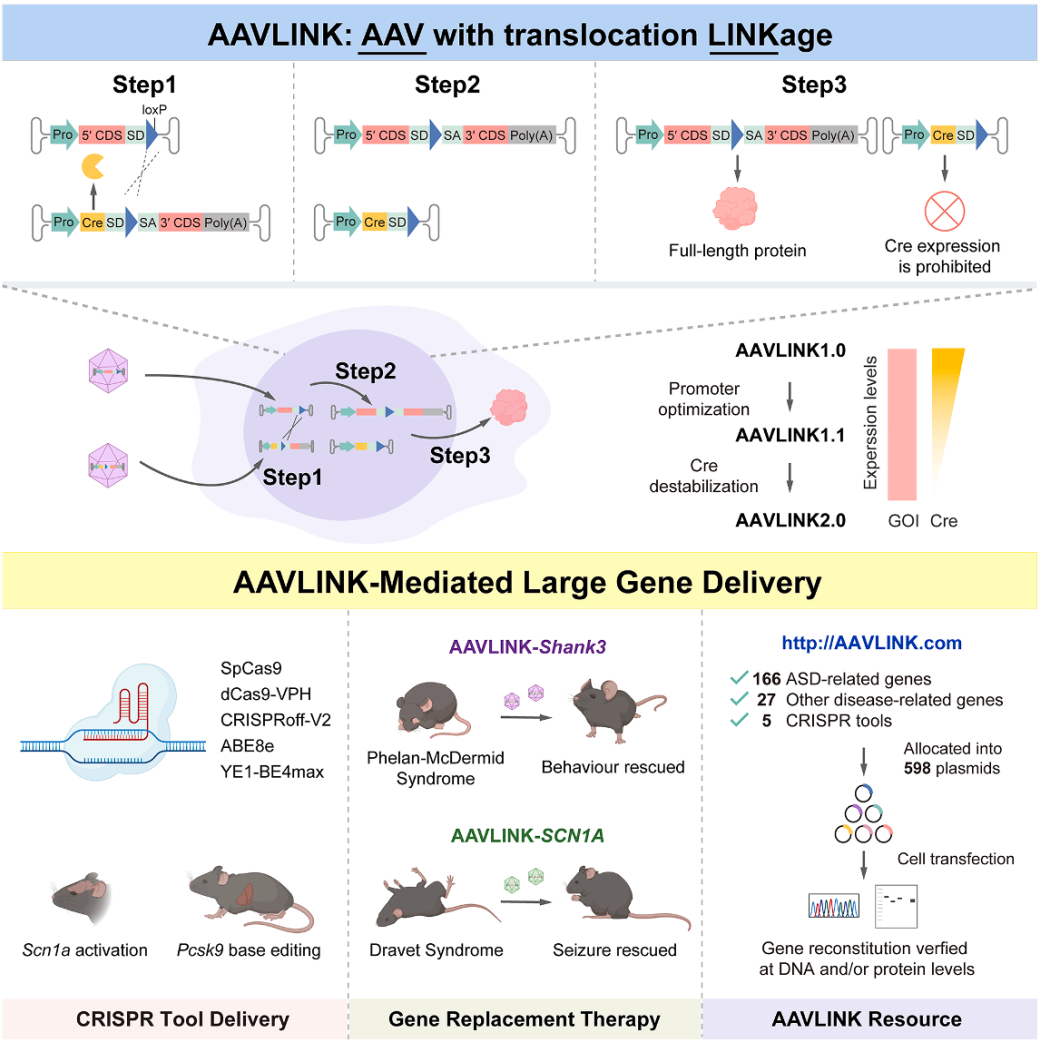
腺相关病毒(AAVs)是基因治疗的常用载体,具有无致病性、可感染分裂/ 非分裂细胞、长期表达等优势,但常规包装容量仅<5kb,无法递送超长治疗基因,限制了其在大基因相关遗传病中的应用。传统解决方案(DNA反式剪接、RNA反式剪接、蛋白反式剪接)存在重组效率低、依赖特定拆分位点、易产生截短蛋白等问题。

2026年2月5日,中国科学院深圳先进技术研究院路中华、刘太安团队与北京大学第一医院姜玉武团队合作在Cell上发表了最新研究:“AAVLINK: A potent DNA-recombination method for large cargo delivery in gene therapy”,开发了AAVLINK这一高效基因递送平台,通过Cre/lox介导的DNA重组技术,突破了AAV的包装容量限制(常规<5kb),可高效递送超长治疗基因(双载体系统可覆盖<6.2kb基因,三载体系统最高可达11kb)和CRISPR工具,且副产物少、安全性高;其升级版本AAVLINK2.0通过优化启动子和添加蛋白不稳定标签降低Cre表达,进一步提升生物安全性;该平台成功在小鼠模型中拯救了Phelan-McDermid综合征(Shank3基因)和Dravet综合征(SCN1A基因)的相关表型,还构建了包含193个疾病相关大基因和5个CRISPR工具的载体库(http://AAVLINK.com/),为大基因相关遗传病的基因治疗提供了强有力的技术支持和资源储备。
双载体设计中,一载体含启动子、目的基因(GOI)5'端、剪接供体(SD)及lox位点;另一载体含启动子、Cre重组酶、lox位点,剪接受体(SA)、GOI 3'端及多聚腺苷酸化(poly(A))信号。两载体共递送至目标细胞后,先产生Cre(步骤1),随后,Cre介导的重组会将第一个载体中的(目的基因5'端-SD)元件与第二个载体中的(SA-目的基因3'端)元件连接起来。在此过程中,Cre表达元件会与SA和3'端poly(A)信号分离,从而限制其后续表达(步骤2)。最终,内含子剪切后,全长目的基因得以重组并表达(步骤3)(图1A)。
为了降低Cre介导易位的可逆性,采用左/右回文臂突变的不对称lox位点(LE/RE)。二者重组产生野生型loxP及双臂突变lox位点,后者无法作为Cre底物,使易位基本不可逆。通过电泳条带比值分析重组效率,证实loxJT15(LE)与loxJTZ17(RE)组合效果最优(图1B)。Sanger测序验证全长EYFP精准重组,此二者被用于AAVLINK设计。AAVLINK中,GOI 5'端mRNA含未剪切SD且无poly(A)信号,3'端作为Cre下游非翻译区转录,故截短蛋白极少,WB检测无截短EYFP(图1C)。时序分析显示EYFP 60小时达峰后稳定,Cre 60小时起显著下降至84小时基础水平(图1D),这是其两大核心优势。将拆分EYFP包装于双载体,仅共转染时培养细胞及小鼠皮层出现荧光,无Cre则无信号(图1E、1F)。食蟹猴大脑实验获类似结果,彰显转化潜力(图1G)。综上,AAVLINK可在体外体内高效精准重组拆分基因,且副产物少。
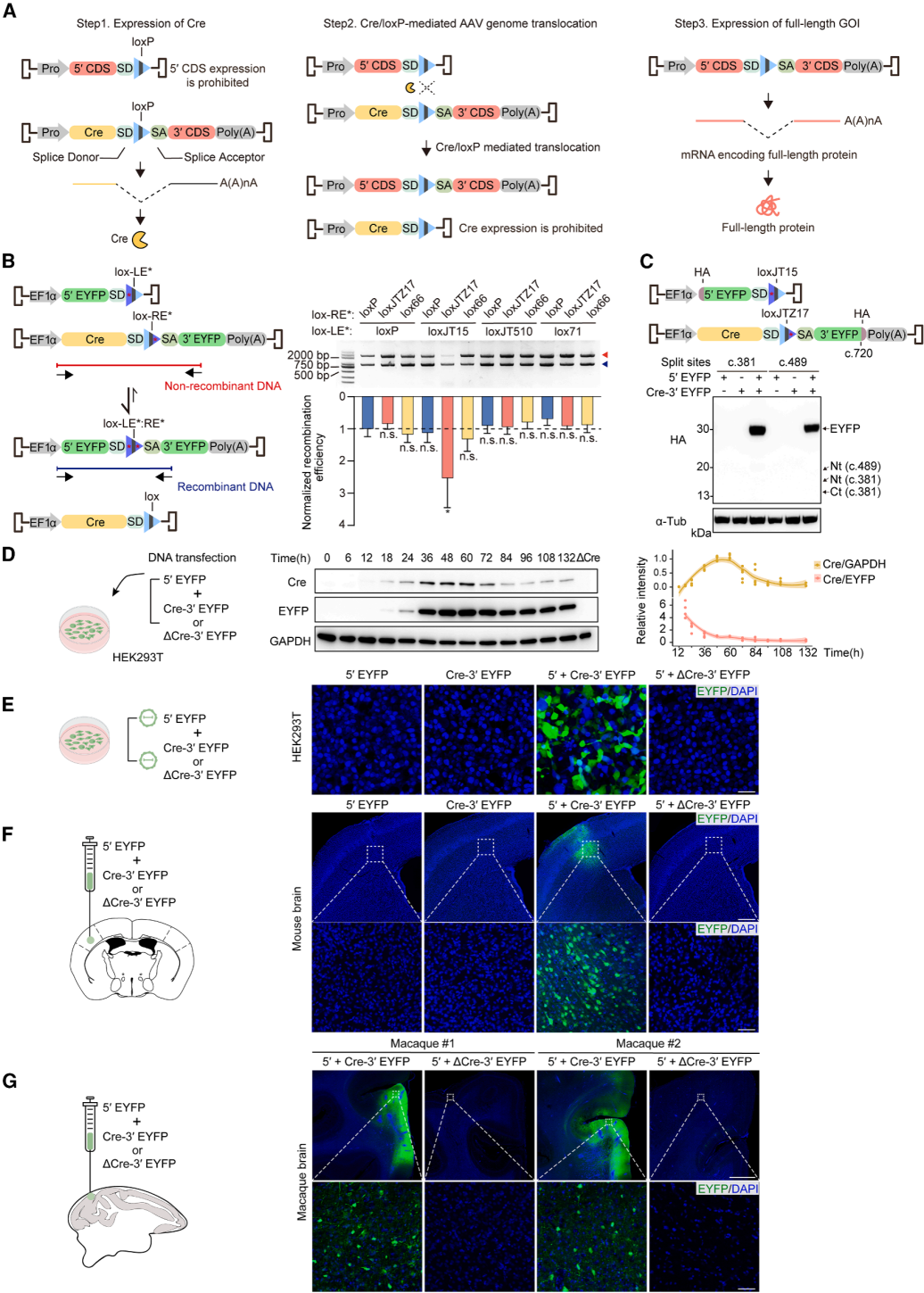
图1. AAVLINK的设计与优化
为了承载双载体无法容纳的更大基因,作者验证了三分体AAVLINK载体的效能。该系统需两对lox位点组装拆分GOI:第一对介导5'端与中间片段重组,第二对含loxJT15/loxJTZ17臂突变及lox2272间隔区突变,介导3'端易位至中间片段下游,lox2272可避免与野生型间隔区lox位点交叉反应(图2A、2B)。为了验证设计,将TagRFP基因拆分为三段并分配至载体(图2C)。HEK293T细胞共转导后,Sanger测序证实全长TagRFP精准重组,WB检测显示其高效表达且无截短产物(图2D)。上述载体分别包装为三个rAAV,转导哺乳动物细胞后,仅三载体共存在且Cre有活性时检测到TagRFP信号(图2E)。体内实验也证实,其在小鼠及食蟹猴皮层高效重组(图2F、2G),结果表明AAVLINK可装载超大基因。单个rAAV基因组容量约4.7kb,排除ITRs、Cre及调控元件后,三载体系统可递送高达11kb遗传物质,覆盖多数人类遗传病相关基因。
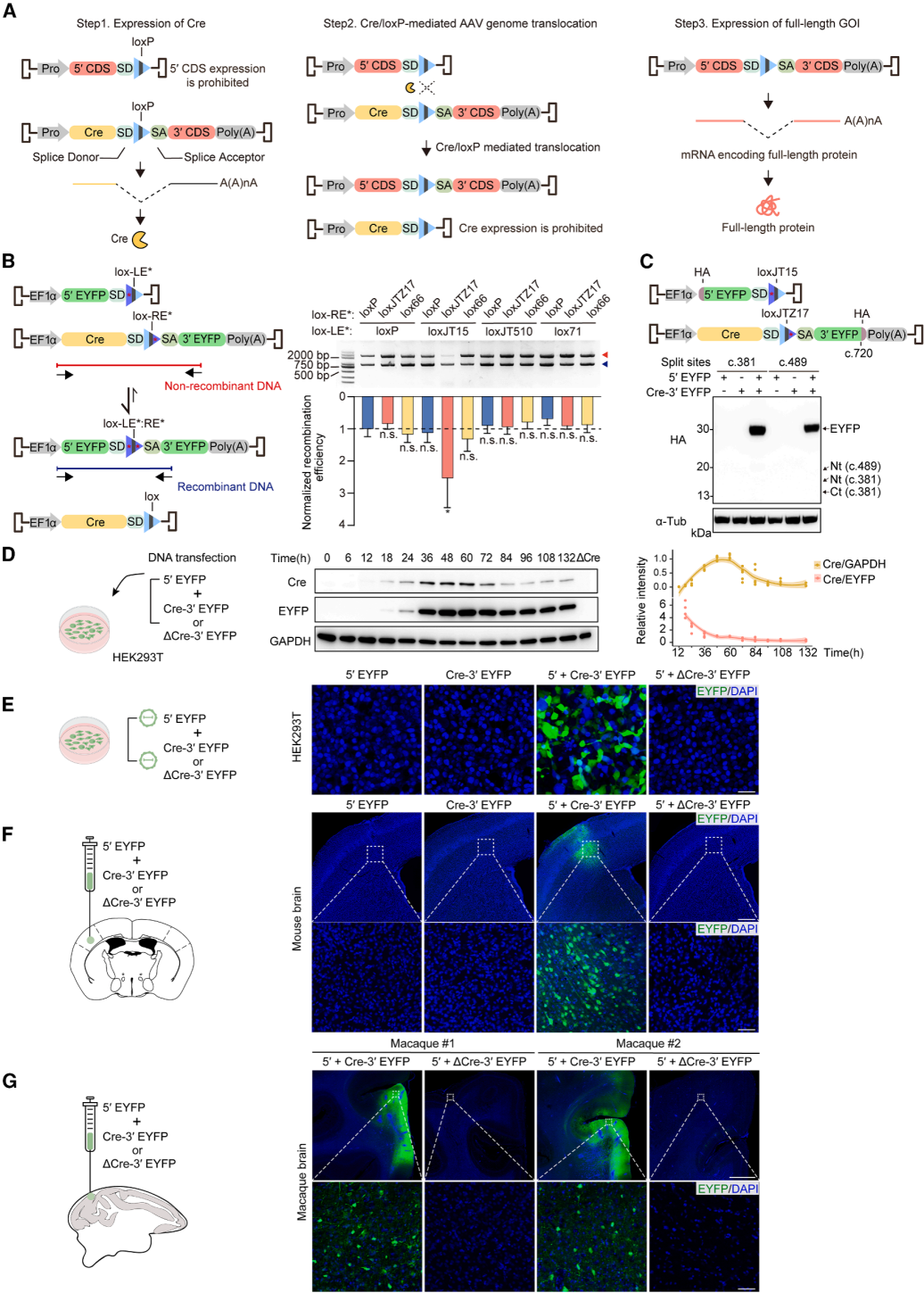
图2. 通过AAVLINK实现的三载体基因递送
对比了AAVLINK与常用内含肽介导蛋白重组技术。以荧光素酶为报告基因,对比两种方法的双/三载体效果。双载体实验中,10个拆分位点下(图3A),最优AAVLINK生物发光强度为内含肽法的23.3±1.3倍(图3B),平均达25.8±10.5倍(图3C),且两组内部位点间效率差异明显。三载体实验中,内含肽法用Npu、Rma正交内含肽保证定向剪接,而AAVLINK重组效率更优(图3D、3E),平均发光强度高245.5±156.7倍(图3F),且全长蛋白多、截短产物少(图2D),优势更显著。小鼠体内实验中,眶后注射载体后4周(图3G),AAVLINK生物发光效率为内含肽法的4.5±1.4倍(图3H、3I),体内外实验均证实其高效性。
重组疾病相关大基因Shank3(5.4kb)和CEP290(7.4kb)时,SHANK3单倍体不足是费兰-麦克德米德综合征(PMS)的主要病因,三个拆分位点下(图3J),内含肽法重组微弱,AAVLINK效率为其36.6±22.1倍,且无截短产物(图3K-3M)。CEP290拆分为两段装入双AAVLINK载体,第三载体供Cre(图3N),其产量比内含肽法高29.8±4.4倍(图3O-3Q)。AAVLINK组全长CEP290占比83.4%±2.4%,内含肽组仅0.2%±0.1%(图3R),证实AAVLINK高效且副产物少。
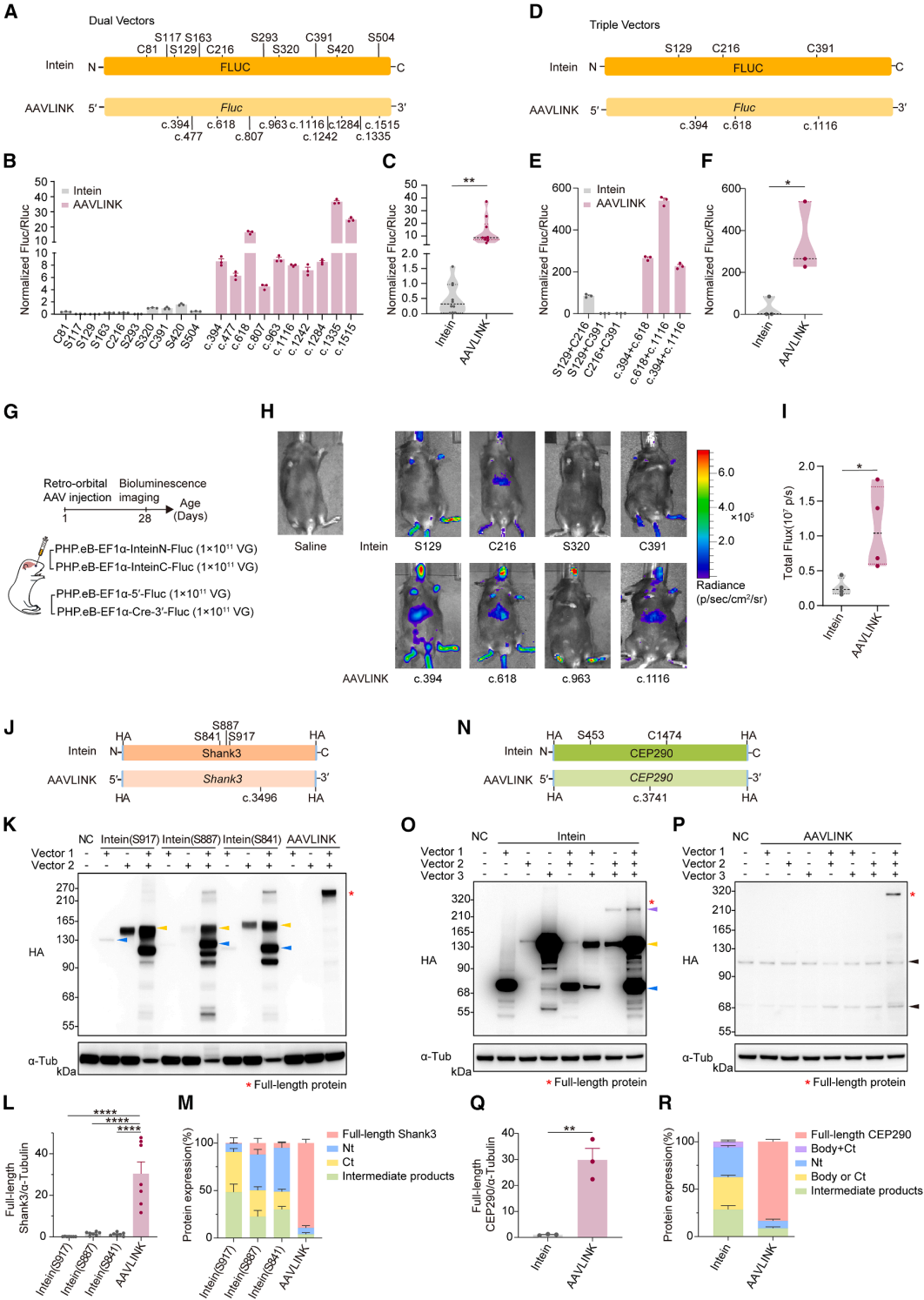
图3. AAVLINK与内含肽介导蛋白重组技术对比
为了验证治疗潜力,用AAVLINK在Shank3突变小鼠中表达该基因。小鼠Shank3缺失会引发突触传递异常及自闭症样行为,重新表达可挽救部分症状,但Shank3基因较大,AAV递送难度高,AAVLINK可解决此问题。将Shank3在c.3496位点拆分,两段分别装入AAVLINK载体(图4A),向4周龄Shank3*InsG3680+/+突变小鼠纹状体注射(其纹状体通路缺陷显著,图4B)。4周后WB检测到强全长Shank3表达(图4C),IHC染色也证实其表达并检测到N/C端表位(图4D),小鼠刻板行为及运动缺陷均被挽救(图4E、4F)。
德拉韦综合征(DS)是耐药性强、破坏性大的癫痫性脑病,80%以上由钠通道编码基因SCN1A单倍体不足导致。其单基因致病特性适合基因替代治疗,尽管SCN1A(6kb)超出AAV装载上限。将携带SCN1A 5'端(c.1-3771)和3'端(c.3772-6030)的rAAV-PHP.eB载体,眶后注射共递送至DS小鼠模型Scn1a+/-小鼠(图4G、4H)。WB和IHC证实,SCN1A编码的Nav1.1蛋白在脑内高效重组表达(图4I、4J),同时治疗组小鼠存活率提升、高热癫痫抵抗力增强(图4K)。治疗实现三项关键生理挽救:(1)海马锥体神经元兴奋性恢复正常;(2)海马快棘突中间神经元活性修复;(3)癫痫相关皮层脑电图(ECoG)活动显著减弱(图4L-4P)。综上,AAVLINK可高效体内递送大型治疗基因。虽脑部共转导效率有限,但仍能实现足够基因重组,产生治疗效益。
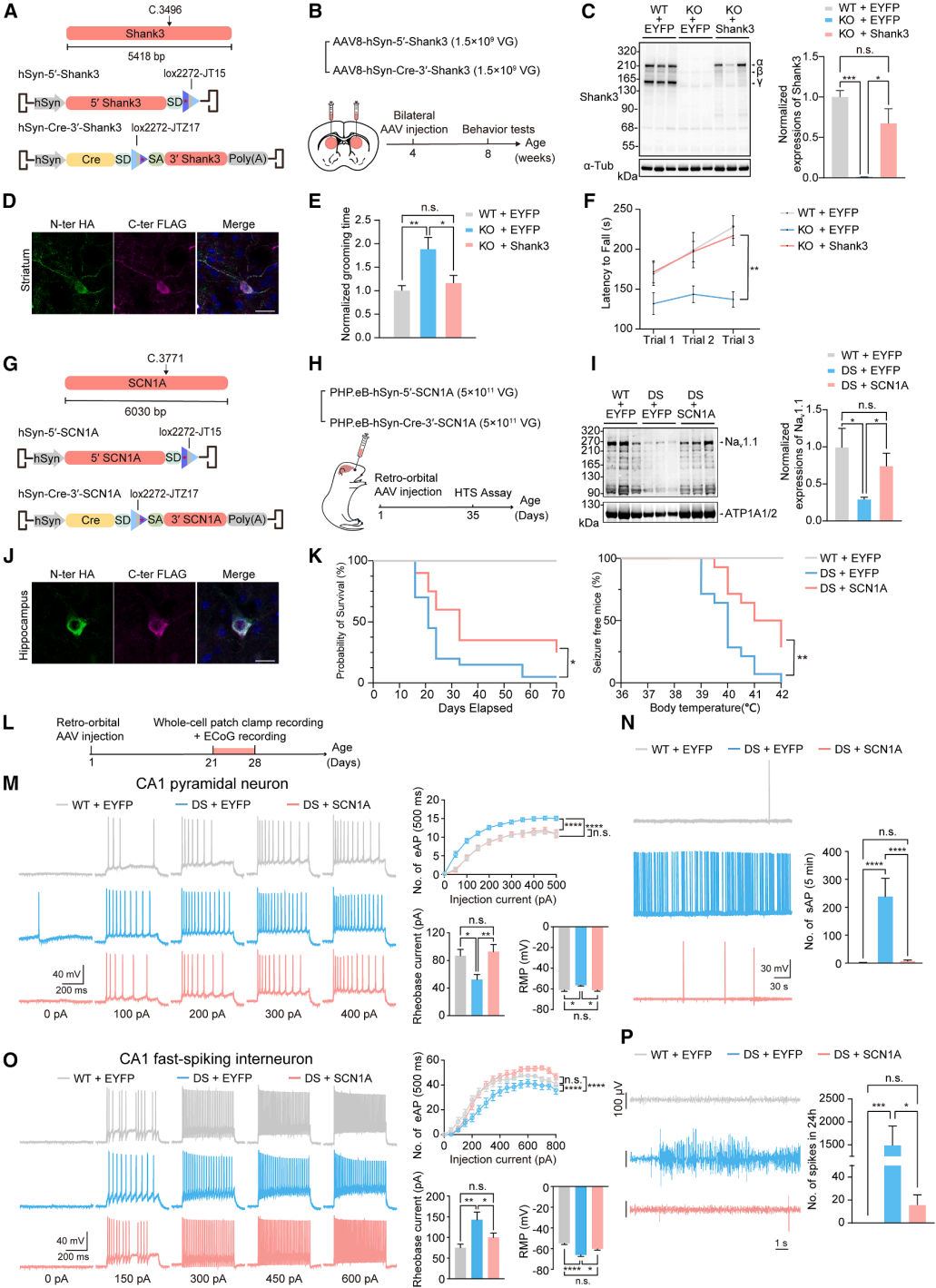
图4. AAVLINK介导的基因替代疗法在PMS和DS小鼠模型中的应用
CRISPR-Cas技术潜力巨大,但相关基因尺寸常超单个AAV包装容量,限制体内应用。作者就此测试了AAVLINK递送该类工具的能力。多数CRISPR-Cas工具基于4.3kb的SpCas9,AAV递送难度大。将其在c.2682位点拆分装入双AAVLINK载体(图5A),转染含靶向PSEN1的sgRNA的COS-7细胞后,成功重组SpCas9并精准删除靶区间片段(图5B、5C)。碱基编辑可精准校正致病突变,用AAVLINK递送两种大型编辑器:腺苷碱基编辑器8e(ABE8e)和含YE1突变的第四代碱基编辑器(YE1-BE4max),二者分别可介导A·T向G·C、C·G向T·A的碱基转换,分别在c.2964、c.3540位点拆分装载体(图5D)。转染HEK293T细胞后,编辑效率最高达80%(图5E、5F)。dCas9融合调控结构域可获CRISPRoff-V2(抑制)和dSpCas9-VPH(激活)。二者分别在c.3675、c.3486位点拆分装载体,转染HEK293T细胞后,可有效抑制或上调目标基因表达(图5G-5I)。体内实验中,AAVLINK向小鼠肝脏递送SpCas9,成功在Rosa26位点诱导断裂(图5J);将靶向Pcsk9基因(降低密度脂蛋白胆固醇的明确靶点)的ABE8e与sgRNA通过AAVLINK包装进两种AAV,对小鼠进行全身给药,4周后A→G转换率16%,Pcsk9表达降低(图5K)。向海马递送dSpCas9-VPH可上调Scn1a(图5L),证实其体内递送可行性。
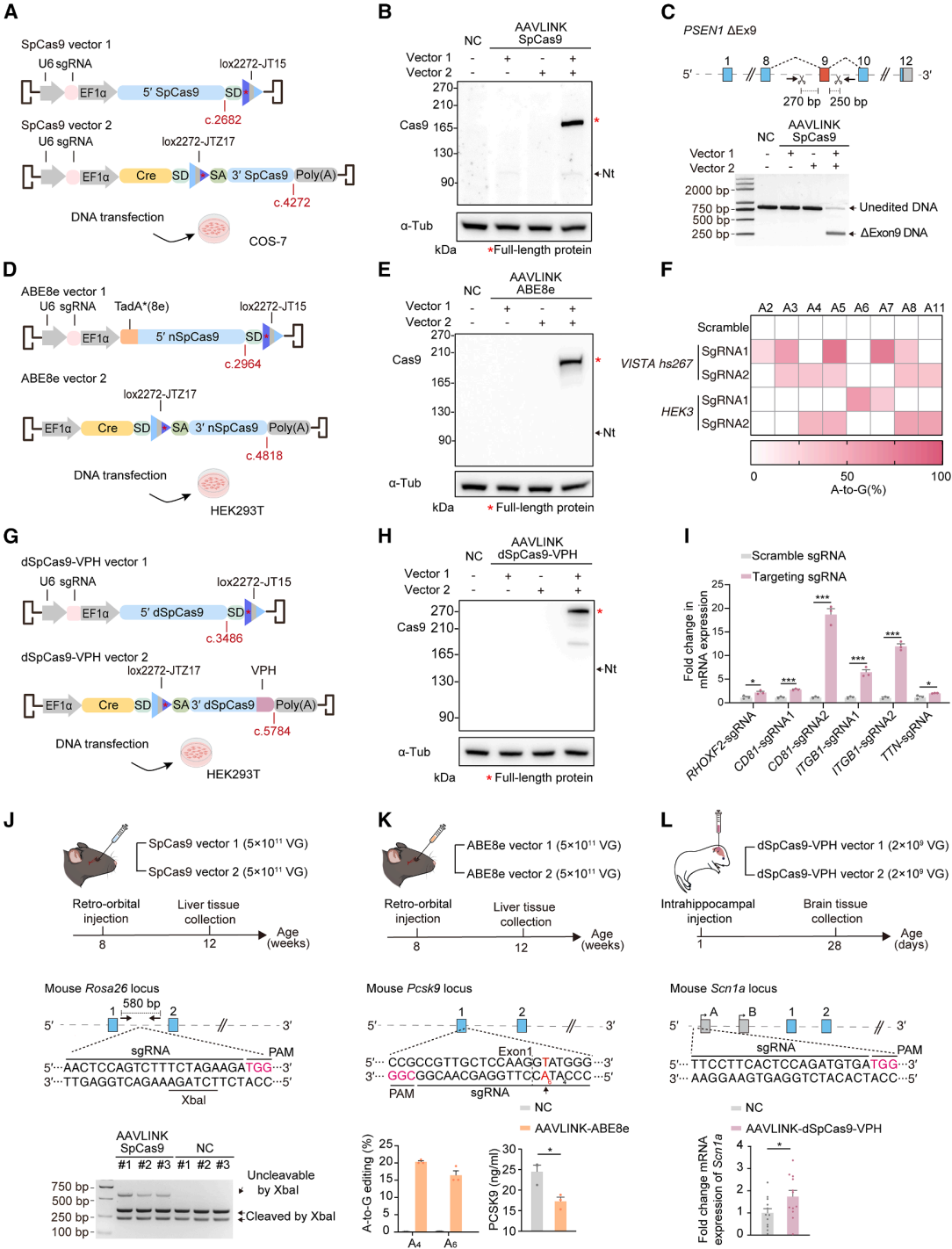
图5. AAVLINK递送的CRISPR工具
外源性Cre重组酶存在潜在生物安全风险,即便AAVLINK中Cre表达具有瞬时性(图1D),仍进一步优化以降低其表达(图6A)。
1. 核心优化策略(从1.0到2.0的迭代)
第一步:筛选弱启动子(AAVLINK1.1)测试6种启动子(EF1α、EFS、UbC、SCP1、CMVmini、BGmini)后,WB和IHC检测结果显示SCP1启动子在维持EYFP高效重组的同时,Cre表达量最低(图6B-6D),据此开发AAVLINK1.1(图6A)。
第二步:添加不稳定标签(AAVLINK2.0)在Cre的C端融合强效蛋白不稳定标签UDeg3a,使Cre几乎检测不到且不影响重组效率(图6E-6G),最终形成AAVLINK2.0(图6A)。
2. 体内验证结果
通过颅内和静脉注射,在小鼠体内对比两种版本Cre表达,AAVLINK1.0:双载体递送后,IHC检测到微弱Cre,WB未检测到,证实Cre会被灭活(图1A、6I、6J、6L、6M);AAVLINK2.0:无论何种递送方式,IHC和WB均未检测到Cre,且目的基因高效表达(图6I、6J、6L、6M)。食蟹猴实验验证AAVLINK2.0无Cre表达,目的基因高效表达(图6N、6O)。AAVLINK2.0通过“弱启动子+蛋白降解标签”双重优化,解决了Cre的生物安全隐患,提升了临床转化潜力。
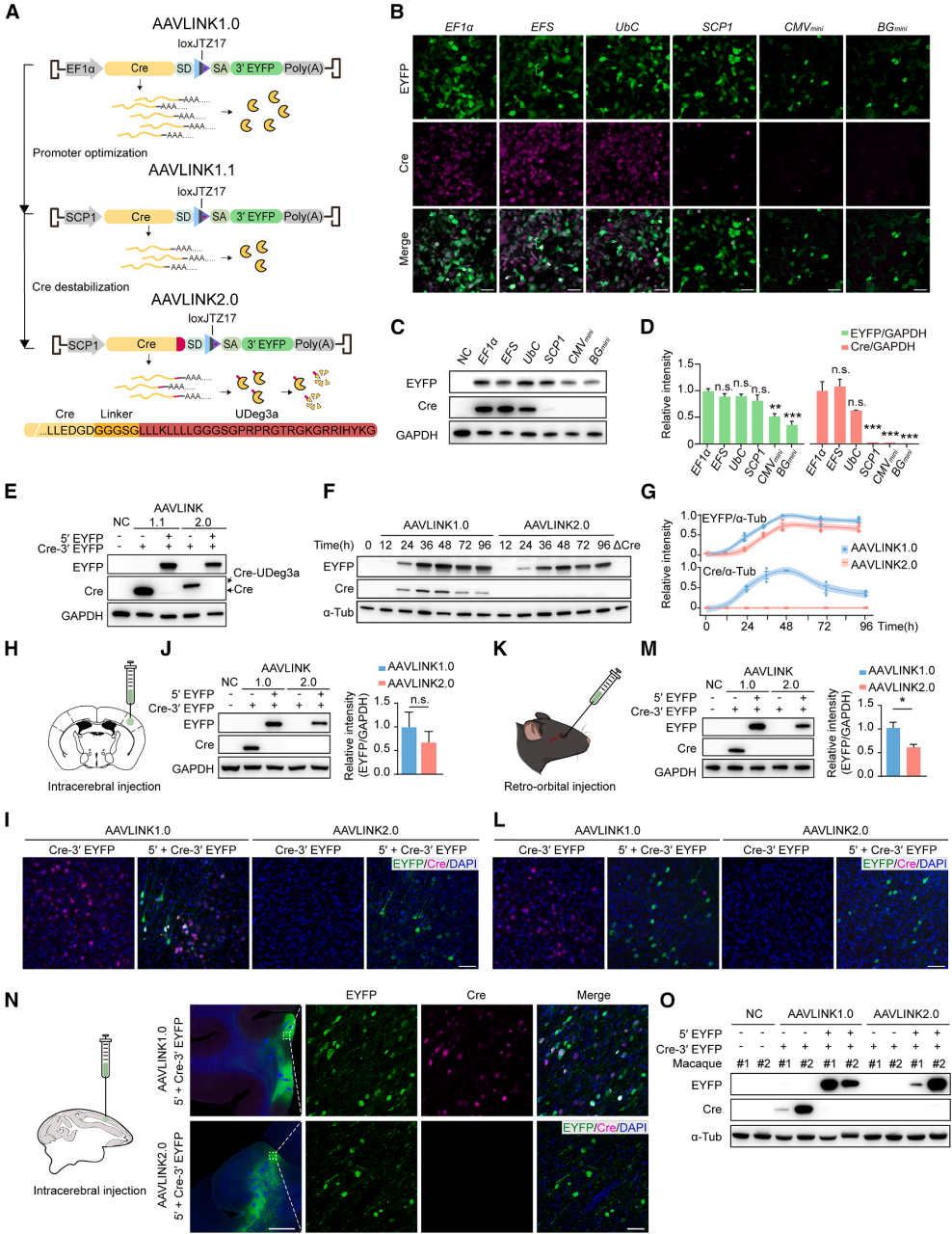
图6. AAVLINK2.0中的最小Cre表达
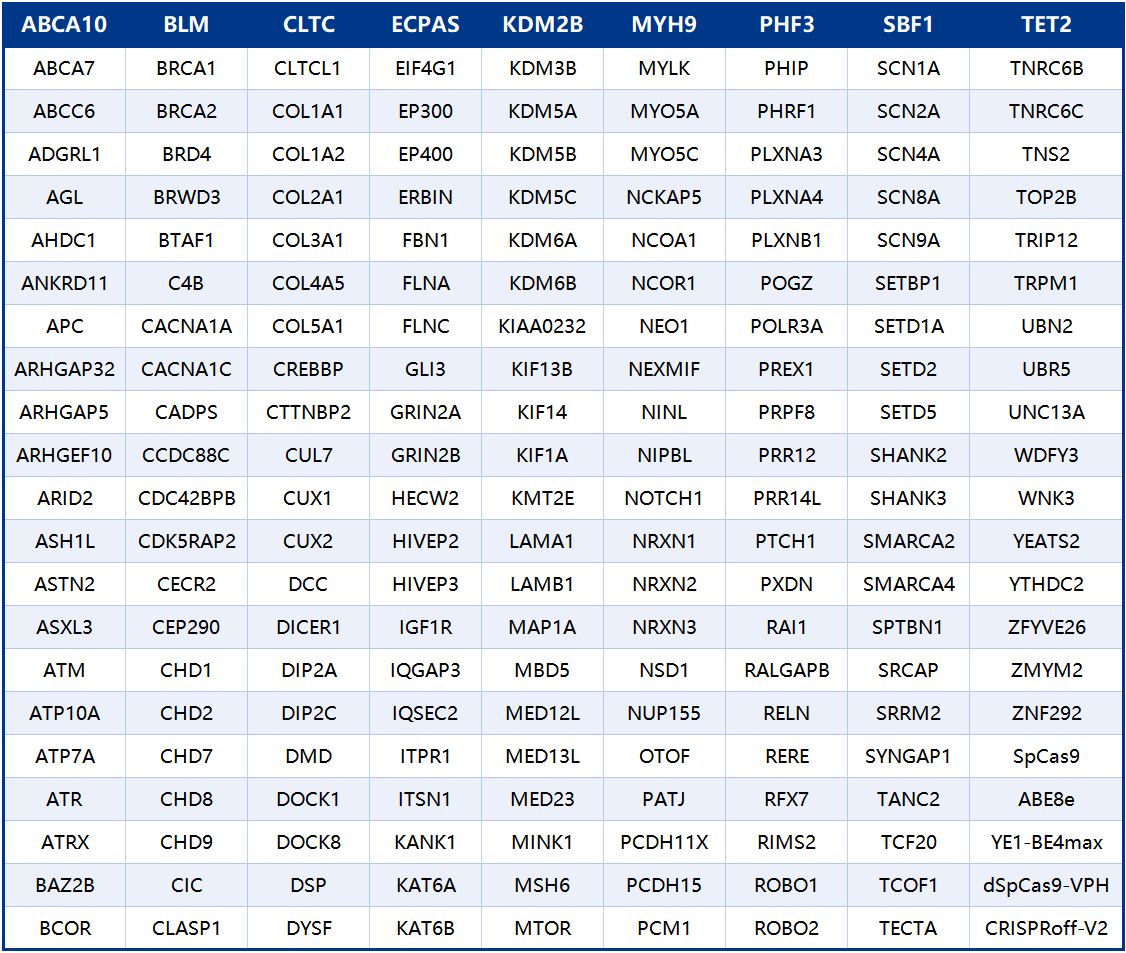
为了提升AAVLINK的实用性,作者构建了遗传病相关大型基因资源库,重点关注自闭症(ASD)风险基因——其遗传关联性强、缺乏有效疗法,单基因病例多为LoF突变(适合基因替代),且多数超过4kb,是理想递送候选。从SFARI数据库克隆了所有>4kb的基因,及27个其他疾病相关基因(如AGL、ATP7A、OTOF,其LoF突变分别致Ⅲ型糖原贮积病等),按基因长度拆分装入双/三载体AAVLINK,在细胞内验证DNA和蛋白水平重组效果。198个基因(193个疾病相关+5个CRISPR相关)先克隆至AAVLINK1.0,后改造为AAVLINK2.0以提升治疗适用性;Sanger测序证实所有基因均实现DNA重组,192个基因的全长蛋白表达经WB验证(图7)。多数基因经单一拆分即可重组,体现AAVLINK稳定性;但不同拆分方案效率有差异,与荧光素酶实验结果一致(图3A-3F),部分基因需筛选最优拆分位点以达最佳效果。资源库详细信息(基因名称、长度、验证状态)见图7L及表S1,同时搭建专门网站(http://AAVLINK.com/),便于研究者查阅。
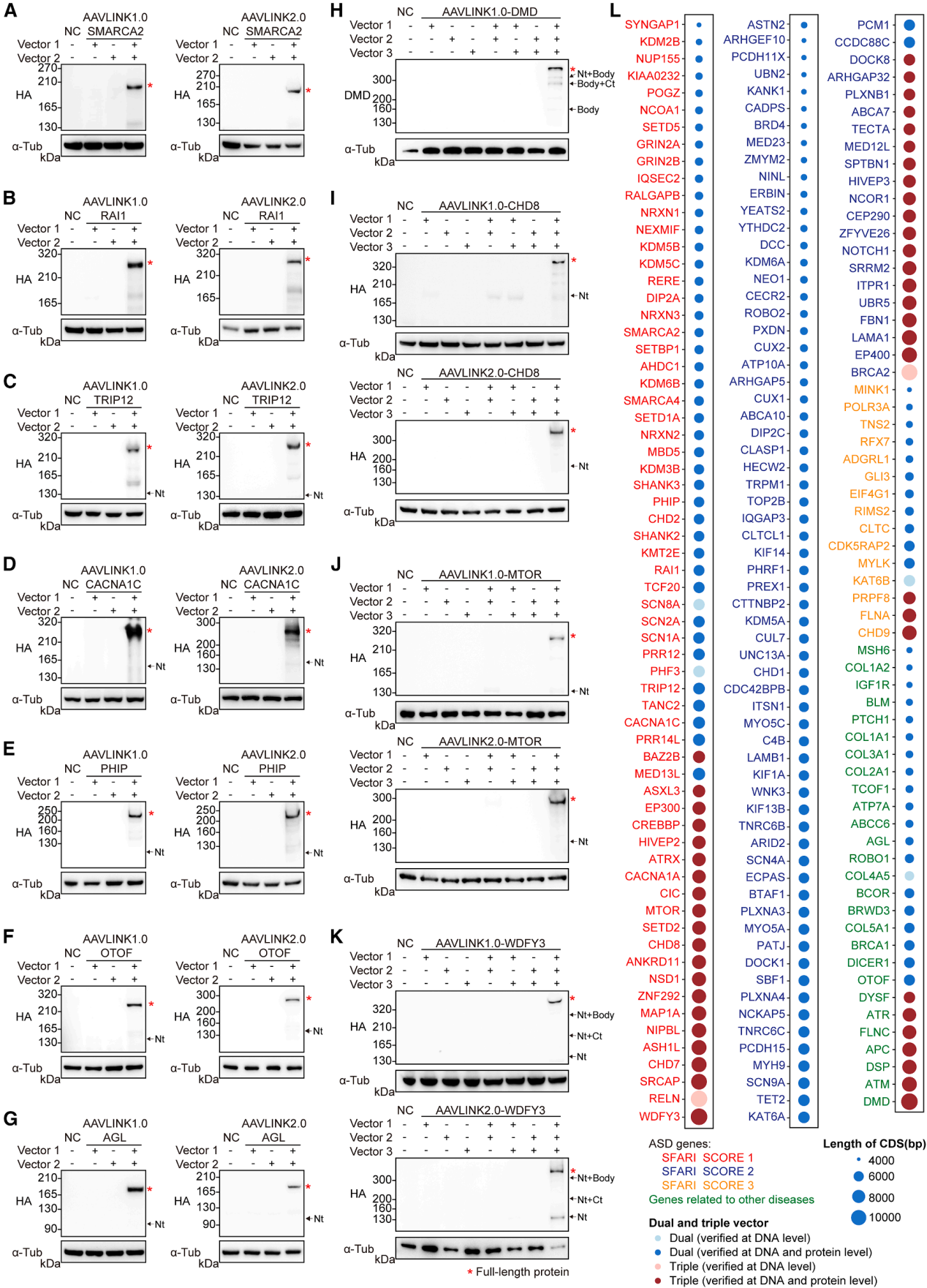
图7. 遗传性疾病相关大基因递送的AAVLINK资源
AAVLINK存在四点局限:灵长类全身给药后AAV共转导效率偏低;基因拆分位点对其影响的机制未明;针对所有疾病相关基因的AAVLINK1.0 3′ CDS载体及CRISPRoffV2均采用pCALM1启动子,以实现脑内神经元选择性表达,非神经元表达需换启动子;细胞特异性或精准表达需优化5′ CDS启动子。
193个疾病相关大基因和5个CRISPR工具的载体库(http://AAVLINK.com/)
198个大型基因被拆分并装载到AAVLINK载体中,其重组效果已在培养细胞中得到验证。