化学遗传学(Chemogenetics)是化学生物学交叉技术,核心为设计性小分子化合物与配体依赖性受体特异性互作激活下游信号以调控细胞活动。只由特定药物微 活 受 体 ( Designer receptors exclusively activated by designer drugs, DREADDs)技术是目前应用最广泛的化学遗传学技术。
DREADDs受体类型:基因工程改造的 G 蛋白偶联受体(GPCR),核心特点是对内源性配体敏感性极低(规避机体自身信号干扰)、与外源性配体 CNO 亲和力高,最常用DREADDs主要分为两类:
激活型Gq-DREADD—hM3Dq:由人毒蕈碱乙酰胆碱受体M3(hM3D)改造而来,仅响应CNO而不被乙酰胆碱激活。CNO结合后启动Gq蛋白偶联信号通路,激活磷脂酶Cβ(PLCβ)降解磷脂酰肌醇二磷酸(PIP2),进而关闭KCNQ外向钾离子通道,促使细胞膜去极化并触发动作电位。
抑制型Gi-DREADD——hM4Di:由人毒蕈碱乙酰胆碱受体M4改造(hM4D)而来,仅响应CNO而不被乙酰胆碱调控。CNO结合后激活Gi蛋白偶联的内向钾离子通道(GIRK),引发细胞膜超极化,抑制神经元的动作电位发放。
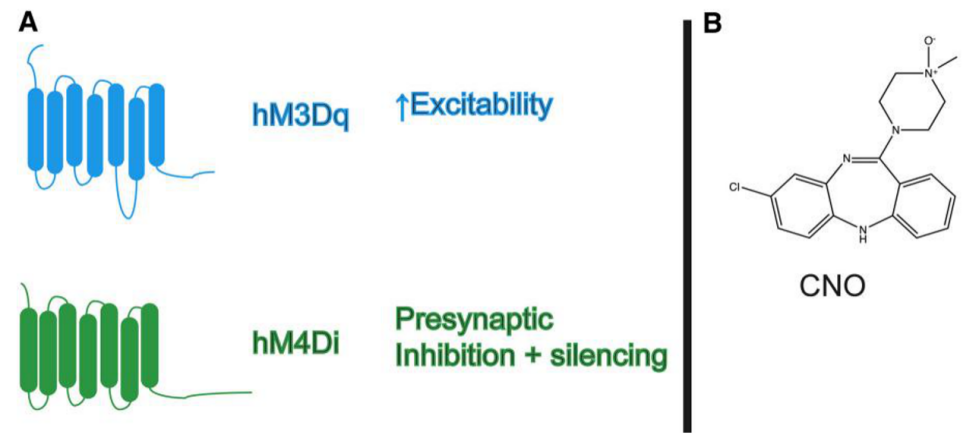
图1 常用DREADDs及其配体CNO[1]
递送载体:借助 AAV 载体,搭配特定血清型与细胞特异性启动子,可实现特定神经元活动精准、可逆调控。
核心配体:CNO,是氯氮平的代谢小分子产物,结合神经元特异性表达的人工受体(hM3Dq、hM4Di等)实现神经元活动精准调控,具有以下优势:
高选择性:仅激活改造后的DREADDs受体,对天然受体无作用,可完全规避非特异性信号干扰。
强穿透性:脂溶性突出,可自由穿透血脑屏障,支持口服、腹腔注射等方式进入中枢神经系统。
可逆性:体内代谢速率快,单次给药后,调控效应持续约6小时,且停药后效应可逆;无显著毒副作用。
受体选择:根据实验目的确定合适的DREADDs受体,激活选hM3Dq,抑制选hM4Di。
病毒载体构建与递送:将DREADDs基因克隆至AAV载体,搭配AAV血清型与细胞特异性启动子实现在体靶细胞特异性感染并表达DREADDs,可选择共表达荧光报告蛋白(如mCherry),用于示踪定位。
CNO给药:病毒充分表达后,通过系统性/局部性给药方式,实现对神经元活动的调控,设置对照组,排除非特异性干扰。
操控有效性验证:表达验证采用组织切片+荧光成像,确认靶脑区表达定位;
功能验证采用电极记录神经元细胞膜内外电压变化。
表型与功能解析:在CNO药效窗口期开展行为学、生理指标等实验检测,对比对照组验证靶神经元功能调控作用。
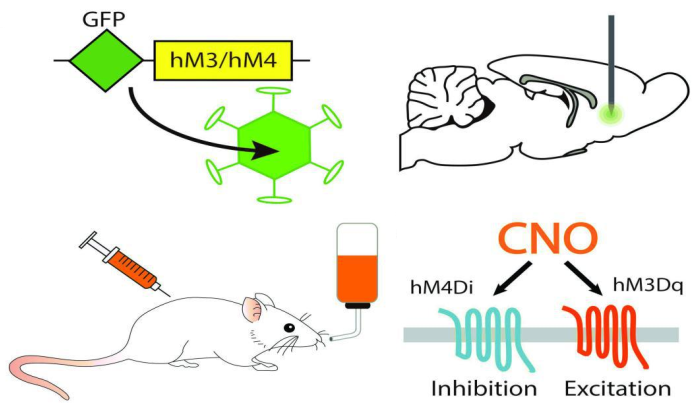
图2 化学遗传学的实验步骤
表1 不同CNO给药方式
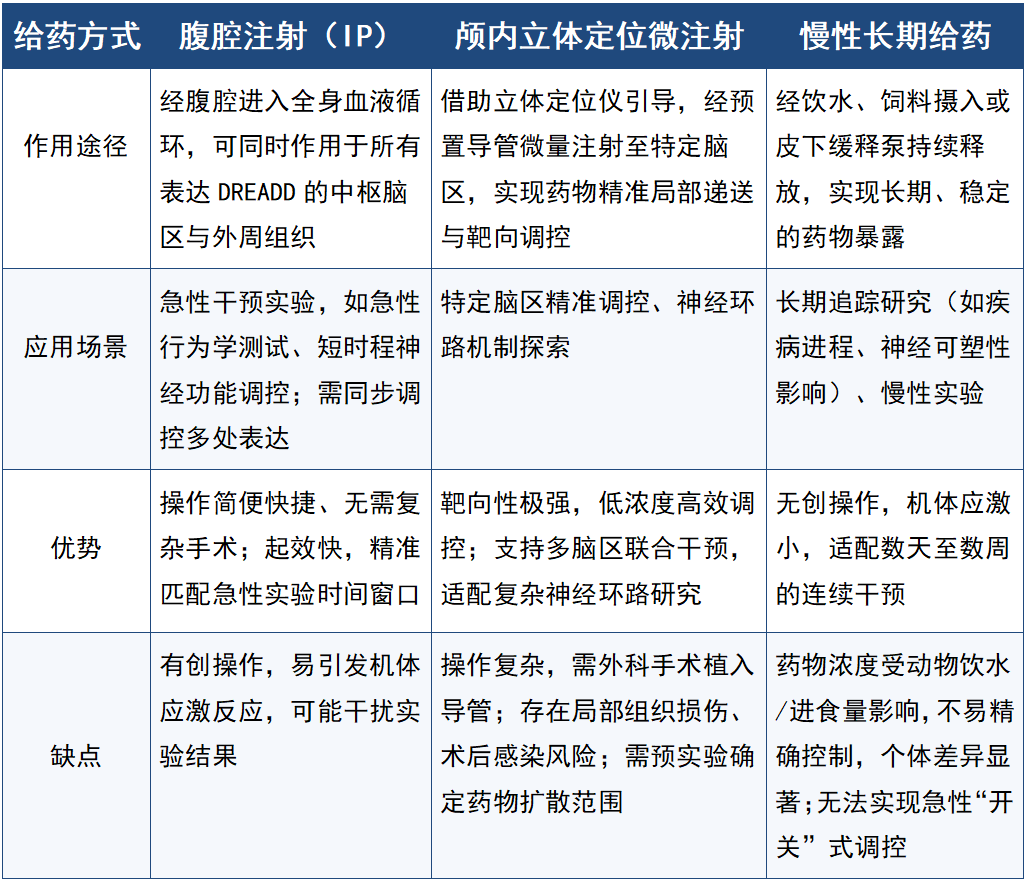
DREADD 配体是一类药理学惰性化合物,除CNO外,已开发多种优化配体,核心信息如下。
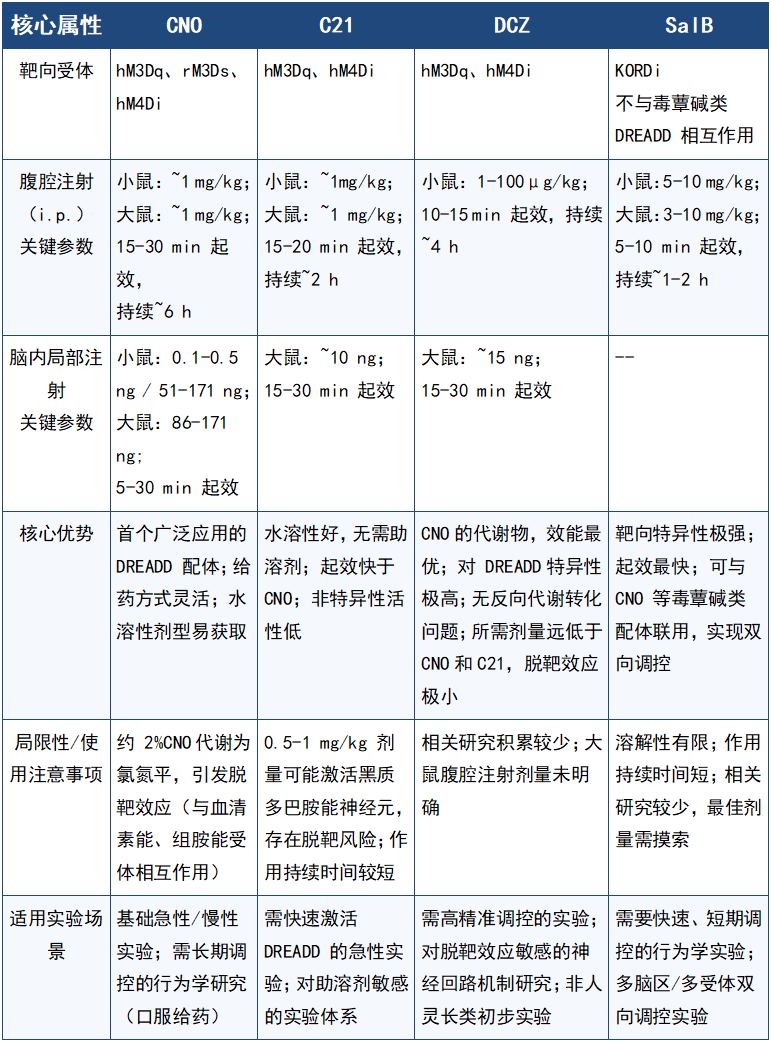
表2不同DREADD配体[2]
1. 短期刺激
实验动物:ThCre小鼠
病毒载体:rAAV-EF1α-DIO-hM3D(Gq)-EGFP或rAAV-EF1α-DIO-hM4D(Gi)-EGFP
注射方式:ACC/VTA,脑立体定位注射,1.0×10¹² vg/ml,300nl
给药方案:病毒表达3周后植入引导套管,恢复1周;以100 nL/min速度输注0.5μL CNO(3μmol/L),停针2min;5min后进行行为学测试
实验结果:为明确投射至前扣带回皮层(ACC)的腹侧被盖区多巴胺能神经元(VTADA)失活是否会引发焦虑样行为及共病性疼痛。研究向ThCre小鼠VTA注射Cre依赖hM4Di病毒(抑制VTADA神经元),表达三周后,在ACC植入引导套管。结果显示,抑制组小鼠在旷场试验(OFT)、高架十字迷宫试验(EPM)和明暗箱试验(DLB)中均出现焦虑样行为,同时出现机械/热痛阈值降低且CPA中表现厌恶;小鼠spared神经损伤(SNI)(慢性神经病理性疼痛模型)术后6周,激活该通路,可完全逆转痛觉超敏、焦虑及厌恶行为,假手术组无显著变化。综上,VTADA-ACC通路调控焦虑样行为与痛觉过敏,VTADA神经元向前投射至ACCGlu神经元传递情绪反馈。
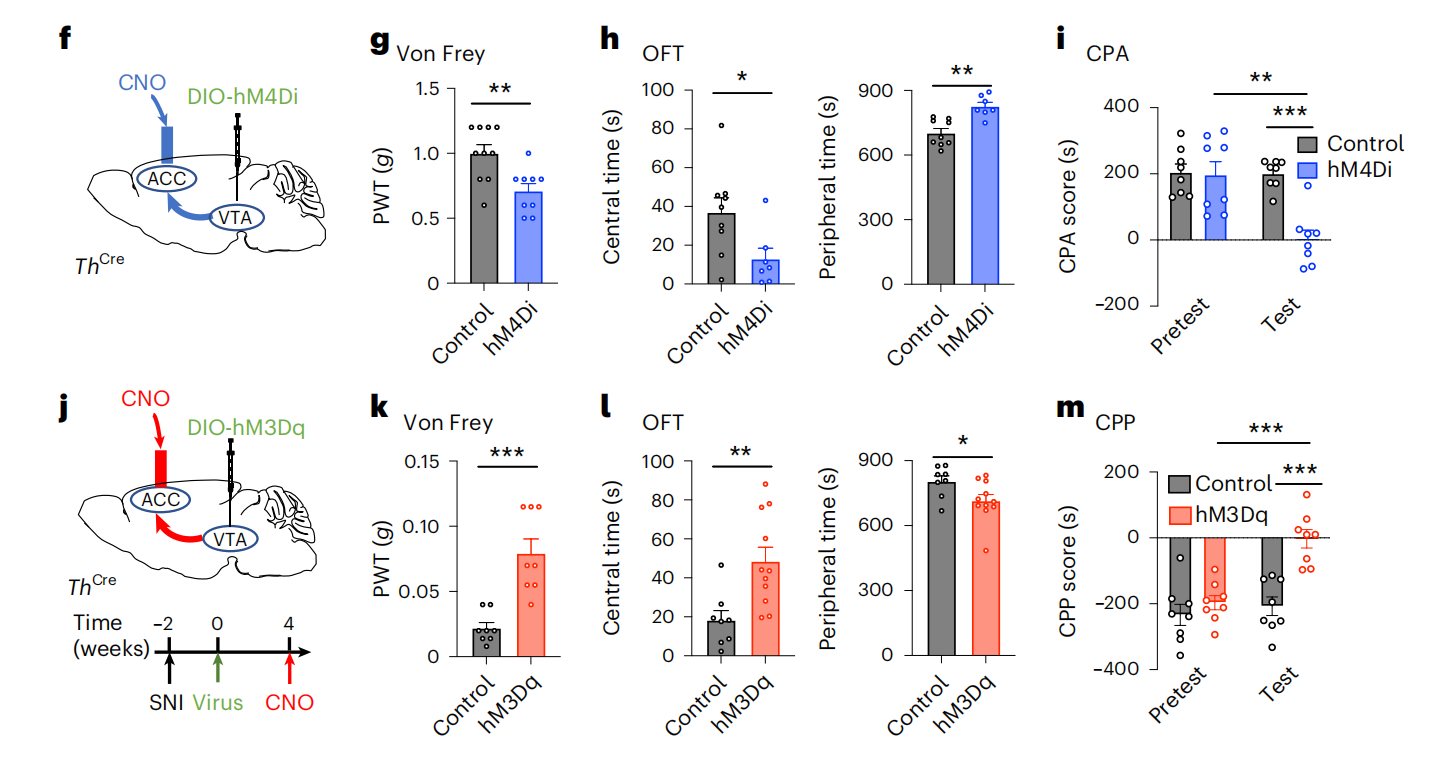
图3 VTADA-ACC通路调控焦虑样行为与痛觉过敏[3]
2. 长期刺激
实验动物:ThCre小鼠/CaMkIIαCre鼠
病毒载体:rAAV-EF1α-DIO-hM3D(Gq)-EGFP或rAAV-EF1α-DIO-hM4D(Gi)-EGFP
注射方式:ACC/VTA,脑立体定位注射,1.0×10¹²vg/ml,300nl
给药方案:病毒表达4周后植入引导套管,恢复1周后,每日一次CNO,持续一周,以模拟长期伤害性刺激
实验结果:为进一步验证ACC谷氨酸能神经元与VTA多巴胺能神经元之间一个关键的正反馈环路(ACC⁺ᴳˡᵘ–VTA⁺ᴳᴬᴮᴬ–VTA⁺ᴰᴬ–ACC⁺ᴳˡᵘ)在慢性疼痛共病情感障碍中的核心作用。向小鼠ACC注射Cre依赖hM3Dq病毒,持续1周CNO干预。结果显示,该干预可降低小鼠机械痛阈、诱发焦虑样行为,且上述行为改变持续超3周,VTADA神经元放电频率亦持续降低4周以上;反向验证中,抑制VTADA→ACC通路,同样诱导出持续≥3周的痛觉过敏与焦虑行为,并伴随ACCGlu神经元放电长时程增强。综上,两种干预均通过增强ACC-VTA正反馈环路活性,介导痛觉超敏与焦虑的长期维持,证实该环路在慢性疼痛进展中的关键作用。
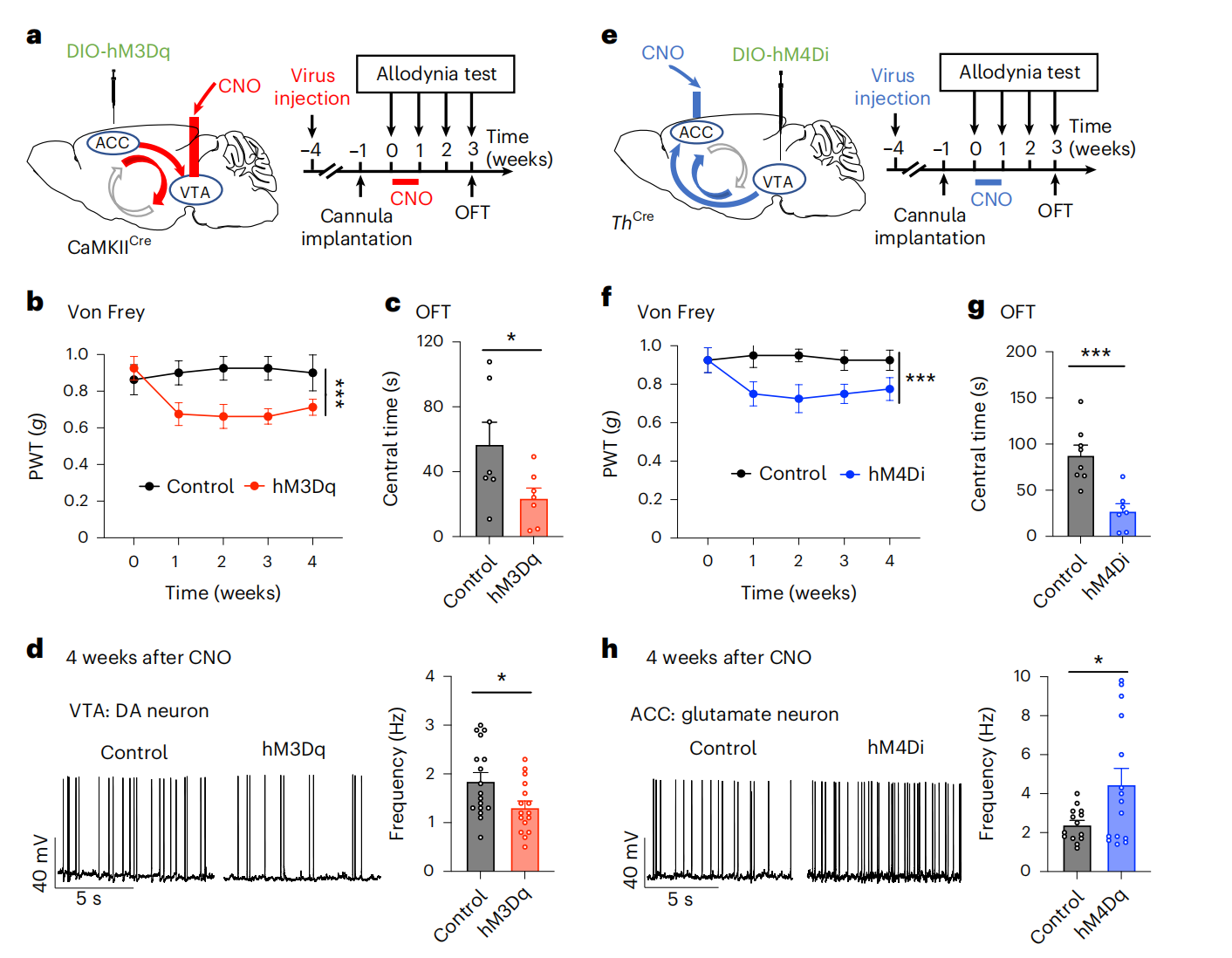
图4 ACC–VTA–ACC反馈环路介导神经病理性疼痛的持续存在[3]
1. 短期给药
实验动物:GAD2-Cre小鼠
病毒载体:rAAV-EF1α-DIO-hM3D(Gq)-mCherry或rAAV-EF1α-DIO-hM4D(Gi)-mCherry
注射方式:ZI区,脑立体定位注射,300nl,表达3周
给药方案:在行为学实验检测前30分钟,通过腹腔注射CNO(1mg/kg,0.5mL)以激活或抑制该ZIvGABA神经元活动。
实验结果:为探究激活ZIvGABA神经元对疼痛相关焦虑行为的缓解作用,向GAD2-Cre小鼠ZI区注射AAV-DIO-hM3Dq-mCherry,腹腔注射CNO激活后ZIvGABA神经元;电生理验证(电流钳模式)显示10μMCNO处理后,神经元去极化并产生动作电位;GAD2-Cre小鼠ZI区注射AAV-DIO-hM3Dq-mCherry,腹腔注射CNO激活后,神经元去极化、产生动作电位;小鼠后爪注射CFA(完全弗氏佐剂)建立疼痛性焦虑样行为模型,注射后第1天开展行为学检测,小鼠机械痛阈升高、焦虑减轻;正常GAD2-Cre小鼠注射AAV-DIO-hM4Di-mCherry,CNO抑制后神经元超极化,小鼠痛敏升高、出现焦虑样行为。综上,ZIvGABA神经元活性降低是CFA诱导急性痛与焦虑的必要充分条件。
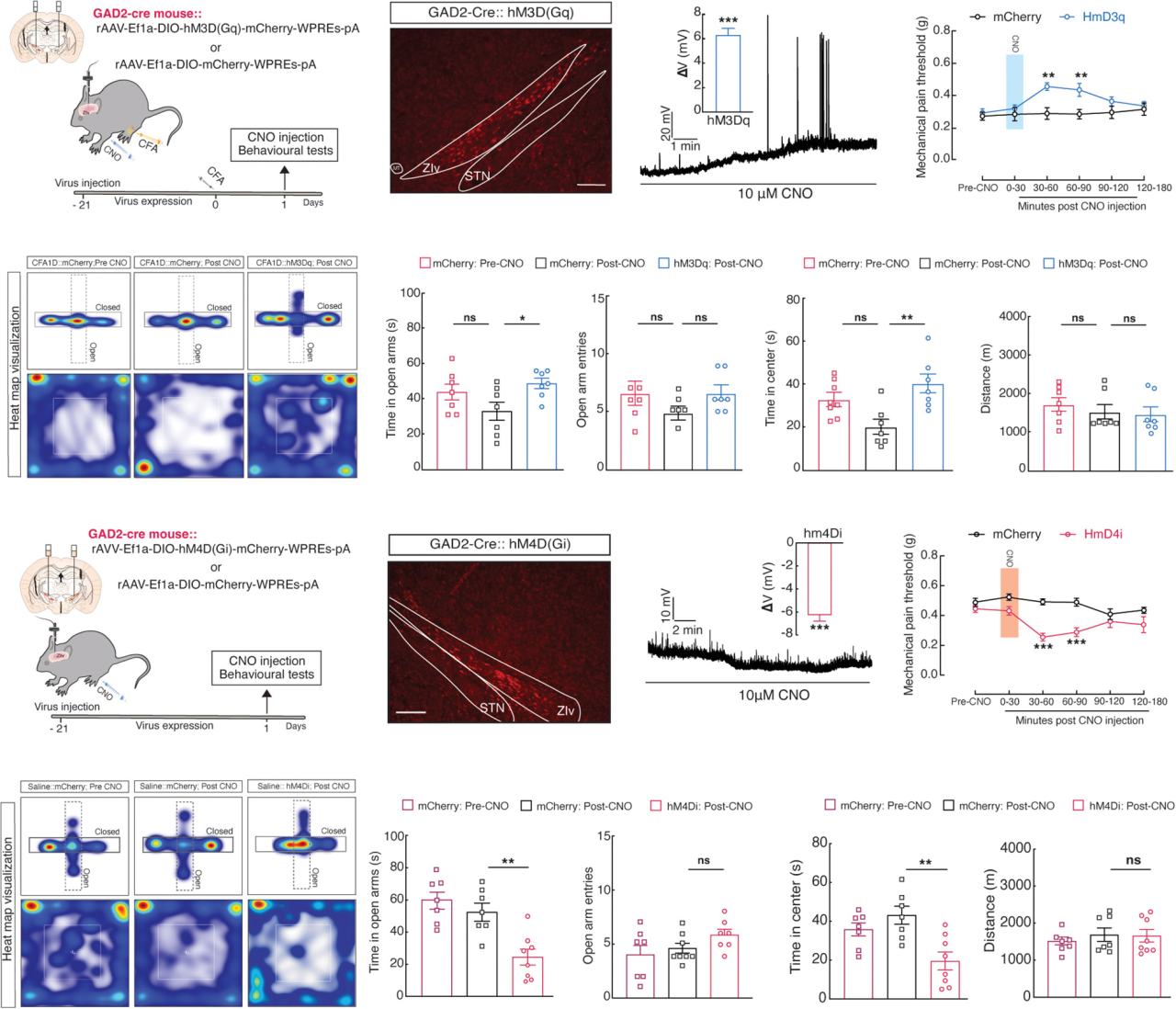
图5 ZIGABA活性的调控可调节疼痛感知及焦虑样行为[4]
2. 长期给药
实验动物:SD大鼠
病毒载体:rAAV-EF1α-DIO-hM3D(Gq)-mCherry或rAAV-EF1α-DIO-hM4D(Gi)-mCherry
注射方式:NTS,脑立体定位注射,200nl,
给药方案:在电针刺激前30分钟,通过腹腔注射CNO(1mg/kg)以激活或抑制该通路的神经活动。
实验结果:为明确孤束核谷氨酸能神经元(NTSGlu)-头端延髓腹外侧区(RVLM)通路在电针(EA)调控交感神经活动及自发性疼痛中的作用。向SD大鼠NTS注射顺行示踪病毒rAAV-CaMKIIα-mCherry,证实NTSGlu可直接投射至RVLM。随后,通过化学遗传学分别抑制与激活该通路:抑制NTSGlu神经元可模拟电针效应,显著降低RVLM神经元放电频率及自发性疼痛评分;而激活该通路则可逆转电针的上述作用。值得注意的是,该通路对机械性疼痛无显著影响,激活亦不能逆转电针对机械痛的改善。综上,电针通过抑制NTSGlu-RVLM通路特异性调控自发性疼痛,提示该通路是电针镇痛作用的重要神经机制之一。
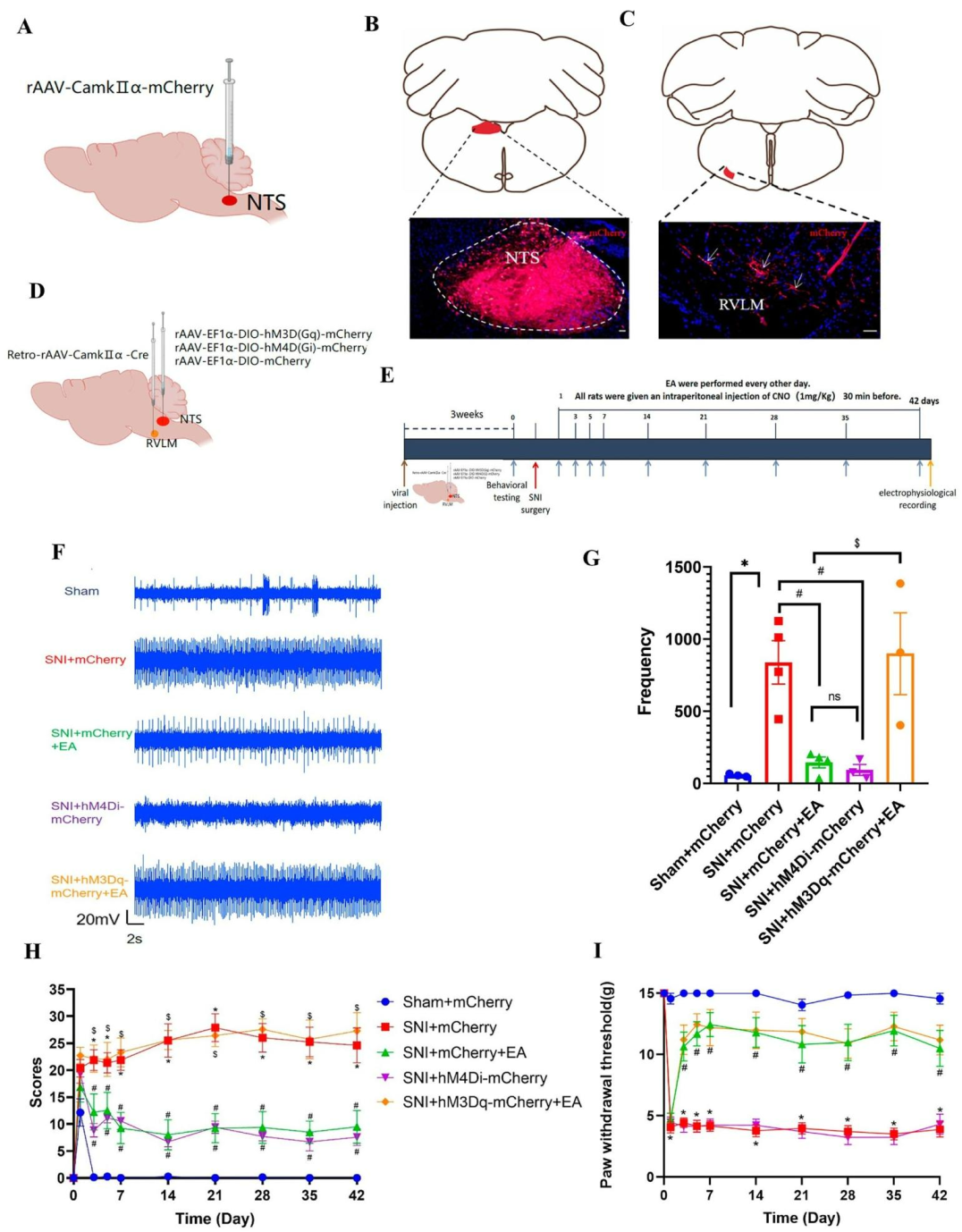
图6 EA通过NTSGlu-RVLM通路缓解自发性疼痛,而非机械性疼痛[5]
实验动物:Th-Cre小鼠
病毒载体:AAV-EF1α-fDIO-hM3Dq-EGFP
注射方式:LC,脑立体定位注射
给药方案:病毒注射三周后,通过饮用水给予CNO,25ug/ml,长期激活rMR投射的NELC神经元。
实验结果:为解析NELC-5-HTrMR神经环路对肝脏再生的调控作用,在Th-Cre小鼠蓝斑核(LC区)注射 AAV-fDIO-hM3Dq-EGFP 或对照病毒,并在中缝背核(rMR)注射AAV2/Retro-DIO-FLP,经饮用水给予CNO长期激活rMR投射的 NELC神经元;全细胞膜片钳记录和c-Fos免疫染色验证了该神经元激活的有效性;70% 肝部分切除(PHx)实验显示,与对照组相比,激活组小鼠的肝脏/体重比及增殖标志物Ki67、PCNA的基因和蛋白表达水平均显著降低,表明化学遗传学激活投射到rMR的NELC神经元可抑制肝脏再生,模拟慢性应激的调控效应。
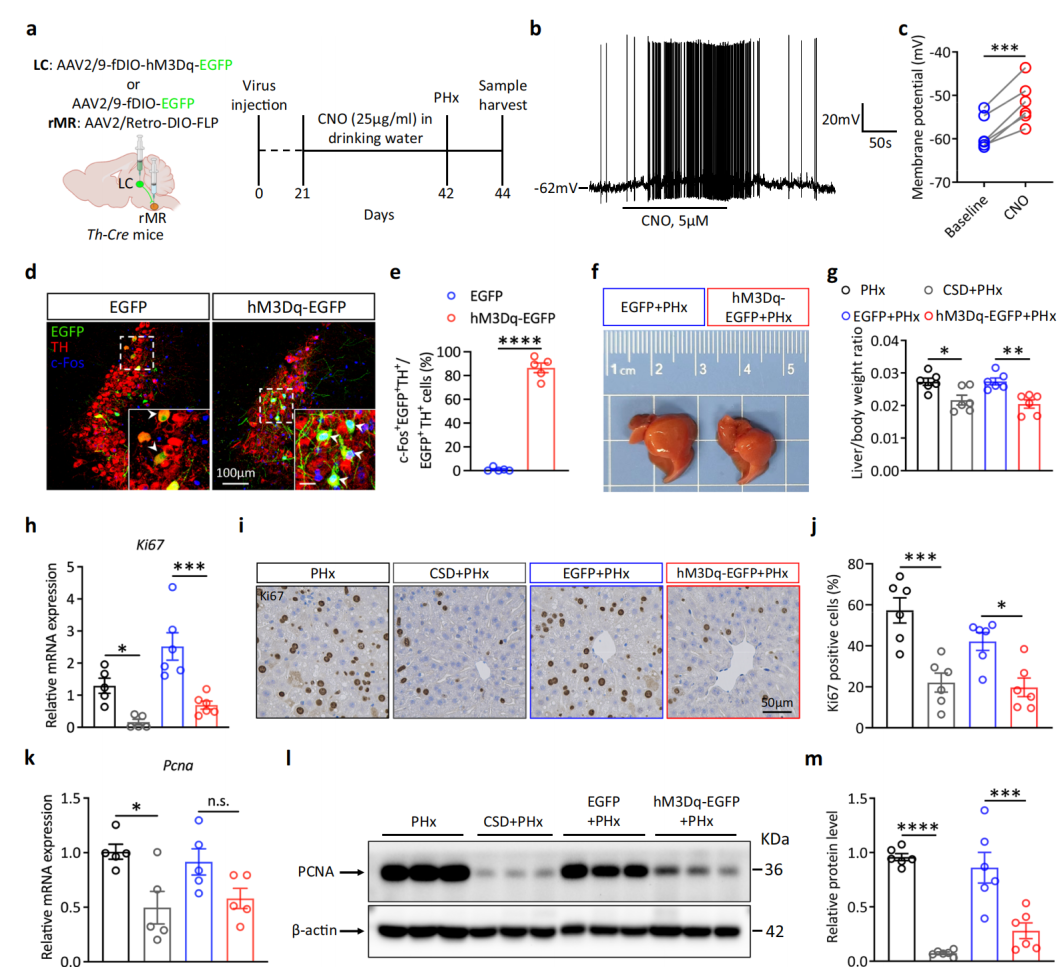
图7 化学遗传学激活投射到rMR的NELC神经元损害肝脏再生[6]
[1] Roth BL. DREADDs for Neuroscientists. Neuron. 2016;89(4):683-694.
[2] Gao J, Ye T, Chen X, et al. Advances in chemogenetics: a review of DREADDs and its application in psychiatric disorders. Mol Psychiatry. 2026;31(1):480-497.
[3] Song Q, Wei A, Xu H, et al. An ACC-VTA-ACC positive-feedback loop mediates the persistence of neuropathic pain and emotional consequences. Nat Neurosci. 2024;27(2):272-285.
[4] Farzinpour Z, Liu A, Cao P, Mao Y, Zhang Z, Jin Y. Microglial Engulfment of Spines in the Ventral Zona Incerta Regulates Anxiety-Like Behaviors in a Mouse Model of Acute Pain. Front Cell Neurosci. 2022;16:898346.
[5] Chen W, Ma X, Fu YM, Liu CZ, Li HP, Shi GX. Electroacupuncture Regulates Sympathetic Nerve Through the NTSGlu-RVLM Circuit to Relieve Spontaneous Pain in SNI Rats. CNS Neurosci Ther. 2025;31(3):e70327.
[6] Zhou Y, Lin X, Jiao Y, et al. A brain-to-liver signal mediates the inhibition of liver regeneration under chronic stress in mice. Nat Commun. 2024;15(1):10361.