焦虑障碍是全球最常见的精神障碍,但现有治疗手段仍存在局限。组胺是一种胺能神经递质,由组氨酸通过组氨酸脱羧酶(HDC)合成。作为一种进化保守的神经调质,近年被证实与神经精神疾病相关。然而,组胺能信号如何动态编码情绪相关信息并调控焦虑,目前尚不清楚。
2026年3月7日,浙江中医药大学陈忠教授、汪仪研究员团队在Neuron上发表题为“Astrocytic H3 Rreceptors regulate anxiety through GABA signaling”的研究论文,发现当小鼠进入焦虑环境时,vCA1区的组胺能活性和组胺释放显著增强,且具有区域特异性。这种组胺能信号会激活并募集星形胶质细胞中的H3受体(H3R)相关信号,触发抑制性胶质递质GABA释放,最终调控焦虑样行为。研究结果揭示了一条此前未被描述的组胺能环路,该环路与vCA1区星形胶质细胞协同作用,共同塑造适应性和病理性焦虑。

该研究的第一作者为浙江中医药大学基础医学院副研究员李玉兰,药学院硕士研究生王艺蓓、浙江大学附属第二医院神经内科李礼轩博士和药学院硕士研究生李新义为论文的共同第一作者,通讯作者为浙江中医药大学陈忠教授和汪仪研究员。该研究受到国家重点研发计划、国家自然科学基金及浙江省自然科学基金的资助。
为探究焦虑相关环境中细胞外组胺水平的变化,通过病毒介导(AAV-GfaABC1D-HA1m)在多个情绪相关脑区的星形胶质细胞中表达细胞外组胺探针GRABHA1m(简称HA1m),包括内侧前额叶皮层(mPFC)、前扣带回皮层(ACC)、海马背侧/腹侧CA1区(dCA1/vCA1)、腹侧被盖区(VTA)和中脑导水管周围灰质(PAG)。并结合光纤光度法,在小鼠OFT实验(OFT)和高架十字迷宫(EPM)实验中实时监测内源性组胺释放(图1A、1B)。结果显示,在焦虑诱导环境中,组胺信号呈现显著的脑区特异性变化:在OFT中,小鼠进入中心区域时,vCA1的HA1m信号显著增强,返回外周后下降;在EPM实验中,从闭合臂进入开放臂时信号增强,返回闭合臂时信号降低,而mPFC、ACC、dCA1、VTA和PAG等脑区均未观察到显著变化且这些脑区在中心区域或开放臂中的HA1m信号显著低于vCA1区(图1C-1F)。
组胺能神经元仅存在于下丘脑的结节乳头核(TMN)。为明确TMN-vCA1组胺能环路是否动态参与焦虑相关行为,通过Cre依赖的病毒递送系统(AAV-EF1α-DIO-axon-GCaMP6s),在组氨酸脱羧酶-CreERT2(HDC-CreERT2)转基因小鼠的TMN中表达钙离子指示剂GCaMP6s,并在vCA1区上方植入光纤。免疫组织化学证实,GCaMP6s在HDC阳性的TMN神经元中表达(图1G)。结果显示,当小鼠从OFT外周区域进入中心区域、从EPM闭合臂转向开放臂时,vCA1区组胺能神经末梢的活性增强,返回时活性降低(图1H、1I、1K、1L)。尽管这些钙离子信号的幅度相对较小(可能归因于组胺能神经末梢本身纤细、低体积的结构),但进一步分析表明,焦虑诱导区域(OFT中心、EPM开放臂)的神经末梢活性与小鼠在这些区域的停留时间呈强正相关,表明vCA1区组胺能信号在焦虑条件下被动态募集(图1J、1M)。
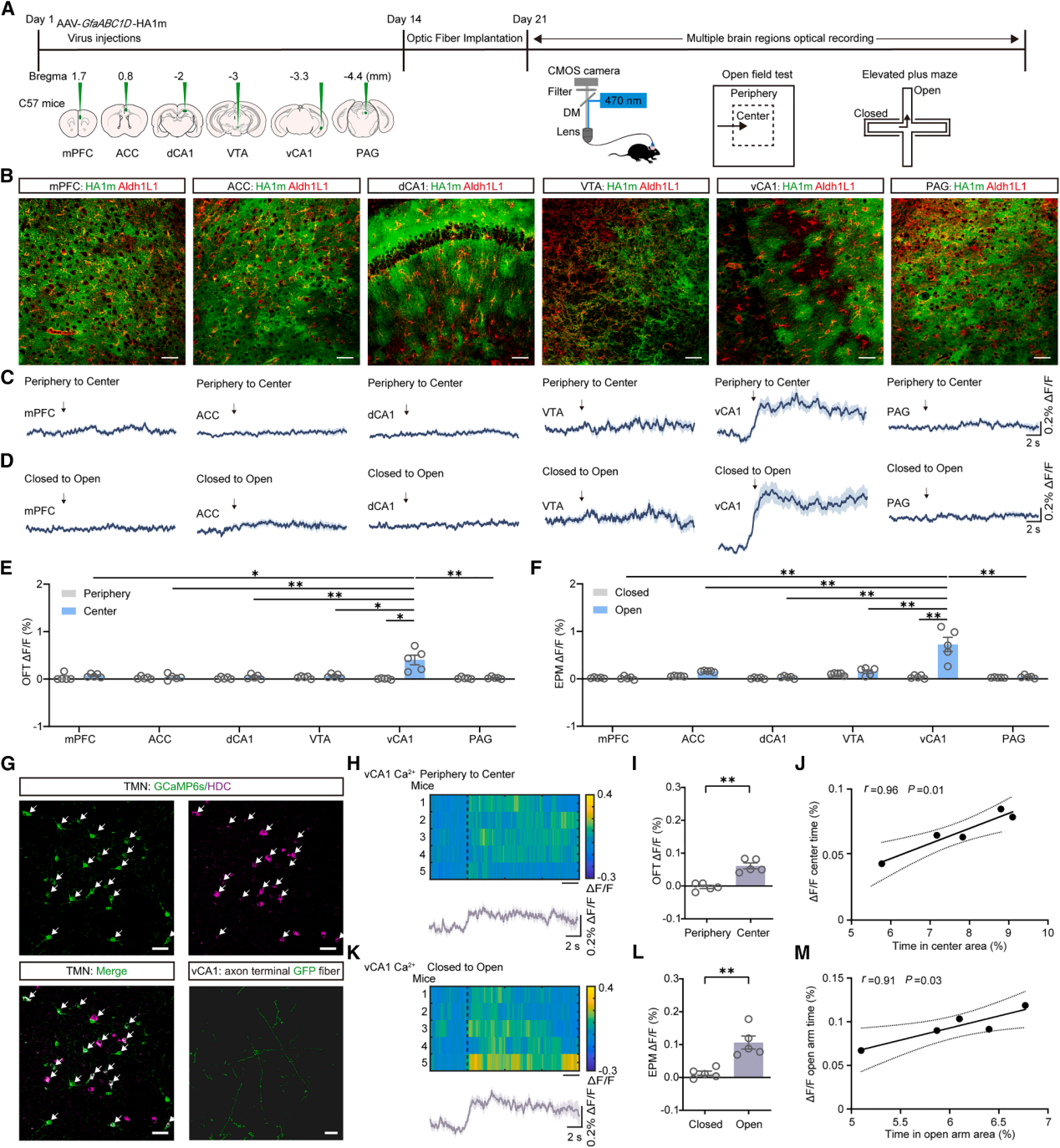
图1 | 焦虑环境下脑区特异性的组胺释放
为探究TMN-vCA1组胺能环路动态在焦虑中的潜在作用,在HDC-CreERT2小鼠的TMN组胺能神经元中,通过Cre依赖的方式病毒表达ArchT,并在vCA1区上方植入光纤以抑制组胺能神经末梢活性(图2A、2B)。与GFP对照组相比,光遗传学抑制组胺能神经末梢((10 ms/pulse, 20 Hz))显著减少了小鼠在OFT中心区域的停留时间和在EPM开放臂的停留时间(图2C、2D);而抑制TMN向mPFC或VTA的组胺能神经末梢,对小鼠在OFT和EPM试验中的焦虑样行为无影响(图2E-2H)。这些结果表明,特异性沉默TMN-vCA1组胺能环路会急性诱导焦虑样行为。为验证vCA1区组胺能神经末梢活性增强是否足以缓解焦虑样行为,在HDC-CreERT2小鼠TMN神经元中通过病毒表达oChIEF,并对vCA1区组胺能末梢进行光遗传激活。结果显示,该激活显著增加小鼠在OFT中心区及EPM开放臂的停留时间(图2I-2L),表明TMN-vCA1组胺能环路可调控焦虑样行为。
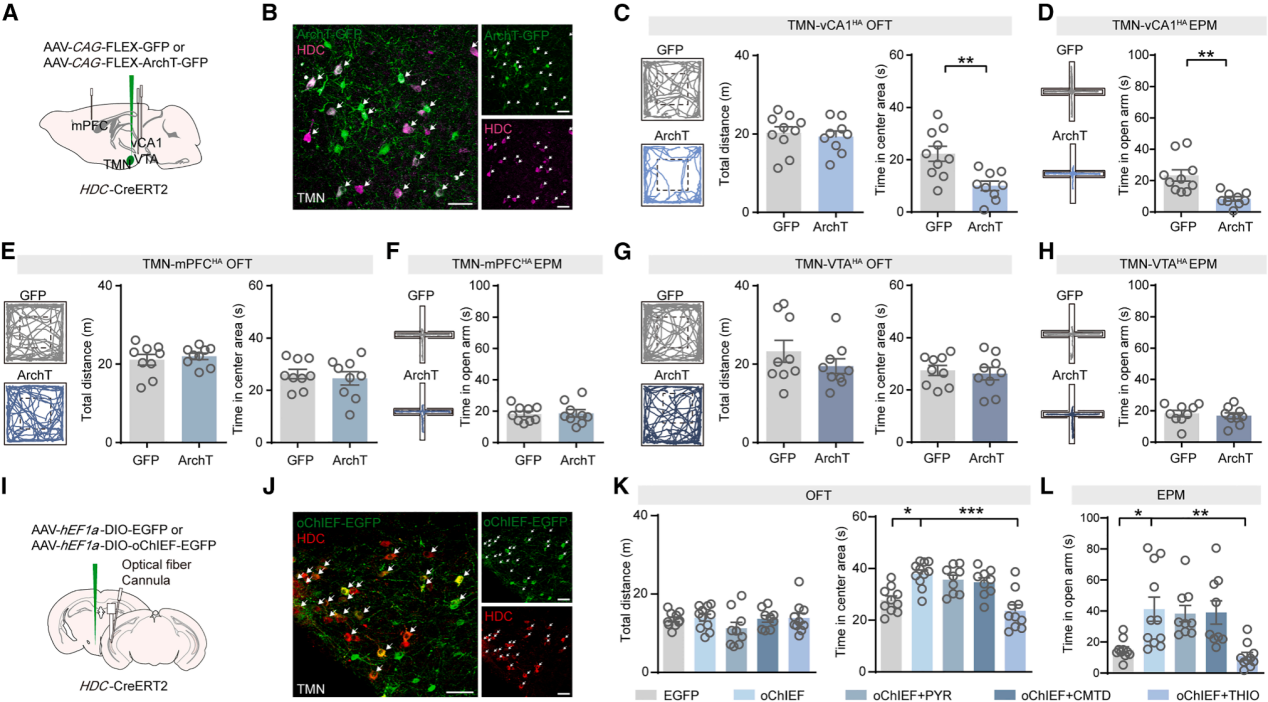
图2 | TMN-vCA1组胺能环路双向调控焦虑样行为
为明确介导焦虑样行为的组胺受体类型(H1R、H2R或H3R),在OFT和EPM试验中,分别微量注射组胺受体拮抗剂,并结合表达oChIEF的组胺能神经末梢光刺激(图2I、2J)。结果显示,与oChIEF组相比,光遗传学激活组胺能神经末梢并联合使用H3R拮抗剂硫丙咪胺(THIO)时,小鼠在OFT中心区域和EPM开放臂的停留时间恢复至EGFP组水平,而联合使用H1受体拮抗剂如吡嗪酮(PYR)或H2受体拮抗剂西咪替丁(CMTD)时无此效果(图2K、2L)。这些结果表明,TMN-vCA1组胺能环路通过H3R介导抗焦虑效应。
为进一步探究组胺信号在焦虑中的细胞类型特异性作用,通过向Hrh3fl/fl小鼠的vCA1区递送AAV-hSyn-Cre-EGFP,敲低神经元H3R水平。原位杂交证实Cre表达小鼠的Hrh3基因转录水平显著降低(图3A-3C)。行为学结果显示,Cre表达小鼠在OFT中心区域的停留时间与EGFP对照组无差异,但运动距离更短;在EPM开放臂的停留时间也无显著变化(图3D-3G)。这些结果表明,敲低vCA1区神经元H3R不影响焦虑样行为,但会轻微影响自主运动活动。
星形胶质细胞是中枢神经系统中最丰富的胶质细胞,是神经环路的关键组成部分,在生理和疾病中发挥重要作用。为进一步评估星形胶质细胞H3R在焦虑中的作用,通过Hrh3fl/fl小鼠的vCA1区星形胶质细胞靶向递送AAV-GfaABC1D-mNeonGreen-IRES-iCre,敲低H3R水平(图3H)。原位杂交证实了敲低效率(图3I、3J)。行为学结果显示,与对照组相比,星形胶质细胞H3R敲低的小鼠在OFT中心区域和EPM开放臂的停留时间显著减少,且未观察到短期或长期识别记忆(新物体识别试验)或联想记忆(恐惧条件反射试验)缺陷(图3K-3N)。这些结果表明,敲低星形胶质细胞H3R会诱导焦虑样行为。
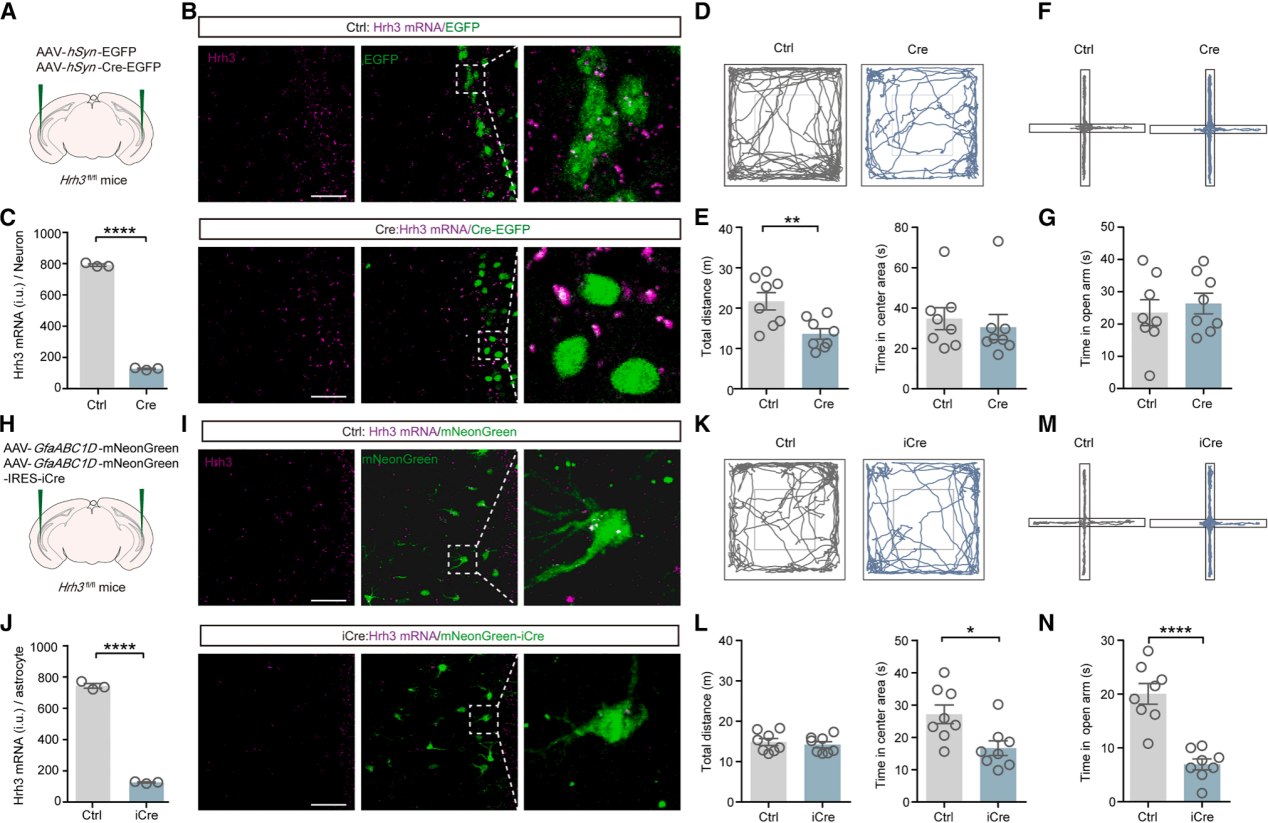
图3 | 敲低vCA1中星形胶质细胞的H3R会诱导类焦虑行为
为验证星形胶质细胞H3R是否足以降低焦虑水平,向vCA1区递送AAV-GfaABC1D-mNeonGreen-IRES-iCre和AAV-EF1α-DIO-OptoH3R-mCherry,通过蓝光刺激激活星形胶质细胞H3R。定量证实,OptoH3R-mCherry在星形胶质细胞中高度特异性表达(图4A-4C)。激活星形胶质细胞H3R显著增加了小鼠在OFT中心区域和EPM开放臂的停留时间(图4D-4F)。为进一步证实星形胶质细胞H3R在抗焦虑效应中的作用,向Aldh1L1-CreERT2小鼠的vCA1区递送AAV-CAG-FLEX-Hrh3-GFP,长期过表达星形胶质细胞H3R(图4G)。原位杂交证实星形胶质细胞Hrh3 mRNA表达显著增加,Western blot结果显示vCA1区H3R蛋白水平显著升高(图4H、4I)。行为学结果显示,尽管星形胶质细胞H3R过表达小鼠在OFT中心区域的探索时间无显著变化,但在EPM开放臂的停留时间显著增加(图4J-4L)。这些结果共同表明,星形胶质细胞H3R对于调控焦虑样行为既是必要的也是充分的。
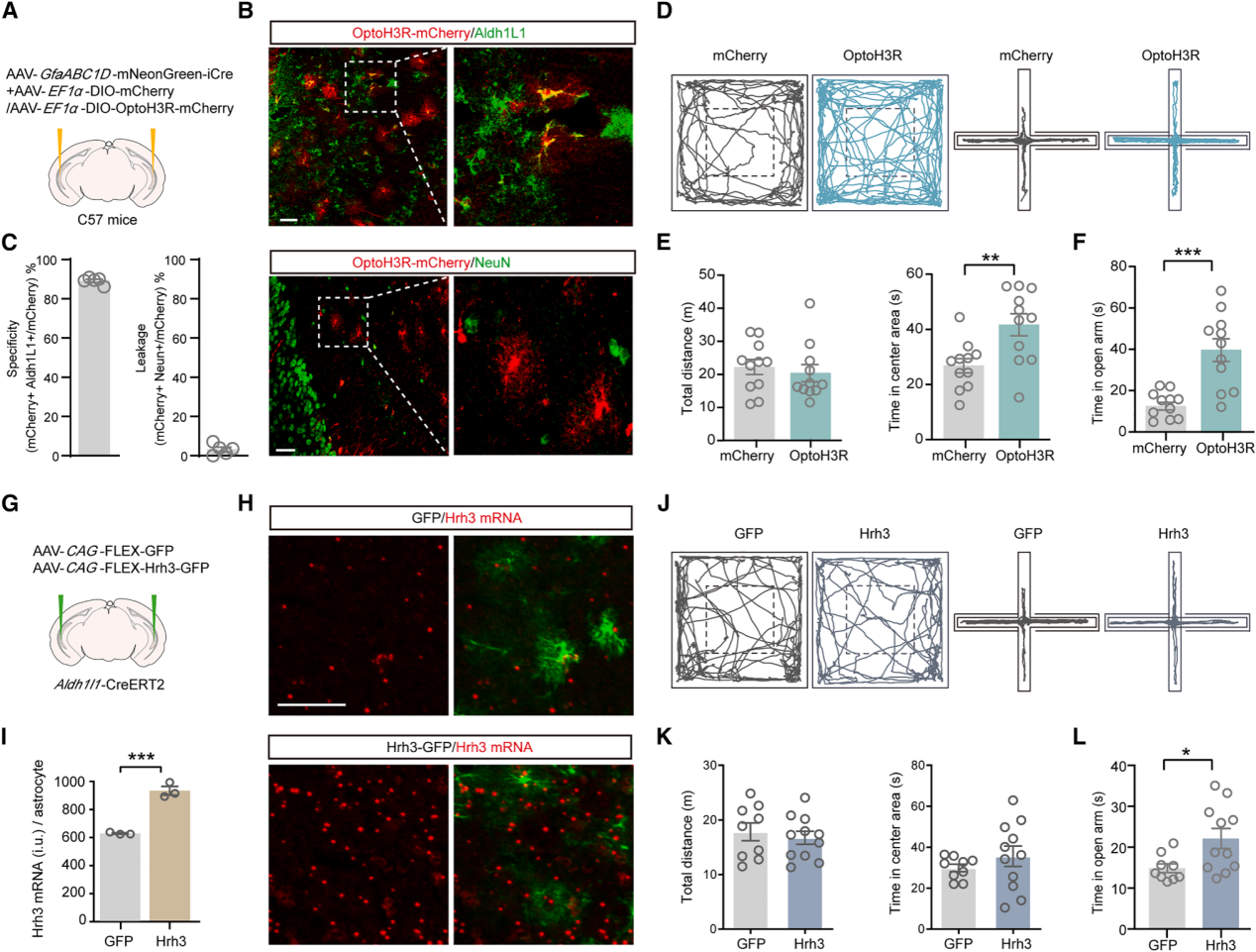
图4 | 增强vCA1区星形胶质细胞H3R信号传导可缓解焦虑样行为
星形胶质细胞通过动态的细胞内钙离子信号响应神经元活动。为验证组胺能输入是否驱动vCA1区星形胶质细胞的钙离子应答,在HDC-CreERT2小鼠的TMN组胺能神经元中表达红光激活的光敏通道蛋白ChrimsonR-tdTomato,并在vCA1区星形胶质细胞中表达GCaMP6f。免疫染色证实病毒表达具有较高特异性与效率(图5A-5C)。通过光遗传学激活vCA1区组胺能轴突神经末梢,光纤光度法记录星形胶质细胞钙离子应答,发现ChrimsonR介导的组胺能神经末梢光激活(638 nm,10 ms/pulse,20 Hz for 20 s))可诱导显著的星形胶质细胞钙离子应答,且该应答可被H3R拮抗剂THIO阻断(图5D-5F),表明H3R介导vCA1区组胺增强的星形胶质细胞钙离子应答。
为探究星形胶质细胞在焦虑中的动态作用,采用在体光纤光度法记录vCA1区星形胶质细胞钙信号(图5G)。结果显示,小鼠在OFT中心区域及从EPM闭合臂进入开放臂时,星形胶质细胞钙活性均显著升高(图5J-5M),提示焦虑诱导环境可激活星形胶质细胞应答。为进一步了解星形胶质细胞H3R水平对焦虑样行为中星形胶质细胞活性的影响,通过向Hrh3fl/fl小鼠的vCA1区星形胶质细胞表达AAV-GfaABC1D-mCherry-IRES-iCre和GCaMP6f,并通过免疫染色验证其特异性与效率(图5H、5I)。结果显示,星形胶质细胞H3R敲低的小鼠,在OFT的外周和中心区域以及EPM的开放臂中,星形胶质细胞钙离子活性显著降低,表明敲低星形胶质细胞H3R可阻断焦虑诱导环境中的星形胶质细胞钙离子应答(图5J-5M)。在vCA1区通过注射AAV表达抑制性DREADDs(hM4Di)以沉默vCA1区局部神经元,并在星形胶质细胞中表达GCaMP6f监测钙信号后发现,无论给予生理盐水还是CNO,星形胶质细胞在OFT和EPM实验中的钙信号平均幅度均无显著变化。该结果表明,星形胶质细胞对焦虑相关环境的钙响应并不依赖局部神经元活性,而更可能由组胺信号驱动。
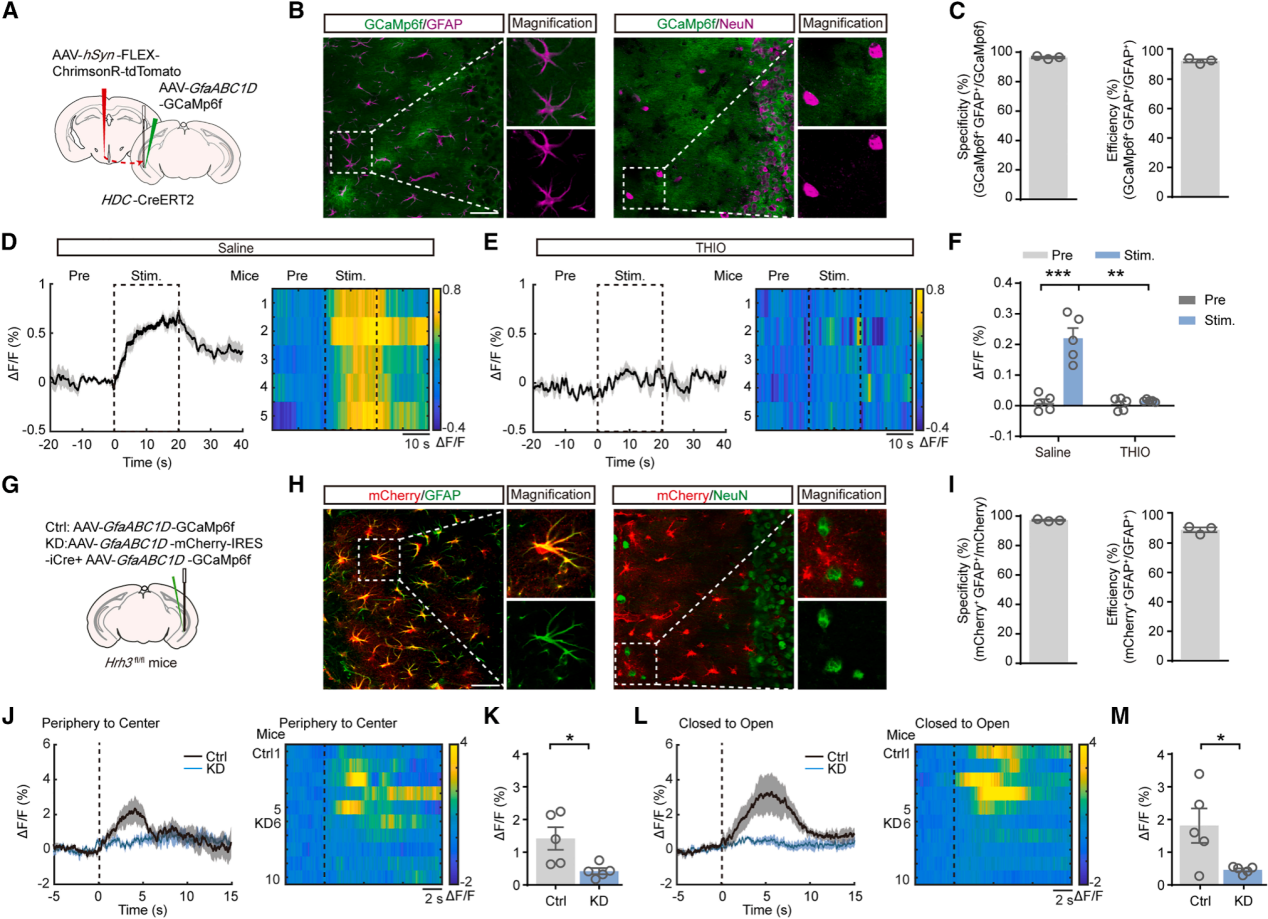
图5 | H3R决定vCA1星形胶质细胞对焦虑相关环境的应答
为评估vCA1区星形胶质细胞钙离子激活在焦虑样行为中的因果作用,向小鼠vCA1区双侧注射对照病毒或星形胶质细胞表达ChR2的病毒,并在vCA1区植入光纤。免疫染色证实病毒表达具有较高特异性与效率(图6A-6C)。在小鼠进行OFT探索时,光遗传学激活vCA1区星形胶质细胞,ChR2激活组小鼠在焦虑诱导的OFT中心区域的停留时间显著增加;在EPM试验中,特异性激活vCA1区星形胶质细胞也增加了小鼠在开放臂的探索时间(图6D-6G)。这些发现证实,激活vCA1区星形胶质细胞可减少焦虑样行为。为进一步验证vCA1区星形胶质细胞在组胺抗焦虑效应中的作用,在该区域星形胶质细胞中表达hPMCA2w/b以降低其钙离子活性(图6H)。免疫染色显示该策略具有较高特异性与效率(图6I、6J)。与mCherry对照组相比,表达hPMCA2w/b显著消除了组胺能神经末梢激活在OFT和EPM中的抗焦虑效应(图6K-6M),表明星形胶质细胞钙信号是该效应所必需的。
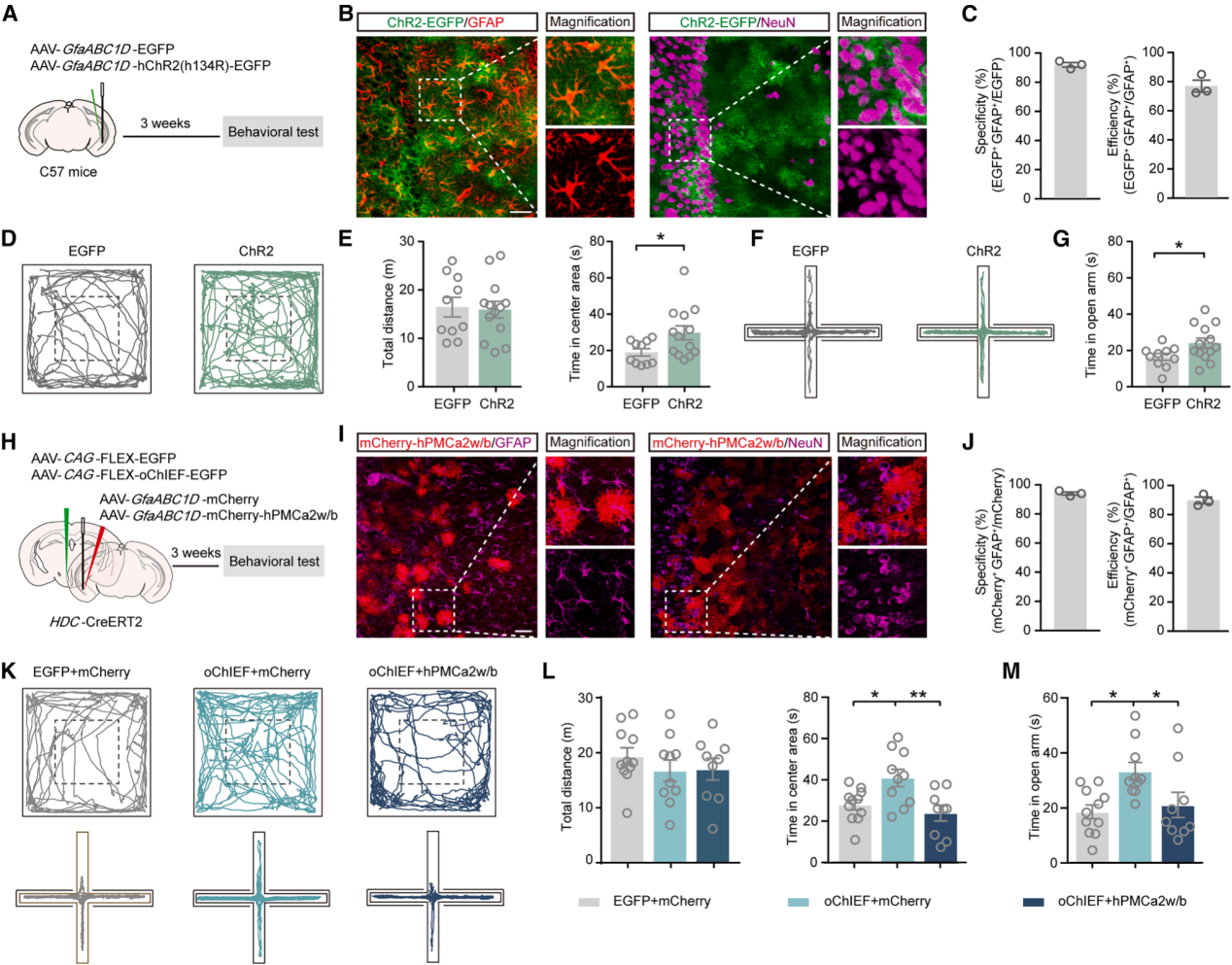
图6 | 星形胶质细胞的活动介导了组胺能神经环路的抗焦虑效应
星形胶质细胞可通过钙依赖性释放胶质递质调控突触可塑性。为探究H3R是否介导相关递质释放,采用ELISA检测Immepip处理后星形胶质细胞培养上清中的递质水平。结果显示,H3R激活显著促进GABA释放,而对ATP和谷氨酸无明显影响,该效应可被THIO阻断(图7A)。为进一步验证GABA在体内的作用,在vCA1区神经元中表达AAV-hSyn-iGABASnFR,并通过光纤光度法记录焦虑样行为期间的GABA释放(图7B、7C)。结果显示,小鼠探索OFT中心区和EPM开放臂时,细胞外GABA水平显著增加(图7D-7G)。进一步在Hrh3fl/fl小鼠的vCA1区共表达AAV-GfaABC1D-mCherry-IRES-iCre和GABA探针(图7B),发现条件性星形胶质细胞H3R敲低会显著减弱旷场中心区域和高架十字迷宫开放臂中的GABA信号(图7D-7G),表明H3R介导星形胶质细胞来源的GABA释放。为评估GABA在抗焦虑效应中的功能作用,在激活H3R的条件下给予GABAA受体拮抗剂荷包牡丹碱(bicuculline)。结果显示,荷包牡丹碱可消除H3R激活在OFT和EPM中的抗焦虑效应(图7H-7K),表明GABAA受体信号对此过程是必需的。此前研究表明,海马谷氨酸能锥体神经元活性增加会促进焦虑行为,研究结果提示,星形胶质细胞H3R激活可能通过GABA信号抑制海马局部兴奋性,从而发挥抗焦虑作用。
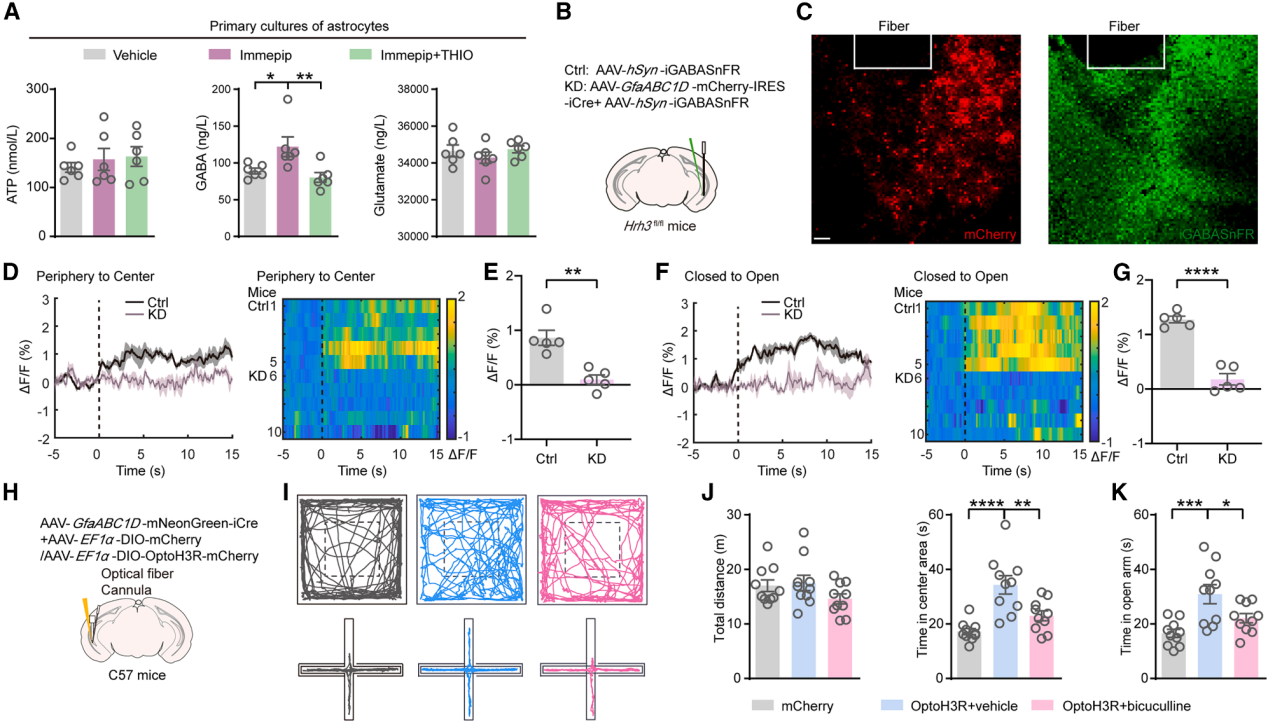
图7 | 星形胶质细胞上的H3R通过释放胶质递质GABA发挥抗焦虑效应
为探究组胺调控的星形胶质细胞在慢性应激中的作用,采用慢性社交挫败应激(CSDS)模型,一种能重现应激环境诱导的焦虑表型的行为学相关模型。连续10天,CSDS组小鼠每天与攻击性定居小鼠接触10分钟,对照组小鼠则通过透明隔板与攻击性定居小鼠分离,持续相同时间。结果显示,当小鼠在CSDS期间遭受攻击时,星形胶质细胞会快速且强烈地应答,表明应激暴露会诱导星形胶质细胞活性(图8A)。进一步通过荧光探针检测发现,CSDS显著上调vCA1区星形胶质细胞中Hrh3 mRNA表达(图8B、8C)。
为明确星形胶质细胞H3R是否调控CSDS诱导的焦虑,在vCA1区注射AAV-GfaABC1D-mNeonGreen-IRES-iCre和AAV-EF1α-DIO-OptoH3R-mCherry,以激活星形胶质细胞H3R(图8D)。结果显示,光遗传学激活星形胶质细胞H3R可逆转CSDS诱导的小鼠在OFT中心区域和EPM开放臂停留时间的减少,表明在慢性应激条件下,激活星形胶质细胞H3R足以产生抗焦虑效应(图8E-8G)。进一步在Aldh1l1-CreERT2小鼠的vCA1注射AAV-CAG-FLEX-Hrh3-GFP实现星形胶质细胞中H3R的长期过表达,同样可逆转CSDS所导致的小鼠在中心区域和开放臂中探索时间的降低(图8H-8K)。综上,这些数据证实,慢性应激会上调vCA1区星形胶质细胞H3R的表达,靶向增强该通路可缓解应激诱导的焦虑相关行为。
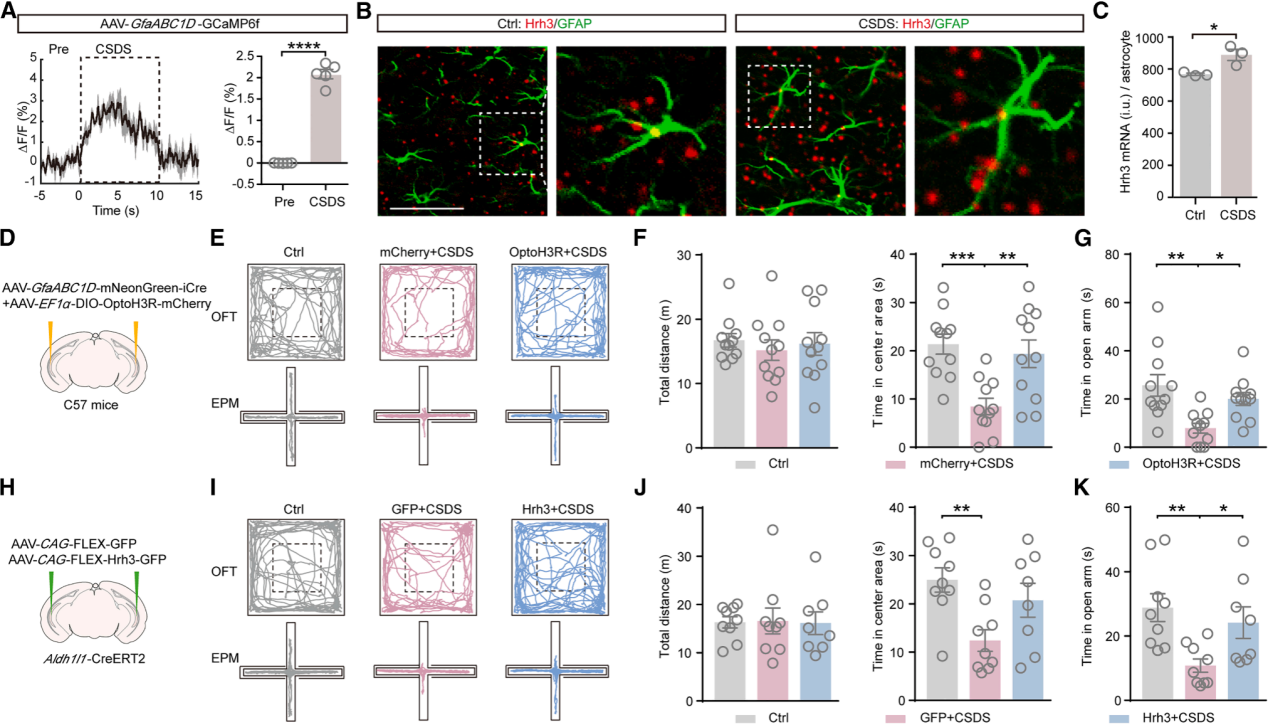
图8 | 星形胶质细胞H3R可改善CSDS诱导的焦虑样行为
研究揭示了组胺系统中焦虑信息的编码方式,以及通路特异性TMN-vCA1组胺能星形胶质细胞信号在调控焦虑相关行为中的作用。识别出调控焦虑相关行为的星形胶质细胞H3R,为焦虑障碍的治疗提供潜在靶点。
本文使用的工具病毒布林凯斯均可提供:
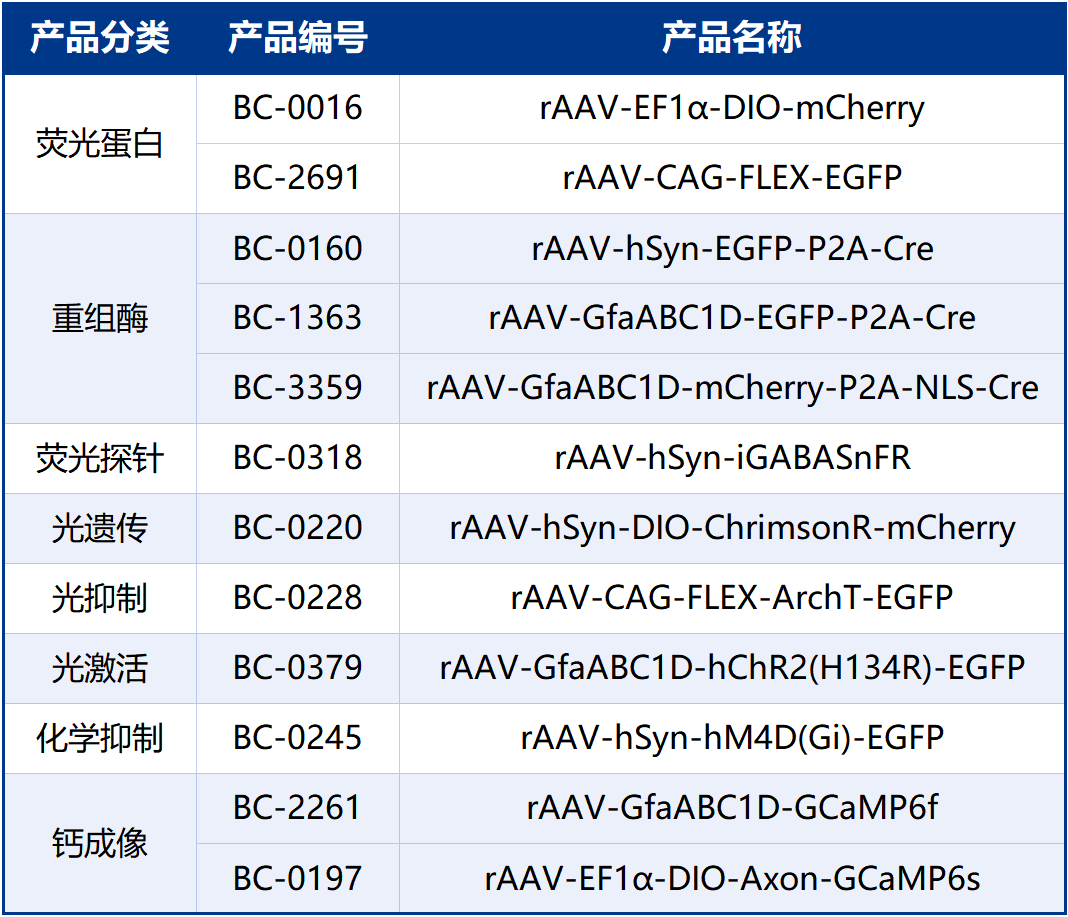
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。