哺乳动物组织再生能力有限,如关节软骨,导致骨关节炎等关节疾病难以治愈。骨关节炎(OA)作为软骨退行性疾病,终身患病风险达40%,现有手术(如微骨折术)和干细胞移植等治疗效果不佳,且再生的软骨多为力学性能差的纤维软骨。临床观察已证实,焦虑、抑郁等精神类疾病是加速骨关节炎发生与发展的重要风险因素,提示了大脑可能调控关节软骨再生,但这一现象未被实验证实。
2026年1月13日,同济大学医学院附属养志康复医院(上海市阳光康复中心)罗剑教授团队,在Annals of the Rheumatic Diseases在线发表了题为“A brain-driven neural circuit contributes to tissue regeneration in joint cartilage”相关文章,首次证实存在下丘脑室旁核促肾上腺皮质激素释放激素神经元(PVNCRH)-关节滑膜交感神经组成的脑-软骨神经环路,通过去甲肾上腺素(NE)/β2-肾上腺素能受体(ADRB2)/PRG4⁺细胞通路调控软骨再生,且新生软骨的形态结构、分子标志物表达及力学性能均与天然透明软骨高度一致。

研究人员利用脑部磁共振成像,发现膝骨关节炎(KOA)患者PVN的部分各向异性(FA,扩散张量成像常用指标,反映脑白质纤维完整性)和低频波动振幅(ALFF,低频波动振幅,静息态功能磁共振指标,反映脑区自发神经活动强度)值升高,且与其软骨损伤呈正相关(图1A,B,C)。此外,利用英国生物样本库(UKB)数据进行验证也得到了一致的结论(图1D)。上述结果表明PVN升高的FA、ALFF值或可作为OA发展的潜在生物标志物。
采用多突触逆行追踪系统,在小鼠膝关节腔注射表达EGFP的PRV,逆行跨突触标记关节上游神经元(图1E)。96小时后,PRV-EGFP逆行至脊髓、脑干及前脑,下丘脑PVN出现明显标记(图1F),证实PVN与关节滑膜神经间存在跨神经元环路。进一步利用光遗传结合电生理记录技术验证该环路功能,结果显示光遗传激活PVN后,关节滑膜神经电活动即刻增强(图1G,H),表明PVN神经元与滑膜神经存在功能性神经连接。
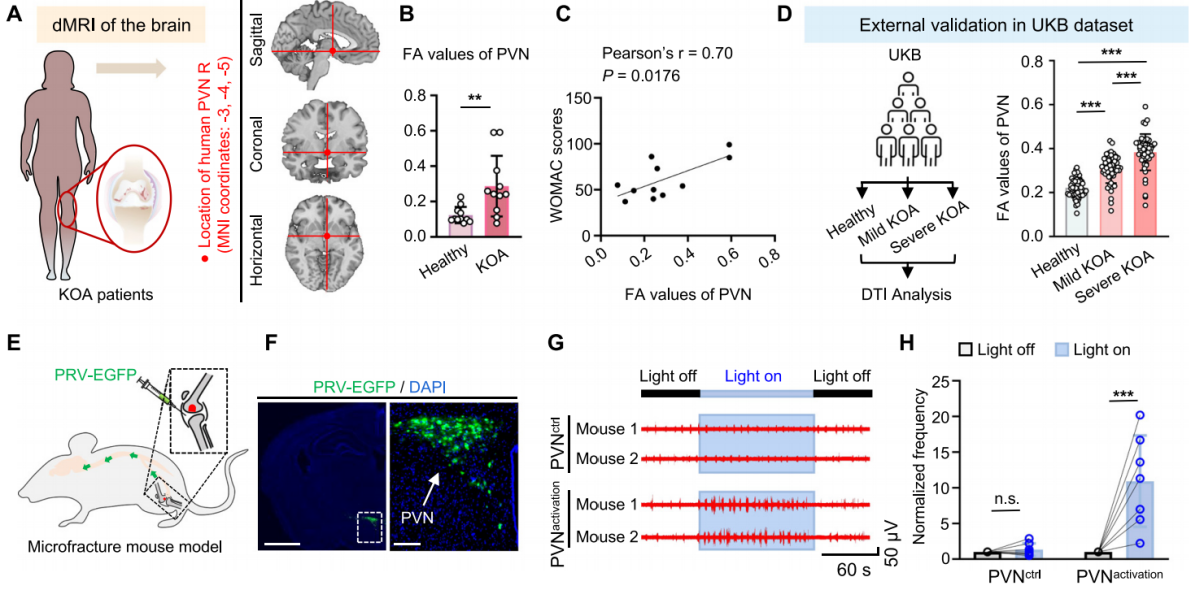
图 1. PVN神经元与关节存在功能性连接
PVNCRH神经元是调控焦虑抑郁的关键神经元类型,推测其活动可通过滑膜神经传出信号调控软骨再生。研究人员进一步通过免疫荧光染色证实了PVNCRH神经元和关节之间存在连接(图2A)。为了验证PVNCRH神经元与滑膜神经的环路,光遗传学激活小鼠PVNCRH神经元并记录滑膜神经电活动。结果显示,激活PVNCRH神经元可即刻诱导滑膜神经电活动增加(图2B,C),证实二者存在功能性连接。为了明确PVNCRH神经元对软骨再生的调控作用,对CRH-Cre小鼠PVN区注射不同AAV载体,再进行软骨缺损或DMM手术(内侧半月板失稳手术,常用骨关节炎动物模型构建方法)构建软骨损伤模型。结果表明,抑制PVNCRH神经元可显著改善软骨再生及OA评分(图2D,I,J),上调PRG4、ACAN、COL2A1表达(软骨合成代谢标志物,图2E-G,K-M),下调COL1A1和MMP13表达(纤维软骨/软骨分解代谢标志物),恢复软骨弹性模量至接近正常水平(图2H),并缓解疼痛。反之,激活PVNCRH神经元会诱导软骨退变(图2I,J),伴随合成标志物下调、分解标志物上调(图2K,L)。综上,进一步证实了PVN中特定神经元(PVNCRH神经元)对关节软骨再生具有重要调控作用(图2N)。
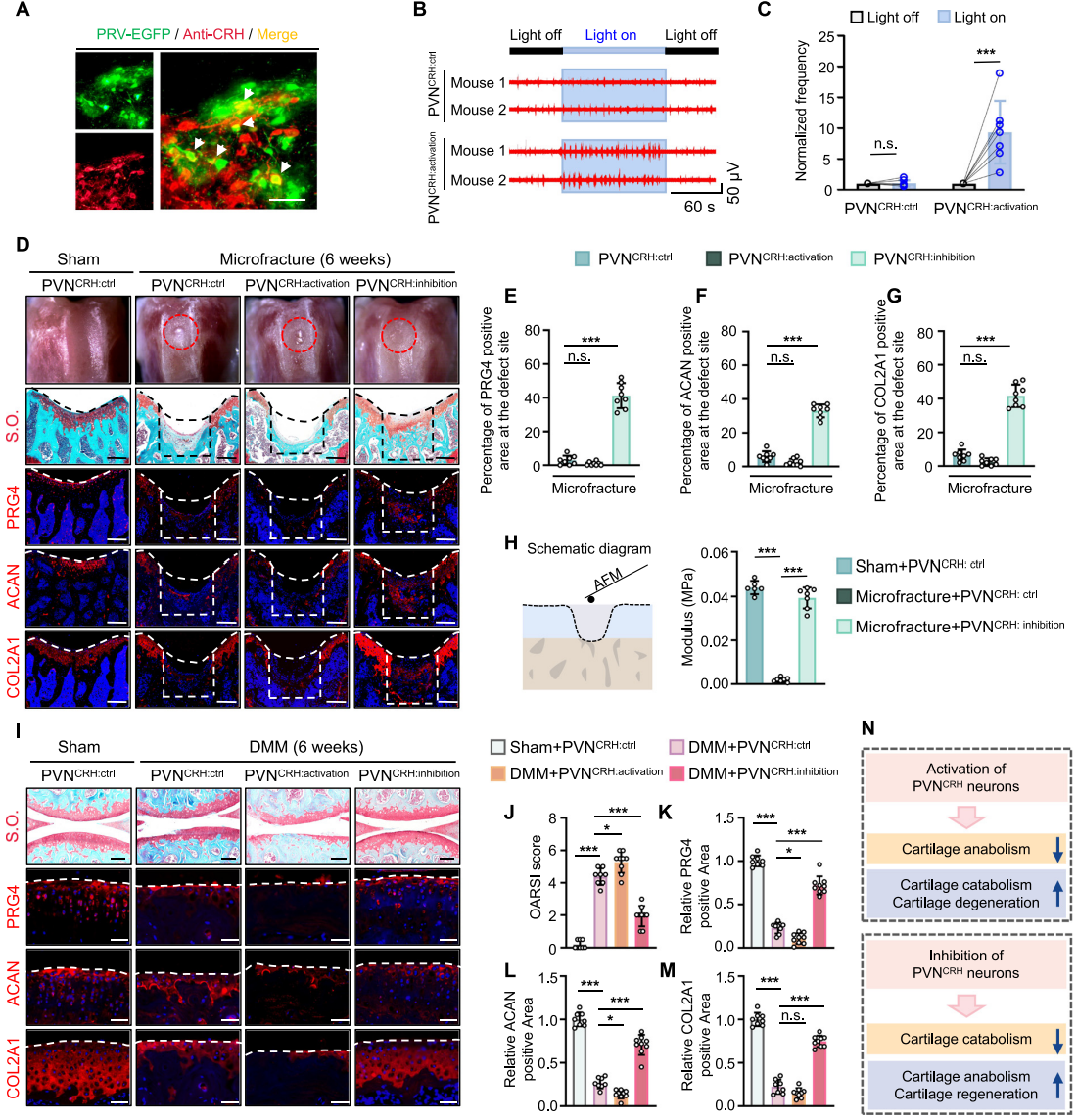
图 2. PVNCRH调控关节软骨再生
现有数据表明激活PVN或PVNCRH神经元会增加关节交感神经NE释放。研究人员进一步通过临床研究,检测KOA患者滑膜液NE浓度,发现其与PVN的FA值、ALFF值及WOMAC评分均呈正相关(图3A-C),提示关节滑液的NE浓度升高与患者PVN神经活动增强、软骨损伤加重密切相关。为了验证关节交感神经与软骨再生的调控关系,研究人员通过关节内注射6-羟基多巴胺(6-OHDA)建立了消融关节交感神经模型(图3D)。研究结果表明消融滑膜交感神经可促进稳定成熟软骨形成(图3E,F),增强软骨合成代谢(图3G,H)及弹性模量(图5I),抑制纤维软骨形成和分解代谢。DMM模型中,该操作可减轻软骨结构损伤(图3J,K),上调PRG4、ACAN、COL2A1表达(图3L-N),下调COL1A1、MMP13表达,同时缓解OA相关疼痛。
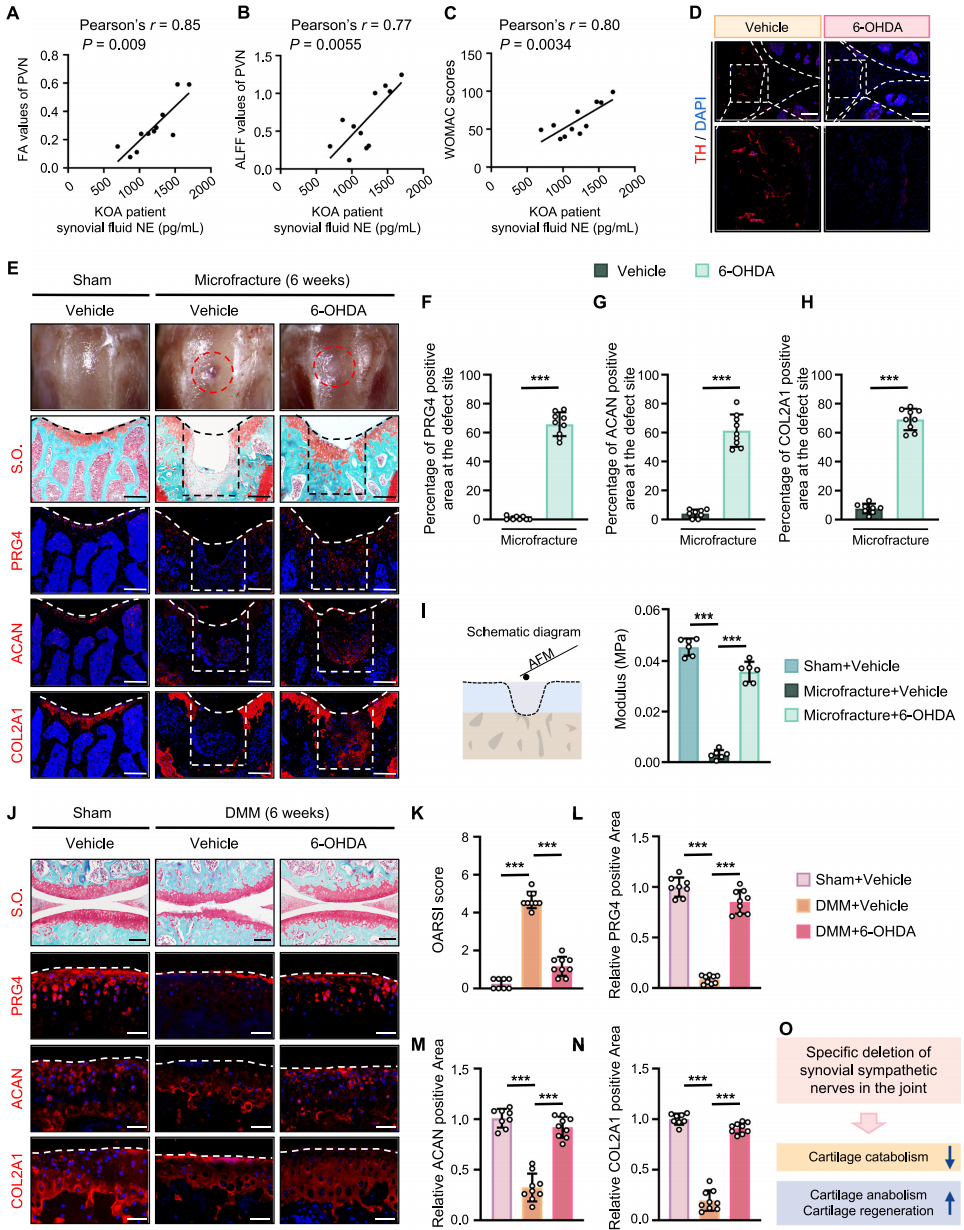
图 3. 特异性消融关节内交感神经可促进关节软骨再生
为了探究交感神经抑制软骨再生的机制,研究人员对软骨损伤手术后小鼠软骨组织进行单细胞RNA测序。结果显示消融交感神经后,软骨再生部位的PRG4⁺软骨祖细胞标记显著增强(图4A,B),提示交感神经信号可能通过调控PRG4⁺细胞抑制软骨再生。检测9种NE受体亚型表达发现,ADRB2在小鼠及人类关节软骨细胞中表达量最高(图4C)。KOA患者软骨样本免疫染色显示,42.4%的PRG4⁺细胞共表达ADRB2,单细胞测序也证实二者高共表达(图4D),表明ADRB2可能通过PRG4⁺细胞调控软骨再生。
在PRG4⁺细胞中条件性敲除Adrb2(Adrb2fl/fl;Prg4-Cre),软骨损伤及DMM模型中均观察到PRG4、ACAN、COL2A1表达上调(图4F-H,L-N),弹性模量恢复(图4I),COL1A1、MMP13表达下调,同时缓解疼痛,促进成熟软骨形成而非纤维软骨(图4O)。此外,使用ADRB2特异性反向激动剂ICI-118551(可特异性阻断ADRB2介导的信号通路)进行关节内注射,在两种软骨损伤模型中均通过增加PRG4⁺细胞数量、增强软骨合成代谢、提升弹性模量,进而促进成熟软骨再生并缓解关节疼痛。
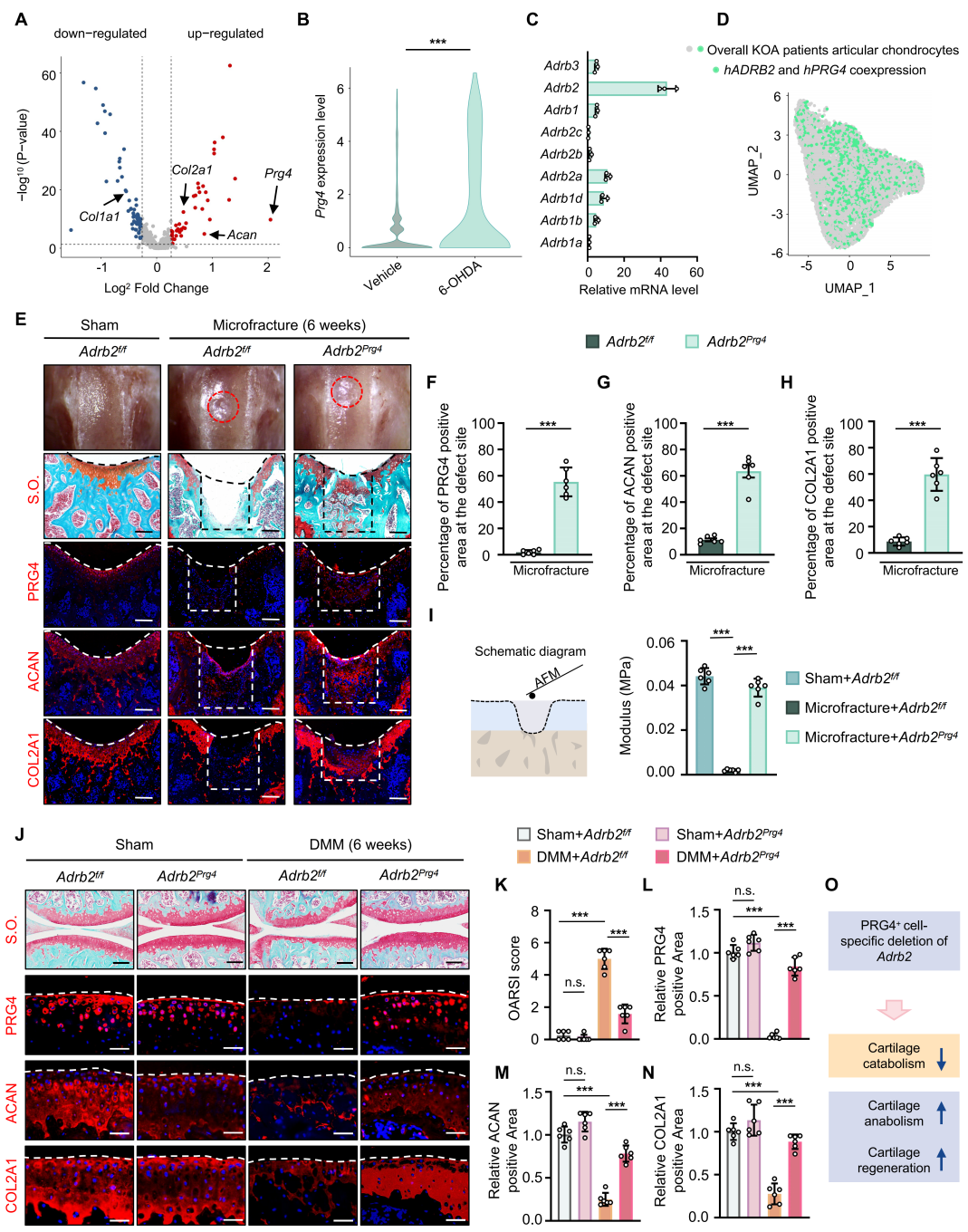
图 4. Prg4⁺细胞中条件性敲除Adrb2基因调控软骨再生
在非损伤关节小鼠模型中探究,关节内注射ADRB2特异性反向激动剂ICI-118551,能否挽救PVNCRH神经元激活引发的软骨退变。结果显示,ICI-118551干预6周即呈现有益效果,10周时保护作用显著(图5A-E),软骨指标近乎恢复正常生理水平,证实抑制ADRB2可有效预防PVNCRH神经元激活导致的软骨退变。
为了探索ADRB2靶向治疗在人类软骨再生中的潜力,将人类关节软骨外植体与ICI-118551共培养1周,并检测软骨再生相关指标(图5F)。结果显示,抑制ADRB2可促进软骨外植体蛋白聚糖面积增加(图5G,H),PRG4和COL2A1表达上调(图5I,J),糖胺聚糖(其释放量增加是软骨降解的重要标志)释放量呈剂量依赖性减少(图5K)。这些结果表明,抑制ADRB2可阻止人类关节软骨外植体降解,凸显了ADRB2作为OA治疗靶点的临床潜力。
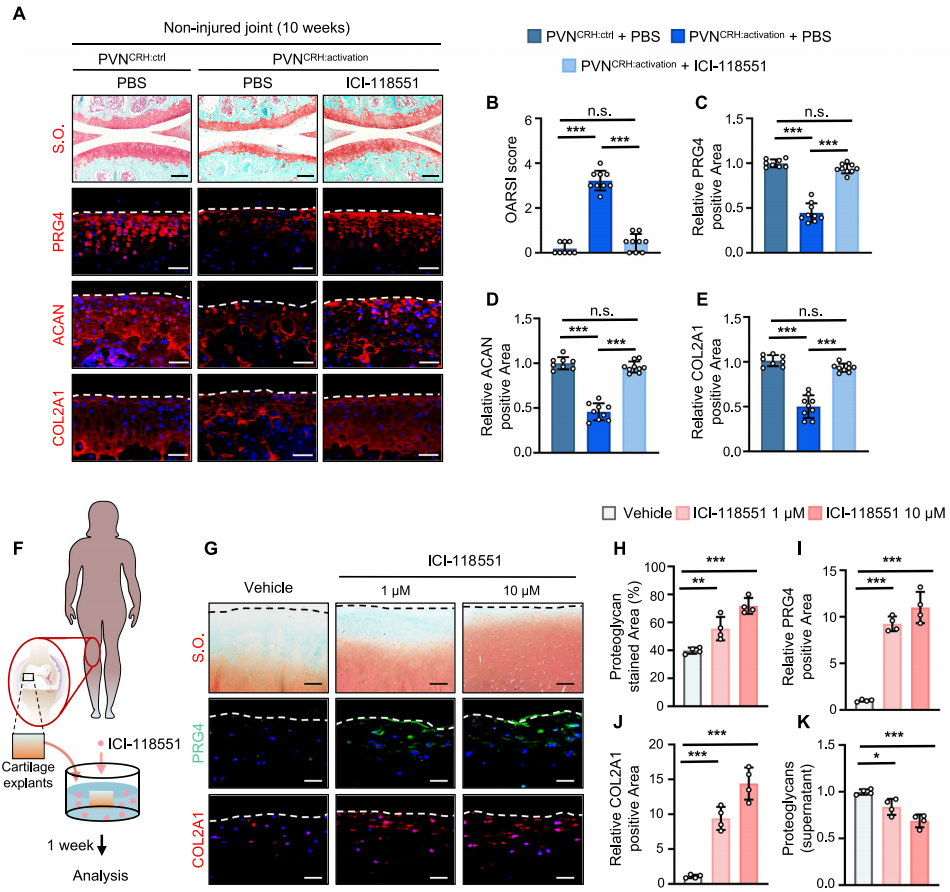
图 5. ADRB2反向激动剂可有效抑制软骨退变
该研究首次揭示脑-软骨神经环路调控外周组织再生的机制,证实中枢神经系统可通过交感神经调控外周干细胞功能。PVN的FA值和ALFF值可作为OA病情严重程度的潜在影像学标志物。明确ADRB2为OA治疗核心靶点,局部应用ADRB2反向激动剂、脑刺激技术(如经颅磁刺激)等为OA提供微创、高效的新治疗策略。
同济大学医学院罗剑教授,王岳主任和上海交通大学附属第六人民医院彭晓春主任为论文的共同通讯作者。同济大学霍孔林博士后、马学斌博士、薛艳博士为该论文的共同第一作者。
文章链接:https://www.sciencedirect.com/science/article/abs/pii/S0003496725045972
本文使用的工具病毒布林凯斯均可提供:
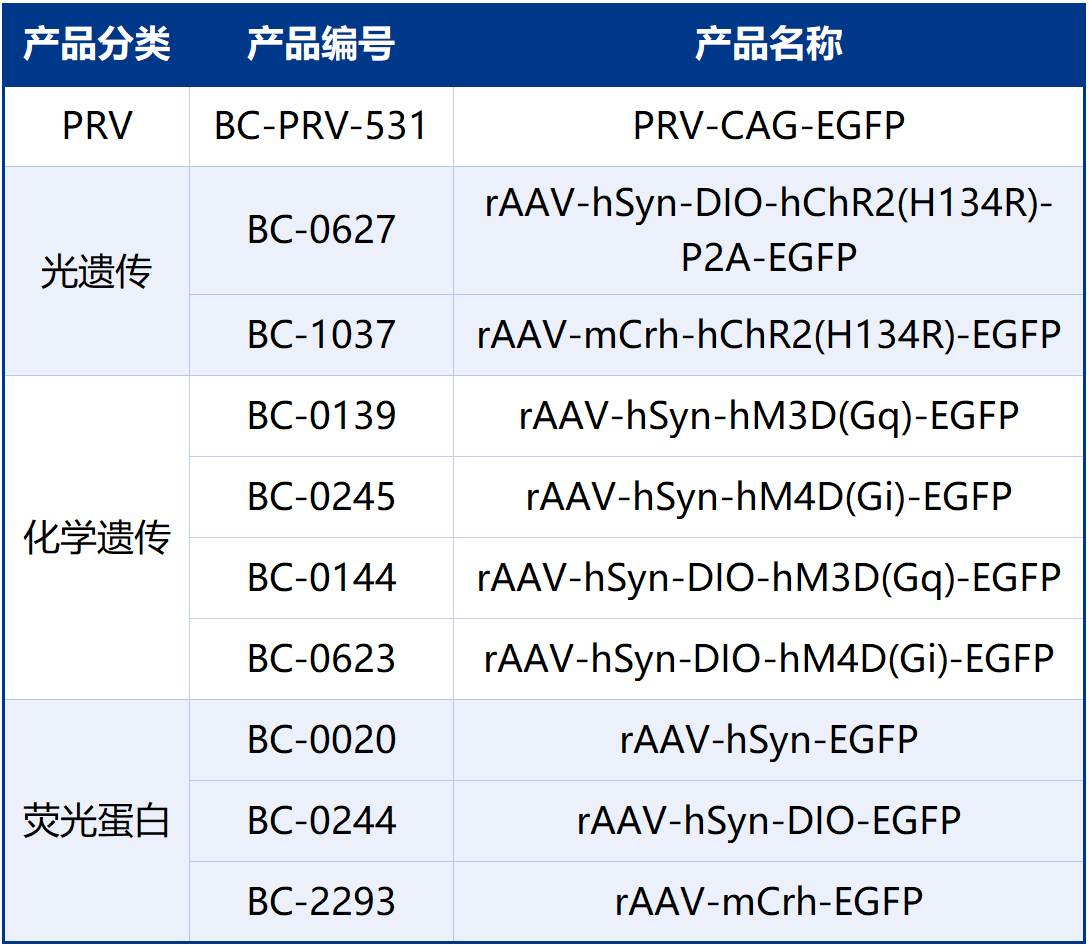
同时布林凯斯也可提供各类定制服务请联系小布:18971216876(微信同号)或者咨询所在区域的销售经理获取更多信息。